多元醇在Fe3O4纳米粒子水热熟化中的效应研究*
2020-06-28孙浩东崔殿鑫毕研平
孙浩东 辛 铭 崔殿鑫 毕研平
药学院,山东第一医科大学(山东省医学科学院),山东 泰安 271016
Fe3O4纳米粒子具有超顺磁性、小尺寸效应、表面效应等性能,使其在催化、磁共振成像、靶向给药、吸附分离等方面显示出广泛的应用前景[1-2]。目前,制备Fe3O4纳米粒子有诸多方法,如共沉淀法、水热法、溶剂热法和金属有机前驱体热分解法等。共沉淀法[3]一般是在二价和三价铁盐的水溶液中加入适当的碱来生成Fe3O4,操作简单且成本较低,但颗粒大小和形状不规则,易发生团聚,影响磁性粒子的性能。金属有机前驱体热分解法是利用铁或钴的有机前驱体物质加热分解而制备[4],其特点是粒子大小均一,形状规则。此法制备的磁性粒子粒径较小(一般小于50 nm)且表面疏水,在生物医学及吸附分离领域的应用受到限制,其反应原料及所需的大量有机反应介质对环境并不友好。溶剂热法一般采用无机铁盐作为铁源,用有机溶剂作反应介质,在高温高压的反应釜中反应生成晶核并逐渐发生聚集和结晶熟化[5],产物可能为二级粒子(即由多个小粒子团聚融合而成),其粒径可在几十纳米至几百纳米之间调控且大小相对均一,此法虽然被广泛采用,但也需要消耗大量有机溶剂。若用水代替其中的有机溶剂,则称为水热法。一般需要先制备磁性纳米粒子母核,再进行水热熟化[6]。因为 Fe3O4在高温高压的水中容易被氧化成α-Fe2O3或转变成其它非磁性的水合结晶,所以研究不多。
综合以上的制备方法,作者提出了一种新的方法来制备磁性纳米粒子,即首先用共沉淀法制备Fe3O4磁性纳米粒子母核,再将母核分散到某些多元醇的水溶液中进行水热反应,母核经过结晶熟化而成为粒径均一、形状规则的磁性纳米粒子。本文主要研究了多元醇的种类及浓度对于水热产物粒子的形貌及磁性的影响。
1 仪器与试剂
1.1仪器
透射电子显微镜(TEM,JEM100CXII,日本电子公司);扫描电子显微镜(SEM,S-4800,日本日立公司);振动样品磁强计(LDJ 9600-1,LDJ Electronic);超声波清洗器(KQ3200E,昆山市超声仪器有限公司);恒温干燥箱(DZF-6030,上海新苗医疗器械制造有限公司);低速离心机(TDL-40B,上海安亭科技仪器厂)。傅里叶变换红外光谱仪(IRAffinity-1S,日本岛津公司)
1.2试剂
FeCl3·6H2O(CP,上海晶纯生化科技股份有限公司);FeSO4·7H2O(AR,天津市科密欧化学试剂开发中心);NaOH(AR,天津市永大化学试剂有限公司);木糖醇(BR,99%,上海源叶生物);甘露醇(AR,99%,国药试剂);聚乙烯醇(PVA05-88和PVA17-88,99%,国药试剂);玉米糊精(AR,国药试剂);羟丙甲纤维素(HPMC 20S,99%,临沂亿群化工);无水乙醇(AR,天津市永大化学试剂有限公司)。
2 实验方法
2.1共沉淀法制备磁性纳米粒母核
称取2.8 g FeCl3·6H2O和1.4 g FeSO4·7H2O于100 ml烧杯中,加入40 ml超纯水超声溶解,用200 μm微孔滤膜过滤,滤液中迅速加入15 ml NaOH(15%,w/w),振摇超声10 min。将此混悬液4000 rpm离心1 min,弃上清,用20 ml超纯水洗涤两次,收集黑色沉淀即为Fe3O4磁性纳米粒母核。
2.2磁性纳米粒母核的水热反应
将2.1制得的磁性纳米粒母核用超纯水超声分散并定容到110 ml超声得到均匀的黑色混悬液(其中Fe3O4理论浓度约为10 mg/ml)。量取混悬液15 ml,置于聚四氟乙烯水热反应釜中,加入一定量的多元醇稳定剂,搅拌并超声5 min后密封,置于温度200℃的烘箱中保温24h,降至室温后取出离心得到沉淀,并用超纯水洗涤并离心(4000rpm,某些样品需20000rpm)两次,收集沉淀进行表征。水热反应中所选择的稳定剂包括丙三醇,赤藓醇,木糖醇,甘露醇等低分子多元醇,也包括糊精、PVA、HPMC等高分子多元醇。
2.3磁性纳米粒的表征
水热反应的产物经洗涤后直接用乙醇超声混悬,滴于铜网上(扫描电镜直接滴至铝台上)自然晾干进行电子显微镜观测。但对于磁性纳米粒的母核,考虑到粒子表面的疏水性容易引起絮凝团聚,所以其制样方法较为特殊,即将3.1制得的磁性纳米粒母核用异丙醇洗涤2次,再加入1.5%(v/v)油酸的石油醚溶液100 ml,超声1h,得到油酸分散的磁性母核纳米混悬液。在其中加入等量无水乙醇,搅拌均匀后离心,弃去上层液体(目的是除去多余油酸),加入适量石油醚使其分散。将分散后的磁性纳米粒母核滴到铜网上自然晾干进行电子显微镜观测。磁性纳米粒子的红外光谱用压片法测定,将真空干燥后的磁性纳米粒子与20倍量的KBr共同研磨均匀,压片后测定,纯KBr压片作为背景扣除。称取约50 mg真空干燥后的磁性纳米粒子,用四氟乙烯带包裹,放于震动样品磁强计中,在室温下测定其磁滞回线,镍标样为仪器自带。从磁滞回线中可计算样品饱和磁化强度和矫顽力。
3 结果与讨论
3.1磁性纳米粒在纯水中的熟化过程
方法3.1是制备Fe3O4纳米粒的经典方法,产物一般呈黑色,有明显的磁响应性。水热反应之前,磁性纳米粒母核的形貌如图1所示。未用油酸分散之前,磁性纳米粒子母核呈几百纳米的不规则团块状(图1a),这些是Fe3O4纳米粒子为了降低其过高的比表面能,在范德华力的作用下自发团聚产生的二级粒子;为了观测一级粒子的真实形貌,我们用油酸来分散并稳定Fe3O4粒子(图1b),可以看到,作为母核的Fe3O4一级粒子约3~10 nm大小,且形状不规则。
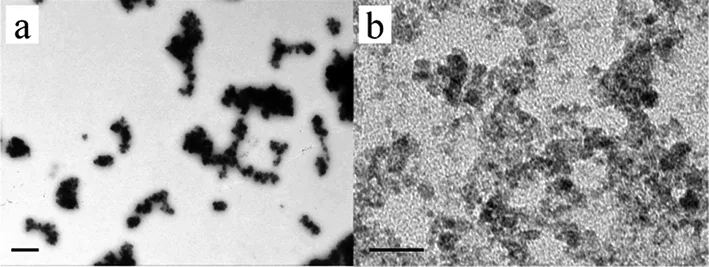
图1 磁性纳米粒子母核(a,标尺为300 nm)及其用油酸分散后(b,标尺为20 nm)在透射电子显微镜下的形貌
将此种粒子作为母核,在纯水中进行水热反应,最终得到红色沉淀,且磁响应性完全消失,说明产物在水热反应过程中转变为α-Fe2O3。我们用扫描电子显微镜记录了水热反应过程中粒子形貌的变化,结果显示,水热反应12 h后,产物中已经出现了大量直径接近1μm的多面体结晶,但这些结晶表面仍覆盖有大量纳米晶(图2a),而反应24 h后,纳米晶已经基本消失,主要为微米级的大结晶(图2b)。这一变化过程与结晶陈化(奥斯瓦尔德熟化,即小晶粒溶解消失,大晶粒逐渐长大的过程)的过程相吻合。因此我们推断,Fe3O4纳米粒子逐渐溶解并且在高温高压下转化更稳定的α-Fe2O3晶体并逐渐长大,24 h可基本完成结晶熟化过程。

图2 磁性纳米粒子母核在纯水中水热反应12h(a)和24h(b)后的扫描电镜图。标尺为1μm
3.2多元醇种类对产物形貌的影响
以纯水作为水热反应的介质显然不能阻止Fe3O4纳米粒子转化为α-Fe2O3,因此产物不具有磁性。要通过水热熟化制备结晶性较好的磁性纳米粒子,需要阻止氧化并且抑制结晶陈化。以2%(w/w)的丙三醇(a)、赤藓醇(b)、木糖醇(c)和甘露醇(d)水溶液作为水热反应介质再次进行实验发现,三元醇(丙三醇)和四元醇(赤藓醇)所得产物为红色且无磁响应性;而五元醇(木糖醇)和六元醇(甘露醇)产物为黑色,具有显著的磁响应性。这说明多元醇阻止Fe3O4氧化的作用与醇羟基数量呈正相关。由产物的透射电镜图可见,三元醇和四元醇(图3a,b)并未有效阻止晶体的长大,而五元醇和六元醇所得产物均为粒径20 nm左右的多面体结晶(图3c,d),原因是醇羟基在纳米粒子表面的吸附常数随醇羟基数量呈指数型增加。水热反应后,纳米粒子的粒径均一且结晶程度有了显著提高,预示着磁性纳米粒子的饱和磁化强度也可能有所提高。

图3 用2%(w/w)丙三醇(a)、赤藓醇(b)、木糖醇(c)和甘露醇(d)水溶液进行水热反应后的粒子形貌
为了进一步验证醇羟基数量对水热反应的影响,我们选择了一些含有大量羟基的聚合物分子来进行实验,包括糊精、HPMC、PVA05-88和PVA17-88来进行水热反应,其产物均为黑色且具有明显的磁性,但产物粒径分布均比甘露醇和木糖醇更宽(图4)。

图4 用2%(w/w)糊精(a)、HPMC(b)、PVA05-88(c)和PVA17-88(d)水溶液进行水热反应后的粒子形貌
3.3甘露醇浓度对产物形貌的影响
对比以上结果,甘露醇作为稳定剂经过水热合成所制得的磁性纳米粒子粒径较为均匀,且在20 nm左右。甘露醇的浓度在0.4%至8%(w/v)变化时,产物的形貌变化并不显著(图5)。

图5 用0.4%(a)和8%(b)(w/v)浓度的甘露醇水溶液进行水热反应之后所得的磁性纳米粒子形貌图
3.4甘露醇作用下水热反应产物的红外光谱及饱和磁化强度表征
2%甘露醇中水热反应所得的磁性纳米粒子表现出超顺磁性(矫顽力为0),其饱和磁化强度可达56.5 emu/g。其红外光谱(6)为Fe3O4的特征峰,而1119和1053波数则是甘露醇的C-O伸缩振动峰,这进一步说明,虽然经过了洗涤,但甘露醇仍然紧密吸附于Fe3O4纳米粒子之上,有利于增加粒子的亲水性和降低表面张力,从而起到稳定作用。
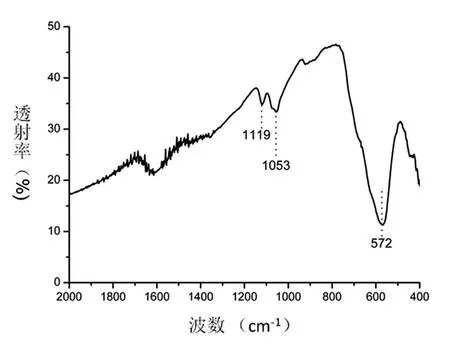
图6 在2%(w/v)甘露醇水溶液中进行水热熟化后磁性纳米粒子的红外光谱
综上,用共沉淀法制备磁性纳米粒子母核,然后在甘露醇水溶液中200℃水热反应24h,可制得20 nm左右粒径均匀、结晶性良好的磁性纳米粒子,该磁性纳米粒子具有超顺磁性,饱和磁化强度可达56.5 emu/g。甘露醇在反应过程中可抑制Fe3O4转化为Fe2O3,且能够提高磁性纳米粒子的亲水性。该方法不需有机试剂且所需甘露醇浓度极低(0.4%即可),对环境较为友好,可用于制备某些生物医用或吸附分离所需的磁性纳米粒子。
