基于解决学生困惑的推断题复习策略
2020-06-19康宏
康宏
摘 要:中考化学试卷中的推断题是学生失分较多的题型,因此汇总并分析了近十年的河北省中考化学试卷中的推断题,以期使大家更加明确考查内容、方向和意图,并能针对学生的困惑,合理选择教学策略以帮助学生走出困境,由此使不同层次学生的分析推理能力得到发展,化学学科核心素养的水平得到提升。
关键词:中考化学;推断分析;教学策略
中图分类号:G633.8 文献标识码:A 文章编号:1009-010X(2020)11-0055-05
一、厘清河北省中考化学推断题的高频考点,找准复习方向
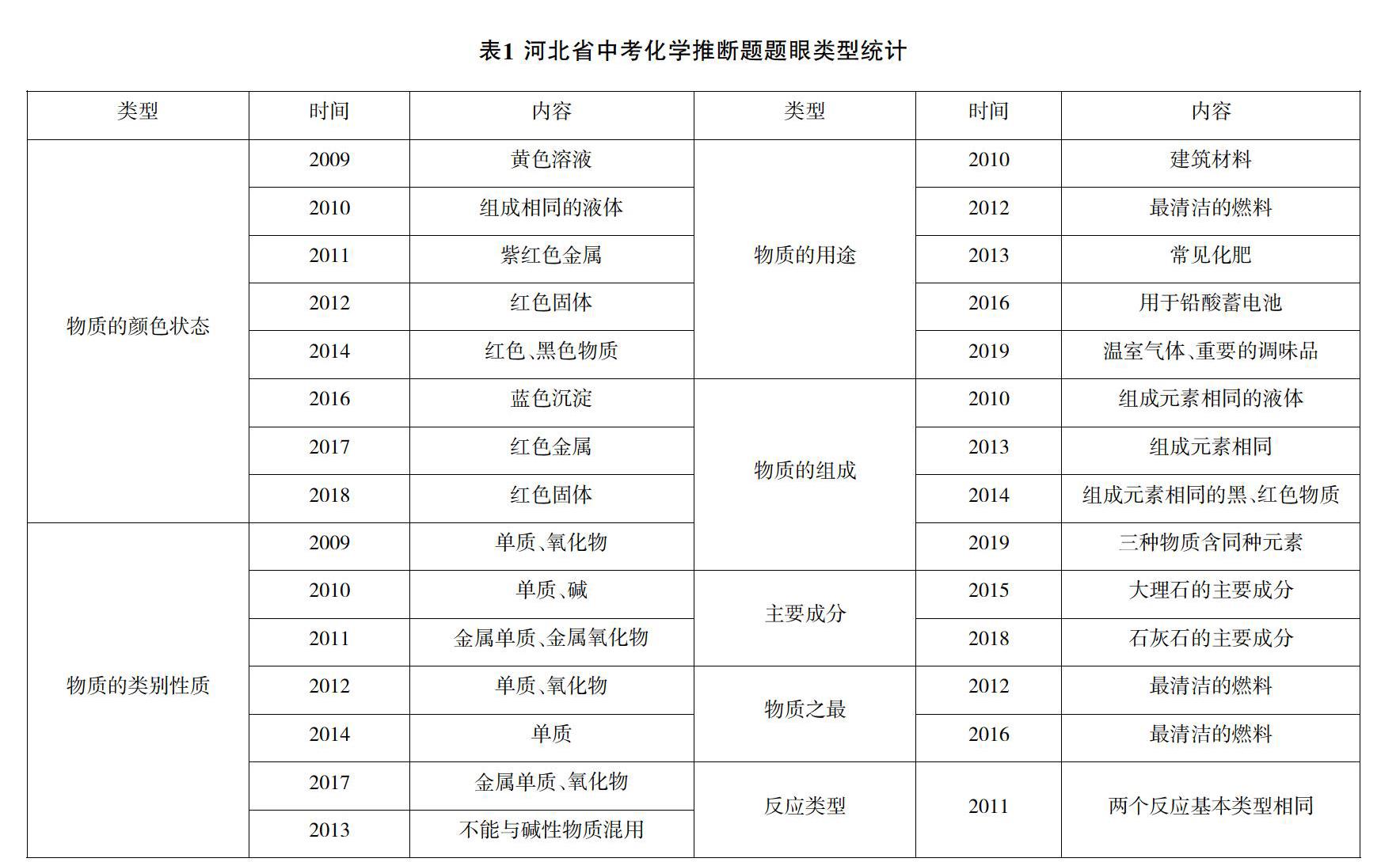
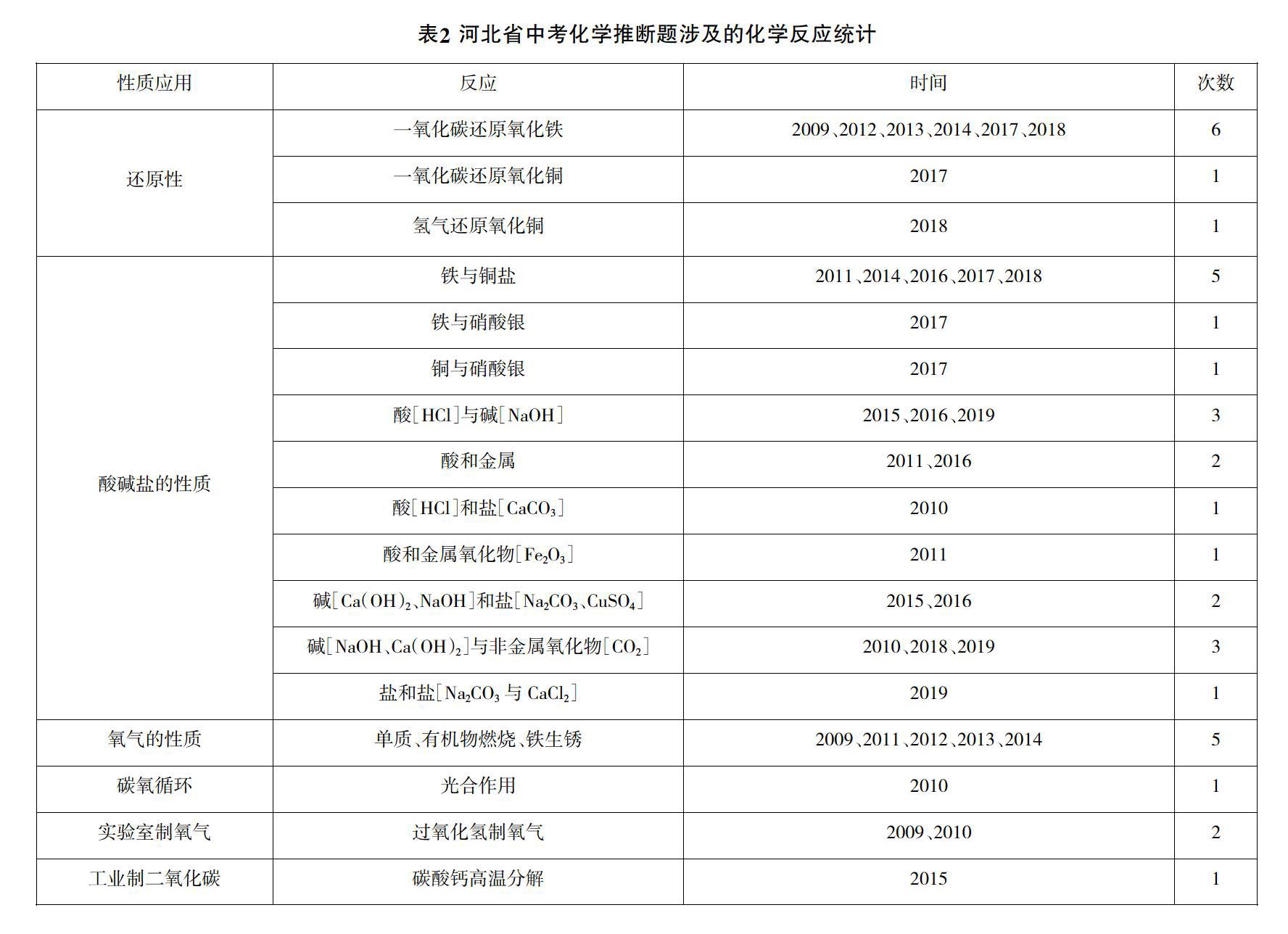
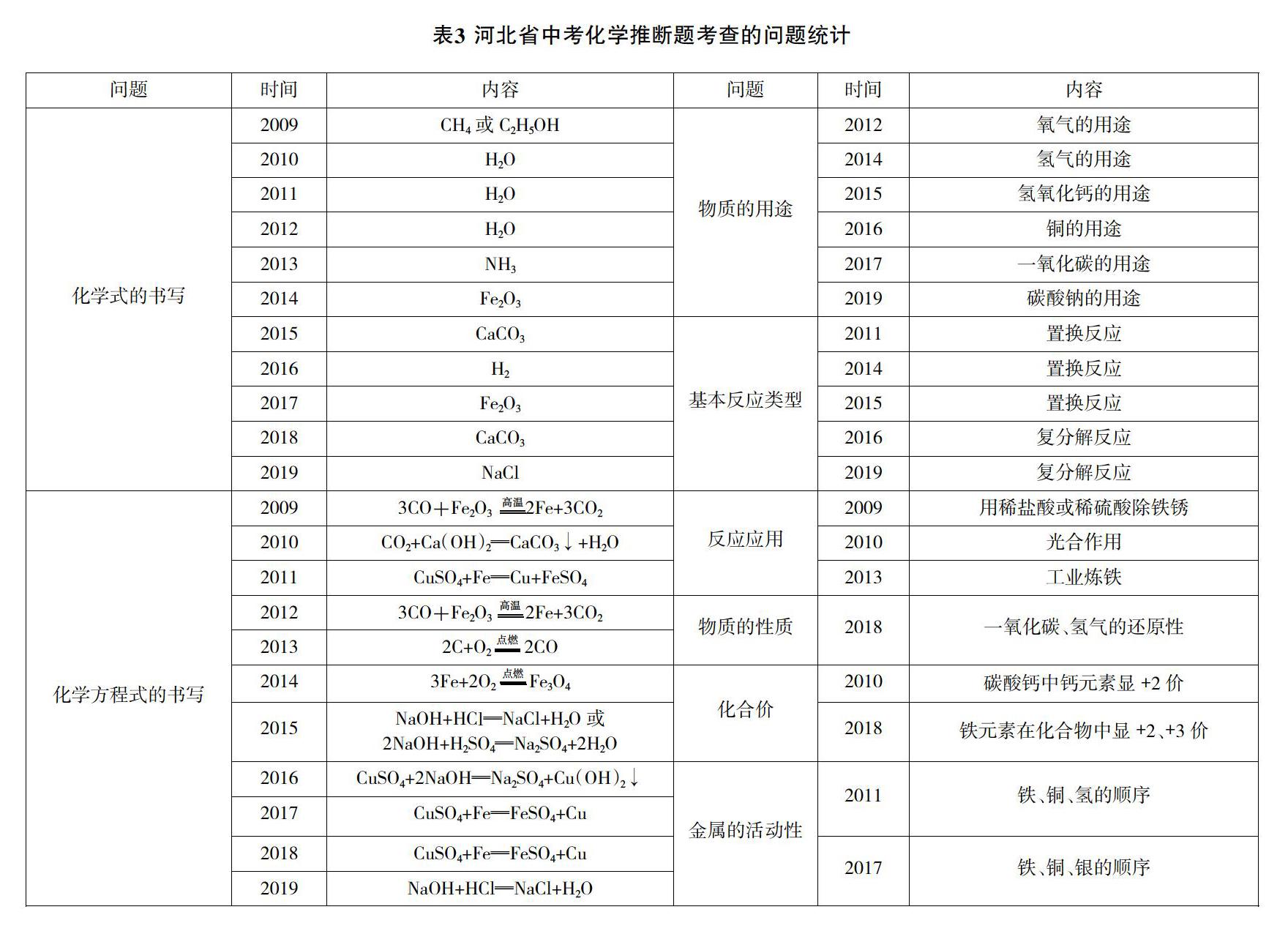
推断题是各地中考化学试卷中的常见题型,也是河北省自2000年以来的固定题目。此类题目具有知识覆盖面广、条件隐含、关系复杂、思维容量大、考点涉及范围广、形式新颖灵活、难度较高等特点。笔者对2009~2019年河北省中考化学试卷中的推断题从题眼类型(表1)、涉及的化学反应(表2)、考查的问题(表3)三个方面进行了汇总分析。
由表中内容可知,推断题涉及“身边的化学物质”“物质构成的奥秘”“物质的化学变化”三个一级主题中的内容;考查的问题涉及化学式、化合价、化学方程式、基本反应类型、物质的性质、物质的用途、金属的活动性顺序等核心知识。其中高頻出现的化学反应有:一氧化碳作还原剂,还原氧化铁或氧化铜的反应;表现氧气助燃性的反应;金属与盐溶液的反应,如铁与硫酸铜溶液的反应;以及酸碱盐之间的复分解反应等。
这类题目考查了学生的阅读能力(包括读文字、读框图)、分析能力、推理能力、应用能力等;锻炼了学生的求异思维、发散思维、抽象思维;还督促学生夯实元素与化合物的知识以构建知识网,找到知识间的联系,由此提高综合运用知识的能力。
二、针对学生的问题,合理选择教学策略
推断题作为中考的必考题型,知识关联性强,要想快速、准确地解答此类试题,考生不仅要对初中化学的核心知识准确记忆和理解,还要能针对不同情境的问题进行合理地分析、归纳、推理。这就导致很多学生在面对此类题目时,底气不足,畏难情绪逐渐滋生。即有的学生干脆放弃,他们说“看不懂图,理不清反应物与生成物的关系”;有的学生说“感觉自己的知识储备不够,很难对号入座,没方向,盲目试,撞大运”;也有学生说“如果题干给的信息充分,感觉还好些,有点儿头绪。如果题干给的信息少,就会乱了方寸,无从下手”。以上是三类学生对推断题的感觉,那么如何才能将这三类学生逐步带出困境呢?
第一类是阅读能力较弱的学生,他们很容易被多种多样的题干表述迷惑,所以要先引导他们学会阅读然后才能正确解答该题。为此可以采用分步阅读法帮他们拨开些许题干的“迷雾”:第一步“读选写”,即边读边将有效信息标注在框图中的相应物质旁;第二步“顺连线”,即读箭头、找关系,顺着线索确定框图中已给出的反应物、生成物,并用相应的字母列出关系式。
过了阅读关,他们就晋级为第二类学生——知识储备不够,解题全靠运气。知识的积累不是一朝一夕的,需要教师与学生共同努力,采用课上课下相结合,线上线下相结合,教师引导方向,学生个人总结,组内交流补充,组间合作扩充的方式,将解决推断题的题眼汇总完善才能完成。为巩固成果,教师可利用课堂小测、组内考查、组间比拼等形式对学生进行考查,以便学生及时查漏补缺。
当学生熟练掌握以上内容后,再遇到信息量充足的推断题,就不再畏惧了。但由于学生对知识间的联系还不熟悉,所以当题干信息量少、需要对框图进行逻辑推理时,他们就会感到迷茫,因此寻找物质间的转化关系并形成知识网就成为解困的关键。这项工作也不是一蹴而就的,需要由简入繁、循序渐进地推进。即首先让学生从已有的知识中找出符合要求的化学方程式并书写“一变二、一变三、二变一、二变二、二变三、两种物质间的相互转化、物质间的三角关系”等,同时在此过程中渗透分类的学科思想,并让学生学会利用某类物质的化学性质进行逻辑推理,进而得出结论。然后以水、二氧化碳等物质为核心,构建知识网,如此可让学生进一步熟悉已有知识,并将知识网络化。最后结合近十年河北省中考化学推断题中的高频反应,让学生找出反应之间的联系,然后自己构建物质转化关系框图,书写化学方程式,并尽量找出达成生成物目标的所有途径,如此可发展学生的求异思维、发散思维。
通过一系列的准备工作,学生逐步树立起信心,可以运用四步法则完成整体推断:
审题——看清题意找已知。
分析——分析已知找“题眼”。
结论——从“题眼”出发,通过正推法、逆推法、假设法得出结论。
验证——将答案代入框图进行检验。
三、部分成果展示
(一)基础知识归纳成果
1.物质的类别及组成
常用单质: 非金属单质:H2、O2、C等;金属单质:Fe、Cu等。
常用氧化物:组成元素相同的有CO和CO2、Fe2O3和Fe3O4等。其他有CuO、CaO等。
常用酸:HCl、H2SO4。
常用碱:Ca(OH)2、NaOH。
常用盐:CaCO3、Na2CO3、CuSO4、CuCl2、FeSO4、FeCl2、Fe2(SO4)3、AgNO3、NaHCO3、NH4HCO3等。
有机物:CH4、C2H5OH。
2.物质的颜色、状态、气味
气体:多数为无色无味。SO2、NH3、HCl气体有刺激性气味。
溶液:多数为无色。含Cu2+的盐溶液为蓝色(或蓝绿色);含Fe3+的盐溶液为黄色;含Fe2+的盐溶液为浅绿色。
固体:多数为白色。C、CuO、MnO2、Fe3O4、Fe等为黑色;Cu、Fe2O3、红磷为红色。Cu(OH)2为蓝色沉淀;Fe(OH)3为红褐色沉淀。
3.特征反应条件
“通电”——电解水。
“高温”——CaCO3分解;碳还原氧化铜;一氧化碳还原铁的氧化物。
“催化剂”——H2O2分解、KClO3分解(反应前后框图中都出现该物质)。
4.物质的用途
CO、H2、CH4——作燃料。
H2O——作溶剂。
NaCl——重要的调味品。
HCl、H2SO4——除铁锈。
CaO——食品干燥剂。
NaHCO3——作发酵粉。
Na2CO3——制玻璃、洗涤剂。
CaCO3——作建筑材料、补钙剂。
CO2——温室气体,光合作用的原料,可用于灭火、人工降雨、制汽水等。
5.物质的俗称或主要成分
Ca(OH)2——熟石灰、消石灰。
CaO——生石灰。
Na2CO3——纯碱、苏打。
NaOH——苛性钠、火碱、烧碱。
NaHCO3——小苏打。
C2H5OH——酒精。
NaCl——食盐的主要成分。
HCl——胃酸、洁厕灵的主要成分。
Fe2O3——铁锈、赤铁矿的主要成分。
CaCO3——石灰石、大理石、水垢等的主要成分。
Fe3O4——磁铁矿的主要成分。
CH4——天然气、沼气、可燃冰的主要成分。
6.物质及元素之最
H2——密度最小的气体、最清洁的燃料。
H2O——相对分子质量最小的氧化物、最常用的溶剂。
Fe——年产量最高的金属、应用最广泛的金属。
CH4——最简单的有机物。
Ca——人体中含量最多的金属元素。
O——地壳中含量最多的元素、地壳中含量最多的非金属元素。
Al——地壳中含量最多的金属元素。
C——组成物质最多的元素。
7.特殊的实验现象
硫在氧气中燃烧——明亮的蓝紫色火焰。
镁带燃烧——耀眼白光。
铁丝在氧气中燃烧——火星四射。
氧化铁被还原——红色固体变黑。
氧化铜被还原——黑色固体变红。
8.反应类型及特征
在未省略部分反应物或生成物的情况下:
题眼对于学生的重要性毋庸置疑,用框图归纳反应类型,不仅能讓学生巩固化学方程式的书写,而且还能将常规书写化学方程式的形式转换成框图的形式,如此可提高学生的读图能力,进而帮助他们更好地理解题意。
(二)建立物质转化关系的部分成果
1.引导学生寻找物质间的相互转化关系
O2?圮H2O O2?圮CO2
CO2?圮CaCO3 Na2CO3?圮NaOH
这项任务,可以让学生将完整的化学方程式逐渐变成省略部分反应物或生成物的转化关系式,如此能帮助学生熟练根据某种反应物找出生成物,或根据某种生成物找出反应物。
2.引导学生寻找物质间的三角转化关系
三角转化关系比相互转化关系稍难,但可以相互转化关系为基础理解,如此可为学生构建自己的知识网奠定基础。
3.引导学生构建以氧气、水等物质为核心的知识网
引导学生有目的地建构知识网,寻找知识间的联系,同时利用分类的思想整理知识,如此可提高学生的站位,拓宽学生的思路,同时这也有利于学生寻找开放性答案。
4.学生构建的常见物质转化关系图
以二氧化碳为核心,充分体现了二氧化碳与碱的反应。
以含碳元素的物质为主线,找出部分常见单质、氧化物、酸、碱、盐之间的联系并构建知识网,如此可体现出这几类物质的化学性质。学生在构建知识网的过程中,需积极寻找结合点,如此可为学生进一步理解、巩固各类物质的化学性质奠定基础(见下图)。
学生能顺利完成框图推断题的作答,并不意味着学生这道题能拿到满分。因为除了严密、正确的逻辑推理外,学生还需在试卷上正确呈现出自己的推断结论才行。所以解题技巧固然重要,但夯实双基才是重中之重。
