扩散峰度成像技术在帕金森患者黑质纹状体区的临床价值
2020-06-17姚佳琪
姚佳琪,陆 鹏,姜 磊,刘 莹,王 红
新疆医科大学第二临床医学院影像中心,新疆 乌鲁木齐 830028
帕金森病(PD)是一种常见于中老年人的缓慢进展的中枢神经系统退化性疾病,其典型特征是静息性震颤,初始运动缓慢,僵硬和全身姿势不稳[1]。过去MRI可以评估中枢系统的早期发育、衰老及病理阶段,并监测评估治疗期间和治疗后的变化,成为神经科学研究的一个重要方法及临床运用[2]。扩散峰度成像(DKI)是一种是一种对脑组织无创性的检查方法,国外有研究通过脑内微观结构对比了弥散张量成像(DTI)与DKI两种技术,认为在研究神经退行性疾病时灰质核团微观结构的复杂改变DKI比DTI更为敏感,DKI的重要性来自于对各向异性和各向同性扩散的检测能力,DKI或许能够成为许多神经退行性疾病早期敏感的生物标志物,该技术为早期诊断提供了一定帮助[3]。也有研究认为与正常对照组对比,PD患者基底节各主要深部核团(壳核、苍白球、尾状核)以及黑质中MK值明显增高。因此,DKI在检测神经元组织病理变化的敏感性上可能优于传统的DTI。然而,DKI参数的变化由于其特异性差而难以解释,且模型比DTI更复杂,故获取时间比DTI长[4]。
有学者将DTI应用于PD患者并对以往相关研究进行了meta分析,得出目前尚不能认为DTI是PD诊断的有效工具的结论[5]。而DKI的出现,弥补了DTI的部分不足,MK值相比各向异性分数(FA)值对于各向同性组织病理改变的检测更有价值,这是因为MK值不依赖于组织结构的空间方向。DKI技术对PD的诊断要比DTI更加敏感。国外学者对PD患者脑组织内某些感兴趣区进行了多模态的探究,包括功能性MRI、磁敏感加权成像及磁共振波谱单体素及多体素、DTI的发展等[6],并无专门探讨黑质纹状体纤维微观结构的异常是否与PD患者生理改变有关的研究;轴向峰度(AK)和径向峰度(RK)的结果可能为PD患者DKI改变的机制提供更多的信息,但现有研究未对DKI参数AK和RK数据进行评估。本研究旨在探讨黑质纹状体区纤维微观结构在DKI中的变化并分析其4个参数值,筛选出DKI参数中能够对早期神经退行性疾病有效的生物学指标,为临床及影像正确认识帕金森病而提供科学依据。
1 资料与方法
1.1 一般资料
选取我院2018年12月~2019年6月确诊的35名PD患者作为观察组,其中男18例,女17例,年龄68.17±8.21岁,病程6.8±4.2年。纳入标准:符合英国帕金森病协会脑库诊断标准,由2名经验丰富的神经内科医生临床诊断为原发性帕金森病;临床症状典型,疾病呈进行性发展;在本次检查前均未接受帕金森病手术治疗;能够配合并耐受头颅常规MR及DKI扫描;能够配合量表评估及检查:知情同意检查目的及过程。排除标准:有明显意识障碍或精神疾病不能配合检查的病人;有多系统萎缩、进行性核上性麻痹等帕金森叠加综合症患者;有幽闭恐惧症、心脏起搏器植入等MRI检查禁忌症的患者等。
同时选取20名性别、年龄匹配的健康志愿者作为对照组,其中男9例,女11例,年龄71.45±7.37岁。每个PD患者根据英国帕金森病协会脑库标准的Hoehn-Yahr量表进行评估,并使用帕金森病统一评分量表(UPDRS)予以分级。Hoehn-Yahr量表分为0~5级,分级越高,病情越严重,其中0~2级为早期患者,2.5~5级为进展期患者。UPDRS量表共分为4个部分,早期<30分,进展期≥30分。将35名PD患者按评分表分为早期组和进展期组,其中早期组13人(男8例,女5例),进展期组22人(男10例,女12例)。参与本研究的所有患者均以被告知检查目的并签署检查知情同意书并通过医院伦理委员会审查。
1.2 检查方法
扫描应用Philips Achieva TX 3.0 T磁共振扫描仪,采用32通道高分辨率头颅线圈。被检查者取仰卧位,以双侧下颌角为中心位置放置成像线圈,将激光定位十字线中心至于线圈中心处,双侧均过患者乳突位置,完成扫描区域定位。行头部常规MRI平扫、扩散加权成像(DWI)及DKI扫描。
常规MRI平扫:T1WI:TR 1960 ms,TE 20 ms,TI 750 ms;T2WI:TR 4200 ms,TE 100 ms;DWI选取b值0、1000 s/mm2,层厚6.5 mm,间隔1.5 mm。DKI扫描:选取3个b值(0、1000、2000 s/mm2),32个扩散方向扫描,层厚2.43 mm,间隔5 mm,TR 3000 ms,TE 90 ms,矩阵128×128,视野(FOV)200 mm×231 mm×119 mm,总扫描时间538s。
1.3 数据处理
得到的所有原始数据传入后处理工作台,将DKI序列的DICOM图像导IMAgenGINE磁共振弥散灌注处理软件对其进行后处理,处理后生成平均弥散分度(MK)图、部分FA图及AK、RK值图。
1.4 感兴趣区(ROI)分析
所有弥散参量图由两名对被检者病史不知情的神经放射学专家评估,均在b=0时的图像作为参照,完成ROI的手动勾画。ROI要小于测量核团,并避开脑脊液、血管等伪影干扰测量值,同等大小ROI测量双侧部位参数值。双侧黑质体素均为188,双侧黑质面积均为50 mm2,在同层面同一个ROI区域内分别测量3次,取其平均值。
1.5 统计学分析
应用SPSS22.0对所有数据资料进行统计学分析,计量资料以均数±标准差表示,计数资料组间比较采用卡方检验,计量资料采用t检验;观察组和对照组的所选感兴趣区MK、FA、AK、RK的均值采用两独立样本t检验进行组间比较,若数据不符合正态分布且方差齐性则采用秩和检验;早期PD组和进展期PD组双侧黑质MK及FA值与病程、临床量表的相关性分析根据数据分布类型选择Spearman或Pearson分析法。以P<0.05为差异有统计学意义。
2 结果
2.1 双侧黑质参数的比较
观察组双侧黑质MK较对照组增高,差异具有统计学意义(P<0.05,表1);FA值较对照组减小,差异具有统计学意义(P<0.05),AK、RK值差异无统计学意义(P>0.05)。
2.2 双侧黑质、MK、FA值与病程及临床量表的相关性
双侧黑质的MK、FA参数值与临床病程进展之间均无相关性(P>0.05,表2)。
2.3 后处理图像
双侧黑质感兴趣区(图1A)、双侧黑质MK图(图1B)、双侧黑质FA图(图1C)、双侧黑质RK图(图1D)、双侧黑质AK图(图1E)。
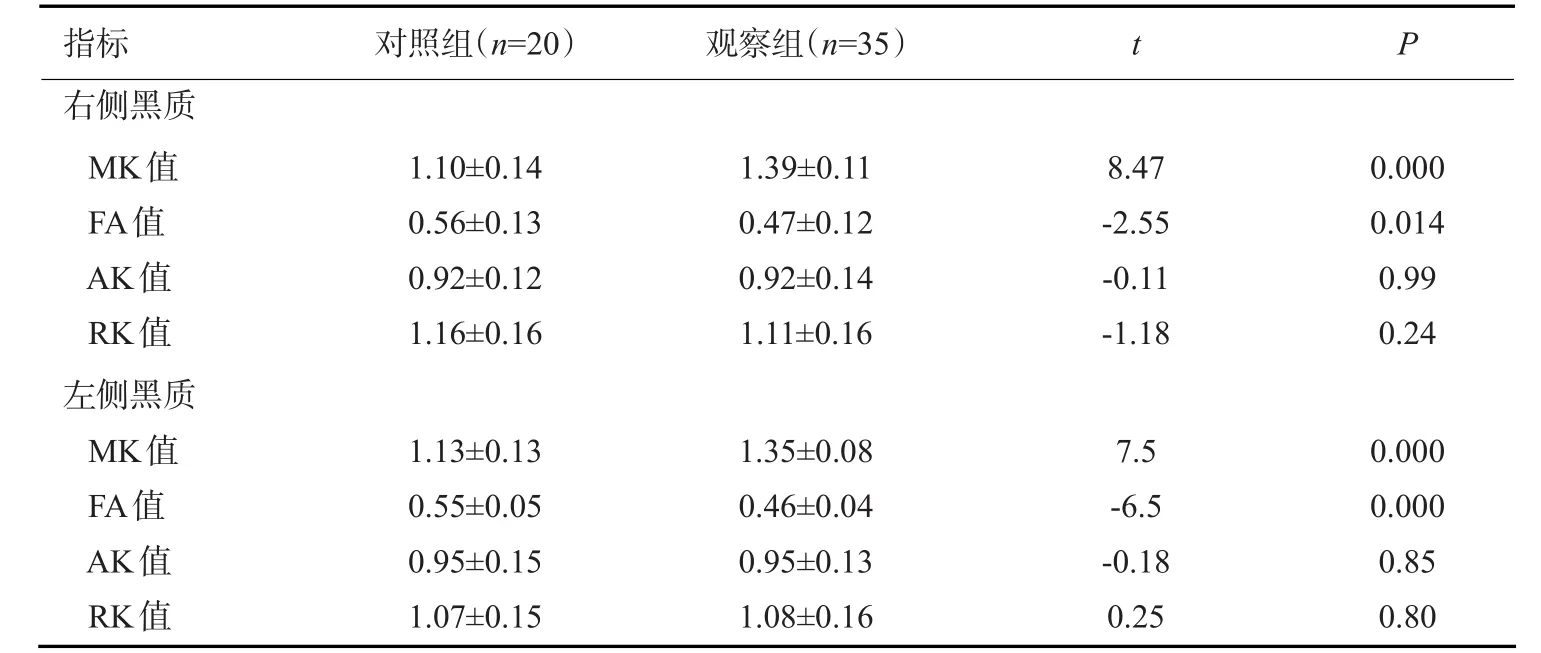
表1 两组患者双侧黑质各参数的比较(Mean±SD)Tab.1 Comparison of parameters of bilateral substantia nigra in patients with two groups
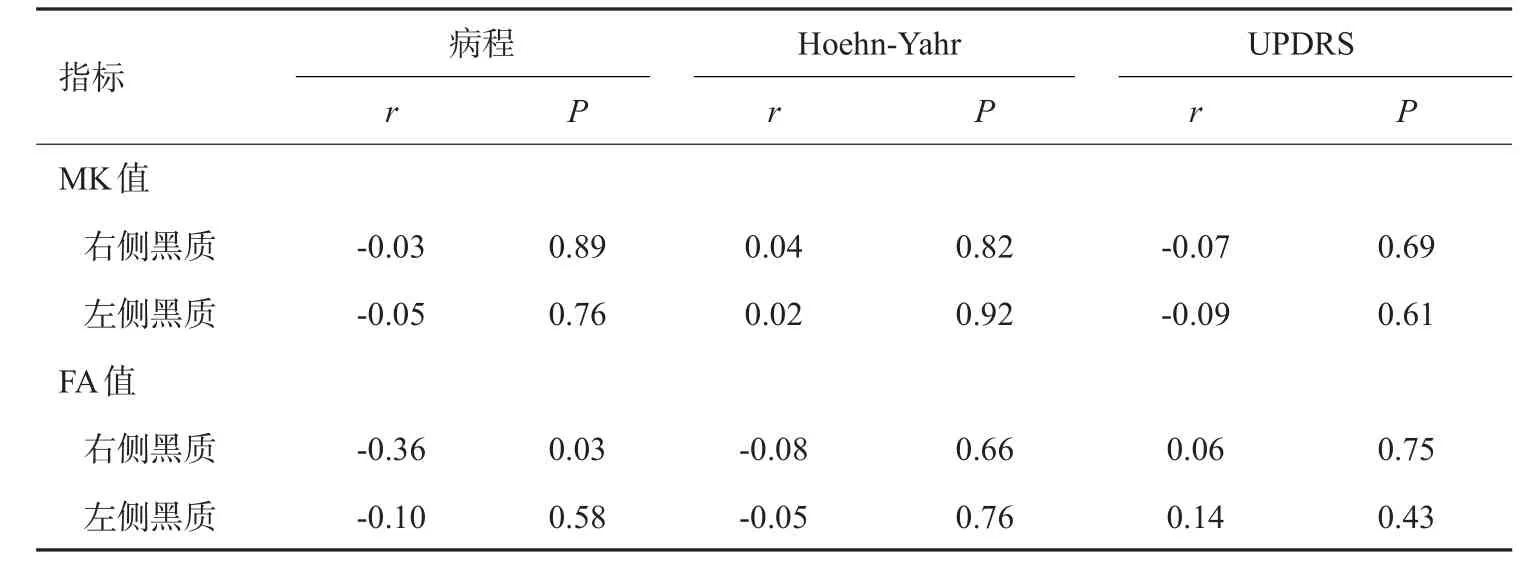
表2 双侧黑质区MK、FA值与病程及临床量表的相关性Tab.2 Correlation analysis results of bilateral substantia nigra MK values with disease course and clinical scale
3 讨论
DKI的原理是在组织结构中检测非正态分布水分子扩散,是一种对脑组织无创性的检查方法,在DTI成像的基础上增加了一个四阶张量修正项来补充,不仅提供了扩散张量度量(AD、RD、MD和FA),还提供了峰度度量,包括AK、RK和MK[7]。MK值是最常用的参数之一,广泛应用于临床及研究中,可以绘述脑内微观结构的变换,它的大小随着感兴趣区内脑组织结构的变化而变化。DKI还扩展了传统的DTI测量方法,不仅在白质(各向异性组织),而且在灰质(各向同性组织)中也可以检测微结构的变化,因为它与结构的空间方向无关,扩散峰度越高,水分子扩散偏离高斯分布越大,说明扩散环境更加受限[8-9]。
PD的典型病理变化是路易体形成和多巴胺能神经病变,后者通常发生在疾病的晚期,此时神经变性率可高达70%,这种变化是由特征性路易小体和神经鞘内含物的积累和扩散所引起的,其中神经鞘内含物是由复杂纤维组成[10]。有研究也报道了PD患者SN中结合蛋白、铁蛋白的显著增加以及Fe2+/Fe3+比率向Fe3+的转变[11-12]。Prakash等[13]认为Fe3+在帕金森病患者的SN中诱导膜脂质过氧化作用,随着这些研究的出现,研究人员开始质疑过量铁与帕金森病DA能神经变性的可能有紧密联系,然而,铁沉积是否代表帕金森病的主要事件仍有争议。
SN是调节运动的重要中枢,PD病理多由SN纹状体系统DA缺失所引起的,因此将其作为ROI。有研究评估了SN中的参数值,并比较了MK/FA在该区域的敏感性,发现MK显著增加,FA显著减少[14],其结论与现有研究一致。本研究中,病例组双侧SN中MK值也较对照组明显增加,MK值大小取决于ROI内组织结构的复杂程度,结构越复杂,非正态分布水分子扩散受限越显著,MK值也越大,每个体素内的正常扩散跟水扩散的因素密切相关,它不是一个各向异性的环境,不像FA值只考虑各向异性环境中扩散的程度,这可能是由不同的因素引起的,例如病理性的蛋白质积累或铁沉积,而峰度的降低可能是神经元丢失的迹象。FA值代表脑组织内纤维素的状态,有文献已经提出,PD患者会发生DA神经元的丢失、髓鞘的完整性受损,因此SN、苍白球及丘脑的FA值与正常老年人相比较,显示FA值均减低[15]。本研究中所选ROI的FA值也有所减低,表明纤维素受损可能。AK值是指沿着扩散轴向的峰度值,因为水分子扩散不受限,所以AK值比较小。RK值主要指扩散正交方向上的峰度平均值,与非正态分布水分子扩散受限呈正相关,值减小则水分子扩散受限越弱,因在脑白质中,细胞膜和髓鞘的限制,水分子扩散受限,偏离了高斯分布,则RK值显著增加[16],但是本次研究中与对照组相比AK及RK值未见明显统计学差异,可能是样本量过少的缘故。研究进一步提供证据表明,在帕金森病的晚期或严重阶段,高水平的铁可能表明并有助于诱发帕金森病病理的加重,而低水平的铁可能是疾病早期的信号,患侧SN中的铁含量显著增加,并且铁的增加与DA能细胞死亡的程度显著相关,表明SN纹状体系统的损伤可以单独诱导SN神经元中的铁积聚[17]。Kosta等[18]认为增加的铁可能有助于SN退化的进展,与对照组相比,PD组黑质、红核、尾状核头及壳核磁化率值均减低,说明PD患者存在铁沉积过多的现象,但各核团磁化率值与对应的PD患者临床严重程度均无明显相关性,说明铁沉积的异常并不能完全反映PD患者各核团微观结构的进展改变,铁的异常沉积只是其中的一个方向,与神经元丢失、神经细胞的活化及纤维素的破坏有关。
本研究将PD病人按Hoehn-Yahr量表评估,分级越高,病程越重,0~2级为PD早期,2.5~5级为晚期。有研究发现与正常对照组相比,早期PD病人、晚期PD病人双侧SN中MK值可见显著下降,而且相对于早期PD病人,进展期PD病人左侧SN中MK值亦见显著下降,差别均有统计学意义。相关性分析发现SN中MK值与UPDRS评分亦呈显著正相关[19],有学者通过对早期PD患者和对照组脑内核团的研究,发现SN及核团中MK值与帕金森评分表呈显著正相关[20]。但也存在相反观点,如Focke等[21]认为SN中弥散各向异性值改变并不显著。有研究纳入了在MDS-UPDRS第3部分和Hoehn及Yahr评分中无显著差异的帕金森病患者[22],考虑运动症状的存在可能干扰了评估非运动异常的能力,本研究所选ROI的4个参数值也均与临床病程无显著相关性,此差异在本研究DKI参数中差异无统计学意义,这与现有研究结果相似,可能的因素是PD患者在临床中有偏身侧差异,与误差、样本量及数据统计等因素有关,也可能与评估分级存在一定的主观性有关,可能与评分时病人未能清晰表达理解问卷中部分问题,造成评估时的误差,还需对PD分组进行更细致的分析。DKI峰度值对灰质及白质中的微观结构较为敏感,与以往研究不同之处在于本次研究的MK及FA值能提示PD患者黑质纹状体区细小结构的改变,如铁的过度沉积或细胞变性,能够及时发现PD患者病理生理的改变,能够为临床提供生物学指标。
本研究的局限性在于,帕金森病SN神经元丢失部位主要位于SN致密部,已有部分研究将SN细化为致密带和网状带,解剖分为嘴部、中间部和尾部进行分析,其主要原因可能是PD患者SN中铁的异常沉积不均匀所导致。但SN本身在脑内是一个较小的核团,在DKI的后处理图中只能认出其外观,无法区分其致密部与网状部结构,应联合其他磁共振成像技术去评估铁水平作为监测帕金森病疾病进展的生物标志物[16,23]。随着DKI技术的发展,越来越多的应用于临床各向研究中,选取最佳参数及感兴趣区,希望今后可以结合其他MR技术细致的区分SN致密部与网状部[24],进一步探索SN的病理生理改变,为临床提供更有价值的帮助,并同时根据临床表现、病程的进展对病人的进行详细分配,综合分析,为临床的诊断、治疗提供有利的帮助。
