引起耳道感染的产生物膜铜绿假单胞菌的流行病学分析*
2020-06-15叶丽艳宋林键杨继勇王成彬罗燕萍
叶丽艳,王 玥,宋林键,赵 强,杨继勇,王成彬,罗燕萍△
(1.解放军总医院第一医学中心医学检验中心,北京 100853;2.重庆医科大学检验医学院,重庆 401331)
耳道感染是耳鼻喉头颈外科中一类常见的疾病,病原菌(如真菌或细菌等)引起的感染是其发生和发展的主要因素。耳道感染主要包括外耳道炎和中耳炎,其中中耳炎是临床上最常见的、影响人群量最大且常造成反复感染的感染性疾病,久治不愈可影响中耳功能与结构,严重者可导致颅内并发症的发生[1]。研究显示,在引起耳道感染的需氧菌中位于首位的革兰阴性杆菌为铜绿假单胞菌(Pae),由于抗菌药物滥用现象极为普遍,使得Pae的种类与耐药剂量不断变化出现强耐药性[2-5]。目前研究可知Pae耐药机制主要为产生抗菌药物灭活或修饰酶、改变抗菌药物作用靶位、膜通透性障碍、主动外排系统及形成生物膜[6]。其中形成生物膜导致的耐药较为普遍[7],细菌生物膜给细菌的生存提供了很强的保护屏障,绝大多数的细菌存在主要生物膜,以此来抵御抗菌药物的作用[8]。有报道细菌生物膜与慢性感染关系密切[9],而在常见的革兰阴性菌中,Pae是细菌中极易形成生物膜的一个菌种[7],因此,研究耳道感染中Pae的生物膜形成对临床上常见的耳道感染疾病的治疗有很重要的意义。
1 材料与方法
1.1标本来源 解放军总医院2013年5月至2017年12月耳鼻喉外科耳道感染患者标本中分离的Pae 106株,同一患者同一标本类型来源选取初次分离株。质控菌株为Pae ATCC27853(美国模式培养物集存库),接种菌种到营养肉汤中进行活化,37 ℃培养18~24 h,备用。
1.2仪器与试剂 实验仪器:Vitek MS质谱仪(生物梅里埃公司,法国),Vitek 2 Compact全自动细菌鉴定药敏仪(生物梅里埃公司,法国),酶标仪(SM-Mk3),微量移液器,生物安全柜,96孔平底组织培养板,电子分析天平。实验试剂:胰蛋白胨大豆肉汤(TSB),磷酸盐缓冲液(PBS),结晶紫(2.00%),乙醇(95.00%),无菌生理盐水,葡萄糖分析纯粉末,壳聚糖季铵盐粉末。
1.3方法
1.3.1分离培养、鉴定、药敏 临床样本按《全国临床检验操作规程》进行分离培养,采用法国生物梅里埃公司Vitek MS质谱仪进行菌种鉴定,采用Vitek 2 Compact GN09药敏卡进行药敏试验。
1.3.2生物膜形成能力测定 参照文献[10],利用96孔平底组织培养板中Pae所形成的生物膜经结晶紫染色后,使用酶标仪检测570 nm下的吸光度(A)值(每株细菌包括3个平行孔,每个96孔平底组织培养板包括3个空白对照),并记录。同样参照文献所述方法根据A值对每株Pae生物膜形成能力进行等级划分。Ac=3×A空白对照标准差+A空白对照平均值。
在96孔平底组织培养板上构建Pae生物膜,并通过结晶紫染色、酶标仪测定对生物膜形成能力进行定量与定性分析,并且分析生物膜形成能力与Pae耐药性之间的关系。
1.3.3生物膜形成影响因素 随后选取11.10 mmol/L葡萄糖和15.00 μg/mL壳聚糖季铵盐加入到生物膜形成因素研究中,探究这两种因素是否与生物膜形成有关。
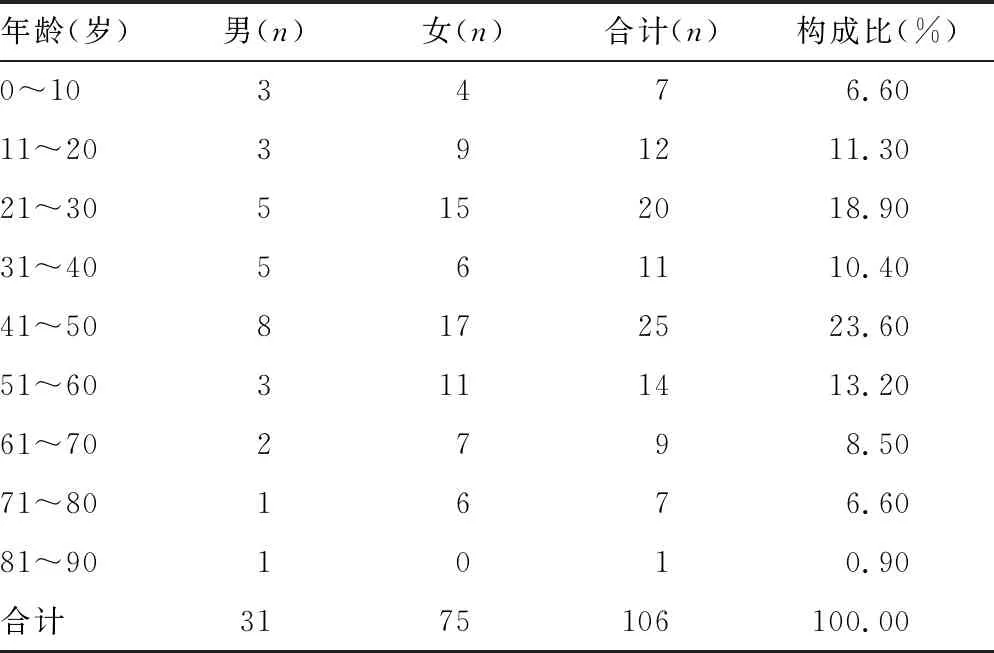
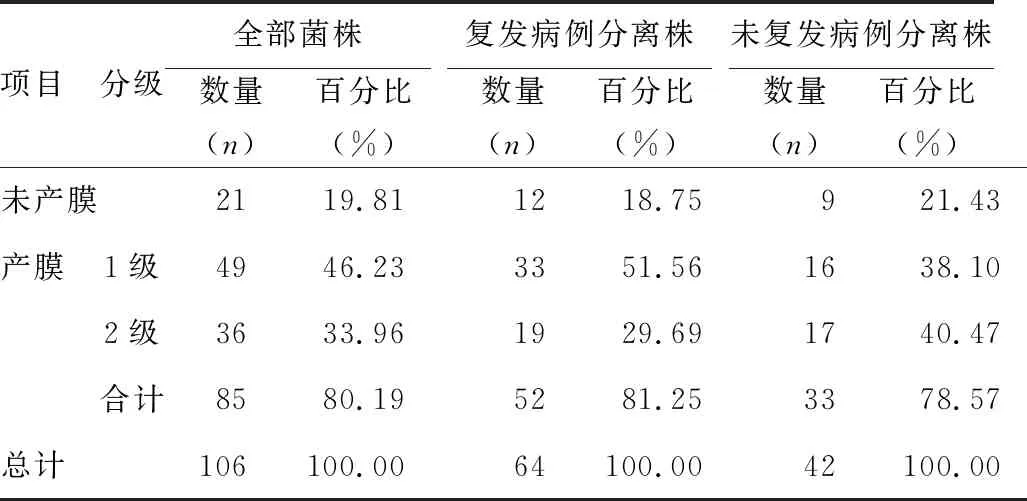
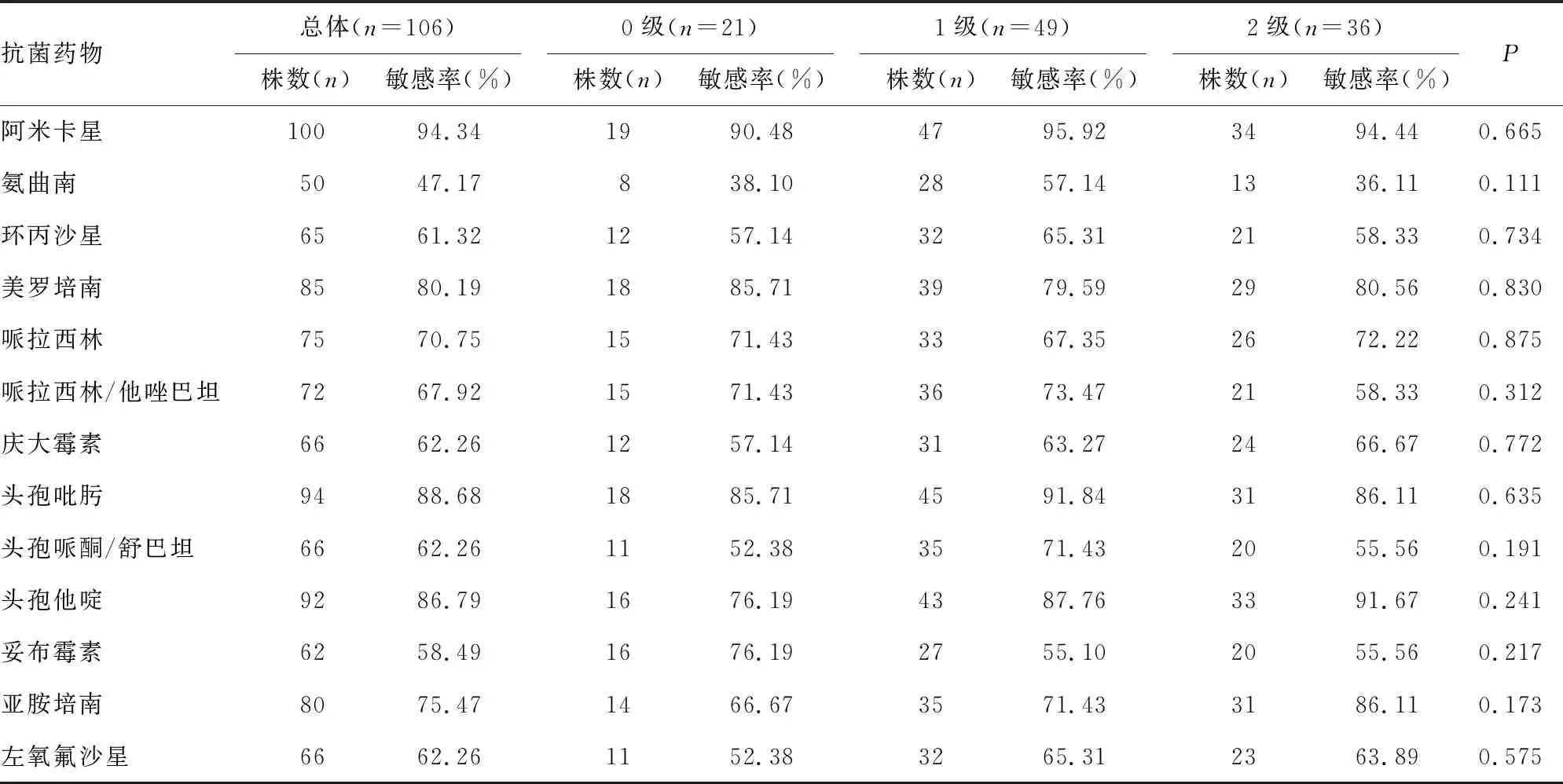
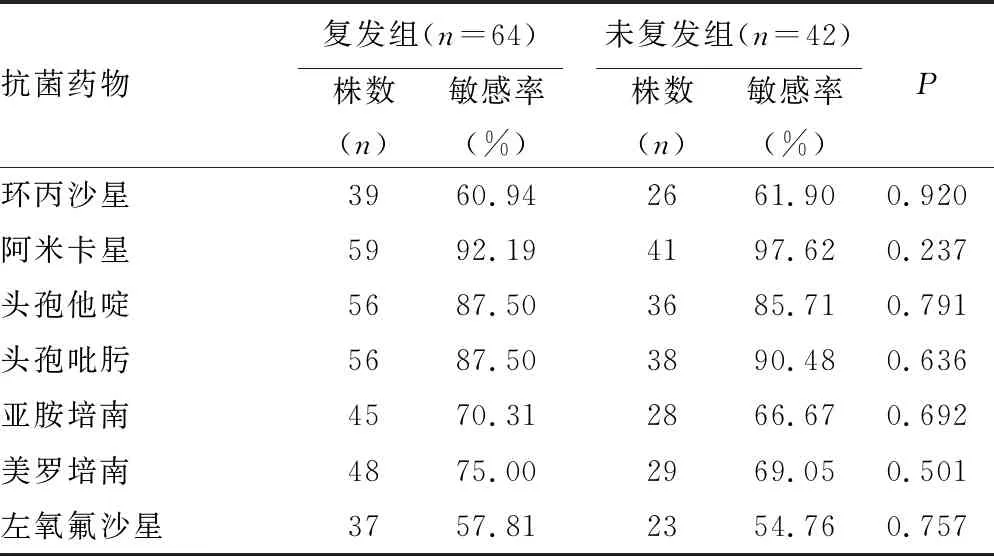
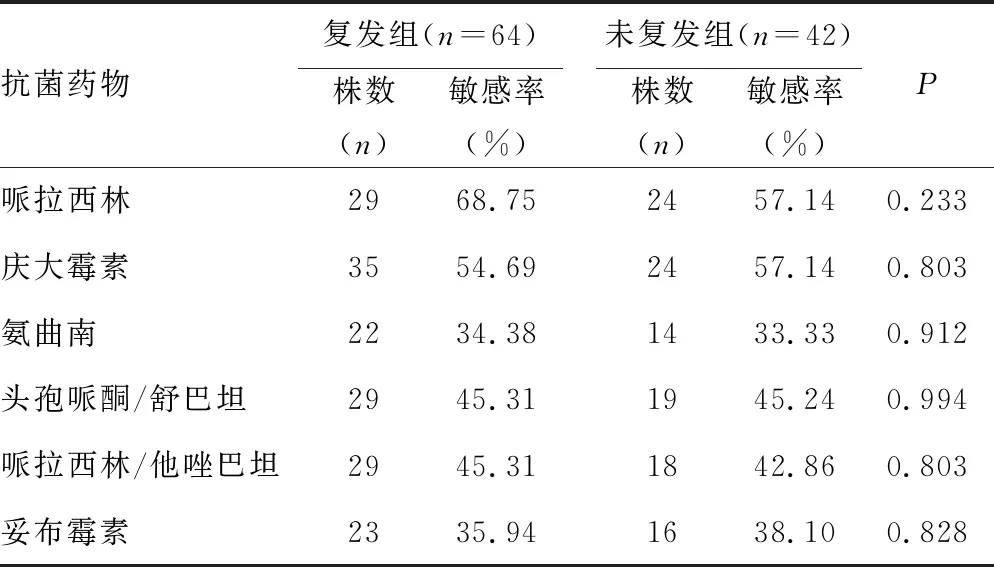
1.3.4生物膜形成能力的分级判定 生物膜形成情况按照参考文献[10]方法进行分级判定:0级(A≤Ac),无成膜能力;1级(Ac 1.4统计学处理 采用MiniTab17.0软件进行统计分析,采用χ2检验,细菌耐药数据分析应用Whonet 5.6软件,按照美国临床实验室标准化协会(CLSI)2016-M100的折点标准进行分析。以P<0.05为差异有统计学意义。 2.1病例资料分析 2.1.1性别、年龄分布 在106例由Pae引起的耳道感染病例中,男31例,女75例。年龄分布以41~50岁为主,占23.60%,见表1。 表1 病例的性别、年龄分布 2.1.2耳道感染病例复发情况 在106例由Pae引起的耳道感染病例中,复发患者64例,未复发患者42例,复发率为60.38%。 2.2生物膜形成情况 在106株Pae中,形成生物膜的菌株占80.20%;生物膜形成能力以1级为主(46.20%);复发病例分离的菌株中可形成生物膜的菌株比例(81.25%)高于未复发病例分离的菌株(78.57%),差异有统计学意义(P<0.05),见表2。 2.3抗菌药物敏感度分析 2.3.1不同生物膜形成能力菌株的药物敏感性分析 引起耳道感染的Pae对常见抗菌药物的敏感率均在50.00%以上(除氨曲南47.17%外),其中阿米卡星最高(94.34%),其次是头孢吡肟(88.68%)、头孢他啶(86.79%)、美罗培南(80.19%)、亚胺培南(75.47%)。不同生物膜形成能力的Pae在临床常见抗菌药物中的药物敏感率虽然没有明显差异,但产生物膜菌株的亚胺培南、头孢他啶和左氧氟沙星敏感率比未产膜菌株敏感率略高,见表3。 表2 106株Pae生物膜形成能力情况 表3 生物膜形成能力及不同生物膜级别菌株的药物敏感率比较 2.3.2复发组与未复发组分离菌株的药物敏感率比较 复发组与未复发组菌株的抗菌药物敏感率比较差异均无统计学意义(P>0.05),复发组的头孢他啶、亚胺培南、美罗培南、左氧氟沙星、哌拉西林、氨曲南和头孢哌酮/舒巴坦的抗菌药敏感率略高于未复发组,见表4。 表4 复发组与未复发组分离菌株的药物敏感率比较 续表4 复发组与未复发组分离菌株的药物敏感率比较 2.4生物膜形成的影响因素分析 在生物膜构建的环境中分别加入11.10 mmol/L葡萄糖及15.00 μg/mL壳聚糖季铵盐后测定Pae生物膜形成情况,并与原始生物膜形成结果进行比较。 2.4.1生物膜形成A值变化比较 11.10 mmol/L葡萄糖可以促进生物膜的形成,A值平均增加1.843;而15.00 μg/mL壳聚糖季铵盐可起到一定的抑制作用,A值平均降低1.936。 2.4.2生物膜形成能力等级变化比较 11.10 mmol/L葡萄糖可以使73.60%的菌株生物膜形成能力提升,以等级上升1级为主(44.30%),上升3级的较少(0.90%);15.00 μg/mL壳聚糖季铵盐对50.00%的菌株起到了抑制生物膜形成的作用,其中以下降1级为主(37.70%)。 耳道感染在耳鼻喉头颈外科疾病中极为常见,Pae作为耳道感染中分离率最高的革兰阴性致病菌,近年来受到广泛关注。在其耐药机制中,生物膜的形成是其逃逸药物作用的常见方式[8]。有学者认为,形成生物膜可能是耳道感染反复发作、久治不愈的原因之一[1,11]。因此,对引起耳道感染的Pae相关特征进行研究,对了解疾病的发生、发展及优化临床治疗方案都有很深远的意义。 解放军总医院共收集到引起耳道感染的Pae 106株,患有耳道感染的患者以41~50岁年龄段相对较多,以女性为主。Pae引起耳道感染的病例复发率达60.38%。在复发组与未复发组菌株比较中发现,复发病例分离菌株的产生物膜情况略高于未复发病例分离菌株,另外复发病例分离菌株对临床常用的抗菌药物(头孢他啶、亚胺培南、美罗培南、左氧氟沙星、哌拉西林、氨曲南和头孢哌酮/舒巴坦等)敏感率略高于未复发病例分离菌株,可见中耳炎的复发与Pae的产生物膜情况及敏感率虽没有直接关系,但菌株的生物膜产生在其中发挥着一定的作用,中耳炎的复发可能受多个因素的共同影响[12],这也是笔者下一步将要研究的内容。 分离的Pae菌株具有形成生物膜的能力高达80.20%,其生物膜形成能力以1级和2级为主,与相关报道基本一致[13]。引起耳道感染的Pae对常见抗菌药物的敏感率均在50.00%以上(除氨曲南47.17%外),不同生物膜形成能力的Pae对临床常见抗菌药物体外敏感率虽然没有明显差异,但是在亚胺培南、头孢他啶和左氧氟沙星3种抗菌药物上,产生物膜菌株的敏感率比未产膜菌株敏感率略高,可见是否产生物膜对细菌的耐药性影响不大,与文献报道的略有差异[1]。可能原因为:(1)Pae耐药机制较复杂,且易发生多重耐药[14];(2)Pae生物膜产生过程较为复杂,受细菌生长的微环境、群体感应系统及与表型相关的基因调控[15]。 在生物膜形成的影响因素研究中,本文发现葡萄糖和壳聚糖季铵盐对Pae生物膜的形成分别有一定促进和抑制作用,这与相关文献基本一致[13,16-17]。国内外一些学者报道,糖尿病是医院内泛耐药Pae感染的独立危险因素[18],这可能与高血糖等代谢紊乱可使中性粒细胞功能下降及表面黏附因子增加,有助于微生物聚集形成生物膜有关。在本研究和相关文献中可以看出,葡萄糖对生物膜的形成有促进作用[16],且水平越高促进作用越强[13];壳聚糖季铵盐对Pae生物膜的形成有一定抑制作用,这与相关报道基本一致[17]。因此,控制血糖或使用壳聚糖季铵盐凝胶对生物膜的抑制将起到一定效果。 引起耳道感染的Pae生物膜形成能力较强,控制血糖水平在正常范围及使用壳聚糖季铵盐凝胶对抑制生物膜形成有一定的作用,这对于预防疾病复发有一定的作用。2 结 果
3 讨 论
4 结 论
