2019冠状病毒病研究纪实:至2020年3月11日
2020-06-09丁翠玲彭浩然戚中田
苗 根,丁翠玲,彭浩然,戚中田
2019年12月1日,武汉市出现首例不明原因肺炎病例;2020年1月8日确认病原体为2019新型冠状病毒(2019-nCoV);2020年1月31日世界卫生组织(WHO)将病原体暂命名为2019新冠病毒(2019-nCoV);2020年2月8日国家卫健委将该不明原因肺炎命名为新型冠状病毒肺炎;2020年2月11日,WHO依据规则将新冠肺炎正式命名为2019冠状病毒病(COVID-19);同日,国际病毒分类委员会将2019新冠病毒正式命名为严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)[1-2]。2020年3月11日,WHO将新冠疫情流行趋势升级为全球大流行状态。2019-nCoV是第7种人类冠状病毒,为有包膜、不分节段的单股正链RNA病毒。不同于一般情况下仅引起上呼吸道感染症状的HCoV-NL63、HCoV-229E、HCoV-OC43和HCoV-HKU1, 2019-nCoV与重症急性呼吸综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV)均为高致病性冠状病毒。本文拟以时间为轴线,从病原体、病毒宿主、流行病学、检测方法、致病机制和临床诊疗6个方面记述2019冠状病毒病研究的重要进展。
1 病原体研究时间轴
2020年1月5日,张永振团队率先公布了2019-nCoV全基因组序列(GenBank: MN908947.3,全长29 903 bp)。2020年1月6日,国家疾病预防控制中心从不明原因肺炎患者临床样本中分离到第1株病毒(CHPC 2020.00001;NPRC 2020.00001)。2020年1月24日,新型冠状病毒国家科技资源服务系统(http://nmdc.cn/#/nCoV)正式启动并发布了我国第一株临床样本分离毒株的信息及电镜照片,此后陆续发布了病毒核酸检测引物和探针序列等重要信息。2020年2月7日,上海市疾病预防控制中心和复旦大学团队利用vero-E6和Huh7细胞分离培养获得病毒毒株。2020年2月21日,瑞士伯尔尼大学利用反向遗传学策略,合成有活性的2019-nCoV[3]。2020年3月7日,Peter Doherty研究人员展示了2019-nCoV的mRNA序列[4]。截至2020年3月10日,国家生物信息中心2019新型冠状病毒信息库[5]共收集2019新型冠状病毒序列408条(其中我国193条),国际GISAID数据库收录2019新型冠状病毒基因组序列264条。
从分类学角度,2019-nCoV与SARS-CoV同属于冠状病毒科、冠状病毒亚科、β 冠状病毒属、类 SARS 冠状病毒种。2020年2月17日,广东省疾病预防控制中心研究指出广东2019-nCoV基因序列与武汉早期病毒基因组之间基本无突变[6],2020年2月21日,Yu 等[7]发现93个2019-nCoV样本基因组同源性超过99%,编码区仅存在120个核苷酸位点差异。2020年3月3日,Tang 等[8]分析了103条2019-nCoV基因组序列,显示共有149个位点突变,整体突变率较低。单核苷酸多态性(single nucleotide polymorphism,SNP)分析显示,病毒目前存在L和S两个亚型,其中L型分布更广(70%),S型相对更古老。2020年3月7日,Shu等[9]分析146个基因组后显示共80个单倍型、183个突变位点,其中85%(156/183)为单突变位点(singleton)。2020年2月7日,中国医学科学院和北京协和医学院研究团队[10]对首次公布的2019-nCoV基因组(GISAID编码:EPI_ISL_402119,EPI_ISL_402120,EPI_ISL_402121)进行注释,发现2019-nCoV编码27种蛋白质,包括15种非结构蛋白(nsp1-nsp10,nsp12-nsp16)、4种结构蛋白(S、E、M和N)和8种辅助蛋白(3a、3b、p6、7a、7b、8b、9b和orf14)。2019-nCoV与SARS-CoV氨基酸序列对比结果显示两者组成相似,但编码的辅助蛋白3b、8b存在显著差异,且2019-nCoV缺失了SARS-CoV编码的8a蛋白。进一步对2019-nCoV与SARS/SARS类似冠状病毒保守序列进行比对,显示存在380个差异性氨基酸位点,其中S蛋白中差异性位点主要分布在受体结合域(receptor-binding domain, RBD)和抗原表位区域,这些可能与2019-nCoV传染性和致病力有关。
2 病毒宿主研究时间轴
中国动物卫生与流行病学中心团队检测了4 800余份近年来收集的猪、禽、犬、猫等动物样品,2019-nCoV核酸检测均为阴性,而在另一项针对武汉华南海鲜市场及其他多家生鲜市场的585份环境标本及动物标本的检测中,有33份阳性,其中31份来自经营野生动物的西区,提示此次疫情可能与野生动物交易有关。
蝙蝠是多种冠状病毒的自然宿主。迄今为止,动物冠状病毒中云南中华菊头蝠携带病毒(Bat CoV RaTG13)与2019-nCoV全基因组序列一致性最高(96.2%),提示云南中华菊头蝠很可能是2019-nCoV的自然宿主[11]。2020年1月22日、2月2日、2月26日的3篇研究分别通过同义密码子相对使用度(RSCU)偏好性、感染模式分析、S蛋白序列对比分析推测蛇、水貂和龟类可能是将2019-nCoV传播给人类的潜在中间宿主[12-14]。2019年10月24日,Liu等[15]通过测序揭示马来西亚穿山甲体内病毒基因组片段与SARS-CoV及类SARS-CoV相应序列一致性高达80%~89%。2020年2月13日-2月20日,美国贝勒医学院、香港大学、华南农业大学、云南大学、广东省生物资源应用研究所等研究发现穿山甲冠状病毒与2019-nCoV RBD氨基酸序列一致性高于97%,但全基因组序列一致性为85.5%~92.4%[16-20],而之前的研究证明SARS-CoV与中间宿主果子狸冠状病毒基因一致性高达99.8%,这似乎并不支持穿山甲为2019-nCoV中间宿主的论点。但2019-nCoV的S蛋白RBD中与受体结合相关的6个氨基酸位点与穿山甲冠状病毒的相应位点完全相同(L455L、F486F、Q493Q、S494S、N501N和Y505Y)(图1),这是在其他冠状病毒都不存在的[18],从适应人类细胞受体看,穿山甲似乎符合2019-nCoV为中间宿主的观点,但是目前尚缺乏进一步的流行病学证据。因此,穿山甲是否为2019-nCoV从蝙蝠到人的中间宿主,尚有待进一步查证。
蝙蝠CoV RaTG13与2019-nCoV的全基因组同源性高达96.2%,但在S蛋白RBD存在关键差别(图1)。蝙蝠CoV RaTG13 的S蛋白RBD中与ACE2结合的6个关键氨基酸位点,在2019-nCoV中突变了5个(L455L、L486F、Y493Q、R494S、D501N和H505Y),但令人诧异的是,这些突变不但没有影响2019-nCoV与其受体ACE2的亲和力,反使它们的结合能力增强了10倍以上,这种功能增强性变异值得进一步研究。

(L455,F486,Q493,S494,N501,Y505)图1 新冠病毒S蛋白受体结合域中发生突变的氨基酸[14-15, 19-20]Fig.1 Amino acid mutations in RBD of 2019-nCoV S protein
3 致病机制研究时间轴
新冠状病毒S蛋白RBD与宿主细胞表面受体ACE2结合从而介导细胞感染[11, 21],宿主细胞蛋白酶TMPRSS2是S蛋白的启动剂,其抑制剂camostat mesylate可以保护细胞免受2019-nCoV感染[22]。因此,进一步解析2019-nCoV S蛋白RBD、ACE2和两者相互作用的复合物结构将有助于阐明感染机制。

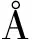
尤其值得注意的是,2019-nCoV基因组的S1和S2亚基交界处多出一段在其他冠状病毒(如SARS-CoV、蝙蝠-CoV和穿山甲-CoV)中不存在的、连续的12个核苷酸序列,编码1个脯氨酸、2个精氨酸和1个丙氨酸(PRRA),从而形成一个弗林酶(furin)酶切位点(RARR)(图2)。研究表明,弗林酶切位点有助于禽流感病毒和新城疫病毒的组装与成熟,与增强传染性和致病性相关[24, 28, 31-32]。
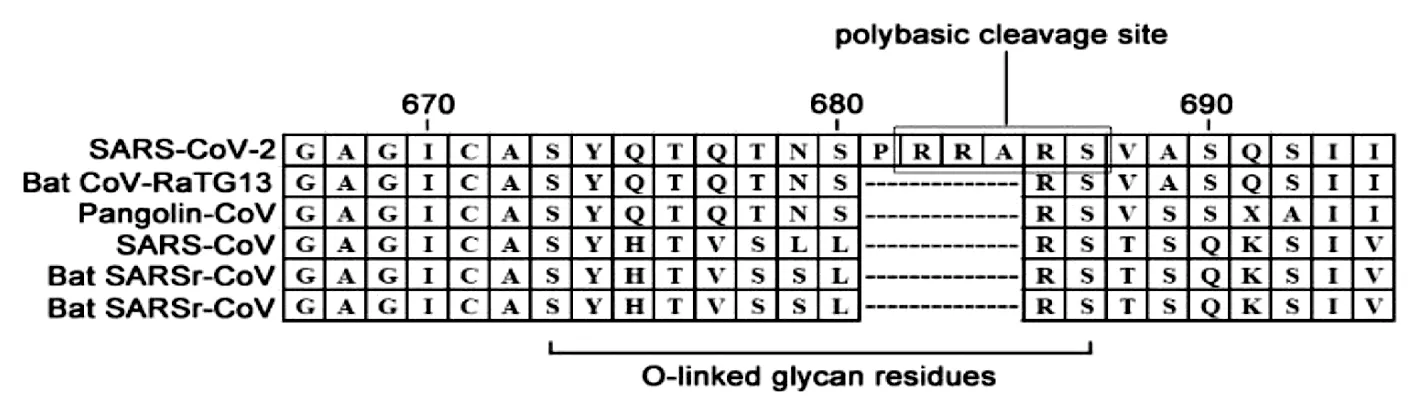
(S673、T678和S686)图2 新冠病毒S1与S2亚基交界处的酶切位点和O-糖基化位点[18, 32-33]Fig.2 S1/S2 site of 2019-nCoV contains a furin-like cleavage site and O-link glycan residues
值得注意的是,COVID-19患者进展为重症乃至死亡与细胞因子风暴的发生发展密切相关。临床观察表明重症患者体内免疫系统过度激活, IL-6、TNF-α、IFN-γ等促炎性细胞因子水平显著升高,可引起急性呼吸窘迫综合征和多器官衰竭,最终威胁生命[33-34]。此外,肺部穿刺病理活检和尸检报告指出COVID-19患者病理主要表现为肺部炎症反应[35]。
4 流行病学研究时间轴
2020年1月20日,新冠肺炎被纳入我国法定报告的乙类传染病,并按甲类传染病采取防控措施。2020年1月23日,全国各省市开始陆续实施大城市隔离政策。至2020年 1月25日2019-nCoV的R0值(R naught,基本再生数)为2.68(95%CI=2.47~2.86)[36]。后续研究显示,全国和武汉总体R0分别为4.5 (95%CI= 4.4~4.6) 和4.4 (95%CI=4.3~4.6)[37]。
SEIR 传染病模型(Susceptible-Exposed-Infectious-Removed)预测显示,国内疫情在2020年2月底达到峰值,4月底将趋于平缓[38],但实际在2月中旬即达到峰值,这可能与全国范围内的强力防控措施有关。武汉是最早公开通报发现疫情的地方,在病原体判定为新型冠状病毒之后,2020年1月11日武汉市卫健委首次通报41例新冠病毒肺炎病例。2020年1月21日国家卫健委首次通报全国疫情共3省(区、市)新增确诊病例77例, 2月4日新增病例数达到3 887例, 2月12日新增病例数达到整个疫情期间峰值15 152例(含湖北临床诊断病例13 332例),此后新增病例数不断减少,至2020年3月7日已降至44例。
世界范围内,自2020年1月13日、15日、20日、22日,泰国、日本、韩国和美国分别开始通报出现首例确诊病例,疫情开始全球蔓延。2020年1月30日,WHO宣布新冠肺炎疫情为“国际关注的突发公共卫生事件”(PHEIC)。停泊日本的“钻石公主号”邮轮(共3 711人)于2020年2月3日开始检疫,2月5日确诊10例,截至3月2日总共确诊706例 。2020年2月28日,WHO将新冠肺炎疫情的风险级别从此前的“高”提至最高级别的“非常高”。2020年3月8日,意大利首次实行隔离,涉及包括伦巴第地区在内的约1 600万人口。截至2020年3月11日上午10时,中国境外共有113个国家/地区报告确诊病例37 371例,死亡484例,3月10日-11日单日新增确诊病例及死亡病例分别超过14%、29%。其中确诊病例意大利10 149例、伊朗8 042例、韩国7 755例、法国1 774例、西班牙1 639例、德国1 296例、美国696例、日本568例。
当前认为传染源主要是新型冠状肺炎病毒感染的患者,无症状感染者也可成为传染源。2020年1月份,河南安阳市和浙江杭州市筛查出2019-nCoV无症状感染者,此后湖北、广东等地陆续出现报道,国外亦有相关报道[39-40]。国内无症状感染者比例约为1.2%(889/44 672)[41]。2020年2月19日的一份研究指出无症状感染者上呼吸道病毒载量与有症状确诊患者相当[42],并可感染同居家庭成员[43]。值得注意的是部分无症状感染者在一段时间后可出现症状,因此真正的无症状感染者相对少见,不是传播的主要因素。
病毒主要传播途径为呼吸道飞沫和密切接触传播,密闭环境中存在气溶胶传播可能。此外多项研究表明除呼吸道和血液样本外,COVID-19患者粪便、尿液、泪液及结膜分泌物中病毒核酸检测亦可阳性,其中部分患者粪便中可分离培养出活病毒[44-45],因此应注意受病毒污染的环境可能造成病毒传播。
人群普遍易感,多数COVID-19患者症状较轻,可以痊愈,但是部分可进展为呼吸困难。纳入病例时间截至2020年1月22日、1月29日、2月20日的三份研究分别推算潜伏期为5.2 d、4 d、5~6 d[44, 46-47],而2020年3月4日《新型冠状病毒感染的肺炎诊疗方案(试行第七版)》中指出潜伏期1~14 d,多为3~7 d。
5 检测方法研究时间轴
核酸检测是疫情暴发初期新冠肺炎疑似病例确诊的金标准。2020年1月26日,之江生物、捷诺生物和华大生物取得国家药监局颁发的第一批新冠病毒核酸检测试剂盒医疗器械注册证,此后不断有新的核酸检测产品投入使用。截至2020年3月8日,国家药品监督管理局已批准10种2019-nCoV核酸检测试剂盒。核酸诊断标本多为血液、上呼吸道标本(咽拭子、鼻拭子、痰液)或下呼吸道标本(肺泡灌洗液、支气管灌洗液)。2020年2月5日,《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》曾将CT影像等纳入临床诊断标准。2020年2月18日,天津研发出CT图像辅助诊断[48]。2020年2月22日和2月29日,4项针对血清IgM/IgG抗体检测试剂盒分别获批(其中两项胶体金法:万孚生物、英诺特(唐山)生物,两项磁微粒化学发光法:博奥赛斯(重庆)生物),《新型冠状病毒感染的肺炎诊疗方案(试行第七版)》将抗体检测纳入血清学诊断标准,2 d后抗体化学发光微粒子免疫检测试剂盒(万泰凯瑞)亦获批准。美国疾病预防控制中心为应对疫情,于2020年2月4日、2月29日分别紧急审批了两项诊断产品“CDC 2019-nCoV Real-Time RT-PCR Diagnostic Panel (CDC)”和“New York 2019-nCoV Real-time Reverse Transcriptase (RT)-PCR Diagnostic Panel”。
同时,一批新的检测技术陆续问世。2020年2月14日,美国张锋团队发布了基于 CRISPR/Cas13检测2019-nCoV的SHERLOCK 技术,仅需3步可在1 h内完成检测,但尚未进行样本验证[49]。2020年2月22日,清华大学参与研发的恒温扩增芯片法新冠病毒检测试剂盒获批(成都博奥品芯)。此外,2020年2月25日,Lamb等[50-51]报告通过环介导等温扩增和反转录相结合(reverse transcriptional-loop-mediated isothermal amplification,RT-LAMP)45 min内检出病毒RNA。2020年3月3日,Wang等[52]通过靶向测序(Nanopore Targeted Sequencing,NTS)检测覆盖病毒基因组及毒力相关重要基因。
6 临床诊疗研究时间轴
截至目前,国家卫健委先后制定了《新型冠状病毒感染的肺炎诊疗方案》(简称诊疗方案,均为试行)共七版。2020年1月21-23日制定了第一至第三版诊疗方案,2020年1月27日公布了第四版,2020年2月5日公布了第五版,2020年2月10日公布了第五版的修正版,2020年2月18日公布了第六版,2020年3月4日公布了第七版。
诊疗方案第二版认为发热、乏力、干咳为COVID-19患者主要表现。有研究收集2020年1月29日之前分布在全国30多个省市、552家医院的1 099个确诊病例信息后,认为发热(入院时43.8%、住院时88.7%)和咳嗽(67.8%)是COVID-19患者最常见的症状,消化系统症状较为少见[46]。 纳入病例时间截至2020年1月29日、2月11日、2月20日的3份报告指出COVID-19的总体粗病死率为1.4%、2.3%、3.8%[41, 44, 46],其中病死率随年龄增长而增加,且男性病死率高于女性。尽管COVID-19病死率低于SARS和MERS,但由于病例数众多,其潜在影响更大。
诊疗方案第二版中提出针对轻型和普通型患者治疗方案主要是尽早隔离,加强支持治疗、及时给予有效氧疗措施和抗病毒治疗,中医方面可根据症候辨证论治,糖皮质激素可酌情短期使用。而针对重型、危重型的治疗原则主要是在对症治疗的基础上,积极防治并发症,治疗基础疾病,预防继发感染,及时进行器官功能支持。其中抗病毒治疗药物主要为α-干扰素或洛匹那韦/利托那韦(ritonavir/ lopinavir)(2020年1月23日武汉金银潭医院开启这两个药物联合治疗的第1个药物临床试验(ChiCTR2000029308))。诊疗方案第四版进一步规范糖皮质激素适用人群,同时提出针对重症、危重症病例,有条件可考虑恢复期血浆治疗。诊疗方案第五版在抗病毒治疗方案中加入利巴韦林(ribaviron,ChiCTR2000029387),基于危重患者体内高炎症反应,可考虑使用体外血液净化技术。4 d后的诊疗方案第五版(修正版)对利巴韦林的用法用量进行了修正。诊疗方案第六版在治疗药物中增加了磷酸氯喹(chloroquine phosphate,ChiCTR2000029609)和阿比多尔(arbidol,ChiCTR2000029621),同时进一步明确了体外血液净化技术包括血浆置换、吸附、灌流、血液/血浆滤过等。
COVID-19患者主要表现为呼吸系统症状,严重者可进展为呼吸窘迫,尸检发现2019-nCoV主要引起深部气道和肺泡损伤为特征的炎性反应[35],因此诊疗方案一直不断更新呼吸支持具体实施细则。诊疗方案第七版提出要保证患者充分通、换气,对急性呼吸窘迫患者,若氧疗或机械通气效果不佳,应尽快考虑体外膜肺氧合(ECMO)。同时为阻断细胞因子风暴,推荐使用IL-6受体抗体托珠单抗(tocilizumab,ChiCTR2000029765)。诊疗方案第七版还新增儿童重型病例标准,并且提出儿童重型、危重型病例可进行丙种球蛋白治疗。此外,有研究指出COVID-19患者还可能合并心肌损害、凝血功能异常、中枢神经系统并发症等,治疗过程中同时需要监测患者肝肾功能,尽早应用干预措施以防止疾病进展为器官衰竭[53-55]。
截至2020年3月3日,在中国临床试验注册中心COVID-19临床研究索引中已有 290个临床试验项目,包括治疗性临床试验、诊断试验、干预性研究、观察研究、流行病学研究等。此外,瑞德西韦(remdesivir)的一项II期临床试验(NCT04280705)和两项III期临床试验(NCT04252664和NCT04257656)已启动。冠状病毒S蛋白是研发抗病毒药物的潜在靶点[56-57],目前处于研究中的SARS特异性人单克隆抗体CR3022[58]、TMPRSS2抑制剂[22]、格瑞弗森(griffithsin)[59]、淋巴细胞抗原6复合体(LY6E)[60]均针对2019-nCoV的S蛋白。Pandolfi等[61]提出CRISPR / Cas13d系统可能是一种潜在的治疗方法,其特异性强且可预防病毒耐药性变异。
疫苗研发有灭活疫苗、mRNA疫苗、重组蛋白疫苗、病毒载体疫苗和DNA疫苗等,目前多支疫苗已进入临床试验,其中国内科兴中维的灭活疫苗进入一期临床试验,康希诺生物的重组腺病毒疫苗、武汉生物的灭活疫苗进入二期临床试验。此外,美国Moderna公司的mRNA疫苗、Inovio公司的DNA疫苗也已进入临床阶段。
7 展 望
新冠疫情是对我国公卫体系、医疗体系和突发公共卫生事件动员能力的一次检验和大考,我国迅速开展流行病学调查、短时间内分离鉴定病毒、开展病原学研究、建立检测方法、完善诊疗方案、探索致病机制、研发药物和疫苗,有效阻止了国内疫情蔓延,也为世界疫情防控赢得了时间窗口。而我国肺炎防控方案也从早期“预防为主、防治结合、科学指导、及时救治”到“早发现、早报告、早诊断、早隔离、早治疗”再到“分区分级精准防控”,根据疫情形势变化及研究进展精准施策。我们记录此次大事记和时间轴,就是为了总结经验补足短板,以进一步加强公共卫生体系建设,健全突发疫情应对处置体系,加强科技储备与紧急动员能力,加强生物安全立法与野生动物保护,为未来可能出现的重大传染病疫情做好充分准备。
