盐酸倍他司汀及其关键中间体的合成综述
2020-05-26俞伟颜国明尹超刘威梁超茗孙茂林叶金星
俞伟 颜国明 尹超 刘威 梁超茗 孙茂林 叶金星



摘 要 盐酸倍他司汀是一种组胺H1受体激动剂,临床上用作血管扩张药,是目前在临床上治疗美尼尔氏综合症最常用的药物之一。本文综述了盐酸倍他司汀和其关键中间体2-羟乙基吡啶以及2-乙烯基吡啶的合成路线,根据原料和中间体不同,报道了5种盐酸倍他司汀的合成方法,根据原料和反应条件不同,总结了7种2-羟乙基吡啶的合成方案和8种2-乙烯基吡啶的合成方案。虽然技术和合成方案在不断优化,但目标产物盐酸倍他司汀的合成和产业化仍有很大发展空间。
关键词 盐酸倍他司汀 组胺H1受体激动剂 2-羟乙基吡啶 2-乙烯基吡啶
中图分类号:O626.321; R972.4 文献标志码:A 文章编号:1006-1533(2020)09-0075-05
Synthesis of betahistine hydrochloride and its key intermediates
YU Wei1*, YAN Guoming1, YIN Chao1, LIU Wei2, LIANG Chaoming2, SUN Maolin2, YE Jinxing2**
(1. Shanghai Zhongxi Sunve Pharmaceutical Co., Ltd., Shanghai 201419, China; 2. Engineering Research Center of Pharmaceutical Process Chemistry, Ministry of Education, School of Pharmacy, East China University of Science and Technology, Shanghai 200237, China)
ABSTRACT Betahistine hydrochloride is a histamine H1 receptor agonist that is clinically used as a vasodilator and is one of the most commonly used drugs for the treatment of Menieres syndrome. The synthesis routes of betahistine hydrochloride and its key intermediates, 2-hydroxyethylpyridine and 2-vinylpyridine, were reviewed. Five synthetic methods of betahistine hydrochloride were reported so far depending on different raw materials and intermediates. The synthesis schemes of 7 kinds of 2-hydroxyethylpyridine and 8 kinds of 2-vinylpyridine were summarized based on the differences of starting materials and reaction conditions. Although the technical and synthetic schemes are continuously being optimized, there is still much room for the development and industrialization of the synthesis of the target product, betahistine hydrochloride.
KEy WORDS betahistine hydrochloride; histamine H1 receptor agonist; 2-hydroxyethylpyridine; 2-vinylpyridine
鹽酸倍他司汀(betahistine hydrochloride)化学名为N-甲基-2-吡啶乙胺二盐酸盐,商品名为美克乐(Microser),是由意大利佛曼蒂(Formenti)制药集团开发的一种组胺H1受体激动剂,在临床上作为一种血管扩张药,主要用来治疗各种眩晕综合症、慢性缺血性脑血管疾病、美尼尔氏综合症和相关的眩晕症状等。盐酸倍他司汀是目前在临床上治疗美尼尔氏综症最常用的药物之一[1]。其与血管平滑肌H1受体结合发挥作用,可以增加心脑血管及周围血管的血流量,改善微循环,并使红细胞聚集度和血小板黏附率下降,从而改善血液黏滞性和高凝状态,使毛细血管壁的通透性增加,促进细胞外液的逆吸收,从而降低血液的黏稠度。
盐酸倍他司汀目前有注射液、口服液和片剂等。盐酸倍他司汀口服易吸收,放射性同位素标记药物结果表明,其口服后能迅速被人体吸收。倍他司汀在人体内代谢产物为2-吡啶乙胺和2-吡啶乙酸,其中2-吡啶乙酸主要以尿液形式排出,同时在24 h内代谢物即可完全排出。有证据表明,这些代谢物中的一种2-吡啶乙胺可能也具有活性,并且在体内壶腹受体上发挥与盐酸倍他司汀类似的作用[2]。
本文对合成盐酸倍他司汀及其关键中间体的化学方法及相关的重要工艺条件作一综述,旨在为盐酸倍他司汀及其关键中间体工业化合成路线的选择提供参考。
1 盐酸倍他司汀的合成工艺综述
目前盐酸倍他司汀主要是由甲醛和2-甲基吡啶为起始原料通过四步法合成,如图1所示:盐酸倍他司汀的合成先由 2-甲基吡啶与多聚甲醛反应制备2-羟乙基吡啶,2-羟乙基吡啶可经两条途径制备盐酸倍他司汀:一是2-羟乙基吡啶在浓碱中脱水为烯,再与甲胺加成生成N-甲基-2-吡啶乙胺;另一途径则是先溴代,再与甲胺缩合,生成N-甲基-2-吡啶乙胺,最后N-甲基-2-吡啶乙胺与浓盐酸成盐即得盐酸倍他司汀。

2005年,魏宏阳等[3]以2-羟乙基吡啶为起始原料,经过脱水后与甲胺盐酸盐合成得到盐酸倍他司汀,该路线总收率为14%。整体工艺避免了高温高压、条件苛刻的操作。
2008年,叶瑾亮等[4]使用2-乙烯基吡啶为原料,在高温下与甲胺盐酸盐水溶液进行加成得到倍他司汀,产率可达88%,然后将倍他司汀溶解在异丙醇中,并导入盐酸气体使得倍他司汀成盐,产率达到95%,两步总收率为80%。该方法反应条件温和,产率较高,应用价值较高。
2012年,蒋敏等[5]以2-甲基吡啶为起始原料对盐酸倍他司汀的合成工艺进行了优化,通过加成、脱水、缩合、成盐四步合成盐酸倍他司汀。通过实验优化发现投料比是影响反应收率的最大因素,并确定了最优的合成工艺条件,2-乙烯基吡啶-甲胺=1∶1.5(摩尔比),在105 ℃下反应8 h,反应收率达到86.8%。该反应的溶剂可以回收使用,反应收率较高且整体工艺符合绿色化学的要求,适用于工业化生产。
2013年,石峰[6]等使用簡单的镍铁催化剂催化氨或胺与醇或伯胺的N-烷基化反应。在没有有机配体和碱的情况下,成功地合成了各种结构的N-烷基胺。将该方法用于倍他司汀的合成(图2),收率达79%。催化剂除了具有优异的催化性能外,本身还具有突出的优越性,即空气和水分稳定。此外,该催化剂的磁性易于从反应混合物中分离,且在不明显失活的情况下可以回收重复使用。但该反应的催化剂制备繁琐,原料价格高,反应时间长,不适合工业化生产。
2015年,陈荣等[7]使用无水硫酸镁与氢氧化钠作为脱水反应的混合脱水剂,以甲胺盐酸盐水溶液和甲苯两相体系作为缩合反应溶剂,成盐反应是使用乙醇与异丙醇的混合溶剂,制备纯度可达到99.99%以上的盐酸倍他司汀。
2016年,Ghasemi等[8]以阴离子杂多酸负载型离子液体催化剂催化2-乙烯基吡啶和甲胺的加成反应(图3),反应总收率85%。含有聚钨酸根阴离子的离子液体负载在磁性硅藻土上,其作为可用磁分离的非均相催化剂在倍他司汀的合成方面提供了很好的结果,同时用磁铁很容易除去固体纳米催化剂。该反应使用的催化剂制备条件苛刻,成本较高,不适合工业化生产。
2018年,Kundu等[9]报道了一种Ru(II)络合物,以甲醇为甲基化剂,由叠氮化物合成N, N-二甲基和N-单甲基胺(图4)。该方法应用于倍他司汀的合成,反应收率66%。但合成中使用到了叠氮化物,不适合工业化生产。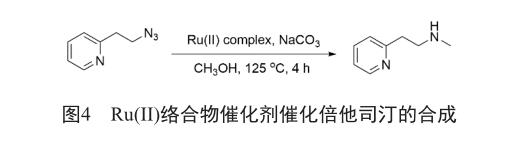
这些倍他司汀的合成工艺,经过多年的优化,合成路线已成熟稳定。2-羟乙基吡啶和2-乙烯基吡啶作为合成过程中的关键中间体,因此实现倍他司汀的工业化生产需重点关注2-羟乙基吡啶和2-乙烯基吡啶的合成。
2 2-羟乙基吡啶的合成工艺
2-羟乙基吡啶的合成主要是通过甲醛和2-甲基吡啶一步法制得(图5)。
1987年,朱秀昌等[10]以2-甲基吡啶和甲醛水溶液为原料,在苯甲酸或乙酸的催化下,在105~128 ℃下反应45~70 h,单程转化率达到40%~60%。然后回收未完全反应的2-甲基吡啶,再加入新的甲醛水溶液和2-甲基吡啶使成为起始比例进行多次反应,直至反应八次后目标产物的收率达到95%左右。反应单程转化率低,时间较长,生产效率低。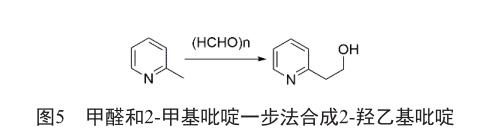
2005年,王宝庆等[11]将多聚甲醛和2-甲基吡啶在苯甲酸催化下于100 ℃下缩合反应30 h得到2-羟乙基吡啶,其中2-甲基吡啶-多聚甲醛-苯甲酸=1∶0.12∶0.012(摩尔比)。该工艺方法原料2-甲基吡啶的使用量过大且得到目标产物2-羟乙基吡啶的量较少,同时回收原料的损失率大,生产成本高。
2012年,闫晓红等[12]以有机碱(甲醇钾、乙醇钠和二异丙基胺基锂等)作为催化剂,且有机碱与2-甲基吡啶摩尔比为1∶1,反应3~5 h即可得到产物2-羟乙基吡啶。由于使用有机碱的原因,因此该方法对反应操作的要求非常严格,并且使用有机碱的价格较为昂贵且难以回收,成本较高,工业化难度高。
2012年,杨海燕等[13]在研究2-羟乙基吡啶的合成过程中探索使用了酸和碱两种催化剂,发现三乙胺非常有利于加成反应,作者优化了催化剂和反应比例等条件,具体投料比为2-甲基吡啶-甲醛=5∶1(摩尔比),在三乙胺的催化下反应40 h得到产物2-羟乙基吡啶。该方法反应时间长,单程转化率低且生产成本较高,不利于工业化生产。
2013年,沙文茜[14]以氢氧化钠或者氢氧化钾作为催化剂合成2-羟乙基吡啶,具体条件为甲醛水溶液和2-甲基吡啶摩尔投料比为1∶10,在0.5 Mpa的高压釜内160 ℃反应1 h得到2-羟乙基吡啶。该方法对工艺设备要求高,反应的副产物较多,且单程转化率低。
2014年,肖国民等[15]使用2-甲基吡啶质量10%的固体超强酸作为催化剂(如SO42-/ZrO2、WO3/TiQ2、SO42-/TiO2或SiO2负载的苯甲酸等)催化合成2-羟乙基吡啶,在高压釜内于140 ℃下反应80 min得到目标产物。虽然该方法的合成效率高,但是副产物较多,后处理繁琐,对设备的要求高。
2016年,孙国新等[16]以乙二酸为起始物料,合成2-羟乙基吡啶,在110~120 ℃下反应30~40 h,再经精馏后得目标产物,单程转化率35.15%,纯度99.0%。该方法虽然得到产物的纯度较高,但是反应的时间较长且单程转化率低,不适于工业化生产。
通过以上分析,发现文献报道的工艺大多存在2-甲基吡啶和甲醛的投料比大,反应的时间长,单程转化率低,副产物较多等缺点,不利于工业化生产。
3 2-乙烯基吡啶合成工艺综述
2-乙烯基吡啶的合成方法主要有:①丙烯腈和乙炔在催化剂下加成;②3-(2-吡啶)基丙烯酸的脱羧合成;③2-乙基吡啶的脱氢反应;④2-甲基吡啶和甲醛通过一步法或者两步法制得。
1981年,Bonnemann等[17]使用环戊二烯基钴催化剂或π-烯丙基钴催化剂在高温下以乙炔和丙烯腈选择性制备2-乙烯基吡啶。该方法条件苛刻,原料成本较高,副产物较多,难以实现工业化(图6)。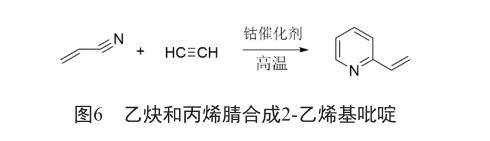
1983年,Calin等[18]以3-(2-吡啶)基丙烯酸为原料高温脱羧制备2-乙烯基吡啶(图7),将3-(2-吡啶)基丙烯酸、对苯二酚和催化剂铜粉混合高温下以65.7%的收率得到目标产物。该方法的收率低,生产成本高,不适合工业化生产。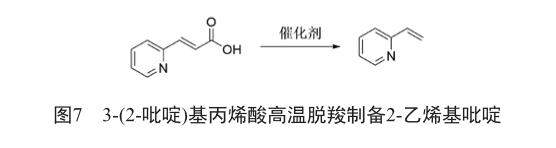
2004年,Kulkarni等[19]使用Cr-Ni催化剂在高温高压下催化2-乙基吡啶脱除一分子氢气制备2-乙烯基吡啶的方法(图8)。该方法对实验条件要求苛刻,且反应收率较低。
2006年,赵鹬等[20]以氢氧化钾改性的HZSM-5沸石分子筛为催化剂通过气相一步法合成2-乙烯基吡啶(图9)。反应温度在360~370 ℃,2-甲基吡啶的转化率达80.26%,选择性为97.59%。该方法虽然反应转化率和选择性较高,但是催化剂合成过程复杂,反应条件苛刻,对设备要求高,不利于工业化生产。
2008年,于景东[21]以2-甲基吡啶和甲醛或多聚甲醛为原料,加入催化剂杂多酸与原料在四级串联式搅拌反应釜中反应,经蒸馏后得2-乙烯基吡啶。该方法工艺成本高,且操作较复杂,不适用于工业化生产。
2012年,徐文辉等[22]考察了酸碱催化剂对脱水反应的影响(图10),最优化条件是100 ℃下反应2 h,收率80.2%,纯度为98.1%,其中氢氧化钾-2-羟乙基吡啶=2∶5(摩尔比)。该方法的反应条件温和,但是反应收率低,脱水反应时间长。
2014年,吕荣明等[23]使用2-甲基吡啶经管道反应器一步合成2-乙烯基吡啶,单程收率为33%,单程转化率为37%。该反应物料硫酸对管道的腐蚀性非常强。
2017年,胡江海等[24]研究了两步合成2-乙烯基吡啶的方法:首先是在釜中加入多聚甲醛和2-甲基吡啶在105~110 ℃下反应45~70 h,未反应的2-甲基吡啶回收套用,直至反应的收率达到95%左右,随后在高温下加入反应液和脱水剂氢氧化钠以及一定量的阻聚剂对叔丁基邻苯二酚,最后再经精馏得到产品2-乙烯基吡啶。该工艺单程转化率低,原料回收损失率高且反应时间较长。
对以上文献分析发现,前三种方法的反应条件都比较苛刻,反应过程不易控制,后处理复杂且反应收率低,很难满足工业化的需求。后面以2-甲基吡啶与甲醛或2-羟乙基吡啶为起始原料的反应条件就相对温和,同时原料的成本较低,但也存在反应产率低,副产物多等情况,有着非常大的优化空间。
4 总结与展望
经过多年的发展和优化,盐酸倍他司汀合成路线已经成熟稳定,其关键中间体2-羟乙基吡啶和2-乙烯基吡啶的合成也不断优化。但目前国内对盐酸倍他司汀及其中间体的合成研究仍依赖于传统的间歇反应设备,且生产工艺大多存在反应时间长、2-甲基吡啶的单程转化率低和生产成本高等缺点。目前,简化盐酸倍他司汀生产工艺、减少三废、降低生产成本成为了很多研究者的目标。因为需要用到甲醛和甲胺等易挥发性的原料,因此笔者认为利用微通道连续流反应器等新技术加快反应速率、提高反应效率、降低生产成本、简化后处理操作将会成为今后研究和产业化的方向。
参考文献
[1] 陈清棠, 赵玉宾. 美克乐治疗眩晕症的开放性研究[J]. 中国新药杂志, 1998, 7(4): 52-54.
[2] Botta L, Mira E, Valli S, et al. Effects of betahistine and of its metabolites on vestibular sensory organs[J]. Acta Otorhinolaryngol Ital, 2001, 21(3 Suppl 66): 24-30.
[3] 魏宏陽, 周波, 刘玉梅. N-甲基-2-吡啶乙胺二盐酸盐的合成[J]. 辽宁化工, 2005, 34(8): 335-336.
[4] 叶瑾亮, 张小春, 陈伟健. N-甲基-2-吡啶乙胺二盐酸盐的合成[J]. 广东化工, 2008, 35(8): 22-23.
[5] 蒋敏, 张春桃, 叶绿行, 等. 正交优化盐酸倍他司汀的合成工艺[J]. 安徽化工, 2012, 38(6): 19-20; 24.
[6] Cui X, Dai X, Deng Y, et al. Development of a general nonnoble metal catalyst for the benign amination of alcohols with amines and ammonia[J]. Chemistry, 2013, 19(11): 3665-3675.
[7] 陈荣, 严家庆, 张智红. 一种盐酸倍他司汀的制备方法: CN105175319A[P]. 2015-12-23.
[8] Ghasemi MH, Kowsari E, Shafiee A. Aza-Michael-type addition reaction catalysed by a supported ionic liquid phase incorporating an anionic heteropoly acid[J]. Tetrahedron Lett, 2016, 57(10): 1150-1153.
[9] Kaushik C, Anju M, Dibyajyoti P, et al. Selective synthesis of mono- and di-methylated amines using methanol and sodium azide as Cl and N1 sources[J]. Green Chem, 2018, 20(14): 3339-3345.
[10] 朱秀昌, 黄伟秋. 乙烯吡碇常压合成法: CN86103091[P]. 1987-11-18.
[11] 王宝庆, 仇传禄, 赵学冉, 等. 工业规模制备2-羟乙基吡啶工艺: CN1580046[P]. 2005-02-16.
[12] 闫晓红, 李善清, 赵庭栋, 等. 一种2-羟乙基吡啶的制备方法: CN102731372A[P]. 2012-10-17.
[13] 杨海燕, 闫晓红, 徐文辉, 等. 2-羟乙基吡啶的常压合成研究[J]. 精细化工中间体, 2012, 42(2): 25-28.
[14] 沙文茜. 合成制备2-乙烯基吡啶的方法: CN102863375A[P]. 2013-01-09.
[15] 肖国民, 高李璟, 张进, 等. 一种高效环保的2-羟乙基吡啶的制备方法: CN104109114A[P]. 2014-10-22.
[16] 孙国新, 李健平, 杨涛, 等. 一种合成2-羟乙基吡啶的新方法: CN105237468A[P]. 2016-01-13.
[17] Bonnemann H, Samson M. Process for preparation of 2-vinylpyridine from acetylene and acrylonitrile: US4266061[P]. 1981-05-05.
[18] Calin S. Methods for the synthesis of vinylpyridines[J]. Rev Chim, 1983, 34(9): 850-854.
[19] Kulkarni SJ, Madhavi G, Viswanathan V. Process for the preparation of vinylpyridine from picoline over modified zeolites: US6727365[P]. 2004-04-27.
[20] 赵鹬, 乔旭, 崔咪芬, 等. 2-甲基吡啶合成2-乙烯基吡啶[J]. 南京工業大学学报, 2006, 28(5): 37-41.
[21] 于景东. 杂多酸催化蒸馏制2-乙烯基吡啶: CN101225071A[P]. 2008-07-23.
[22] 徐文辉, 闫晓红, 杨海燕, 等. 脱水反应生成2-乙烯基吡啶的研究[J]. 山东化工, 2012, 41(11): 12-14.
[23] 吕荣明, 杨亮鸿, 蔺继朋, 等. 一种2-乙烯基吡啶的制备方法: CN104016905A[P]. 2014-09-03.
[24] 胡江海, 张晓磊, 于飞. 一种乙烯基吡啶生产工艺: CN106748977A[P]. 2017-05-31.
