腐殖酸联合铁氧化物去除水体中重金属的研究进展
2020-05-25刘诗婷刘竞依陈会姗
刘诗婷 ,么 强 ,陈 芳 ,刘竞依 ,陈会姗
(1.东北大学秦皇岛分校资源与材料学院,河北秦皇岛066004;2.河北农业大学海洋学院,河北秦皇岛066003)
随着我国工业化程度的提高,重金属污染问题俨然成为危害我国环境安全的重要因素。重金属污染不仅来源广泛,且往往具有毒性大、难以代谢、易被生物富集等特性〔1〕。当前,重金属污染的治理方法主要有化学、物理、生物三类,其中化学吸附法效率高且适用范围较广,且具有经济性与高效性〔2〕。
腐殖酸主要来自水体、土壤以及植物体腐败分解后的沉积物,是一种复杂的高分子聚合物有机质的总称,是自然界最丰富的有机质之一〔3〕。同时,复杂的来源决定了腐殖酸结构的多样性,不同结构的腐殖酸中存在着复杂多样的活性官能团,如醇羟基、酚羟基、羧基等,这使得腐殖酸具有多样的理化性质,如吸附、络合、阳离子交换等能力〔4〕。但由于腐殖酸不易分离,吸附性能不稳定,所以目前仍然无法将其直接作为吸附剂加以应用〔5〕。
铁氧化物种类众多、成本低廉、安全性强,其本身具有的比表面积较大,可作为吸附剂应用于水处理,同时又因为其自身具有一定的磁性,也便于水处理材料的回收利用,减轻后续处理的成本负担〔6〕。
目前,关于铁氧化物对常见重金属污染物吸附机制、影响因素等方面已有报道〔7〕。但是,在土壤中铁氧化物难以单独存在,常通过物理化学作用与有机质结合成铁氧化物-有机质复合物,不仅提高了铁氧化物的吸附能力,还使得腐殖酸在土壤中趋于稳定〔8〕。本研究从腐殖酸、铁氧化物、腐殖酸-铁氧化物复合材料对重金属的吸附机理,以及铁氧化物和腐殖酸的交互反应等方面展开综述,以期推动腐殖酸-铁氧化物复合材料今后在重金属水体污染治理中的推广和应用。
1 铁氧化物
1.1 铁氧化物概况
自然环境中的铁氧化物主要分布于土壤环境及水体沉积物中〔9〕。由于铁氧化物具有较大的比表面积和较高的表面电荷,常被用作吸附材料基质〔10〕。主要包括铁的氧化物和氢氧化物,不同种类铁氧化物具有不同晶型,在一定条件下可以相互转化〔11〕。目前已知存在16种铁氧化物,其中广泛分布于环境中的有 12 种〔12〕,详见表 1。

表1 环境中常见铁的氢氧化物和铁的氧化物
由于铁氧化物表面的羟基与水体中的氢离子缔合,使其表面带有两类电荷:可变电荷和永久结构电荷,而水体中的pH则会影响铁氧化物表面电荷符号与数量〔13〕。 铁氧化物表面性质以电荷零点(ZPC)作为一个重要指标:当水体pH>pHZPC时,铁氧化物表面带负电荷,使得其对重金属离子的吸附能力减弱〔14〕。
研究表明,在一定条件下,铁氧化物表面可以聚集大量的—OH官能团,形成羟基化表面,在溶液中容易与其他物质发生表面络合配位反应〔15〕。pH、温度、颗粒形貌及粒径等因素也会影响铁氧化物表面的理化性质,进一步影响其对重金属的去除效果〔16〕。
1.2 铁氧化物对重金属的去除
刘文莉等〔17〕研究表明,针铁矿对 Cu2+、Pb2+的吸附强度与pH大小成正相关,针铁矿表面的羟基是其吸附和固化金属离子的主要原因,利用酸碱滴定法和格氏图处理方法,计算出了针铁矿表面活性位点密度为9.107 site/nm2。研究者对针铁矿吸附Cu2+前后的红外光谱进行对比,结果表明Cu2+主要与针铁矿Fe—O—(H)结构中的表面羟基发生反应,取代了表面羟基中的 H+,生成了 Fe—O—(Cu)〔18-19〕。庞禄〔20〕制备出磁性针铁矿和水铁矿,利用傅立叶变换红外光谱仪(FTIR)表征发现,其制备的样品上具有—OH,并通过研究发现,该具有超顺磁性的样品与Cr(Ⅵ)可以发生配体交换作用、静电作用、内层络合作用。
上述研究表明针铁矿表面含有大量游离羟基,使得铁氧化物表面活性位点密度大,具有强吸附性能,由此可知游离羟基是吸附金属离子的主要原因,而因为pH会影响羟基活性,因此成为了影响铁氧化物吸附性能大小的重要因素,众多研究表明pH与铁氧化物吸附能力成正相关。
2 腐殖酸
2.1 腐殖酸物理化学性质
土壤腐殖酸可分为三类,即胡敏酸、富里酸、胡敏素,其主要组成元素有C、H、O、N和少量的S、P等,其中C和O的含量最高〔21〕。腐殖酸结构复杂,主要官能团有羧基、羟基、羰基等,其中羧基约占总基团的60%~90%〔22〕。复杂的结构特性和活性功能基团使得腐殖酸表现出特殊的物理和化学性质和较高的反应活性,可与氧化物、金属离子、有机物等发生交互作用,从而对这些物质在自然环境中的存在形态等产生影响〔23〕。
腐殖酸较强的螯合能力使得其对于重金属具有较强的吸附作用。研究表明,腐殖酸中所含的羧基邻位酚羟基会对重金属螯合起到十分积极的作用。腐殖酸对重金属去除机理的主要影响因素是重金属离子的初始浓度,腐殖酸与重金属在高环境浓度时主要发生交换吸附作用,低环境浓度时主要发生螯合作用〔24〕。
2.2 腐殖酸对重金属的吸附研究
程亮等〔25〕探究了平均粒径为60 nm的腐殖酸动态吸附镉离子的吸附解吸能力,研究表明,其所制备的纳米腐殖酸经30次吸附、再生后基本无形貌变化,其所含的氨基等活性官能团对镉离子的吸附起到了积极影响。胡立芳等〔26〕以危废焚烧残渣中的铜为处理对象,研究了腐殖酸与钙盐对其产生的作用,研究结果表明,残渣中铜的浸出毒性降低程度与腐殖酸、钙盐的添加量有一定关系,而腐殖酸与钙盐的协同稳定化作用比单因素腐殖酸或钙盐具有更强的稳定化效果。蒋海燕等〔27〕将腐殖酸进行改性,制备出不溶性腐殖酸,从等温吸附、热力学吸附等方面分析其对铀的吸附,同时,以FTIR与扫描电子显微镜(SEM)分析不溶性腐殖酸对铀的去除机理,研究表明,在35℃,pH=5的条件下,1.4 g/L的不溶性腐殖酸对铀的去除率可达到99.37%,其对铀的吸附是自发、放热反应,且疏水基团增多,不溶性增强,主要通过羧基与酚羟基和铀发生离子交换以及氨基与醇羟基和铀发生络合作用吸附铀。王维等〔28〕将水铁矿、腐殖酸掺杂黄河乌海段沉积物制成吸附剂,研究该吸附剂对水体中镉的吸附效果及影响因素,研究表明,掺杂腐殖酸的沉积物比掺杂水铁矿的沉积物吸附效果更优越,沉积物对Cd2+的吸附量随着腐殖酸掺杂比例的升高而增大。
这些研究显示,腐殖酸中所含的酚羟基、醇羟基、羧基、氨基等活性官能团对重金属吸附起到主导作用,在pH较低时吸附性能非常优越。在腐殖酸中掺杂其他材料如盐类、铁氧化物等,制得的吸附剂稳定性较单体系腐殖酸大大增加,且解吸率低。
3 腐殖酸-铁氧化物复合材料
3.1 腐殖酸-铁氧化物作用机制
腐殖酸与铁氧化物可通过配位交换、疏水作用、范德华力等方式结合。其中配位交换被大多研究认为是腐殖酸与铁氧化物之间最主要的结合机理,即:腐殖酸中呈酸性的羧基等官能团与铁氧化物表面呈碱性的羟基发生配位反应〔29〕。有研究表明,疏水作用也能促使腐殖酸附着在铁氧化物表面〔30〕。在背景电解质浓度较高时,范德华力才会对铁氧化物表面吸附过程产生较大的影响,一般情况下对吸附过程的作用较小〔31〕。铁氧化物与腐殖酸的结合态分为吸附态与共沉淀态2种。吸附态即腐殖酸包裹在铁氧化物表面上;共沉淀态则是当铁氧化物对腐殖酸达到吸附饱和状态时,腐殖酸在其表面形成一层薄膜,从而改变铁氧化物的表面形态〔32〕。
研究表明,在腐殖酸与铁氧化物的吸附或共沉淀过程中,pH、离子强度、腐殖酸种类等外界因素都会对其交互过程产生影响:在pH较低时,铁氧化物表面会出现质子化,使得吸附腐殖酸的能力增强;在pH较高时,铁氧化物表面会出现高度亲和腐殖酸的吸附位点,使得吸附腐殖酸能力增强〔33〕。范德华力与配体交换作用等使得离子强度上升,也会增加铁氧化物表面对腐殖酸的吸附量〔34〕。腐殖酸种类繁多,因此其活性官能团种类与性质丰富多样,致使铁氧化物表面对不同种类腐殖酸的吸附能力也有显著不同,如具有羧基等酸性官能团的含量高、芳香族结构含量较大、分子质量较大等性质的腐殖酸都更易被铁氧化物吸附。
铁氧化物对腐殖酸吸附或共沉淀的过程会使得铁氧化物表面性质发生变化。主要表现为:表面电荷电位降低,使得复合材料凝结力升高;粗糙度增大;比表面积与孔径大小均有下降;团聚现象更加明显〔35〕。
3.2 腐殖酸-铁氧化物对重金属的吸附研究
管宇立〔15〕制备了多种铁碳比的水铁矿-腐殖酸共沉物,从吸附动力学、等温线等方面分析共沉物对Cd2+的吸附过程,同时以X射线衍射仪(XRD)与SEM等手段分析共沉物对Cd2+的去除机理。结果表明,虽然相较于水铁矿,共沉物的比表面积、孔隙容量、孔径大小均略有降低,但是共沉物在等温吸附实验中显示出更大的吸附容量。研究显示,吸附大致分为两个阶段,前期过程出现的是外部液膜扩散,随后直到吸附平衡则呈现为颗粒内扩散过程,并且解吸量都很小。
谢水波等〔36〕制备了腐殖酸改性针铁矿,在一定条件和作用时间下,几乎能完全去除5 mg/L含铀废水中的铀,其机理主要是改性针铁矿表面所含的羟基和羧基等与铀作用,表现为离子交换、内层络合作用。
罗文倩等〔37〕研究了针铁矿-腐殖酸复合胶体对Cd2+的吸附性能。结果表明,相较于单体系针铁矿,针铁矿-腐殖酸复合胶体的吸附性能有显著提高,且解吸量有所降低。通过计算吸附自由能变化量,推测Cd2+在复合胶体中的吸附行为是物理吸附,氢键、范德华力等作用可能是其吸附机理。
肖萍〔38〕研究了胡敏酸-针铁矿复合胶体对Pb2+环境行为的影响,研究表明,在一定温度条件与离子强度下,且pH为4.0~7.0时,酸度与复合胶体对Pb2+的吸附强度和饱和吸附量成正相关,吸附平衡常数也随之增大。相较于单体系的胡敏酸与针铁矿,复合胶体的吸附能力增强、解吸率降低。
王丹丽等〔39〕制备了针铁矿-腐殖质复合胶体,研究了其对重金属离子吸附-解吸的性能。研究发现,在25℃、pH=4时,与针铁矿、腐殖质的单体系比较,针铁矿-腐殖质复合胶体对Cu2+、Zn2+的吸附作用更加强烈,并且与单体系针铁矿和腐殖酸相比,该复合胶体在水溶液中均匀性好,能实现稳定沉降。
上述研究中不同铁氧化物-腐殖酸复合物对不同种重金属离子的吸附作用情况见表2。
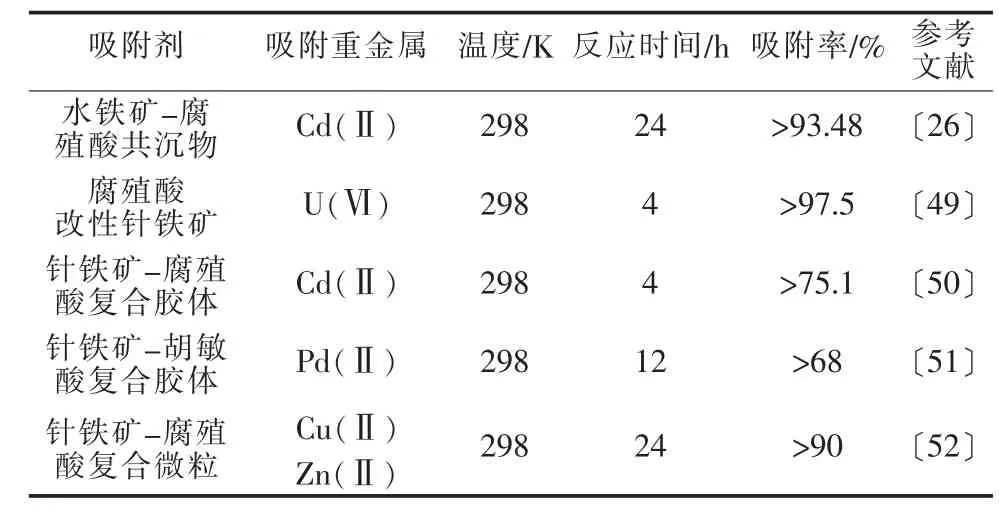
表2 不同铁氧化物-腐殖酸复合物对重金属离子的吸附作用
由表2可知,相较于单体系腐殖酸与单体系铁氧化物,腐殖酸-铁氧化物复合材料对重金属表现出更大的吸附能力,且材料均匀性增强,解吸率降低。腐殖酸-铁氧化物对重金属的吸附机理可能为络合作用、范德华力作用等。pH为复合材料吸附性能的主要影响因素,pH越低,复合材料对重金属的饱和吸附量与吸附强度、吸附平衡常数越大。
4 目前存在的问题与展望
4.1 目前存在的问题
当前关于腐殖酸-铁氧化物复合材料的研究主体大多为水体中的重金属,但复合材料密度大于水,投加量过大会使得复合材料堆积在水底,实际参加反应的复合材料与投加量有差距,导致重金属污染物去除效果低于预期值,可以考虑通过外加机械作用,利用搅拌形式将复合处理与待处理废水充分混合,提高反应效率。
虽然已有大量研究表明腐殖酸-铁氧化物复合材料对重金属吸附性能良好,易使重金属离子聚合沉淀,且解吸率低。但是目前仍缺少处理负载重金属复合材料废渣的研究报道,若按照传统铁氧体沉淀法处理废渣的方法〔40〕,需要将负载重金属的吸附材料废渣暴露在环境温度为70℃以上的空气中进行缓慢氧化,操作时间长、能耗大,不利于资源充分利用。关于腐殖酸-铁氧化物复合材料处理重金属的研究,pH均有限定范围,在酸性条件下复合材料吸附能力会增强,但在偏碱性条件下则需将pH调节至酸性,在实际应用中无形中增加了处理成本,今后的研究可以从复合材料改性入手,扩大其适用pH范围。从已有研究来看,腐殖酸-铁氧化物复合材料对大多数重金属离子的吸附性能较好,但无法处理低浓度的重金属污水,在实际应用中需要进行后续处理才能达到排水标准,增加了处理成本、限制了该复合材料的实际应用。
4.2 展望
腐殖酸作为一种来源众多且广泛分布于自然环境中的高分子有机物,含有大量复杂多样的活性基团,广泛应用于各领域中,而铁氧化物具有较大的比表面积以及分布着大量可变电荷的高活性表面,优良的理化性质决定了其对于去除重金属有较好的效果。因此腐殖酸-铁氧化物复合材料在处理重金属污染物方面有其独特的优势,是一类潜力极高的吸附材料。结合目前研究中出现的问题,今后应该着重对于腐殖酸-铁氧化物复合材料的回收、在低浓度重金属污染废水中的应用以及扩大其适用的pH、温度范围等方面深入研究,推动腐殖酸-铁氧化物复合材料在水处理中的广泛应用。
