放射性核素示踪技术在化学创新药人体物质平衡中的应用
2020-05-23周晓雯居文政朱萱萱施文佳王文俊阮小庶
周晓雯,居文政,朱萱萱,马 铮,施文佳,王文俊,阮小庶*
1 江苏省中医院,南京 210000;2 江苏杜瑞制药有限公司,南京 210000;3 南京百益恒安生物科技有限公司,南京 210000
放射性核素用于研究被标记的化学分子在生物体系或外界环境中的客观存在及其变化规律的一类核医学技术,示踪技术是以放射性核素或其标记的化学分子作为示踪剂,它应用核射线探测仪器通过探测放射性核素在发生核衰变过程中发射出来的射线,来显示被标记的化学分子的踪迹,达到示踪目的,在生命科学领域是一项悠久而实用的技术。
据统计,美国食品药品监督管理局(FDA)在2018年批准了59个新药[1]。除去生物制剂、多肽、内源性物质、含放射性的药物及诊断试剂外,还有开展人体物质平衡研究的新分子实体(不论剂型)41个(见表1)。内中获批的新药有30个开展了放射性核素示踪的人体物质平衡研究;余下11个新分子实体因为半衰期过长、局部用药系统暴露很低、原型回收率很高等,未开展放射性核素示踪人体物质平衡的研究。
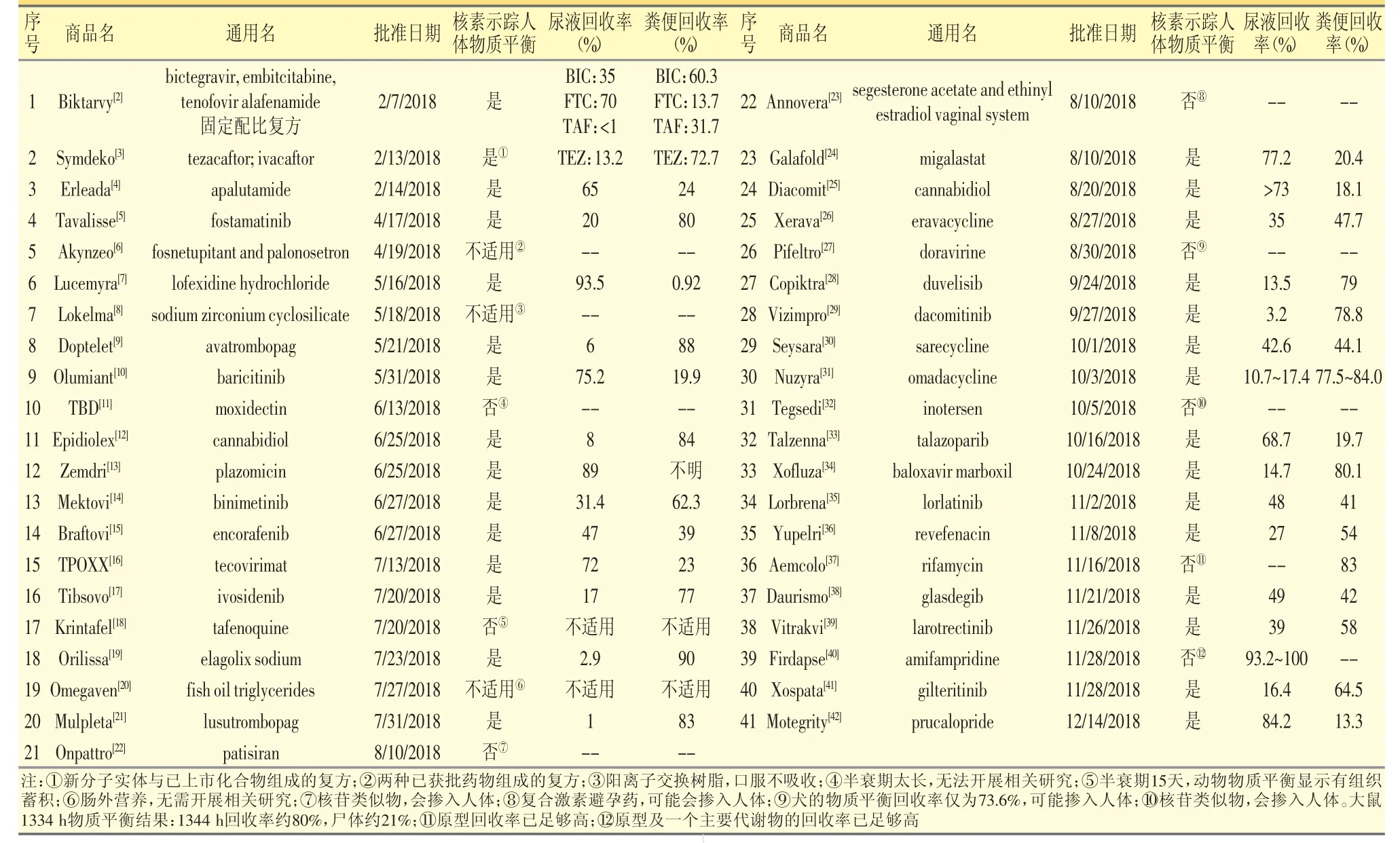
表1 2018年美国FDA批准的化药新药中应用核素示踪人体物质平衡研究的结果汇总[1]
1 放射性核素示踪的人体物质平衡研究
经14C标记的化合物分子,其结构中14C的放射性恒定,既不会增加,也不会在短期内无故消失。14C标记化合物进入人体并经代谢后,放射性核素会从原型药物转移至代谢物,最终会随着人体对化学异物的排泄过程进入粪便及尿液。放射性核素示踪的基本原理在于通过检测其放射性,由放射性的守恒来计算物质平衡。
1.1 核素选择
14C及3H为最常用的标记核素。14C及3H的半衰期足够长(分别为5730年及12.3年),使用时不需进行衰减校正。14C标记的优势是新药分子均含碳元素,14C标记不会改变标记化合物的理化性质;缺点是费用相对昂贵。3H标记的优势是标记过程简单且价格低廉,为结构复杂的天然产物标记的首选,缺点是非定位标记的3H标记化合物,其放射性易随氚-水交换而丢失。
此外,单个14C原子标记化合物的比活度为60.22 mCi·mmol-1,则100 μCi分子量400的14C标记化合物质量约为100 μCi÷60.22 mCi·mmol-1×400 g·mol-1≈664 μg。对此化合物而言,给药剂量低于664 μg无法以14C标记法进行人体物质平衡研究。由于3H标记的比活度(指放射源的放射性活度与其质量比)远高于14C,因此这种情况下若开展核素示踪人体物质平衡研究必须采取3H标记。
在人体放射性核素示踪的相关研究中,一般首选14C作为标记核素。如选择以3H标记开展体内研究,需充分验证在体内环境下不会发生氚-水交换。由于3H在人体物质平衡中应用较少,因此本文所言的放射性核素仅指14C。
1.2 标记与检测方法
一般仅将目标化合物中的一个12C原子替换为一个14C原子,以实现放射性核素标记。14C的标记位点的选择需综合考虑体外及体内代谢物鉴别的结果,选择代谢稳定位点,确保目标化合物上的14C原子不会因体内代谢而丢失。14C标记化合物的放化纯度与化学纯度一般均应≥95%,并不含有>1%的单一杂质[43]。
在放射性高效液相色谱(HPLC-FSA)法出现前,生物样品中不同代谢物的分离与放射性测定(示踪)是两个完全独立的过程:按一定的时间间隔接收HPLC分离后的馏分,以液体闪烁分析(LSC)检测每个馏分的放射性活度(DPM)后,以时间点为横坐标,以DPM为纵坐标,作离线重建代谢产物的谱图。每一个峰即代表一个代谢产物。此方法显而易见:①14C标记后以β 射线示踪具有极高的特异性,对于代谢产物的鉴别一目了然,不会漏掉主要代谢产物;②通常所有代谢产物都只含有1个14C原子,因此离线重建的DPM谱图上,每个峰的响应因子均一致,可根据峰面积比直接计算出各代谢物的浓度。此方法的主要缺点包括采集间隔过长可能导致代谢产物分离不充分、灵敏度较低、耗时长等。
FSA也可称为在线液体闪烁计数,其检测原理本质上是LSC:经色谱分离的馏分与闪烁液在检测室混合后直接进行放射性强度计数。HPLC-FSA法利用了HPLC法的高效分离能力及LSC对β 射线检测的特异性,极大地缩短了检测耗时。
1.3 给药剂量
临床试验中,给药剂量常为拟定的2期临床有效剂量。
1.4 给药方案
给药途径应与临床拟定的给药途径一致。给药频率多为单次给药,也可在多次给予未标记化合物后,再单次给予同位素标记化合物,以考察受试药物达到稳态时的人体物质平衡及血浆各代谢物的浓度。
1.5 药物配制
同位素给药辐射剂量应尽可能低。根据美国FDA颁布的《最大射线照射限值和综合安全条例》(21 CFR 361.1),受试者接受的14C的辐射剂量多为每人100~150 μCi。
在此类研究中,非标记化合物的生产应符合GMP规范。需将标记化合物与未标记化合物按照计算所得的比例均匀混合(也称为同位素稀释)后,以混悬液或填充胶囊的形式给药。
根据14C标记化合物的比活度、给药总剂量(标记及未标记化合物质量之和)、给药体积、受试者人数,可以计算出所需混合的未标记化合物质量(mg)及标记化合物的DPM,并可建立起药物浓度与DPM的换算关系:1 ng=n DPM、LSC测得n DPM及表示样品中含有1 ng的药物及其代谢产物。
1.6 受试人群
为充分保障受试者且为了减小受试者个体差异导致的结果波动,一般仅选取成年男性作为受试者。也可根据拟定的适应症选取育龄期结束的女性受试者或相应的病人。
1.7 受试者保护
以同位素标记化合物口服或静脉注射给药后,人体将受到一次内照射。人体各脏器受到的内照射损伤,取决于标记核素种类、药物相关物质在各脏器的分布、停留时间。根据同位素标记的动物物质平衡、组织分布及消除数据,受试者预计接受的内照射剂量应满足《GB_T 16148-2009放射性核素摄入量及内照射剂量估算规范》及《GB18871-2002电离辐射防护与辐射源安全基本标准》的相关规定,应符合职业照射人员连续5年每年平均有效剂量不超过20 mSv的规定。
应根据动物的14C标记药物的组织分布和/或QWBA结果,推断人体不同脏器的放射性核素暴露数据,并符合相关规定。根据我国《GB-4792-1984放射卫生防护基本标准》,对公众中个人的全身剂量限值规定如下:放射工作人员受到全身均匀照射时的年剂量当量不应超过50 mSv,5年不应超过100 mSv;公众中个人受到的年剂量当量应<5 mSv,当长期持续受到电离辐射的照射时,公众中个人在其一生中每年的全身照射的年剂量当量的限值应不高于1 mSv。
1.8 生物样本采集
在人体物质平衡研究中,采集的生物样本主要为排泄物(尿液和粪便)。此类研究通常也同时研究血浆中的主要代谢物及药物相关物质的整体清除率,因此也采集给药后不同时间点的全血及血浆样品。
尿液及粪便样品的采集方式为分别采集每位受试者给药后不同时间段内所有的尿液及粪便样品。采样的时间需足够长,一般需采集受试者服药后7~10天的所有尿液及粪便,直至排出90%以上的放射性核素,或直至受试者连续两天每天经尿液及粪便排出的放射性核素总量小于1%[44]。
全血样品的采集时间点依据原型药物的人体药代动力学结果设置。由于代谢物的半衰期可能显著长于原型药物,因此人体物质平衡研究中的全血样品采集一般会长于原型药物的采集。
1.9 样本处理
对于受试者每一时段内的所有尿液及粪便样品,均需记录重量或体积。每一位受试者各时段内采集到的粪便样品,常按1∶3的比例制备匀浆后以LSC测定总放射性(DPM·g-1)。尿液及血浆样品在脱色处理后,以LSC测定其总放射性(DPM·mL-1)。
以HPLC-FSA法进行放射性示踪的代谢物谱研究,粪便、尿液及血浆样品均需以常规的液液萃取或固相萃取法进行样品处理,并需特别关注样品预处理过程中的回收率。指导原则中指出:“样品处理(如液体样品离心去固体杂质、血浆、粪便及组织提取等)和分析(如应用HPLC和在线或离线放射性检测仪联用获得放射性代谢产物谱)应密切关注放射性的回收率,一般总回收率≥85%。应根据放射性代谢产物谱、研究获得的各代谢产物的血浆暴露量百分比和在排泄物中占给药百分率,选择需要鉴定的代谢产物,并使用HPLC在线或离线放射性检测仪帮助鉴定工作中对代谢产物的监测”[43]。
1.10 粪便、尿液及血浆中的代谢物谱
对于尿液、粪便匀浆及血浆样品,均需以HPLC-FSA法或AMS法研究代谢物谱并确定主要代谢物。由于14C标记示踪的特异性,HPLC-FSA法及AMS技术可无遗漏地鉴别出血浆、尿液、粪便中的主要代谢物的放射性谱图。然而,HPLC-FSA法及AMS技术本身均无法提供任何代谢物的结构信息。因此,还需综合质谱的碎片信息推断代谢物的结构,必要时可能还需制备标准品、确定代谢物的结构。在实际应用中,常在HPLC法对样品分离后,在色谱柱后将流动相按适当比例进行分流:一部分流动性进入FSA,对代谢物的放射性色谱峰进行定位;另一部分流动性进入质谱获得结构信息。
1.11 数据处理
粪便匀浆及尿液样品中的放射强度(DPM·g-1或DPM·mL-1)与各时段内粪便匀浆的总重量(g)或尿液体积(mL)相乘,即可得到各时段内经粪便或尿液排泄的总放射性m DPM。按上述DPM与药物相关物质含量的换算关系1 ng=n DPM,此时间段内经粪便或尿液排出体外的药物相关物质为m/nng。
综合HPLC-FSA法所得放射性色谱图及对应保留时间的质谱结果,即可无遗漏地推断出各代谢物定量结构信息。根据面积归一化法,在放射性色谱图上各色谱峰的峰面积比即为各代谢物的含量之比。
2 与传统技术的比较
在新药研发过程中,必须阐明化合物进入人体后的排泄途径。因此,人体物质平衡是其研究目的,而放射性核素示踪技术是达到这一目的的主要研究手段。对于代谢稳定性较高,尿液及粪便中主要代谢物较少的化合物,在鉴别出主要代谢物的绝对构型后,也可合成代谢物标准品以质谱定量法探明人体物质平衡。以质谱定量法进行人体物质平衡研究的难点主要来自以下3个方面:
2.1 确定主要代谢物
对于创新化学药而言,需探明给药后人体尿液、粪便及全血中的代谢物谱,并鉴别出主要代谢物,即暴露水平高于所有与药物相关物质总暴露量10%的代谢产物。
原型药物与其代谢产物的质谱及紫外因相应结构差而并不一致,无法仅凭峰面积归一化法进行绝对定量,因此以质谱定量法开展此类研究必须确定所有代谢物的绝对构型并获得相应的标准品。显然,实际操作中无法通过定量各基质中原型药物及所有代谢产物来计算各代谢产物的系统暴露比例,进而确定主要代谢物。
2.2 代谢物标准品的制备
质谱定量必须使用标准品。首先,确定代谢物的绝对构型、即是一个耗时耗力的过程;其次,即便确定了代谢物的绝对构型,在某些场合下对于结构复杂的代谢物的标准品合成,常在耗费了大量时间、费用后才发现难以实现,此时只能以更为耗时耗力、分离制备法以获得代谢物标准品。对于与时间竞赛的新药研发而言,这无疑是难以接受的。
2.3 低给药剂量下的代谢物定量
随着现代药物研发手段的不断进步,研究化学药物的药理学活性已显著增强,具体表现在药物分子量增加、结构复杂、给药剂量降低。例如,在lofexidine登记的临床物质平衡研究中,总给药剂量为400 μg,93.5%的药物相关物质经尿液排泄,原型只占15%~20%。若以质谱定量法进行人体物质平衡研究,即便能够顺利鉴定出尿中的数个主要代谢产物,后续以质谱对尿液中的微量代谢产物定量仍是一个巨大的挑战。
在人体物质平衡研究中,放射性同位素标记示踪法完全没有质谱法的上述局限性。根据放射性同位素示踪原理可知,药物原型及其所有代谢产物均通过检测其结构中标记的1个14C原子所释放的β 射线进行示踪。由于14C所释放的β射线的特异性,在HPLC-FSA谱图上只有药物原型及其代谢物能够形成14C色谱峰。在分离良好的情况下,一个14C色谱峰及代表一个原型药物/代谢产物。由于原型药物及代谢产物的响应因子一致,因此可根据面积归一化法可容易判定主要代谢物。根据各14C色谱峰保留时间的质谱碎片信息,可推断出各14C色谱峰对应的代谢物的结构。最后,结合LSC测得的样品中所有药物相关物质总浓度,即可对原型药物及各代谢物进行绝对定量,获得各生物基质中的代谢物谱。
3 实例分析
卡普韦林(capravirine)是由辉瑞公司研发的非核苷类逆转录酶抑制剂。5名健康男性受试者口服1.4 g卡普韦林及50 μCi14C卡普韦林后,其168 h内的尿液及粪便回收率分别为44.3%及42.0%。尿液和粪便样品中的原型药物浓度几乎可以忽略[45]。在0~24 h尿液样品中,至少有8个代谢物的排泄量>给药量的1%;在24~48 h粪便样品中,至少有4个代谢物的排泄量>给药量的1%。根据上述结果,如以质谱定量法进行人体物质平衡研究,则至少需鉴别并合成9个代谢产物的标准品[44]。
根据已知的人体物质平衡结果进行反推,在探索人体物质平衡结果的过程中,以质谱定量法进行卡普韦林人体物质平衡研究,需耗费大量时间、精力来合成代谢物标准品,实际上很难实现。放大看去,在创新药研发过程中,即便有充分的动物DMPK数据,判断人体的主要代谢物已是一个十分复杂的过程,后续的代谢物绝对构型鉴别及质谱定量过程实际上不具有可操作性。
4 我国核素示踪人体物质平衡研究的现状
至2019年10月,在www.chinadrugtrials.org.cn药物临床试验公示平台上,以“14C”为关键词搜索,共有24条结果。经分析,21项研究使用了14C标记化合物,20条包含了14C标记的人体物质平衡研究的相关内容。由表2看,我国放射性核素示踪人体物质平衡研究起步较晚,但近年发展较为迅速。
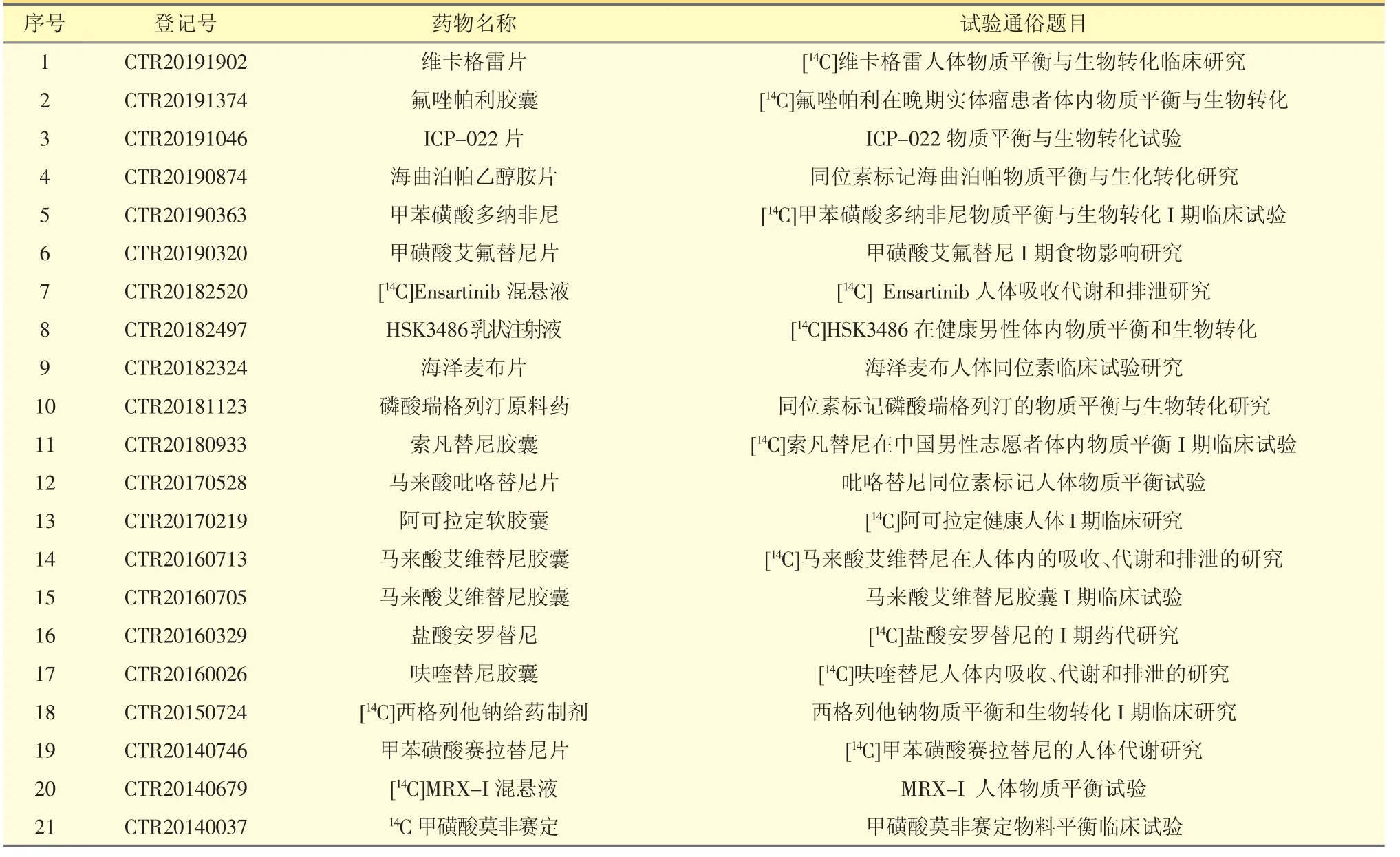
表2 我国14C相关研究开展结果
5 放射性核素示踪技术在推动我国创新药研发上的重要作用及广阔应用前景
放射性核素物质平衡研究能获得药物的排泄途径,阐明药物在体内主要生物转化途径,能有效进行代谢产物鉴定,确定人体循环中是否存在不成比例的代谢物,判定临床前的药理及毒理研究是否充分,同时考察潜在的代谢相互作用。同位素示踪研究能动态监测药物在体内的分布情况,阐明药物的靶标结合和脱靶情况,为实现早期疗效预测提供有效方法。放射性同位素及影像示踪技术在物质平衡、药代药效学评估、药物临床研究中具有不可替代的优势。放射性示踪技术为解决我国临床药物治疗应用的精准化、个性化提供了一种技术手段。目前国内没有发布同位素人体临床试验相关指导原则。相信随着新药、尤其是一类新药的不断上市,相关主管部门的政策导向也是推动同位素及影像示踪技术发展的关键之一。建设同位素示踪技术平台,建立相应的指导原则及相关研究体系势在必行。
6 小 结
无论以加速器质谱检测14C原子,还是以离线/在线液体闪烁计数检测14C原子释放的β 射线,放射性核素示踪技术在人体物质平衡研究中被广泛应用的根本原因在于其示踪的高度特异性。该技术的优势有两点:①在不知代谢物谱及无需标准品的情况下迅速准确地获得生物基质中所有药物相关物质的总量;②14C标记的原型药物及其所有代谢物在示踪检测中的响应值一致,因此可根据面积归一化法确定各代谢物含量的比例,进而无标准品下实现对各代谢物定量。
通过回顾不难看出,美国FDA近年来批准的新分子实体药物绝大多数均通过放射性核素示踪技术,完成了人体物质平衡研究,由此看出,现阶段该技术在人体物质平衡研究中的“金标准”地位。随着我国近年来在创新药研发领域的蓬勃发展,可以预见放射性核素示踪技术必将在人体物质平衡研究中有着广阔的应用前景。
