低度恶性纤维黏液样肉瘤3例临床病理分析
2020-05-22江锦良
詹 媛,江锦良,蔡 勇
低度恶性纤维黏液样肉瘤(low grade fibromyxoid sarcoma, LGFMS)属罕见的纤维肉瘤亚型,好发于青年人,男性多于女性。常发生于下肢、躯干,表现为局部缓慢生长的软组织肿块[1-2]。LGFMS表现为“良性”的形态学特点,却具有低度恶性的生物学行为,本文回顾性分析3例LGFMS的临床病理学特征、免疫表型等,并复习相关文献,旨在提高对该病的认识水平。
1 材料与方法
1.1 临床资料 例1男性,48岁。因发现左侧胸前肿块入院。体检:肿物大小6 cm×3 cm,界限尚清,质硬、无压痛,皮温不高,触痛觉正常。胸部CT示左侧胸小肌见境界欠清的稍低密度肿块,最大断面6.8 cm×3.3 cm,左侧第4肋骨前段局部骨密度不均匀,考虑软组织恶性肿瘤。遂行手术切除术,术后标本送病理检查。例2男性,61岁。自述平日无明显症状,偶然发现右大腿肿物,大小12 cm×8 cm,边界尚清,质地较硬,活动后稍感压痛,无局部搏动感。MRI示右侧股外侧肌内占位,考虑恶性黏液性软组织肿瘤(黏液性纤维肉瘤)可能性大。例3男性,46岁。无意间发现左臀部肿物,当地医院MRI检查提示左侧臀大肌占位,考虑软组织恶性肿瘤。后入住我院进一步治疗。体检:肿物表面皮肤颜色正常,皮温略高,无红肿、压痛,肿物大小6 cm×4 cm,界限清楚,活动度尚可,质地较韧。
1.2 方法 将标本均匀切开后置于10%中性福尔马林中充分固定12~24 h,经脱水、包埋、切片、HE染色后光镜观察。采用免疫组化EnVision法进行染色,所用抗体包括MUC-4、CD34、vimentin、SMA、desmin、CK、actin、Ki-67、BCL-2等。抗体试剂盒购自于福州迈新公司,操作步骤严格按试剂说明书操作。
2 结果
2.1 眼观 例1肋骨及周围软组织切除标本,大小10 cm×7 cm×3 cm,肋骨旁见一灰白色质中肿块,大小7.2 cm×6 cm×3 cm,肿瘤破坏肋骨皮质。例2组织一块,带少许皮肤,组织大小15 cm×12 cm×7 cm,切开见一大小10 cm×7.2 cm×5.4 cm的黄白色质中肿块,部分区有黏液。例3带皮组织一块,大小14.5 cm×9 cm×4.5 cm,切开见一灰白、灰黄色肿物。肿物大小6.5 cm×4.6 cm×4 cm,质韧,内可见一囊,直径3.6 cm。
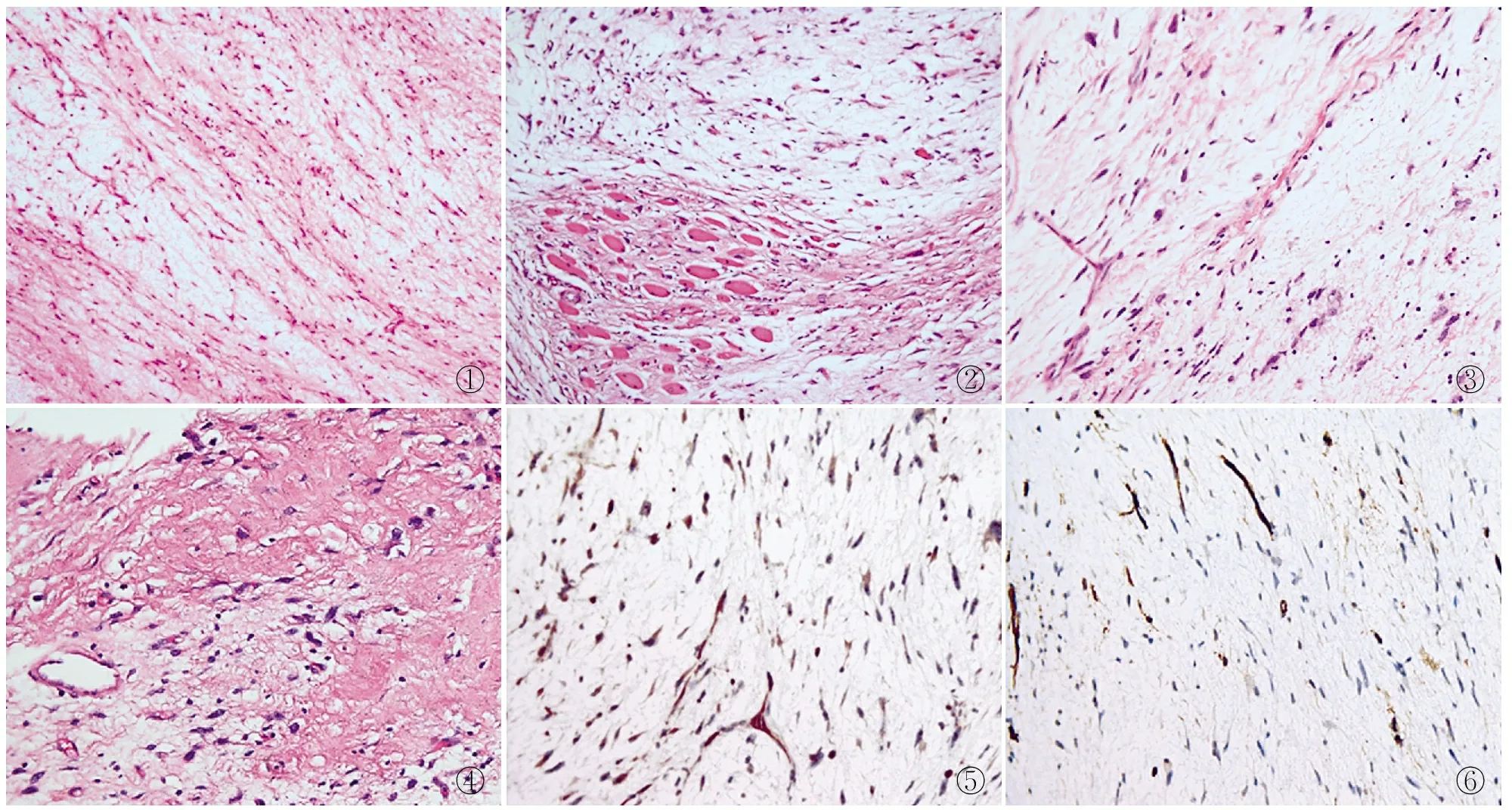
2.2 镜检 肿瘤由交替性的黏液样区和胶原纤维区组成(图1),肿瘤侵犯横纹肌组织,呈浸润性生长,形成横纹肌岛(图2),肿瘤由形态上温和的梭形细胞构成,核深染、卵圆形,异型性小,核分裂少见。细胞呈束状、涡旋状排列,间质中见少量曲线形小血管(图3)。肿瘤组织中具有特征性的圆形或不规则形巨菊形团结构(图4)。
2.3 免疫表型 肿瘤细胞MUC-4(图5)和vimentin(+),SMA少量(+),CD34(-)(图6),Ki-67增殖指数为10%。
2.4 病理诊断 3例均为LGFMS。
3 讨论
3.1 临床表现 LGFMS于1987年由Evans等首次报道并命名,采用临床病理学及分子遗传学研究证实其为纤维肉瘤的特殊亚型,故又被称为“纤维黏液样型纤维肉瘤”[1-2]。该肿瘤可发生于任何年龄段,年龄2~78岁,以中青年多见,男性多于女性。LGFMS多位于大腿、躯干、臀部,也见于腹膜后、头颈部、消化道、网膜等部位。临床表现为缓慢生长的无痛性软组织肿块,直径1~18 cm,肿物可持续数年且不易被发现[3-4]。肿瘤多位于筋膜下或肌肉内,发生于浅表部位者多为儿童和青少年。临床上LGFMS主要行手术切除治疗,局部复发率较高,但总体预后较好[5]。本组3例患者均为中年男性,年龄48~61岁,平均51岁,临床以“无痛性软组织肿块”为首要症状,发生部位分别为胸壁、下肢及臀部。肿物直径较大(6.5~10 cm),均于横纹肌组织内生长,其中1例有周围骨质破坏。
①②③④⑤⑥
图1 丰富的胶原纤维束与黏液样区相间排列 图2 肿瘤侵犯横纹肌组织 图3 肿瘤细胞无明显异型,间质内可见弧线形小血管 图4 特征性的不规则形巨菊形团结构 图5 肿瘤细胞MUC-4(+),EnVision法 图6 肿瘤细胞CD34(-),EnVision法
3.2 病理及分子遗传学特征 LGFMS为低度恶性的软组织肿瘤,具有较为“温和”的形态学特点,但却向周围组织内呈浸润性生长。镜下表现为丰富的胶原样区与黏液样区相间排列,以胶原样区为主。肿瘤细胞呈梭形或短梭形,无明显异型性。核深染、卵圆形,有一个或多个核仁,核分裂象少见。肿瘤细胞呈短束状和特征性的涡旋结构排列,间质内可见少量曲线形的小血管[6-7]。40%病例在肿瘤组织中具有特征性的圆形或不规则形巨菊形团结构,其中央为致密的透明变性胶原纤维,周围围绕圆形或卵圆形细胞,故又被称为“伴巨大菊形团的玻璃样变梭形细胞肿瘤”。在复发或转移的病例中肿瘤细胞丰富、密度明显增加,并可见核分裂象[8]。当病理形态不典型时,免疫组化对诊断则提供很大的帮助。肿瘤细胞中MUC-4弥漫强表达且阳性率近乎100%,可表达vimentin及肌源性标志物(SMA、MSA)。有研究发现LGFMS偶可表达BCL-2、CD99、p63、EMA,不表达CK、S-100、CD34、β-catenin。近年来,有关LGFMS的分子遗传学研究取得一系列进展,研究发现超过90%LGFMS病例存在t(7;16)(q32-34;p11),形成FUS-CREB3L2基因融合。部分病例则t(11;16)(p11;p11),形成FUS-CREB3L1基因融合[9]。免疫组化及分子检测的广泛应用为我们诊断LGFMS提供依据。但值得注意的是虽MUC-4可表达于所有的LGFMS病例,但并不是绝对特异性标志物。MUC-4可在滑膜肉瘤(30%~90%)及硬化性上皮样纤维肉瘤(78%)中表达[10],而后者也存在FUS-CREB3L1基因融合。
3.3 鉴别诊断 LGFMS需与以下几种软组织肿瘤鉴别:(1)黏液样纤维肉瘤(myxofibrosacoma, MFS),好发于老年患者,平均年龄60岁,多位于皮下组织。MFS低倍镜下呈结节状,由不完整的纤维组织分隔。其黏液的分布较为广泛,细胞具有明显异型性及多形性,可见假脂肪母细胞及核分裂象,免疫组化标记MUC-4(-),CD68(+);LGFMS好发于青年人,平均年龄30岁,多位于深部肌肉组织内。LGFMS中黏液区与纤维区交替分布,细胞无或轻度异型性及核分裂象,具有特征性的巨菊形团结构,免疫组化标记MUC-4(+),CD68少量(+)。(2)黏液样神经纤维瘤,肿瘤背景呈黏液样或胶原黏液样,细胞呈短梭形或卵圆形,具有更为纤细和卷曲的细胞核,免疫组化标记S-100(+)。(3)富细胞性黏液瘤,极易误诊为LGFMS,形态学上可寻找是否存在特征性巨菊形团结构及交替分布的黏液纤维区,并结合免疫组化MUC4、vimentin的表达予以鉴别。(4)黏液样隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans, DFSP),发生于浅表部位的LGFMS与DFSP较难鉴别。DFSP常侵犯周围脂肪组织,肿瘤具有席纹状的排列方式,无交替分布的黏液纤维区,免疫组化标记CD34(+),MUC4(-)。
综上所述,LGFMS是一种罕见的纤维肉瘤亚型,以中青年多见。肿瘤好发于软组织深部,故疾病初期患者往往不易察觉。我们在诊断过程中需要充分结合患者的临床表现、影像学资料及病理形态特征,必要时可通过免疫组化(尤其是MUC-4)及分子检测加以鉴别,避免误诊。
