老年骨科大手术患者术前衰弱风险评估模型的构建与评价
2020-05-21胡雁真王蕾曹志丹王燕陈晓英
胡雁真,王蕾,曹志丹,王燕,陈晓英
衰弱作为一种生物综合征,是指个体由于生理功能储备减少或失衡,从而对外界压力源的抵抗力下降、易损性增加的一种状态[1]。依据2016版《中国骨科大手术静脉血栓栓塞症预防指南》[2],本研究将骨科大手术定义为膝关节置换术、髋关节置换术及髋部周围骨折手术。一项来自英国国家统计局的数据显示,膝髋关节置换术中仅15%的患者年龄在60岁以下[3],而在髋部骨折中,60岁以上老年患者的比例高达90%[4]。多项研究表明,骨科大手术患者术前衰弱是影响术后并发症、住院时间及病死率的独立危险因素[5-7],但衰弱仍未成为术前评估的常规内容。依据衰弱循环理论,由于年龄、疾病等因素导致患者肌质量及总能量消耗下降,引发营养不良的发生,进一步加重肌肉萎缩,从而形成恶性循环,最终导致衰弱[8]。依据健康累计缺陷理论,可认为衰弱是一种多维动态的过程,与个体躯体、功能、心理、社会等方面均相关[9]。鉴于目前国内外对衰弱的金标准缺乏普遍共识[10],各工具间的异质性较大[11],影响对骨科大手术老年患者衰弱的判断。本研究旨在探讨骨科大手术老年患者术前衰弱的相关因素,构建风险评估模型,为护理人员早期识别衰弱高危人群、制定术前优化策略提供参考。
1 对象与方法
1.1对象 采用便利抽样法,纳入2019年9~12月在天津医院关节外科及髋关节病区择期骨科大手术患者。纳入标准:年龄≥60岁;拟行膝髋关节置换或髋部骨折手术;意识清楚,能进行交流;患者及家属知情同意。排除标准:重度听力及认知障碍;合并恶性肿瘤或处于疾病终末期。共纳入384例患者,男75例,女309例;年龄60~94(71.36±7.98)岁。膝关节置换术162例,髋关节置换术132例,髋部周围手术90例。
1.2方法
1.2.1研究工具
1.2.1.1一般资料调查表 由研究者通过文献回顾后自行设计,包括性别、年龄、月收入、文化程度、居住方式、婚姻状况等。
1.2.1.2FRAIL衰弱量表 用于评估患者术前衰弱状态,由国际老年营养学会提出[12],是中华医学会老年医学专家推荐使用的术前衰弱评估量表[13]。共包含5个条目:过去1个月常感疲倦;独自上一层楼有困难;独自行走一个街区(500 m)有困难;患有5种以上疾病;最近1年内不明原因体质量下降5%以上。符合3项以上表示存在衰弱,1~2项表示衰弱前期。本研究将衰弱前期与健康状态统称为非衰弱。
1.2.1.3查尔斯共病评估表(Charlson Comorbidity Index,CCI) 用于评估患者术前共病情况。由疾病评估、严重程度评估及评分系统3部分组成,共包括19种疾病,根据疾病严重程度分别赋疾病1、2、3、6分;根据年龄进行分值调整,50~59岁计1分,每增长10岁,增加1分[14]。
1.2.1.4运动耐量评估表 用于评估患者入院前的体力活动强度即代谢当量(METs)[13]。该量表为自我报告式量表,共10个条目,3个METs等级:前4个条目为1 METs,表示运动耐量差,最后1个条目为10 METs,表示运动耐量良好,其余为4 METs,表示运动耐量中等(4 METs相当于能够从事简单的家务劳动、爬一段楼梯或小山坡)。
1.2.1.5简版老年抑郁量表(Geriatric Depression Scale-15,GDS-15) 用于评估患者1周内的心理状况。唐丹[15]将该量表应用于大陆老年人,其Cronbach′s α系数为0.793,1周重测信度为0.728,信度良好。问卷包括不愉快、冷漠和焦虑、失去希望、记忆丧失和社会活动减少4个维度,共15个条目,其中4个条目反向计分(回答“否”表示抑郁)[16]。总分0~15分,得分≥6分表示有抑郁倾向,分数越高,抑郁倾向越显著。
1.2.1.6微型营养评定简表(Short-Form Mini-Nutritional Assessment,MNA-SF) 用于评估老年个体的营养状况。由Kaiser等[17]在MNA的基础上修订,共6个条目,总分0~14分,12~14分为营养状况正常,8~11分为有营养不良风险,<8分为营养不良。有研究将MNA-SF与MNA比较发现,两量表一致性高度一致[18],但MNA-SF操作方便,内容精简,更适用于住院患者。
1.2.2资料收集方法 研究者在征得医院同意后采用面对面访谈的方式完成问卷填写,FRAIL量表在术前1 d评估,其余量表在患者入院当天测评。调查过程中采用统一的指导语,如有视物模糊、填写不便者,调查员协助完成。问卷由调查员检查无误后当场收回。
1.2.3统计学方法 使用SPSS20.0软件对数据进行t检验、Mann-WhitneyU检验、χ2检验;检验水准α=0.05。采用Logistic回归分析构建预测模型。使用Medcale软件对模型进行受试者操作特征(ROC)曲线分析,计算曲线下面积(AUC)、灵敏度、特异度、约登指数。AUC 0.5~表示预测效能低,0.7~表示预测效能中等,0.9~1.0表示预测效能高。
2 结果
2.1骨科大手术患者术前衰弱发生情况 本组患者存在衰弱194例(50.5%);5个衰弱指标发生率由高到低依次为:独自行走一个街区有困难255例(66.4%);独自上一层楼有困难231例(60.2%);过去1个月常感疲倦167例(43.5%);不明原因的体质量下降139例(36.2%);患有5种以上疾病112例(29.2%)。
2.2骨科大手术患者术前衰弱影响因素分析
2.2.1骨科大手术患者术前衰弱的单因素分析 不同特征骨科大手术患者术前衰弱发生率比较,见表1。是否衰弱患者入院前运动耐量、营养状况、CCI得分、抑郁得分比较,见表2。

表1 不同特征患者衰弱发生率比较 例
2.2.2骨科大手术患者术前衰弱多因素分析 以是否存在衰弱(0=无衰弱,1=衰弱)为因变量,将单因素分析结果中有统计学意义的因素作为自变量,纳入二元Logistic回归分析(α入=0.05,α出=0.10),结果显示,年龄、记忆丧失与社会活动减少、营养不良、共病是其独立危险因素结果见表3。对Logistic回归分析结果中各自变量的β值以最小β值0.334为基数,其他变量β值与其相除,得出各变量赋值分数,最终得出公式:Y=10×X1+17×X2+38×X3+13×X4。变量赋值分数见表4。各变量的具体计算方式为:若患者年龄≥80岁,则X1为2,≤80岁则为0;若患者被评为营养不良,则X3为2,不符合则为0;记忆丧失和社会活动减少(X2)、CCI得分(X4)均以该患者的实际得分进行计算。

表2 衰弱与非衰弱组运动耐量、营养状况抑郁得分、CCI得分比较

表3 预测患者术前衰弱的Logistic回归分析结果
注:自变量赋值营养良好=0,有营养不良风险=1,营养不良=2;年龄60~69岁=0,70~79岁=1,≥80岁=2;CCI得分、记忆丧失和社会活动减少按实际分值代入。
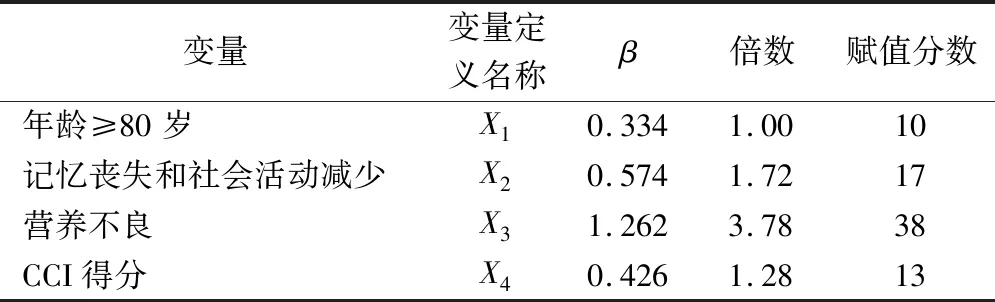
表4 变量赋值分数
2.3ROC曲线对预测模型的诊断效能 根据预测模型公式计算患者得分,以该得分为检验变量,以FRAIL衰弱量表得分为预测变量,绘制ROC曲线(图1),结果显示ROC曲线下面积为0.727,95%CI(0.675~0.778),与面积为0.5相比,差异有统计学意义(P<0.05)。当预测模型分数为72时,约登指数最大(0.422),其灵敏度为0.722,特异度为0.700,因此72分作为术前衰弱风险预测模型的最佳临界分值。

图1 预测患者术前衰弱的ROC曲线
3 讨论
3.1骨科大手术老年患者术前衰弱相关因素分析
3.1.1年龄 研究结果显示,年龄与衰弱发生风险呈正相关,≥80岁患者发生衰弱的风险是60~69岁患者的1.321倍,本研究中衰弱的年龄分界与方海燕[19]研究结果一致,但高于社区及内科住院老年患者,其原因可能是接受骨科大手术的身体条件需达到手术标准,因此参与本研究的低龄老年患者相对健康。但≥80岁老年人骨密度流失多,肌肉质量下降,更易诱发骨折。但为减少保守治疗的并发症及病死率,骨科大手术仍是高龄老年人的首选治疗方法。Belmont等[20]研究表明,年龄≥80岁是髋部骨折患者术后出现并发症的主要危险因素,扭转衰弱状态可以减少术后并发症的发生。因此,医护人员应重点关注高龄患者的术前状况,筛查衰弱高危人群,充分评估其对手术的耐受状况。另外,为高龄患者制定专门的术后锻炼可能更有利于术后康复。
3.1.2记忆丧失与社会活动 研究结果显示,老年患者记忆丧失和社会活动减少每增加1分,发生衰弱的风险增高1.775倍,本研究将老年抑郁量表的4个维度分别进行因素分析,仅该维度进入回归方程模型。郑静等[21]研究发现,老年人衰弱与记忆力下降有关,记忆力下降是轻度认知障碍的危险因素,而认知障碍与衰弱有共同的病理生理机制。因此,医护人员应及早采取认知干预措施,预防术后谵妄的发生。有研究表明,社会活动减少是增加老年人失能、发病率和病死率的危险因素[22]。骨质疏松引起的骨性关节炎及骨折是老年人接受骨科大手术的主要原因,而由骨质疏松症导致的疼痛削弱患者的治愈信心,降低社交意愿,从而产生社会孤立和孤独感,加快衰弱进程。医护人员可对患者采取病友同伴支持干预,鼓励患者间沟通交流,改善抑郁症状。
3.1.3营养不良 本研究发现,营养不良患者发生衰弱风险是营养良好患者的3.531倍。骨科老年患者术前由于饮食习惯改变,营养摄入减少,精神状态及机体逐渐退化,从而增加术前营养不良的风险[23]。营养不良患者更容易出现骨质疏松和肌肉质量下降,后者是引起肌少症的重要因素,肌少症与衰弱相互重叠[24],因此营养不良可作为衰弱的一个关键特征[25]。由于老年患者肌肉质量和力量的维持依赖于日常蛋白质的摄入,因此需调整其饮食结构,增加蛋白质摄入。亚太临床实践指南[26]推荐老年人补充必需氨基酸,如富含亮氨酸的乳清蛋白会增加老年肌少症患者的肌肉质量,提高其腿部功能。
3.1.4共病指数 表3显示,CCI得分每增加1分,术前衰弱风险升高1.532倍。英国一项研究发现,同时患有4种以上疾病的老年患者发生衰弱的风险显著升高(OR=27.1)[27]。有报道称,我国老年髋部骨折合并基础疾病的患病率在45%以上[28]。因此,医护人员应充分做好骨科大手术老年患者的术前基础疾病筛查,评估手术风险,加强多学科团队协作,减少术前衰弱的发生。
3.2骨科大手术患者术前衰弱风险预测模型的研究意义 有关衰弱常用的两个测量工具分别为Fried衰弱表型(Frail Phenotype,FP)及Rockwood衰弱指数(Frail Index,FI)[29],但该诊断工具不适用于骨科手术患者的快速术前评估,FP需要现场测量患者自然状态下的行走速度[30],FI则包含30~70项条目,数量繁多。因此本研究选用最快速简便的FRAIL衰弱量表以确定衰弱类别。
衰弱是预测骨科大手术患者死亡的独立危险因素[31]。术前衰弱增加术后并发症及死亡风险。本研究结果表明接受骨科大手术患者的术前衰弱发生率较高,若未得到及时有效的处理,必然会影响患者术后功能恢复及生活质量。因此通过构建衰弱风险评估模型,帮助临床护士简单高效地识别衰弱高危人群,有目的地应对患者当前存在的衰弱风险因素,当评估分数接近72分时,提示存在衰弱的风险,护理人员应提高警惕,有针对性地进行干预,帮助患者摄入足够的营养,及时纠正患者的营养水平。积极采取多学科协作模式,对患有基础疾病的患者提供相应的干预措施。重点关注高龄及抑郁患者,与患者建立信任关系,引导其缓解抑郁情绪等。此外,在实际工作中护理人员应根据患者的特征及自身专业判断对模型进行适当调整,在不断更新中更好地使模型适用于临床情景。
4 小结
本研究发现,拟行骨科大手术的老年患者术前衰弱发生率较高,但衰弱评估目前尚未纳入常规术前评估。本研究构建的术前衰弱预测模型,通过多维度综合预测骨科大手术术前衰弱患者,可考虑推广应用。但仍需通过大样本、多中心的前瞻性数据继续修订调整,以适应临床需要。
