硝酸体系中Pt催化肼的分解
2020-05-20肖松涛李辉波欧阳应根
王 妍,肖松涛,李辉波,欧阳应根
中国原子能科学研究院 放射化学研究所,北京 102413
肼,作为铀钚还原分离系统的支持还原剂[1-2],在后处理过程中已经得到了广泛应用。在后处理流程中,为了抑制1B、2B萃取器中亚硝酸的破坏作用,需向体系中加入支持还原剂,它不仅能保护还原剂,还能防止还原产物Pu(Ⅲ)不再被氧化。在进入钚纯化之前,必须将1BP中残留的支持还原剂肼破坏,然后再选用适合的氧化剂将Pu(Ⅲ)氧化为Pu(Ⅳ)。
Pt具有良好的催化性能,可用Pt催化法分解肼[3-4]。与传统的亚硝酸钠或亚硝气氧化法破坏肼相比,Pt催化法分解肼具有不引入其它离子、废液或废气处理量小等优点,是值得在后处理工艺中研究的方法。
从20世纪90年代末开始,国内外的学者先后发表了许多关于Pt催化氧化肼的文献。例如,Ananiev等[4-6]分别考察了硝酸、非硝酸以及弱碱体系下Pt/SiO2催化分解肼的动力学并推测了其反应机理;常利等[7]研究了在硝酸介质中温度、酸度等条件对Pt催化肼分解的影响。
然而,后处理过程的最大特点是处理的对象是经过解体的强放射性物料,具有极强的放射性(如α、β、γ、中子等)。在实际反应体系中,用Pt催化法破坏后处理料液中的肼时,就不得不考虑放射性对催化过程的影响,而这些影响可能会抑制或促进催化体系的效率。已有的研究表明[8],β放射性对催化氧化还原反应具有提高作用,可以提高合金在氧化还原反应中的催化作用。不仅如此,在后处理过程中,裂片产物合金颗粒中的β放射性同位素(99Tc、107Pd及196Ru),也能够提高裂片元素的催化作用[9]。
本工作结合后处理流程的实际需要,拟通过实验探究硝酸体系中肼的初始浓度、温度、硝酸浓度、催化剂的用量(S/V)等对Pt催化分解肼的影响。实验采用电子加速器产生的电子束模拟β放射性,初步探究β放射性对硝酸体系中Pt催化分解肼行为的影响,从而为后处理过程中肼分解的工艺提供一定的基础数据。
1 实验部分
1.1 主要试剂和仪器
硝酸、水合肼、甲烷磺酸等试剂,均为分析纯,北京化学试剂公司。催化剂:Ti基Pt材料(以下简称Pt-Ti网),环网状,佛山市金誉五金筛网有限公司。其中镀铂层厚度为4 μm,高度为30 mm,直径为60~200 mm,直径不同Pt催化剂的量也不同。通过循环伏安法测定,该材料的活性面积约为几何面积的1.3倍。
恒温磁力搅拌器,德国IKA仪器有限公司;CIC-100型离子色谱仪,青岛盛瀚色谱技术有限公司,阳离子交换色谱柱为Thermo Fisher Ion Pac CS12A分析柱(250 mm×4 mm),淋洗液为8 mmol/L MSA,流速为1.2 mL/min,进样量为50 μL;DC-1010型低温恒温循环器,南京瞬玛仪器设备有限公司;电子加速器,最大束功率12 MeV,50 kW,中国原子能科学研究院计量测试部。
1.2 实验方法
通过测定反应过程中N2H4浓度的变化来表征Pt催化分解肼的反应。实验前,首先按不同的实验条件配制一定浓度的HNO3和肼的反应溶液。降温使带水浴夹套的玻璃装置温度达到设定值,然后向玻璃装置中加入总体积为450 mL的反应溶液,当温度达到设定值后,机械搅拌条件下(600 r/min)加入不同比表面积的Pt-Ti网催化剂,反应同时开始计时,根据溶液反应情况,每隔一段时间取样分析溶液中肼浓度等随时间的变化。肼浓度的测定采用离子色谱法,并依据标准曲线计算肼的浓度。
1.3 动力学处理方法
(1)
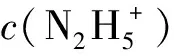
(2)
其中:
k′=kcb(HNO3)
(3)
对上式积分并整理得:
(4)
2 结果与讨论
2.1 反应对级数的确定

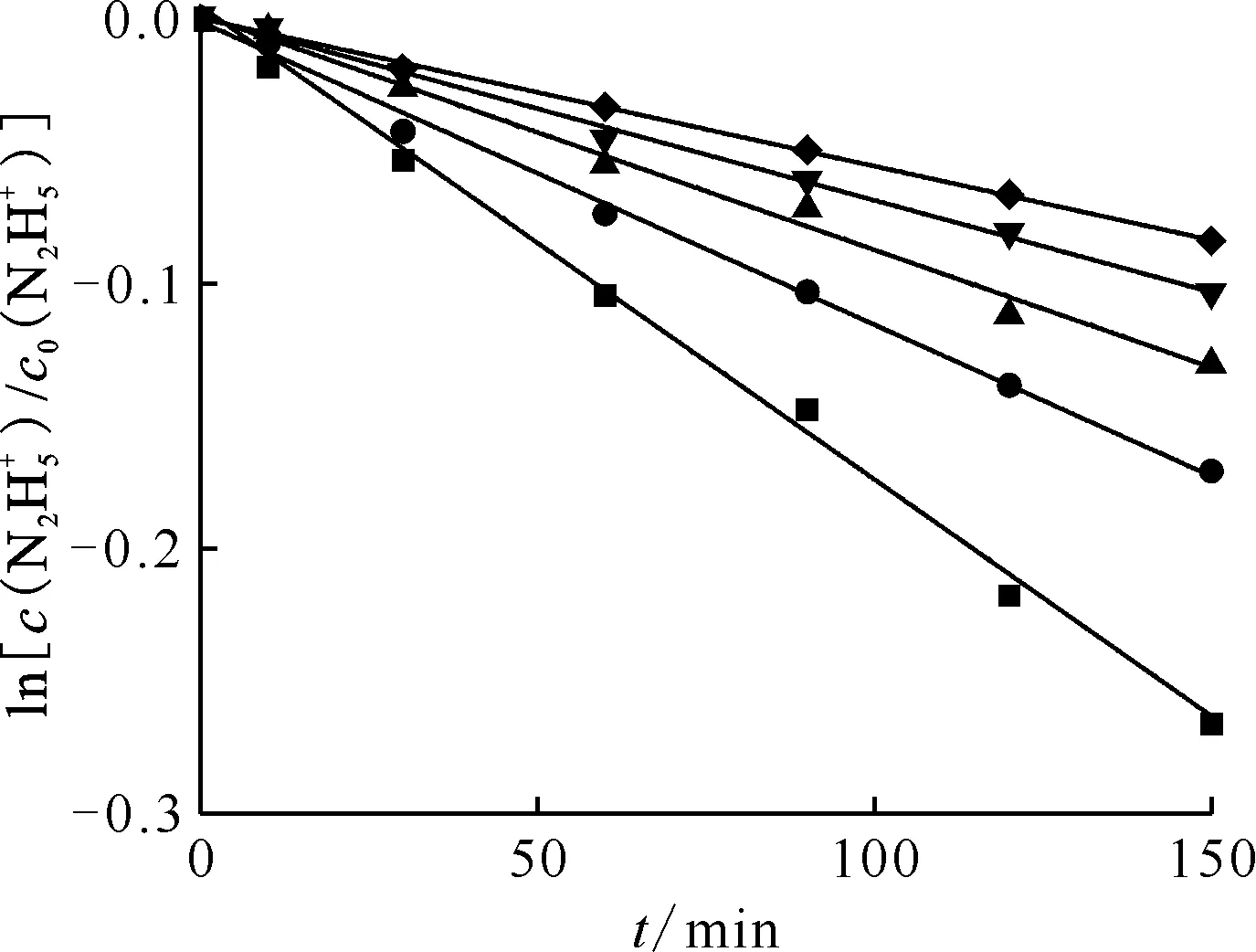
催化剂的用量 0.63 cm2/mL,T=296 K,c0(HNO3)=0.020 mol/L ■——0.055,y=-1.79×10-3x+4.78×10-3,r2=0.99;●——0.040,y=-1.14×10-3x-1.01×10-3,r2=0.99;▲——0.035,y=-8.88×10-4x+1.60×10-3,r2=0.99;▼——0.025,y=-6.92×10-4x+7.93×10-4,r2=0.99;◆——0.020, y=-5.58×10-3x+2.68×10-4,r2=0.99
2.2 硝酸初始浓度对反应速率的影响

同样经处理后,求出不同HNO3浓度下反应的表观速率常数k′,并以HNO3起始浓度的对数对lnk′作图得图3。图3表明,lnc0(HNO3)与lnk′呈直线关系,直线的斜率是-0.39,即反应对HNO3的反应级数为-0.39。反应级数为负说明H+不直接参与Pt催化肼的分解反应,相反由于它和肼分子之间存在竞争吸附催化剂上活性位的关系,在反应体系S/V不变的情况下,随着酸度增加,H+占活性位的比例增加,吸附肼的活性位相应的较少,导致肼的分解速率下降。

c0(HNO3),mol/L:■——0.010,y=-6.92×10-4x-2.88×10-3,r2=0.99;●——0.020,y=-5.50×10-4x-5.97×10-5,r2=0.99;▲——0.030,y=-4.63×10-4x+2.30×10-3,r2=0.99;▼——0.040,y=-4.05×10-4x+1.61×10-5,r2=0.99;◆——0.050,y=-3.69×10-4x-9.74×10-5,r2=0.99

图3 不同硝酸初始浓度对表观速率常数的拟合曲线
各种不同起始条件下的速率常数列入表1。
综上所述,Pt催化肼分解的初始表观动力学速率方程可表示为:
(5)

表1 Pt催化肼分解的k和k′值
T=296 K,催化剂用量S/V=0.63 cm2/mL时,速率常数k=(5.90±0.35)×10-3mol/(L·min)。
2.3 催化剂用量对反应速率的影响
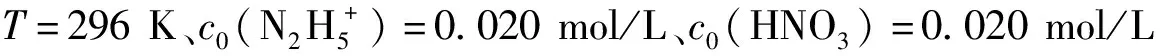
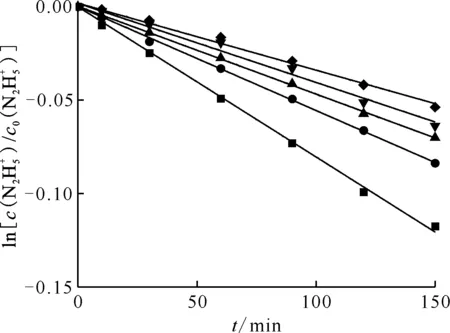
c0(HNO3)=0.020 mol/L 催化剂用量,cm2/mL:■——0.91,y=-8.04×10-4x-5.94×10-5,r2=0.99;●——0.63,y=-5.57×10-4x+8.40×10-5,r2=0.99;▲——0.56,y=-4.69×10-4x+1.29×10-5,r2=0.99;▼——0.49,y=-4.23×10-4x+1.78×10-3,r2=0.99;◆——0.42,y=-3.58×10-4x+1.80×10-3,r2=0.99
2.4 温度对反应速率的影响
维持其他条件不变,单独改变反应体系的温度,在280~310 K研究温度对反应的影响。反应温度与表观速率常数的关系通常用Arrhenius定理表示:
k′=Ae-Ea/RT
(6)
其中:Ea,该反应的活化能,J/mol;A,指前因子,mol/(min·L);R,气体摩尔常数,R=8.314 J/(mol·K)。

图5 催化剂用量对表观速率常数的拟合曲线
图6为不同温度下肼分解的一级拟合曲线。由图6可知:随着温度升高,表观速率常数由1.19×10-4min-1(286 K)增加到7.53×10-4min-1(306 K),并由公式(6)求得反应的活化能Ea=(333.3±2.9) J/mol(图7)。

催化剂用量 c0(HNO3)=0.020 mol/L ■——286 K,y=-1.19×10-4x+3.67×10-4,r2=0.99;●——291 K,y=-3.05×10-4x+8.35×10-4,r2=0.99;▲——296K,y=-5.50×10-4x-5.96×10-4,r2=0.99;▼——301 K,y=-6.26×10-4x-2.76×10-3,r2=0.99;◆——306 K,y=-7.53×10-4x-2.63×10-3,r2=0.99
2.5 β放射性对反应速率的影响
如前所述,在实际的后处理过程中,所处理的料液具有强放射性,为了探究后处理溶液中β放射性对反应可能的影响,利用电子加速器来模拟β放射性进行研究,其最大束功率为2.0 MeV,50 kW。辐照样品置于距电子加速器钛窗口约30 cm处进行辐照实验,使电子束仅辐照反应溶液,电子束流强度为0.065 mA。实验中,由薄膜剂量计测得样品的辐照吸收剂量为31.2 kGy(20 min)。

催化剂用量 c0(HNO3)=0.020 mol/L

催化剂用量 c0(HNO3)=0.020 mol/L ■——β辐照Pt表面(Pt/β),y=-1.64×10-2x-9.78×10-3,r2=0.99;●——β辐照溶液(Pt/β),y=-1.10×10-2x-2.29×10-3,r2=0.99;▼——β辐照,y=-8.14×10-3x-3.76×10-3,r2=0.99;▲——Pt催化 ,y=-5.67×10-4x-3.51×10-4,r2=0.99
不同实验条件下肼的分解曲线示于图8。由图8可知:单独采用Pt催化,硝酸体系中肼分解的表观速率常数为5.67×10-4min-1;单独采用β辐照处理,硝酸体系中肼分解的表观速率常数为8.14×10-3min-1;在相同时间、相同条件下,采用Pt/β联合处理工艺,肼分解的表观速率常数为1.10×10-2min-1,是单独Pt催化法的19.3倍,是单独β辐照的1.35倍。这表明,当溶液中存在β放射性时,可以显著提高体系中Pt催化肼分解的分解速率。同时可看出,Pt/β联合作用时肼的表观分解速率(1.10×10-2min-1)大于单独Pt催化与单独β辐照的常数之和(8.71×10-3min-1),这说明当引入β放射性时,β放射性和Pt催化氧化反应产生了一种叠加效应或者说协同效应,并且这种协同作用与体系中的自由基反应有关[10-11]。

3 可能的反应机理
通过以上反应动力学数据分析,可以对硝酸体系中Pt催化肼分解的反应机理进行初步推测。

Pt催化肼分解反应过程中,在反应瞬间就有气体生成表明该过程有自由基参与。反应发生于Pt催化剂的表面,H+和N2H4首先扩散并吸附到Pt催化剂表面的活性中心处(式(7)、(8)),当Pt催化剂活性点一定时,增加肼的浓度或降低酸度有利于肼的吸附,从而加速肼的分解,动力学方程中对肼的级数为正可以验证。c(N2H4)的一级反应级数取决于吸附平衡式(8)。通常来说,吸附在催化剂上的肼的解离脱氢(式(12))为整个反应的限制步骤。在反应过程中,肼氧化还原分解的反应为式(9)—(12)。下标sol表示溶液,ads表示吸附在催化剂表面。
(7)
(8)
(9)
(10)
(11)
(12)

因此,当将β放射性引入溶液中时,溶液中产生了大量的活性粒子如HO·、eaq·等,它们可以很快地与吸附在Pt催化剂上的肼或其中间产物反应,从而导致肼的分解速率加快,可能发生的反应如式(13)、(14)。然而其真实的作用与机理有待进一步考证和研究。
(13)
(14)
4 结 论
(1) 本实验条件下,在硝酸体系中Pt催化肼分解的反应动力学方程为:
296 K、催化剂的量S/V=0.63 cm2/mL时,速率常数k=(5.90±0.35)×10-3mol/(L·min)。
(2) 推测了硝酸体系下Pt催化肼分解的反应机理,肼在催化剂表面的吸附分解是整个反应的控制步骤。升温、减小硝酸浓度、增大催化剂Pt的量均可以使肼的分解速率加快。
(3) β放射性对Pt催化体系中肼的分解速率有显著的提高作用,其表观速率常数比单独Pt催化提高了19.3倍,比单独β辐照提高了1.35倍,β放射性辐照位置不同肼的分解速率也不同。据推测,是由于β射线与水溶液反应生成的活性粒子与吸附在Pt催化剂表面的肼及中间产物发生了一系列氧化还原反应导致肼的分解速率加快。
