虎杖标准汤剂质量标准研究
2020-05-13陈玉梅胡昌江许润春
李 燕,刘 聪,陈玉梅,胡昌江*,许润春
(1.成都中医药大学 药学院,四川 成都611137;2.四川新绿色药业科技发展有限公司/国家企业技术中心/国家中医药管理局“中药配方颗粒质量与疗效评价”重点研究室,四川 成都 611900)
虎杖来源于蓼科植物虎杖PolygonumcuspidatumSieb.et Zucc.的干燥根茎和根[1],为常用清热药,主产于华东、中南、西南等地,包括四川、贵州、浙江、安徽、陕西、广东等省市[2]。具有利湿退黄、清热解毒、散瘀止痛、止咳化痰等功效,用于治疗湿热黄疸、淋浊、带下、风湿痹痛等症[1]。虎杖主要化学成分包括蒽醌类、二苯乙烯类、黄酮类、香豆素类以及一些脂肪酸类化合物等,具有抗菌、抗病毒、扩血管、抗血栓等多种药理作用[3-7]。根据2016年国家药典委员会发布的《中药配方颗粒质量控制与标准制定技术要求(征求意见稿)》,中药标准汤剂系遵循中医药理论,采用合格饮片按照临床汤剂煎煮方法规范化煎煮,固液分离,经适当浓缩制得或经适宜方法干燥制得,作为衡量中药配方颗粒是否与临床汤剂基本一致的标准参照物[8]。标准汤剂系由不少于15批原料分别制得,计算相关平均值,并规定其变化可接受的范围。中药配方颗粒的所有药学研究均须与标准汤剂进行对比,以保证与标准汤剂质量的一致性。
虎杖作为中药的重要品种,目前对其标准汤剂的研究报道较少。本研究严格遵循相关文件中标准汤剂制备的要求,收集主产区的20批虎杖药材制备标准汤剂,以虎杖苷和大黄素为指标成分,测定其含量,计算转移率和出膏率范围,并进行指纹图谱研究,为虎杖标准汤剂质量标准的制定提供研究数据,同时为虎杖配方颗粒质量标准研究提供参考。
1 材料
1.1 仪器
安捷伦1260型高效液相色谱仪(美国安捷伦科技有限公司);CT-C-3型热风循环烘箱(杭州金竺机械有限公司);MS205DU型电子分析天平(梅特勒-托利多仪器有限公司);ME204E/02型电子分析天平(梅特勒-托利多仪器有限公司);细胞型1810A超纯水机(上海摩勒科学仪器有限公司);KQ5200DB型超声波清洗器(600 W,40 kHz;昆山市超声仪器有限公司);分体式陶瓷煎药壶4 L(美味世家);LGJ-100F型真空冷冻干燥机(北京松源华兴科技发展有限公司)。
1.2 药品及试剂
按照《中药配方颗粒质量控制与标准制定技术要求》(征求意见稿)的要求共收集20批来自四川、贵州、浙江、安徽、陕西等主产区的虎杖药材(经成都中医药大学胡昌江教授鉴定为蓼科植物虎杖PolygonumcuspidatumSieb.et Zucc.的干燥根茎和根),并加工成饮片,饮片具体信息见表1。虎杖苷(中国食品药品检定研究院,批号:111575-201603,含量以87.3%计),大黄素(中国食品药品检定研究院,批号:110756-201512,含量以98.7%计),白藜芦醇(中国食品药品检定研究院,批号:11535-201703,含量以99.4%计);乙腈、磷酸为色谱纯,水为超纯水,其余试剂均为分析纯。
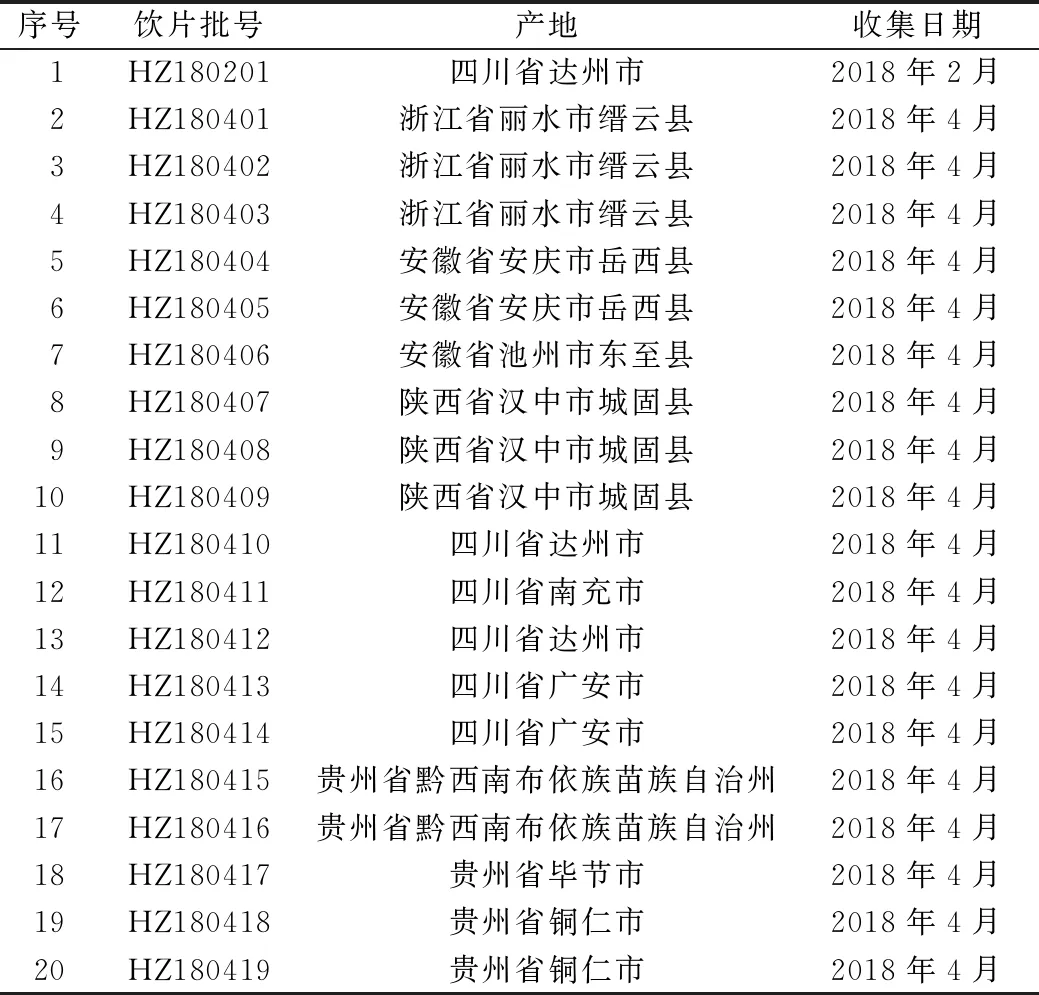
表1 饮片产地信息
2 方法和结果
2.1 虎杖饮片含量测定
采用 《中国药典》 2015版方法,以Agilent ZORBAX Extend-C18为色谱柱,以甲醇-0.1%磷酸溶液(80∶20)为流动相;检测波长为254 nm,测定饮片的大黄素含量;以乙腈-水(23∶77)为流动相;检测波长为306 nm,测定饮片的虎杖苷含量。结果见表3。
2.2 虎杖标准汤剂制备[9]
根据前期的预实验,确定虎杖标准汤剂制备方法为:取虎杖饮片150 g,加水煎煮二次,一煎加8倍水,浸泡30 min,煮沸,保持微沸煎煮20 min,200目筛网过滤;二煎加6倍水,煮沸,保持微沸煎煮15 min,200目筛网过滤,合并水煎液,立即冷却至室温,进行真空冷冻干燥,得到虎杖标准汤剂干燥粉末,收膏率见表2。
续表2
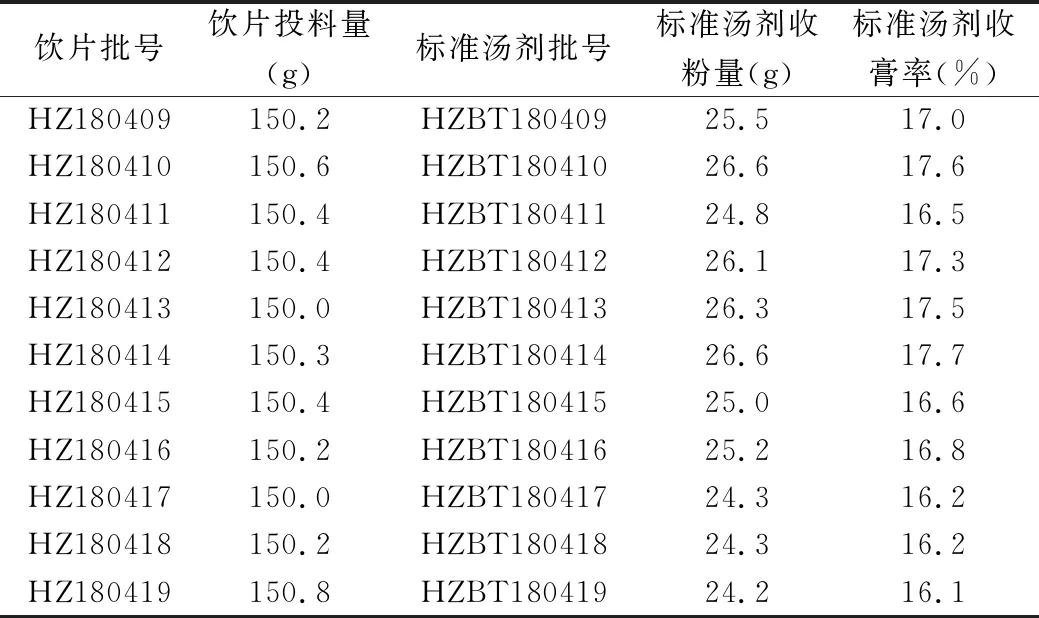
饮片批号饮片投料量(g)标准汤剂批号标准汤剂收粉量(g)标准汤剂收膏率(%)HZ180409150.2HZBT18040925.517.0HZ180410150.6HZBT18041026.617.6HZ180411150.4HZBT18041124.816.5HZ180412150.4HZBT18041226.117.3HZ180413150.0HZBT18041326.317.5HZ180414150.3HZBT18041426.617.7HZ180415150.4HZBT18041525.016.6HZ180416150.2HZBT18041625.216.8HZ180417150.0HZBT18041724.316.2HZ180418150.2HZBT18041824.316.2HZ180419150.8HZBT18041924.216.1
由表2计算可知,20批虎杖标准汤剂出膏率的范围为14.9%~19.0%,平均值为17.1%,平均值的70%~130%的范围为12.0%~22.2%。
2.3 虎杖标准汤剂含量测定
2.3.1 色谱条件 采用Agilent ZORBAX Extend-C18色谱柱(柱长为250 mm,内径为4.6 mm,粒度为5 μm);流动相为乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~45 min,15%~65%A);流速为mL·min-1;柱温25 ℃;检测波长分别为254 nm(大黄素)、306 nm(虎杖苷);进样体积10 μL。色谱见图1。
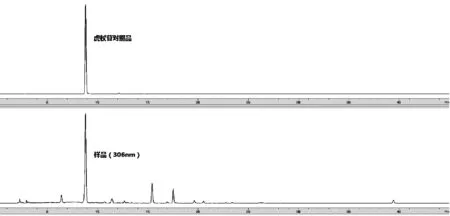
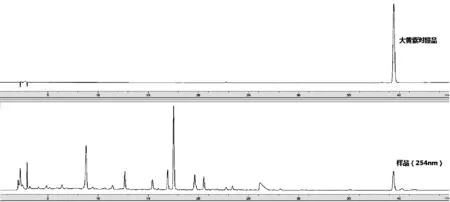
图1 虎杖苷、大黄素对照品和样品HPLC色谱
2.3.2 供试品溶液的制备 取本品约0.1 g,置具塞锥形瓶中,精密加入甲醇40 mL,密塞,称定重量,超声处理(功率600 W,频率40 kHz)20 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3.3 线性关系考察 分别取混合对照品溶液(虎杖苷302.8 μg·mL-1;大黄素23.4 μg·mL-1)1 μL、2 μL、3 μL、4 μL、6 μL、8 μL注入液相色谱仪,分别得到峰面积,以进样量(X,μg)为横坐标,峰面积(Y)为纵坐标计算得到回归方程,虎杖苷Y=4744X-22.66,r=0.999,线性范围0.263 4~2.107 5 μg;大黄素Y=5326X-4.133,r=0.999,线性范围0.263 4~2.107 5 μg,0.023 1~0.184 5 μg;虎杖苷和大黄素在各自范围内均呈良好线性关系。
2.3.4 精密度实验 取配置的混合对照品溶液按“2.3.1”项下方法连续进样6次,记录虎杖苷和大黄素的峰面积,计算得到虎杖苷峰面积的RSD为1.3%(n=6),大黄素峰面积的RSD为0.8%(n=6),表明仪器精密度良好。
2.3.5 重复性实验 取本品(批号HZBT180218)0.1 g,精密称定6份,按照拟定的方法制成供试品溶液,按“2.3.1”项下方法进样分析,计算6份供试品含量的RSD值,得到虎杖苷含量RSD为1.2%(n=6),大黄素RSD为0.6%(n=6),符合要求,表明该方法重复性良好。
2.3.6 稳定性实验 取同一供试品溶液,分别在0,2,4,8,12,24 h测定虎杖苷和大黄素色谱峰面积,计算得到虎杖苷峰面积的RSD为0.6%(n=6),大黄素峰面积的RSD为0.9%(n=6),表明供试品溶液在24 h内稳定。
2.3.7 加样回收实验 取已知含量的供试品(批号HZBT180218,虎杖苷5.52%,大黄素0.29%)0.05 g,共6份,精密称定,根据标准汤剂中两成分的含量按1∶1 的比例添加虎杖苷对照品和大黄素对照品,按拟定的方法进行供试品溶液的制备并测定,计算回收率,得虎杖苷平均回收率为101.86%,RSD为1.03%(n=6);大黄素平均回收率为97.54%,RSD为0.52%(n=6),表明该方法的准确度良好。
2.3.8 虎杖标准汤剂含量测定 按拟定的方法对20批虎杖标准汤剂进行虎杖苷和大黄素含量测定,并计算其转移率(转移率=标准汤剂中虎杖苷(大黄素)量/饮片中虎杖苷(大黄素)量×100%),结果见表3。
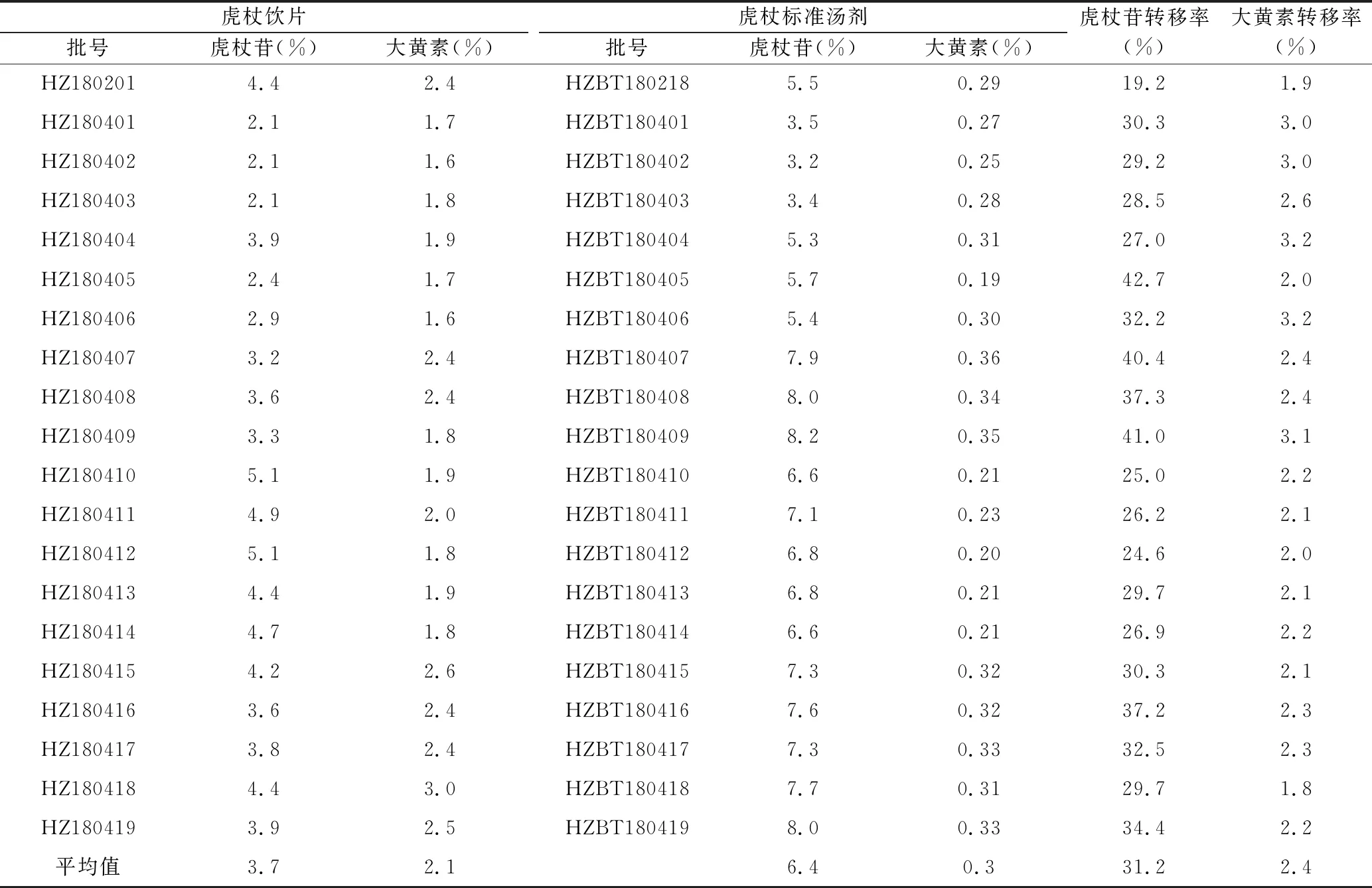
表3 虎杖标准汤剂含量测定结果
结果表明,虎杖标准汤剂中虎杖苷含量范围为3.2%~8.2%,均值为6.4%,大黄素含量范围为0.2%~0.4%,均值为0.3%;虎杖苷转移率为19.2%~42.7%,平均值31.2%;大黄素转移率为1.8%~3.2%,平均值2.4%。
2.4 指纹图谱的建立
2.4.1 色谱条件 采用Agilent ZORBAX Extend-C18色谱柱;(柱长为250 mm,内径为4.6 mm,粒度为5 μm);流动相为乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~45 min,15%~65%A);流速为1.0 mL/min;柱温25 ℃;检测波长为280 nm;进样体积10 μL。样品图谱见图2。
2.4.2 对照品溶液制备 取虎杖苷、大黄素、白藜芦醇对照品适量,加甲醇分别制成每1 mL各含50 μg的溶液,即得。对照品图谱见图2。
2.4.3 供试品溶液的制备 同“2.3.2”项下供试品溶液制备方法。
2.4.4 精密度试验 取同一批虎杖标准汤剂供试品溶液,按“2.4.1”项下方法连续进样6 次,以虎杖苷(2号峰)为参照峰,计算各共有峰保留时间和峰面积的RSD,结果表明各峰保留时间RSD<0.1%(n=6),相对峰面积RSD<2.0%(n=6),表明仪器精密度良好。
2.4.5 重复性试验 平行制备6 份虎杖标准汤剂供试品溶液,按“2.4.1”项下方法进样,测定供试品溶液中各共有峰的保留时间和峰面积。以虎杖苷(2号峰)为参照峰,计算各共有峰相对保留时间和相对峰面积的RSD,结果表明各峰相对保留时间的RSD<0.10%(n=6),相对峰面积的RSD<1.8%(n=6),表明该方法重复性较好。
2.4.6 稳定性试验 取虎杖标准汤剂供试品溶液,分别于供第0、2、4、8、12、20、24 h按“2.4.1”项下方法进样测定,以虎杖苷( 2号峰) 为参照峰,计算各共有峰相对保留时间和相对峰面积的RSD。结果各峰相对保留时间的RSD<0.10%(n=6),相对峰面积的RSD<3.0%(n=6),表明虎杖标准汤剂供试品溶液在24 h 内稳定。
2.4.7 样品检测与分析 分别取20批虎杖标准汤剂,按“2.3.2”项下方法制备供试品溶液,再按“2.4.1”项下色谱条件分别测定,记录HPLC 图,生成对照图谱,见图3。将20批供试品色谱图导入中药色谱指纹图谱相似度评价系统软件(2012版),以HZBT180218色谱图为参照,采用中位数法,时间窗为0.1,进行相似度计算,见图4、表4。结果发现20 批虎杖标准汤剂与对照指纹图谱相似度均大于0.95,表明各批次虎杖标准汤剂具有较好的一致性。
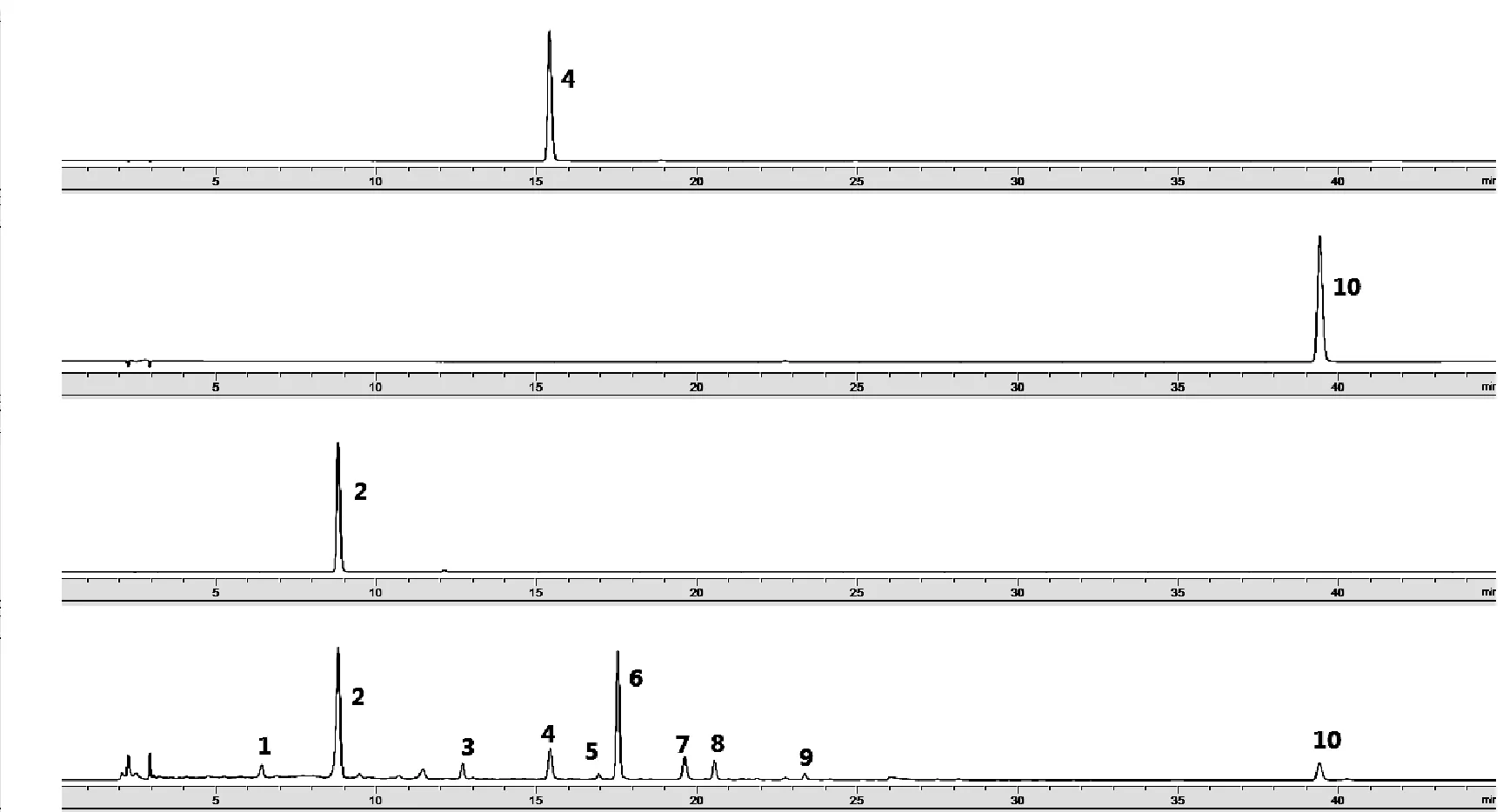
2.虎杖苷;4.白藜芦醇;10.大黄素

2.虎杖苷;4.白藜芦醇;10.大黄素
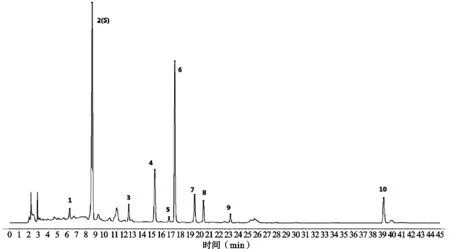
图4 20批标准汤剂HPLC色谱
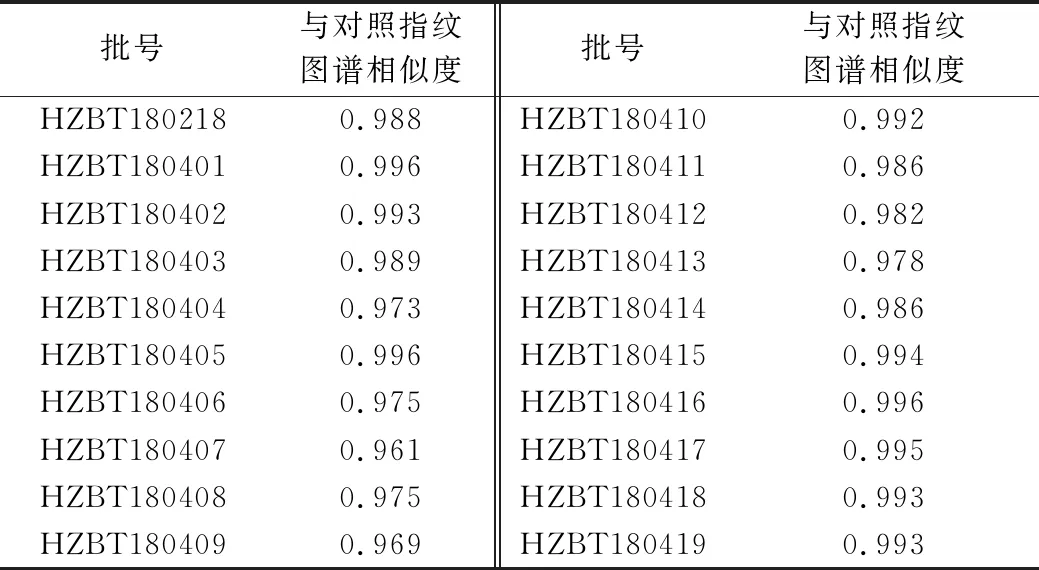
表4 20批标准汤剂指纹图谱相似度计算结果
3 讨论
3.1 虎杖样品来源
产区调查表明,虎杖药材现主产于四川、贵州、浙江、安徽、陕西等省。本研究收集了20批来自四川达州、南充、广安,浙江丽水,安徽安庆、池州,陕西汉中,贵州毕节、铜仁等多个省市的虎杖药材,产地来源基本覆盖了虎杖的传统产区、主产区和主要种植区,样品收集具有较强的代表性,能充分反映目前市场上的虎杖药材情况。
3.2 标准汤剂制备工艺的合理性
本研究中虎杖标准汤剂参照国家药典委员会公布的《中药配方颗粒质量控制与标准制定技术要求(征求意见稿)》和《医疗机构中药煎药室管理规范》中的相关规定,遵循中医药理论,按照临床汤剂煎煮方法规范化煎煮,固液分离,利用真空冷冻干燥设备进行干燥,制得干燥粉末,最大限度保存了水煎液中的成分,达到与传统汤剂基本一致。
3.3 标准汤剂的含量测定和指纹图谱分析
本研究建立的分析方法是采用同一个梯度洗脱系统,同时采集三个波长进行虎杖苷(306 nm)、大黄素(254 nm)和指纹图谱(280 nm)分析,该方法简便快捷,可应用于虎杖标准汤剂分析。
分析结果表明20批标汤中的虎杖苷含量远高于饮片,但大黄素含量远低于饮片,转移率虎杖苷可达30%以上,但大黄素不足4%;这应跟两成分的水溶性有关:虎杖苷微溶于水,而大黄素几乎不溶于水。20 批虎杖标准汤剂与对照指纹图谱相似度均在0.95以上,表明各批次虎杖标准汤剂具有较好的一致性,质量相对较稳定,说明本实验建立的虎杖饮片指纹图谱中10 个共有峰及对照指纹图谱可反映其指纹特征,具有鉴别评价意义。
3.4 标准汤剂的应用及意义
中药配方颗粒具有服用方便、易于携带、质量稳定等特点,这种新的饮片用药形式是对传统饮片的有益补充,但也存在标准不明确、剂量不统一、临床合理性有待进一步论证等各种问题。中药临床多为汤剂,汤剂也是我国传统医学中应用最早、目前临床应用最广泛的剂型,所以,亟需建立中药饮片标准汤剂用于标准化中药配方颗粒[9]。
本研究制备了 20批虎杖标准汤剂样品,并以虎杖苷、大黄素等有效成分为质控指标,结合指纹图谱对标准汤剂的化学成分进行整体把控,得到相关数据结果,该研究可以为虎杖配方颗粒质量标准的研究建立提供参考依据,保证成品与标准汤剂的质量一致性。
