基于LSS管理法的临床分子诊断设备管理策略研究
2020-04-01顾燕芳
费 敏 顾燕芳 陈 瑛 杨 岚
国家卫生健康委员会《2017年我国卫生健康事业发展统计公报》[1]数据显示,从2016-2017年,我国新生儿、婴儿和5岁以下儿童的病亡率分别下降到4.5‰、6.8‰和9.1‰,孕产妇病亡率从19.9/10万下降到19.6/10万,出生缺陷渐成我国儿童病亡的主要原因[2]。我国《健康中国2030》规划对提高妇幼健康水平做了重要指示,将预防出生缺陷列为妇幼保健服务的重要内容,而妇幼保健机构是保障妇女儿童健康的重要医疗卫生专业机构[3-4]。
基因遗传病的诊断是在胎儿出生前,通过检测预先得知胎儿的缺陷或疾病。目前,出生缺陷的筛查及诊断技术很多,>80%的出生缺陷疾病是由遗传因素单独或协同作用所导致,可采用斑点杂交、限制性酶切基因图、DNA限制性片段长度多态性、寡核苷酸杂交和多聚酶链反应等技术进行基因遗传病的诊断[5-7]。染色体微阵列基因芯片系统、二代高通量测序仪、液相基因芯片检测平台等设备的出现极大提高了胎儿染色体异常和常见染色体微缺失和(或)微重复的检出率[8-9]。然而,分子诊断类设备均为分子生物学、微电子及计算机等多学科结合的产物,因此,该类设备对工作环境与操作要求严格,同时伴随维修难度大等特点,近年来反复出现红细胞分布宽度变异系数偏高、假阳性率、样本错误率、漏检率以及复检率增高等问题时有发生。基于此,本研究使用精益六西格玛(lean six sigma,LSS)管理方法,制定并优化分子诊断设备管理策略,旨在降低分子诊断类设备非常规错误的发生。
1 LSS管理方法
1.1 LSS管理法定义
LSS是精益生产与六西格玛管理的结合,其本质是消除浪费。LSS管理的目的是通过整合精益生产与六西格玛管理,吸收两种生产模式的优点,弥补单个生产模式的不足,达到更佳的管理效果。LSS不是精益生产和六西格玛的简单相加,而是二者的互相补充和有机结合[10-11]。
1.2 测量阶段
测量阶段是对关键问题界定后,搜集相关数据,测定目前过程能力的阶段。过程能力指数也称为工序能力指数,是指工序保证质量的能力[11]。组织系统模型(supplier input process output customer,SIPOC)是质量大师戴明提出的组织系统模型,是一门最有用且最常用的,用于流程管理和改进的技术,是过程管理和改进的常用技术,也是作为识别核心过程的首选方法[13-14]。SIPOC模型由supplier(供应者)、input(输入)、process(流程)、output(输出)和customer(客户)相互关联和互动的5个部分组成,本研究通过绘制分子诊断的SIPOC流程图,从组织层面将LSS聚焦于过程管理,系统的对LSS管理模式展开一系列研究。分子诊断SIPOC流程见图1。
1.3 问题分析
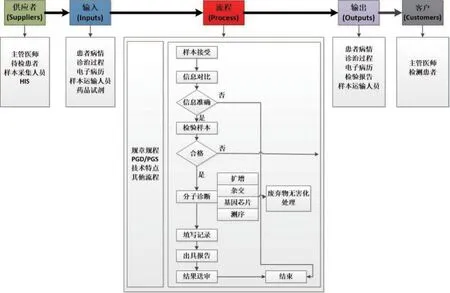
图1 分子诊断SIPOC流程
在SIPOC流程图的基础上,建立分子诊断类设备非常规错误发生率的影响因素鱼骨图,经过头脑风暴,通过分析评估,找出影响分子诊断类设备非常规错误发生率的潜在影响因素及存在问题,为后续的对策制定及问题改善提出参考因素。分子诊断类设备非常规错误发生率影响因素见图2。
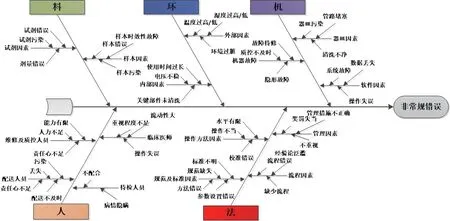
图2 分子诊断类设备非常规错误发生率影响因素鱼骨图
1.4 改进与实施
制定控制计划确保项目顺利实施,通过识别关键指标对流程进行持续监管,并制定具体计划及时纠正改进策略实施过程中出现的偏差。
(1)质量控制。加强分子诊断类设备质量控制,设立科室质量控制小组,负责对分子诊断类设备进行质量控制、数据记录、分析和上报工作,并不定期对各环节进行抽查。
(2)定期培训。对业务能力有限的采集人员和检验人员进行定期技能培训、医疗卫生常识培训及制度流程等方面培训,不定期对参训人员进行考核,并制定采集和检验的基本规范和标准。
(3)筛选重点问题。筛选非常规错误事件作为检查重点,制定追述解决方案,把控问题,寻找并记录非常规错误事件发生的因素。
(4)闭环管理模式。记录、统计分子诊断类设备非常规错误事件,分析错误事件相关性因素,针对相关因素进行集中学习,加强管理,并将致错因素落实到下一循环的具体环节中,动态监控同类非常规错误事件的发生。
(5)制定奖惩制度。对经常发生非常规错误事件的直接或间接人员予以相应警告,对重大非常规错误予以相应的惩戒。
(6)发挥绩效作用。将分子诊断类设备非常规错误率作为科室和(或)院内的绩效考核指标,以及个人年度评先评优的指标之一。
(7)集中学习制度。定期开展科室检验经验讲座,相互交流、集中学习。
2 LSS管理方法应用
2.1 研究资料与方法
(1)采用无锡市妇幼保健院染色体微阵列Agilent 4200Tape Station基因芯片系统(美国安捷伦科技公司)、二代高通量DNBSEQ-200型(深圳华大基因股份有限公司)和NextSeq 550AR型[安诺优达基因科技(北京)有限公司]基因测序仪、液相基因芯片Luminex100检测平台(美国路名克斯科技公司)以及靶向分子基因芯片Affymetrix GeneAtlas U219检测系统(美国昂飞公司)等分子诊断类设备,并于2016年1月成立质量控制小组,研究LSS管理法降低分子诊断类设备非常规错误发生率,将LSS管理法执行前的2014年1月至2015年12月分子诊断类设备非常规错误事件纳入对照组,总检验28934人次;将LSS管理法执行后的2017年1月至2018年12月数据纳入实验组,总检验27635人次。
(2)采用SPSS19.0软件进行数据统计学分析,对比分析两组分子诊断类设备假阳性率、样本错误率、漏检率、复检率以及设备故障发生率,其中,设备故障发生率=设备故障总时长÷设备使用总时长×1000‰。计数资料用率(‰)表示,采用x2检验,以P<0.05为差异有统计学意义。
2.2 应用结果
(1)对照组的分子诊断类设备假阳性率为0.83‰,实验组为0.40‰,降幅52%,两组比较差异有统计学意义(x2=4.25,P<0.05);对照组的分子诊断类设备样本错误率为1.11‰,实验组为0.33‰,降幅70.6%,两组比较差异有统计学意义(x2=11.88,P<0.05);两组分子诊断类设备样本漏检率和复检率均无统计学意义。分子诊断类设备非常规错误发生率比较见图3,分子诊断类设备非常规错误发生率统计见表1。
(2)对照组的分子诊断类设备故障总时长为197 h,实验组为144 h,降幅26.9%,对照组的设备故障发生率为22.49‰,实验组为16.44‰,两组比较差异有统计学意义(x2=8.40,P<0.05)。
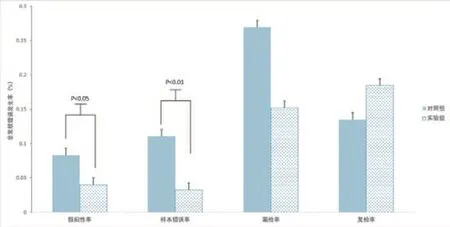
图3 分子诊断类设备非常规错误发生率比较

表1 分子诊断类设备非常规错误发生率统计(‰,例)
3 讨论
中国合格评定国家认可委员会2018年3月1日发布了《医学实验室质量和能力认可准则在分子诊断领域的应用说明》(CNAS-CL02-A009),从管理和技术方面提出了明确要求,为临床科室和实验室提供了指导意见[15-16]。在此过程中,医疗设备的使用和全生命周期管理显得尤为重要,如何确保检测结果的准确性和有效性,保障项目的顺利开展,确保仪器设备的正常运行,已成为设备管理和使用人员研究的综合型课题[17]。
(1)设备维修管理技术要求高。分子诊断设备的科技含量高,对维护保养要求更高,更需专业维护保养人员对其进行管理。设备的引入,尤其是先进医疗设备的引入,使得医学工程人员管理和维修难度大幅度增加。设备的使用准则、维修方法在一定程度上依赖厂家,厂家的售后服务能力参差不齐,响应时间和维修时间往往不能保证,供需矛盾突出[18-20]。
(2)设备质量控制无标准。由于分子诊断类设备操作复杂,国内对分子诊断技术的检测机构较少,多数检测机构属于手工操作,缺少规范、标准的质量监督体系。尤其是分子诊断类设备,缺少系统、科学的实验室,实验室的室内控制、室间比较以及行业监督等均有不足。
(3)检验流程涉及面广。分子诊断类检验需要待检患者、临床医师、样本采集人员、样本配送人员、样本检验人员以及报告配送人员等的参与,需要多种试剂联合使用,容错点多,涉及范围广,使得分子诊断类设备的致错因素多而杂,闭环管理难度大。
通过LSS管理法的SIPOC流程分析、鱼骨图等管理工具,对多种分子诊断类设备非常规错误事件进行梳理,成立由医疗设备管理部门牵头,检验科人员和临床质量控制医师参与的专项质量控制小组,定期召开例会,通过头脑风暴进行一系列流程优化、系统改造和加强培训考核等措施,改进分子诊断类设备非常规错误事件填报的质量控制,可保证分子诊断类设备诊断质量的安全性和可靠性。
(4)完善分子诊断设备管理流程架构。医疗器械的管理必须建立从院领导、管理职能部门到临床医疗科室的三级管理体系,将管理制度分解到各部门,落实到人。针对分子诊断设备,必须根据《医学实验室质量和能力认可准则在分子诊断领域的应用说明》《医疗机构临床基因扩增检验实验室管理办法》《临床基因诊断实验室管理暂行办法》及《临床基因诊断实验室工作规范》等要求,进一步充实细化采购、验收、使用、保管、维修、保养和档案等环节的管理制度,加强器械管理。
(5)加强分子诊断设备风险管理意识。增强风险管理理念,提高风险管理意识,转变固有的事后维修服务理念为重视预防性维修维护,同时积极与临床医疗科室沟通配合,互通有无,将工作重点由被动维修转为程序性预防维护;加强维修人员的培训,使其掌握新设备日常运行的维护保养知识、维修技巧和运行原理,方便日后设备的日常管理和维修。针对分子类诊断设备的“高、精、尖”特性,专业评估分析制订每台设备的操作和维护保养手册,操作人员与维修人员要落实责任,力争做到专项培训,推行“一人一机一本”管理模式,保证设备的正常运行和维保以及维修记录的详实。
(6)建立分子诊断设备质量控制体系。结合全国分子诊断类设备使用状况,探索制定统一的分子诊断类设备质量控制体系。根据分子诊断要求,完善分子诊断项目标准及质量控制与改进措施。当前,国家已批准体外诊断产品(in vitro diagnostic device,IVD)和医学检验实验室自建检测方法(laboratory developed tests,LDT)监管等[21]。妇幼保健机构要积极与卫生行政部门、质量控制中心及临床检验中心沟通交流,全面落实分子诊断类设备质量控制体系,时刻监督分子诊断类设备的应用与管理,综合分子诊断技术未来发展,不断更新分子诊断类设备质量控制测评和诊断能力,填补分子诊断类设备管理监督空白。
4 结论
妇幼保健机构医疗设备的专科性和特殊性使得设备管理有别于综合医院,不断发展的分子诊断类设备对设备管理人员提出了更高的要求,在提升自身素质和加强临床专业知识学习的同时,还需制定全面的管理方案,针对设备每个环节加以完善,提高分子诊断类设备管理质量。
基于LSS的管理方法,在SIPOC流程图的基础上,建立分子诊断类设备非常规错误发生率的影响因素鱼骨图,进行根因分析,找出影响分子诊断类设备非常规错误发生率的潜在影响因素及存在问题,从多方面改进了分子诊断类设备质量控制工作,优化了分子诊断类设备管理策略,保证了分子诊断类设备稳步进行,可确保医疗设备发挥真正的价值,提高妇幼保健服务和管理能力。
