不同干燥方法对牡丹皮药材中化学成分的影响△
2020-03-28赵秋龙卞晓坤钱大玮张丽陈菲菲郭盛严辉王团结赵建军段金廒
赵秋龙,卞晓坤,钱大玮*,张丽,陈菲菲 ,郭盛,严辉,王团结,赵建军,段金廒
1.南京中医药大学 江苏省中药资源产业化过程协同创新中心/江苏省方剂高技术研究重点实验室/中药资源产业化与方剂创新药物国家地方联合工程研究中心,江苏 南京 210023;2.江苏康缘药业股份有限公司,江苏 连云港 222001;3.宁夏医科大学 药学院,宁夏 银川 750004
牡丹皮为毛茛科植物牡丹PaeoniasuffruticosaAndr.的干燥根皮,性苦、辛,微寒,有清热凉血、活血化瘀之效[1]。现代研究表明,牡丹皮中主要含有酚及酚苷类、单萜苷类、有机酸类、黄酮类、苯丙素类及鞣质类等化学成分[2-3],这些成分多具有显著的生物活性,为牡丹皮发挥传统功效提供物质基础。牡丹皮产地传统加工方法为夏、秋二季,选晴天,分次采割后晒干。传统干燥方法存在干燥周期长、易受天气条件影响、干燥后药材质量不均一等弊端[4]。近年来,基于现代干燥原理与技术的干燥方法逐渐应用于中药材产地加工过程中,并表现为效率高、条件可控、产品质量稳定等优点[5]。
本研究拟通过分析不同干燥条件处理后牡丹皮中各类成分的含量变化规律,优化和建立牡丹皮药材适宜的干燥方法及条件,为牡丹皮药材的产地干燥提供依据。
1 材料
电热鼓风干燥机(上海一恒科学仪器有限公司);隧道式中短波红外干燥机(江苏泰州圣泰科红外科技有限公司);隧道式微波干燥机(南京研正微波设备厂);ACQUITY UPLC系统(四元泵溶剂系统,在线脱气机,自动进样器,二极管阵列检测器;Waters公司);Xevo TQ检测器(Waters公司);MassLynx4.1质谱工作站(Waters公司);ML204电子分析天平、MS105电子分析天平(万分之一,梅特勒-托尼多仪器有限公司);水分测定仪(德国Adam公司);KQ-250E型超声波清洗仪(昆山禾创仪器有限公司);D2012高速台式离心机(大龙兴创实验仪器北京有限公司)。
牡丹皮新鲜药材采挖于安徽亳州谯城区谯东镇牡丹皮种植基地,经南京中医药大学严辉副教授鉴定为毛茛科植物牡丹的新鲜根皮,凭证标本存放于江苏省中药资源产业化过程协同创新中心。对照品:丹皮酚原苷(批号:DPYG20161220)、牡丹皮苷C(批号:MDGC20151211)、丹皮酚(批号:DPF20160828)、氧化芍药苷(批号:YHYG20151121)、芍药苷(批号:SYG20160108)、没食子酰芍药苷(批号:MSYG20160601)、苯甲酰芍药苷(批号:BJYG20161011)、没食子酸(批号:MSZS20140901)、对羟基苯甲酸(批号:DQJS20141212)、没食子酸甲酯(批号:MSJZ20161013)、苯甲酸(批号:BJS20161109)、儿茶素(批号:ECS20160315)、槲皮素(批号:HPS20160618)、6-羟基香豆素(批号:QJDS20160921)、1,2,3,4,6-五没食子酰葡萄糖(批号:QMTT20160811)、香草乙酮(批号:XCYT20161102)均购自南京春秋生物工程有限公司,纯度≥98%;甲醇(南京化学试剂有限公司)为分析纯,乙腈(Merck)及甲酸(美国ACS公司)均为色谱纯,超纯水由Milli-Q纯水机制备。
2 方法
2.1 干燥加工方法
取牡丹皮新鲜药材,清洗摊晒,待表面水分挥干,混合均匀,随机分成14份,每份约1 kg,按表1所示加工方法进行干燥。干燥前取适量新鲜药材,测定其初始含水率,干燥过程观察、称质量并计算实时含水率,当含水率达到13.0%时,停止干燥并留样。
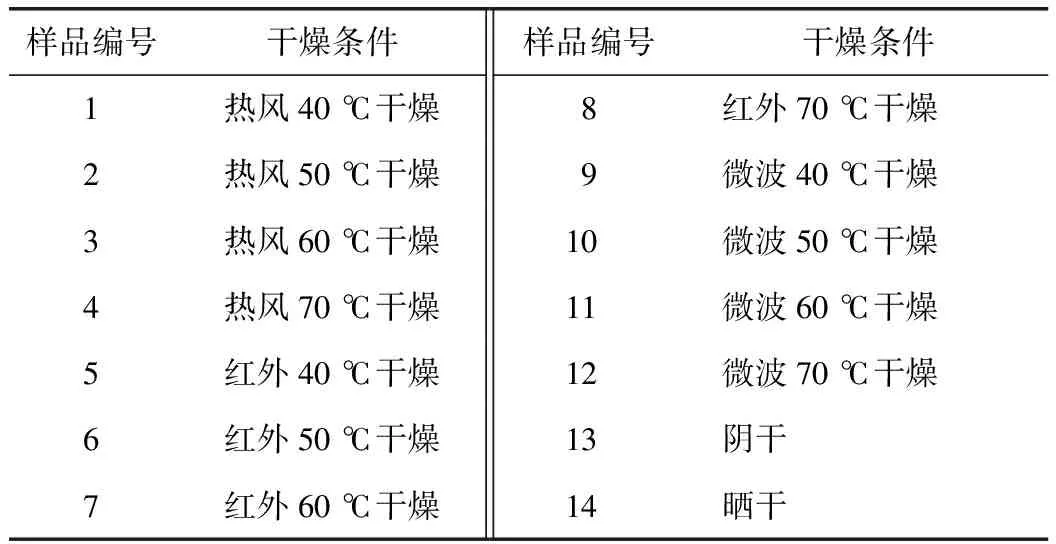
表1 牡丹皮药材不同干燥方法样品信息
2.2 色谱及质谱条件
色谱分析条件:Waters Acquity UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm);以0.1%甲酸水溶液(A)和乙腈(B)为流动相,梯度洗脱(0~5 min,95%~90%A;5~7 min,90%~75%A;7~10 min,75%~50%A;10~15 min,50%~5%A);流速:0.4 mL·min-1;柱温:35 ℃;进样量:3 μL。进样前以流动相初始条件平衡5 min。
质谱检测条件:ESI源;扫描方式ESI+、ESI-模式;多反应监测(MRM);毛细管电压:3 kV,锥孔电压:20 V,萃取电压:3 V,离子源温度:150 ℃,脱溶剂气温度:400 ℃;锥孔气流量:50 L·h-1;辅助气流:0.15 mL·min-1;各种成分的质谱参数见表2。
2.3 对照品溶液的制备
分别精密称取丹皮酚原苷、牡丹皮苷C、丹皮酚、氧化芍药苷、芍药苷、没食子酰芍药苷、苯甲酰芍药苷、没食子酸、对羟基苯甲酸、没食子酸甲酯、苯甲酸、儿茶素、槲皮素、6-羟基香豆素、1,2,3,4,6-五没食子酰葡萄糖、香草乙酮对照品适量,以甲醇溶解并定容制成各对照品储备液。精密量取各对照品储备液适量,置于同一量瓶中,制成混合对照品溶液,其中各成分的质量浓度分别为72.4、63.6、129.4、95.6、121.4、100.7、110.6、122.2、125.7、179.4、121.5、109.1、91.6、120.3、99.40、100.0 μg·mL-1。并将上述混合对照品溶液用甲醇稀释成不同浓度的混合工作液。
2.4 供试品溶液的制备
取牡丹皮药材粉末(过4号筛)约1 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定质量,超声处理(功率250 W,频率33 kHz)45 min,放至室温,称定质量,用甲醇补足减失质量,摇匀,13 000 r·min-1(离心半径4.6 cm)离心10 min,取上清液,过0.22 μm微孔滤膜,即得。
2.5 方法学考察
2.5.1线性关系考察与检测下限、定量下限测定 精密量取2.3项下混合对照品工作液3 μL,按2.2项下的分析条件进行测定。以被测化合物质量浓度X为横坐标,相应峰面积Y为纵坐标,进行线性回归,并按信噪比(S/N)为10和3分别计算被测成分的定量下限(LOQ)和检测下限(LOD)。结果见表3,各成分线性良好,r均在0.990 0以上。
2.5.2精密度试验 取中浓度混合对照品工作液,按2.2项下色谱条件下连续进样6次以测定待测成分的峰面积,各指标成分峰面积的RSD值评价仪器精密度,结果见表4。
2.5.3重复性试验 取1号样品6份,按2.4项下方法制备供试品溶液,分别进样分析,以各指标峰面积的RSD值评价重复性,结果见表4。
2.5.4稳定性试验 取1号样品,按2.4项下方法制备供试品溶液,分别于制备后0、2、4、8、12、24 h进样测定,以样品中各指标成分峰面积计算RSD,结果见表4。
2.5.5加样回收率试验 取0.5 g已知含量的1号样品6份,每份精密称定,加入与样品中各成分含量相近的各对照品,按2.4项下方法制备供试品溶液并按上述条件测定,计算平均回收率和RSD值。结果见表4。
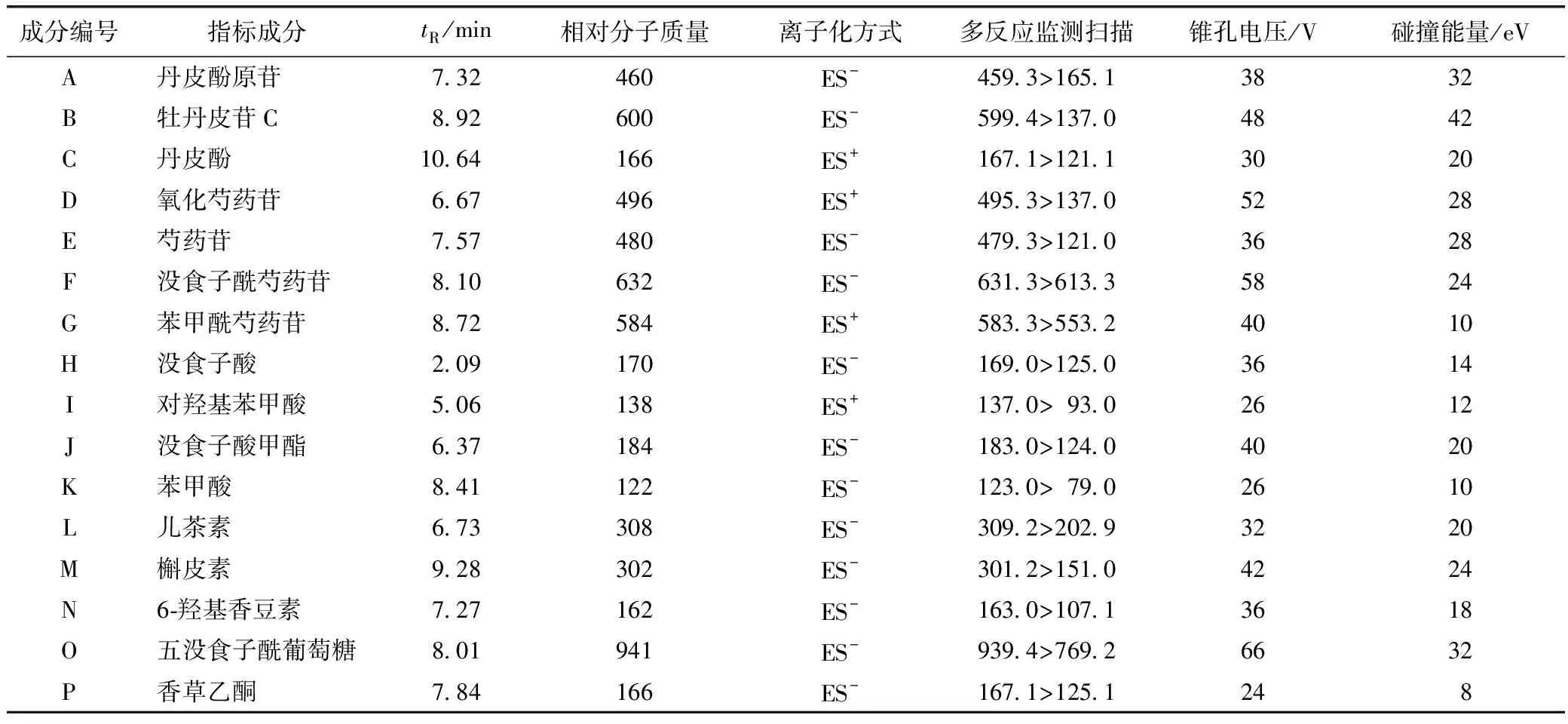
表2 牡丹皮中各成分MRM参数
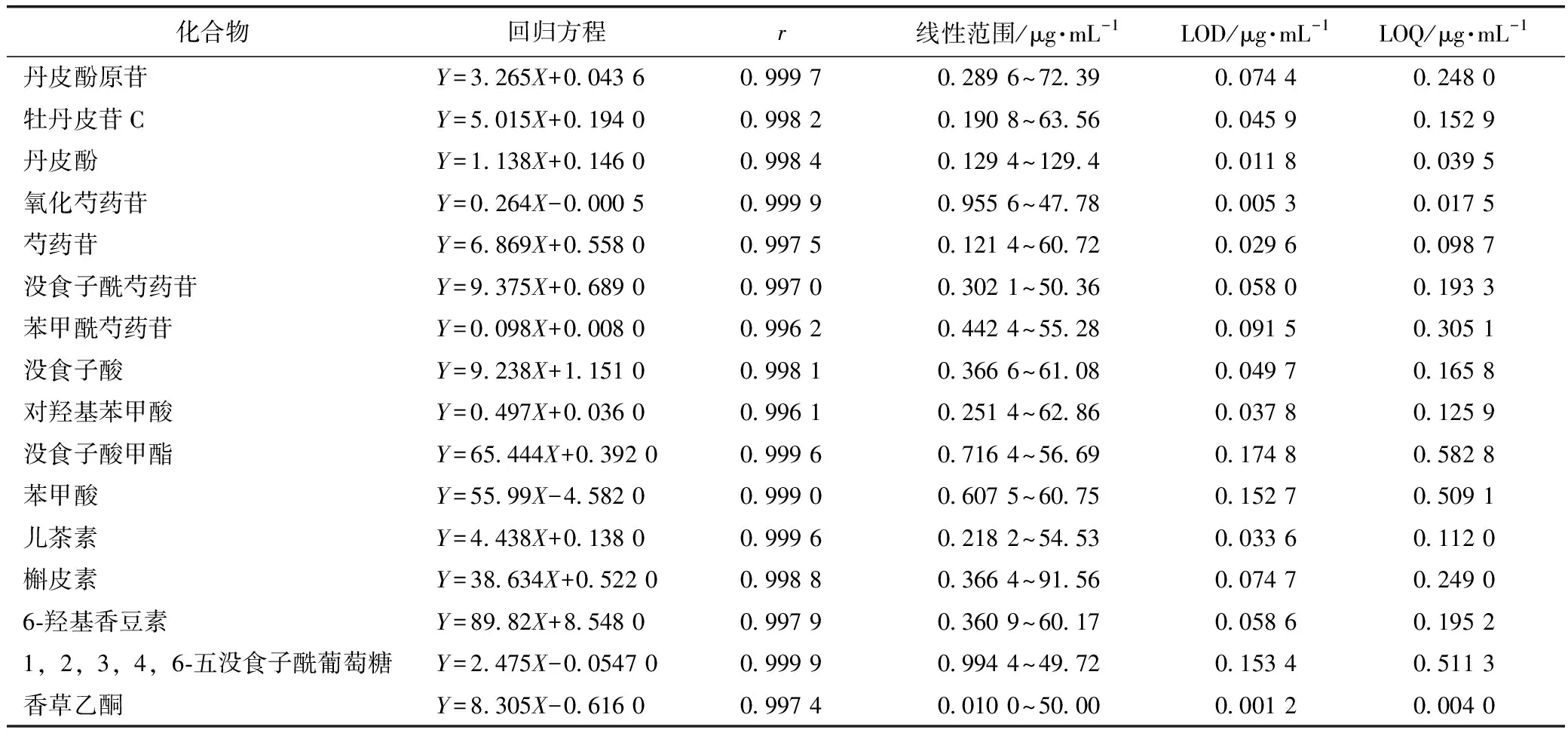
表3 各成分回归方程、线性范围、检测下限与定量下限
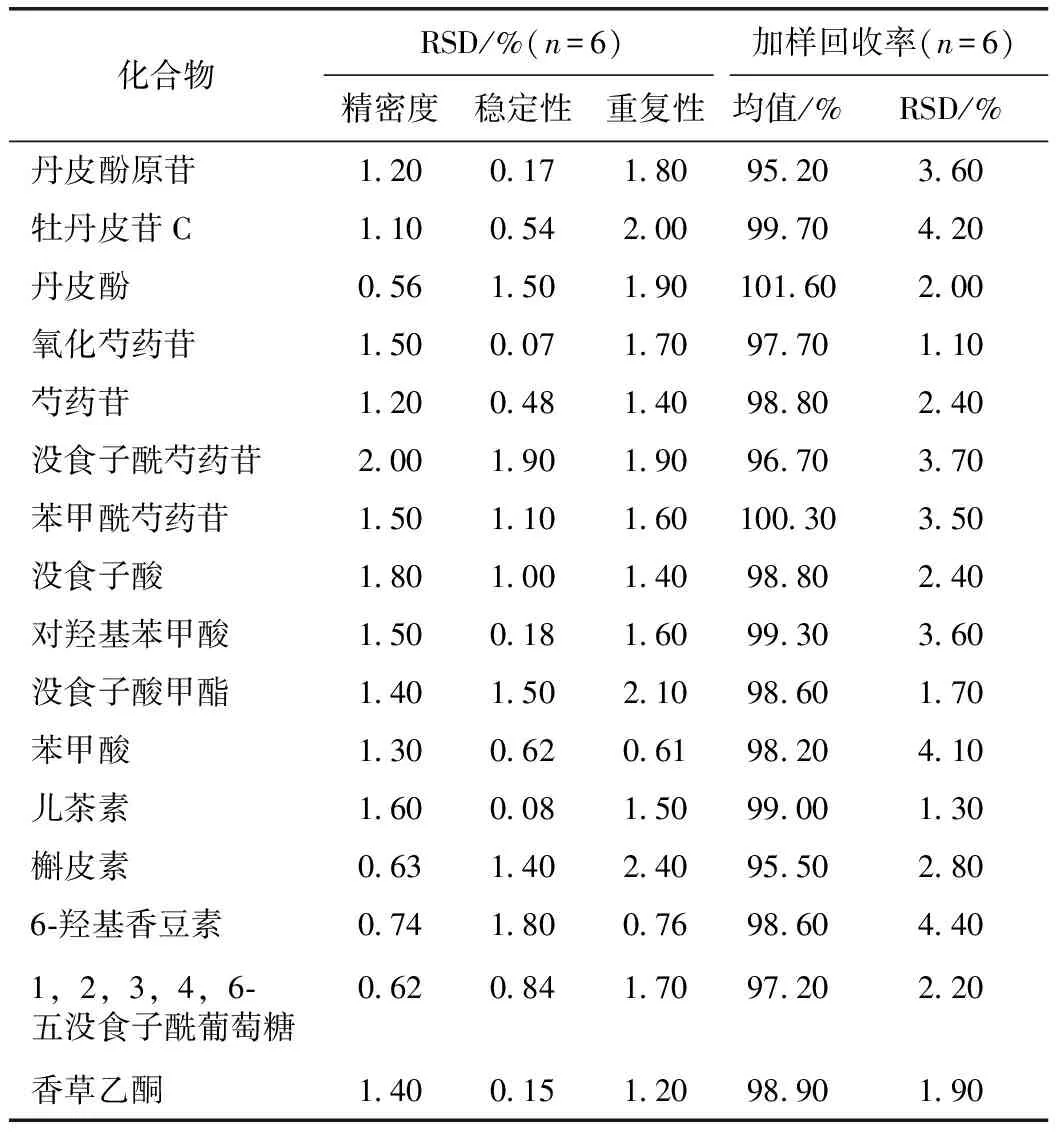
表4 各成分方法学考察
2.6 样品测定
取不同干燥方法处理的样品及一份鲜品适量,制备供试品溶液,按2.2项下色谱条件进样测定。每个样品平行3次,以均值作为测定结果,见表5。
3 结果与分析
3.1 主成分分析(PCA)
为综合评价不同干燥方法对牡丹皮化学成分的影响,以1~14号干燥品各类成分含量组成14×16矩阵,采用SPSS 22.0对矩阵进行主成分分析(PCA)。
前4个主成分的特征值均大于或接近1,见表6,说明前4个因子在反映牡丹皮不同干燥品的内在质量起着主导作用,4个主成分的累计贡献率达82.844%,能够较客观地反映牡丹皮不同干燥品的内在质量,故选取4个主成分进行分析。
牡丹皮苷C、芍药苷、没食子酰芍药苷、苯甲酰芍药苷、儿茶素、6-羟基香豆素、1,2,3,4,6-五没食子酰葡萄糖在PC1上有较高载荷,见表7,说明PC1主要反映了这些物质的信息;同理,PC2主要反应了丹皮酚、氧化芍药苷、没食子酸甲酯、苯甲酸、香草乙酮等成分的信息;PC3主要反应了对羟基苯甲酸、槲皮素的信息;PC4主要反应了丹皮酚原苷、没食子酸的信息。即前4个主成分基本包含了所测牡丹皮16个成分的信息。
采用4个主成分对牡丹皮不同干燥方法进行评价。以各主成分因子得分与方差贡献率乘积之和相加,得出各牡丹皮干燥品各类成分总因子得分值F,其综合评价函数为:F=0.342 61F1+0.234 77F2+0.143 22F3+0.107 84F4。
按综合评价函数计算出不同干燥品的综合得分(F),见表8。由综合得分可知,红外40 ℃干燥得分最高,红外50 ℃次之。
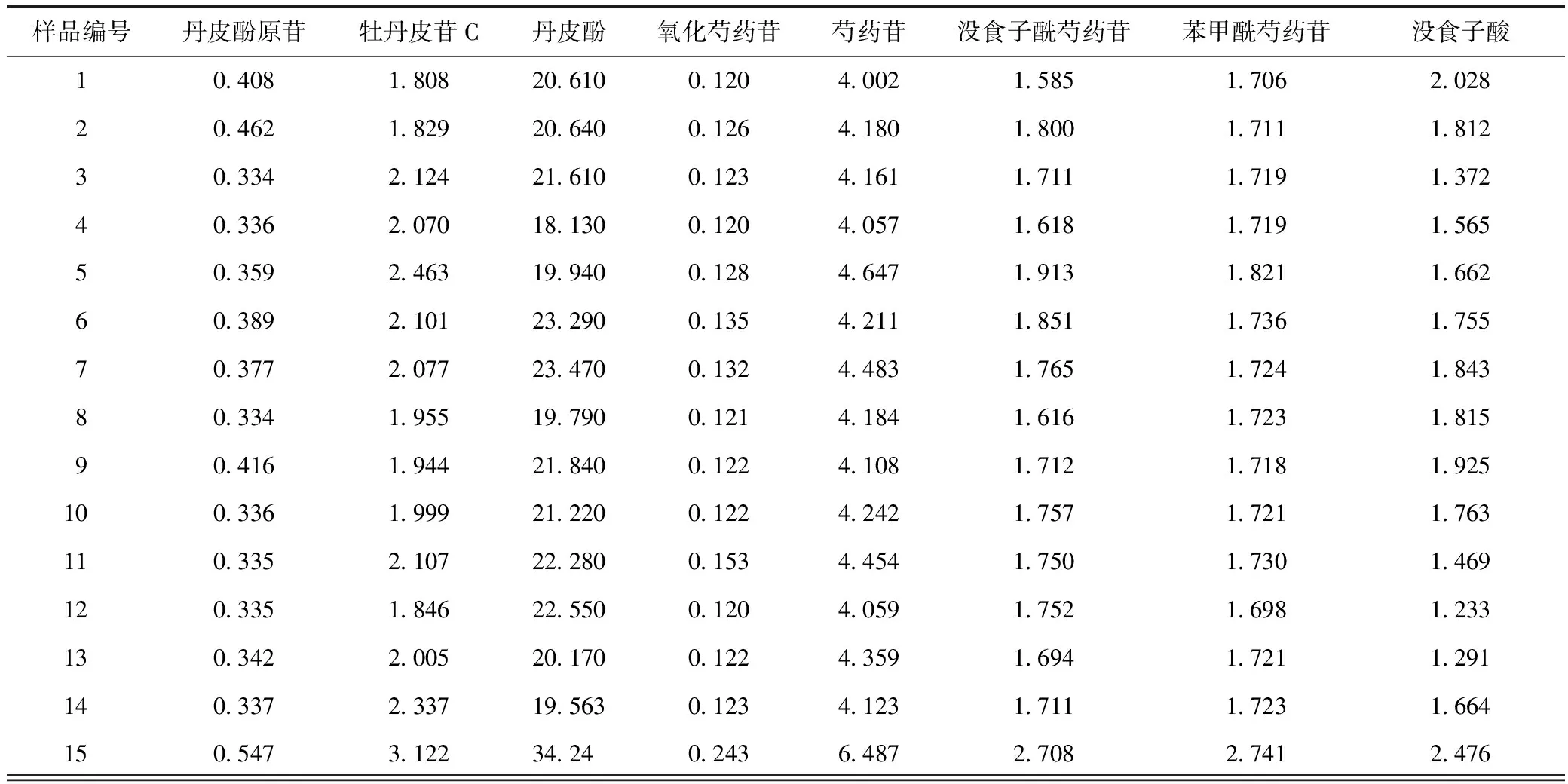
表5 不同干燥方法牡丹皮样品中各成分的质量分数(n=3) mg·g-1
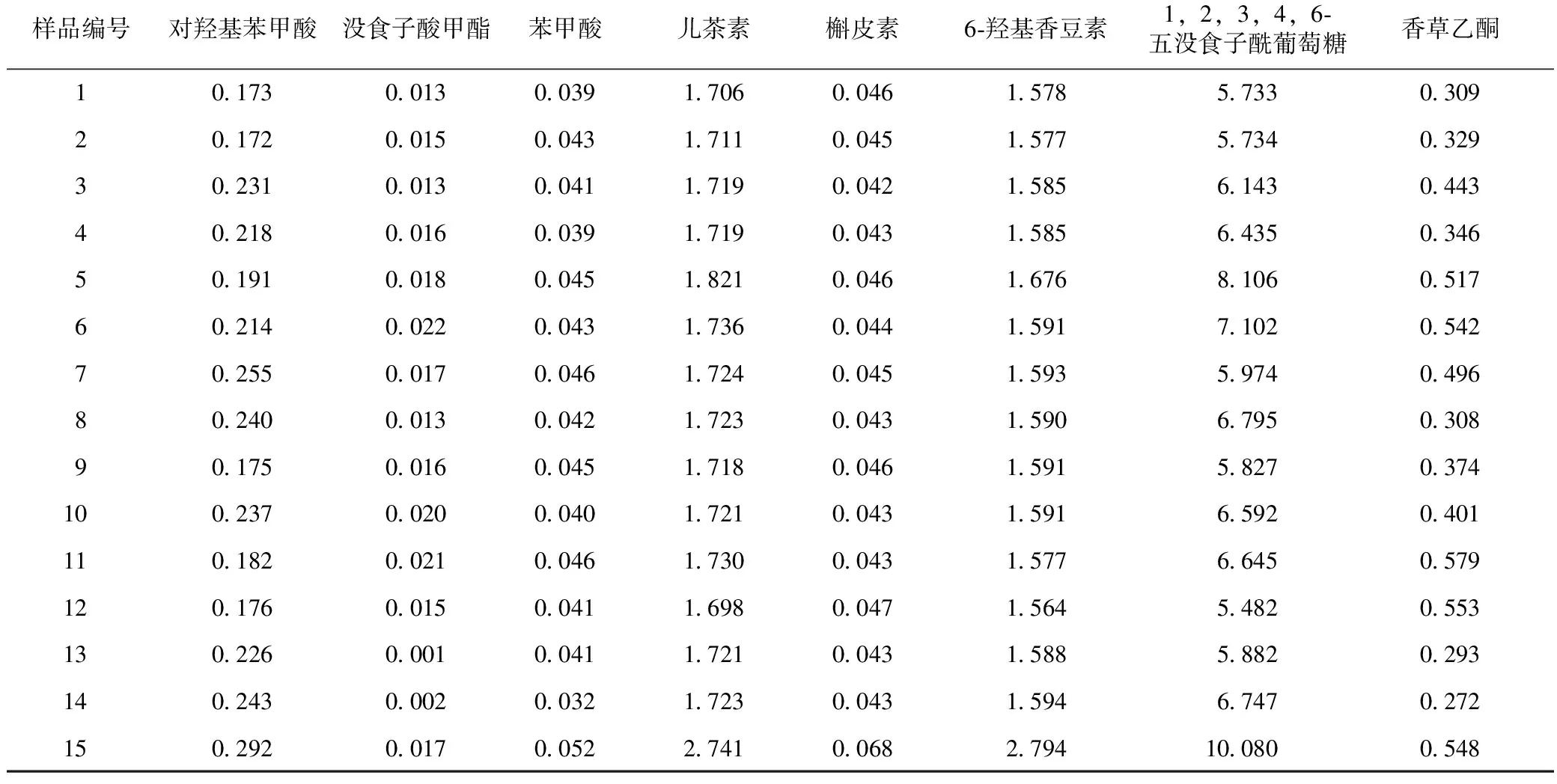
样品编号对羟基苯甲酸没食子酸甲酯苯甲酸儿茶素槲皮素6-羟基香豆素1,2,3,4,6-五没食子酰葡萄糖香草乙酮10.1730.0130.0391.7060.0461.5785.7330.30920.1720.0150.0431.7110.0451.5775.7340.32930.2310.0130.0411.7190.0421.5856.1430.44340.2180.0160.0391.7190.0431.5856.4350.34650.1910.0180.0451.8210.0461.6768.1060.51760.2140.0220.0431.7360.0441.5917.1020.54270.2550.0170.0461.7240.0451.5935.9740.49680.2400.0130.0421.7230.0431.5906.7950.30890.1750.0160.0451.7180.0461.5915.8270.374100.2370.0200.0401.7210.0431.5916.5920.401110.1820.0210.0461.7300.0431.5776.6450.579120.1760.0150.0411.6980.0471.5645.4820.553130.2260.0010.0411.7210.0431.5885.8820.293140.2430.0020.0321.7230.0431.5946.7470.272150.2920.0170.0522.7410.0682.79410.0800.548

表6 主成分的特征值及贡献率
4 讨论
通过分析不同干燥方法对牡丹皮中各类成分的影响发现,干燥后干燥品中酚及酚苷类成分(丹皮酚原苷、牡丹皮苷C、丹皮酚)含量变化最大、变化范围宽。研究表明,酚类物质在植物体内的生物合成及代谢易受多酚氧化酶(PPO酶)的影响而氧化成醌类成分[6-7]。上述酚类成分的变化可能由不同干燥条件下PPO酶活性的不同引起的。此外,丹皮酚为牡丹皮药材中最主要的成分,除微波干燥外,在其他两种现代干燥方式下,随着干燥温度升高,丹皮酚含量先升高后降低,60 ℃时达到最大,这可能由于:60 ℃以下,随着温度升高,丹皮酚含量损失时间变短,此阶段干燥时间是主要因素;60 ℃以后,随着温度升高,丹皮酚受热挥发含量降低,此阶段温度是主要因素[8]。
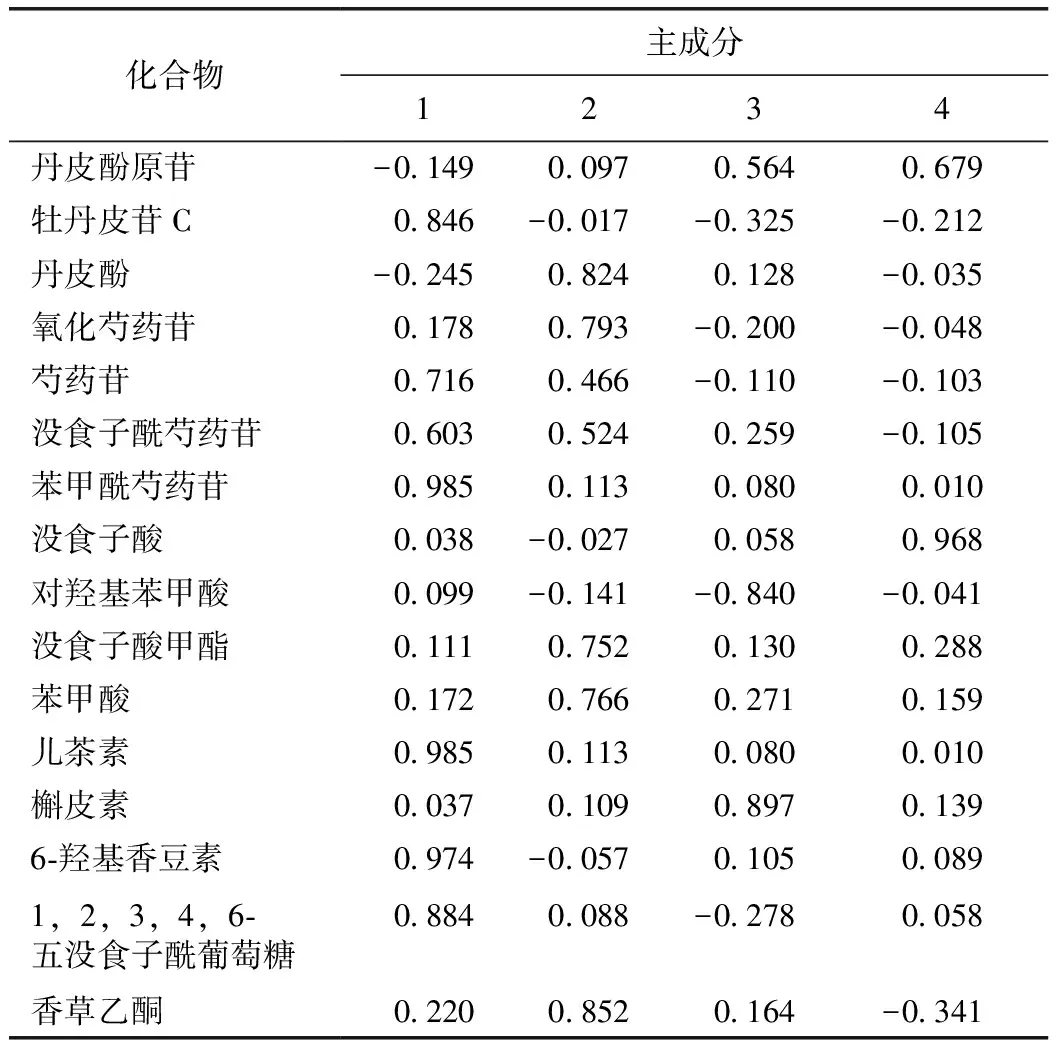
表7 旋转变换后的因子载荷矩阵
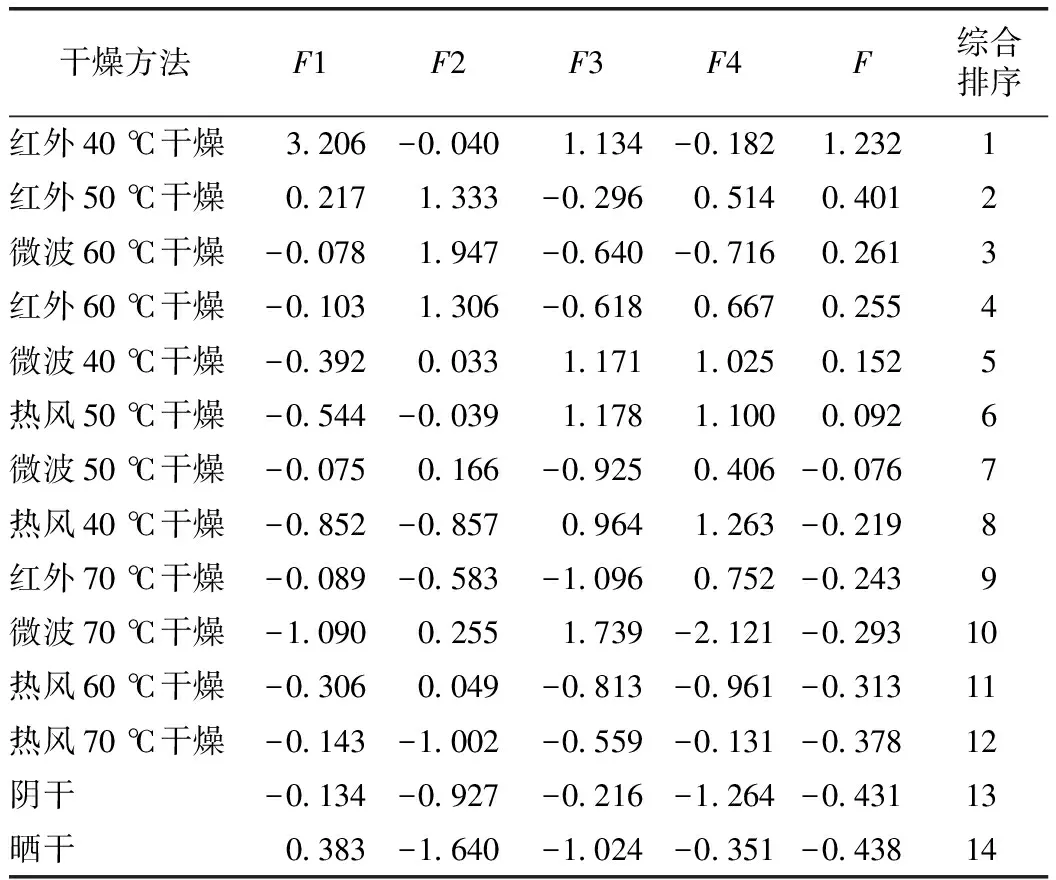
表8 不同干燥加工方法处理的牡丹皮成分含量综合评分
单萜苷类成分(氧化芍药苷、苯甲酰芍药苷、没食子酰芍药苷及芍药苷)含量变化趋势相似,红外>微波>热风,这可能由于热风干燥速率慢,物料内部不能迅速脱水,干燥时间较长使得单萜苷类水解损失较多[9]。微波虽然干燥速率较快,但在干燥初期有一个瞬间升温的过程,此过程可能对牡丹皮中单萜苷类成分造成破坏损失。
有机酸类成分(没食子酸甲酯、苯甲酸、对羟基苯甲酸、没食子酸)中没食子酸是主要成分,含量较高,干燥温度对没食子酸含量影响较大,快速低温干燥提高了没食子酸的稳定性[10],且40~60 ℃没食子酸含量较高。
黄酮类成分槲皮素、儿茶素两者在晒干后含量下降最多,有研究表明光照促进了槲皮素、儿茶素这两个成分分解。1,2,3,4,6-五没食子酰葡萄糖为鞣质类成分,其在干燥后含量较鲜品均降低,这可能由于鞣质类成分对湿热较敏感,采用一般的干燥方法不能保存其主要成分,其在湿热条件下可能会降解[11]。而6-羟基香豆素为苯丙素类,其在3种现代干燥方式下变化趋势相似,均随温度升高,含量先升高后降低,在温度为50~60 ℃时含量较高,且干燥后含量均低于鲜品,晒干样品中的6-羟基香豆素含量最高[12]。这可能由于6-羟基香豆素为苯丙素类,具有邻羟基桂皮酸内酯结构,具有热不稳定性,干燥温度低有利于有效物质的保留[13]。
本研究分析了不同条件干燥后各样品成分含量,发现红外40 ℃干燥综合得分最高,说明药材的综合品质最好,并且分析了不同干燥方式下牡丹皮药材中各类成分含量的变化,为后续牡丹皮药材产地干燥过程中稳定药材品质提供了支撑,也为根类药材产地加工共性技术的形成提供了有益的探索和实践。
