GOD 在MspA 和BLM 修饰玻碳电极表面上的直接电化学和电催化研究
2020-03-27曹远福
曹远福
(江西有色地质勘查二队,江西 赣州 341000)
葡萄糖氧化酶属于氧化还原酶类。GOD 的氧化还原反应的实质是氢转移反应,其在体内主要的生理功能是在O2存在的条件下,催化葡萄糖氧化成葡萄糖内脂的同时生成H2O2,所以,将GOD 作为生物燃料电池阳极催化剂和葡萄糖生物传感器的研究有重要意义。但由于GOD 的氧化还原活性中心FAD 深埋在酶分子内部,通常情况下难以进行直接的电化学反应。到目前为止GOD 可以在介孔分子筛上进行直接电化学反应,在生物燃料电池中,GOD 在修饰电极上的直接电化学反应研究也较多,这也是生物燃料电池阳极催化剂的发展趋势。
1 材料与方法
1.1 化学试剂
双肉豆蔻磷脂酰胆碱(DMPC)(纯度≥99%),铁氰化钾,高纯氯仿,凝蛋白度为4.09 的孔蛋白,葡萄糖氧化酶来自美国Sigma 公司。磷酸盐缓冲溶液(PBS),无水乙醇,0.1 mol L-1葡萄糖溶液,0.05mol L-1葡萄糖溶液(北京化学试剂厂,由tris+kcl 配制,使用前在室温条件下放置过夜),C12H10FeO4,粉末状,配成0.02mmol/L 的FMCA 的pH=6.62 的PBS 溶液, 除非特殊提到的地方所有的水溶液均用二次水[1]。
1.2 GOD/MSPA/BLM/GC 电极的制备
制备膜液:取2mgDMPC 溶解于1ml 的氯仿中。在制备磷脂双分子层以前,在抛光布上用Al2O3对电极进行抛光,并在5mmol/L 铁氰化钾溶液中进行循环伏安测量,在得到氧化还原电势差≤160mV,才算电极磨好。并在去离子水中超声。然后用氮气将电极吹干,再吸取10uL 膜液滴在电极表面,待氯仿挥发后磷脂双分子层即已形成。吸取一定量的孔蛋白溶液滴在磷脂双分子层的表面,待电极表面干后,则固定了孔蛋白的磷脂双分子层的电极表面形成,最后吸取一定量的葡萄糖氧化酶溶液滴在上述电极表面,等电极干后,则葡萄糖氧化酶嵌在了孔蛋白上,GOD/MSPA/BLM/GC 电极制备成功。
2 结果与讨论
2.1 紫外光谱表征
UV-Vis是监控蛋白质二级结构变化的强有力探针。我们分别做了纯GOD溶液,GOD/MspA/BLM的紫外吸收光谱,由左图可得:在波长377nm和446nm处,GOD的氨基酸残基特征吸收峰、GOD活性中心FAD的特征吸收峰被分别地展现出来。由右图可得:GOD/MSPA/BLM电极上氨基酸残基特征吸收峰由377nm处蓝移至358nm, FAD的特征吸收峰从446nm 蓝移至435nm处。表征结果表明:GOD被孔蛋白固定后其空间的二级结构发生了改变。

图1 纯GOD(左)和GOD/MspA/BLM(右)的紫外吸收光谱图
2.2 电化学表征
用K3[Fe(CN)6作为标记离子,其在玻碳电极和在玻碳电极上形成有磷脂膜的电化学响应如图2 所示。在裸玻碳电极上出现K3[Fe(CN)6]/K4[Fe(CN)6]可逆氧化还原峰电流,在表面覆盖有DMPC 膜电极上明显降低,而且氧化峰和还原峰的电位差值ΔEp 也明显增大,这说明[Fe(CN)6]3-到达电极表面产生电化学响应的过程在一定程度上受到阻碍,这是由于季铵盐磷脂分子是一种致密且有序排列的、膜内通道均处于关闭状态的结构,大量的K3[Fe(CN)6]/K4[Fe(CN)6]不能穿过膜到达电极表面,同时这样的结果也预示着我们已经在玻碳电极上成功的制备出磷脂双分子层,正是磷脂膜阻碍了K3[Fe(CN)6]的电化学响应[2]。
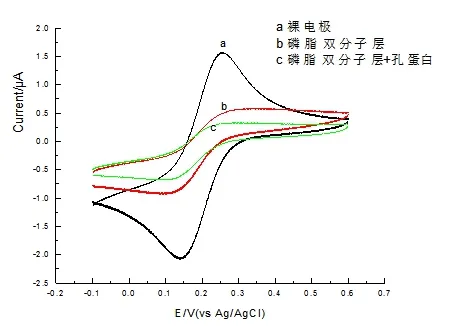
图2 玻碳电极在1mmol/LK3[Fe(CN)6]中的循环伏安响应
2.3 不同扫速时,GOD/MSPA-BLM/GC 电极的表征
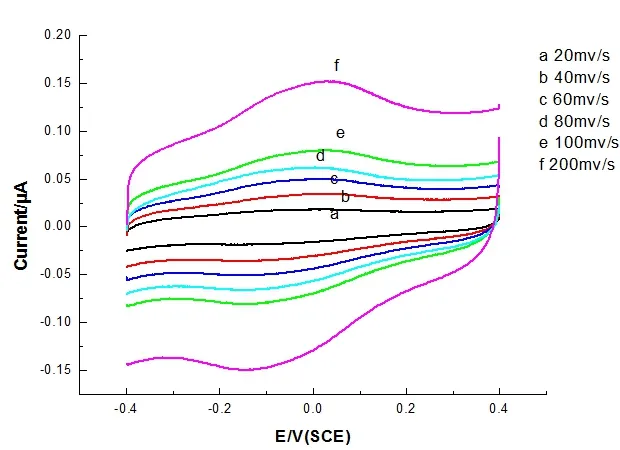
图3 玻碳电极在0.1mol/L 磷酸盐缓冲溶液(pH=7.0)中不同扫速时的循环伏安图
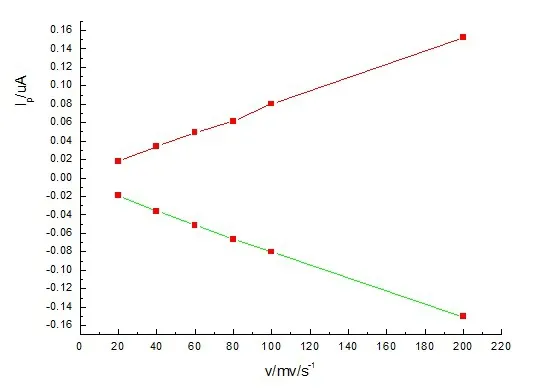
图4 pH=7 时,玻碳电极的阳极峰与阴极峰电流与扫速的线性关系
由图3 可知:随着扫速的增加,玻碳电极的氧化峰电位与还原峰电位几乎不移动。在扫速为20-200mV/s 范围内,无论玻碳电极的阳极峰电流还是玻碳电极的阴极峰电流,均随扫速线性相关(图4),方程分别为:Pa: y=-4.0872×10-8+7.42293×10-9x,r=0.99955: Pc: y=-6.98803×10-8-7.21284×10-9x, r=-0.99942,这表明:电极上GOD 的氧化还原反应,是一个表面控制的过程。根据Laviron 计算出速度常数(ks)为3.89 s-1,这个数值比经过打磨的SWNTP (1.7s-1)电极,电镀阳极(1.6s-1)都高,这说明GOD/MSPA-BLM/GC 电极的直接电子转移速率很快。
2.4 不 同pH 的PBS 溶 液 对GOD/MSPA-BLM/GC 电 极 的表征

图5 GOD/MSPA-BLM/GC电极在不同pH值的磷酸盐缓冲液中的循环伏安图

图6 E0 与pH 的线性关系
图5 GOD/MSPA-BLM/GC 电极在扫速为200mV/s, 0.1M的PBS 中,pH 分别为2.00 (a), 4.00(b), 6.00(c), 8.00(d)和10.00(e)时的循环伏安图。很显然在不同pH 值的PBS 中,玻碳电极上的GOD 均能产生一对稳定的几乎可逆的氧化还原峰,且随着pH 值由2 到10 的递增,其氧化、还原的峰电位均发生负移,而且GOD/MSPA-BLM/GC 电极上,GOD 的最大氧化峰电流和还原峰电流均出现在pH 值为2 的PBS 中。由图6 可知:在pH 值2.00~10.00 的区间内标准电极电位 E0 与PBS 的pH 值呈线性相关,其斜率为-51.23mV/pH,该数值与可逆电化学反应过程的理论值(-55.87mV/pH)相接近。结果表明:葡萄糖氧化酶修饰的玻碳电极上,GOD 发生直接电化学反应的同时还包含着两个质子和两个电子的传递。
2.5 GOD/MSPA-BLM/GC 电极上GOD 催化活性研究
实验结果证明,修饰电极上的GOD 同样具有功能活性,测试固定酶的活性,需看其对底物的催化能力是否存在。图7 给出了GOD/MSPA-BLM/GC 电极在氧气饱和(a)、空气饱和(b)、氮气饱和(c)的0.1M PBS 中的循环伏安图,其扫描速率为100mV/s。由图可知:在氮气饱和的条件下,得到的是一对清晰且对称的氧化还原峰 (曲线c),说明GOD/MSPA-BLM/GC 电极上的GOD 能发生近乎可逆的、直接的电化学反应。当被空气饱和时,氧化峰消失,还原峰增大(曲线b),说明电极上的GOD 对氧气有催化还原的作用。被氧气饱和,观察到了一个巨大的还原峰(曲线a),且a>b,说明:氧气浓度越高,GOD 的催化还原能力越强。
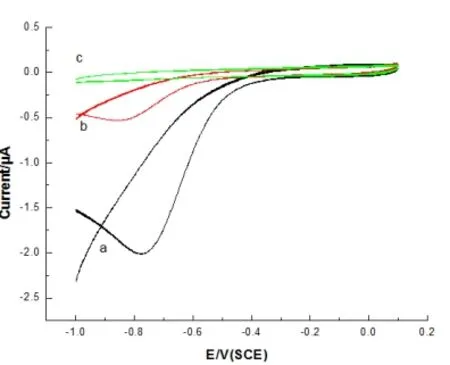
图7 GOD/MSPA-BLM/GC 电极在氧气饱和(a)、空气饱和(b)、氮气饱和(c)的0.1M PBS 中循环伏安图
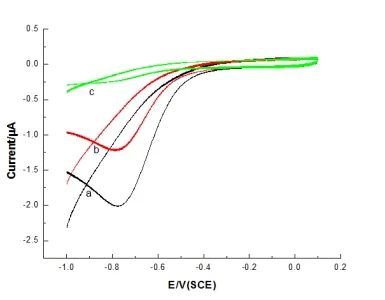
图8 被氧气饱和的PBS 缓冲溶液与存在4.55mM(b)的葡萄糖和存在8.33 mM(c)葡萄糖的循环伏安图
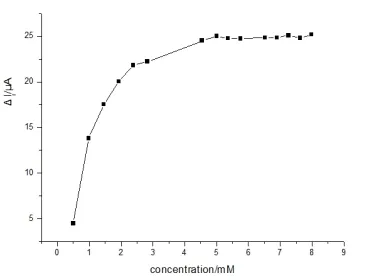
图9 ΔIr 与葡萄糖的线性关系图
由图8 可知:GOD/MSPA-BLM/GC 电极上,GOD 对底物葡萄糖的电催化作用,可通过观察氧气还原峰峰电位(-1.0~-0.1 V 范围内)的变化来实现。当向氧气饱和的PBS 中加入葡萄糖到时,GOD 对氧气的催化还原峰电流随葡萄糖浓度的增大而减小。在图9 中,发现ΔIr(缓冲溶液中不存在葡萄糖与存在葡萄糖时还原峰电流的差值)只在葡萄糖浓度从0 mM 到2.0mM 范围时,ΔIr与葡萄糖浓度线性相关,这样狭窄的线性范围是由于实验过程中氧气的消耗,氧气分压逐渐减小,对反应起抑制作用而引起的,当葡萄糖浓度高于2.0mM 时,ΔIr基本保持不变,展现出典型的米氏反应的特征[3,4]。
3 结语
本文使用孔蛋白作为葡萄糖氧化酶的载体。采用物理吸附法成功制备成了GOD/MSPA-BLM/GC 工作电极,运用循环伏安法研究了GOD/MSPA-BLM/GC 电极的直接电化学行为。研究表明,首先在K3[Fe(CN)6]溶液中,可以得出磷脂双分子层已成功铺在玻碳电极上,而且孔蛋白也已成功的嵌在磷脂双分子层上。其次,在磷酸盐缓冲溶液中(PBS),GOD/MSPA-BLM/GC 电极上的GOD 发生了直接的,近乎可逆的两电子两质子表面控制的电化学反应。
