复方脑肽节苷脂注射液对急性脑梗死的临床疗效及对患者Lp-PLA2 hs-CRP NSE水平的影响
2020-03-26李兴明刘娟娟陈俊斌刘建祥焦臣泽
李兴明, 刘娟娟, 陈俊斌, 刘建祥, 焦臣泽
(汕头大学医学院附属粤北人民医院神经内科, 广东 汕头 512026)
急性脑梗死约占全部脑卒中的70%~80%,目前国内外推荐最有效的治疗方法是早期闭塞血管再通,但由于大部分患者对此认识有限,溶栓或者介入治疗时间窗内接受治疗的患者比例约为2.6%,因此早期积极有效的保护神经及阻断神经损伤显得尤为重要[1]。急性脑梗死可由多个病理环节参与,动脉粥样硬化斑块易损性是缺血性脑卒中的病理过程之一,近年来的研究表明炎症在动脉粥样硬化中起着重要作用,炎症标志物揭示了卒中的亚临床变[2]。研究表明,血清脂蛋白相关磷脂酶A2(LP-PLA2)、超敏C反应蛋白(hs-CRP)、神经元特异性烯醇化酶(NSE)可直接参与动脉粥样硬化形成以及脑组织神经元水肿、变性、坏死的多个环节,为判定急性脑梗死严重程度及判断预后的灵敏指标[3]。复方脑肽节苷脂注射液(CPCGI)为一种治疗急性脑梗死的新型药物,对于急性脑梗死神经保护及抗炎方面具有重要作用[4]。本文旨在探讨复方脑肽节苷脂注射液治疗急性脑梗死早期(48h内)的临床疗效及对血清Lp-PLA2、hs-CRP、NSE水平的影响。
1 资料与方法
1.1一般资料:选取2017年1月至2018年6月期间,在我院住院治疗的急性脑梗死患者160例,随机分为对照组和治疗组,各80例。对照组男49例,女31例,年龄45~79岁,平均(65.03±8.12)岁;治疗组男43例,女37例,年龄48~78岁,平均(66.30±7.35)岁。纳入标准:按《中国急性缺血性脑卒中诊治指南2018》诊断标准,诊断为急性脑梗死患者,发病48h以内,美国国立卫生研究院卒中量表(National Institute of HealthStroke Scale, NIHSS)为5~25分,年龄≥18岁的男性或女性患者。排除标准:发病8h内行静脉溶栓或血管内治疗,严重的心、肺、肝、肾全身性疾病(丙氨酸转氨酶(ALT)或天冬氨酸转氨酶(AST)>2倍正常值上限,肌酐>1.5倍正常值上限,急性发作哮喘或慢性阻塞性肺病(COPD)或心功能IV级),出血或有出血倾向,孕妇、哺乳期妇女,肢体功能障碍、精神障碍、认知功能障碍,复方脑肽节苷脂注射液过敏或禁忌,在三个月内参加另一临床试验的患者。记录两组患者基线资料(既往史、卒中类型)及实验室指标,包括血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、血肌酐(Scr)。这项研究已得到我院伦理委员会的批准,所有患者均签署知情同意书。
1.2治疗方法:所有入组患者入院后根据《中国急性缺血性脑卒中诊治指南2018》予以抗血小板、调脂、控制血压、血糖等基础治疗,治疗组在此基础上加用复方脑肽节苷脂注射液(国药准字H22026472吉林步长公司 规格2mL/支)12mL+0.9%氯化钠注射液或5%葡糖糖注射液250mL中,缓慢滴注(2mL/分),每日1次,14d为一疗程。治疗期间如病情加重或对所使用药物的副反应无法耐受者则中断治疗。
1.3观察指标:检测治疗前后空腹抽血检测血清Lp-PLA2、、hs-CRP、NSE。Lp-PLA2采用连续监测法(速率法),hs-CRP采用免疫荧光干式定量法测定法,NSE采用电化学发光法。依据美国国立卫生研究院卒中量表(National Institute of HealthStroke Scale, NIHSS)分别对治疗前后及随访3个月患者进行神经功能评分(包括意识水平,意识水平提问及指令,凝视,视野面瘫,上下肢运动、肢体共济失调等共11项,总分0~42 分),评分越高,表示神经功能缺损越严重。依据日常生活能力量表(ADL)选用Barthel指数(BI)记分法分别对治疗前后及随访3个月患者进行日常生活活动能力评分,满分100分,分数越高,说明生活自理能力越强,以及治疗前后肝肾功能指标检测(包括ALT、AST及Scr)及皮疹、恶性和呕吐等不良反应。

2 结 果
2.1两组患者临床基线资料比较:两组患者的年龄、性别、吸烟、饮酒、高血压、糖尿病、心脏病、高血脂、卒中病史及梗死类型、实验室指标(ALT、AST、Scr)等相比,差异均无统计学差异(P>0.05),见表1。
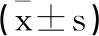
表1 两组患者临床基线资料对比
2.2两组患者治疗前后Lp-PLA2、hs-CRP和NSE水平比较:两组患者治疗前Lp-PLA2,hs-CRP和NSE水平比较差异无统计学意义(P>0.05)。治疗后,上述指标均有显著下降(P<0.05);且治疗组患者的Lp-PLA2、hs-CRP和NSE水平显著低于对照组(P<0.05),见表2。
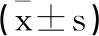
表2 两组患者治疗前后Lp-PLA2 hs-CRP NSE的比较

表3 两组患者治疗前后和用药3个月后NIHSS、ADL评分的比较分)
2.3两组患者治疗前后及随访3个月后NIHSS和ADL评分比较:两组患者治疗前NIHSS和ADL评分比较差异无统计学意义(P>0.05)。治疗后,NIHSS评分显著下降,而ADL评分显著上升(P<0.05)。治疗后及随访3月后,治疗组NIHSS水平显著低于对照组,ADL水平显著高于对照组(P<0.05),详见表3。
2.4不良反应发生情况:治疗后,治疗组出现肝功能异常3例,对照组出现肝功能异常2例,差异无统计学意义(χ2=0.207, P=0.650),治疗组出现肾功能异常2例,对照组出现肾功能异常4例,差异无统计学意义(χ2=0.693, P=0.405),两组患者均无皮疹、恶性呕吐等情况的发生。
3 讨 论
复方脑肽节苷脂注射液是治疗急性脑梗死的神经保护剂,研究表明复方脑肽节苷脂注射液能够促进缺血脑组织的新陈代谢,其可参与神经细胞的生长、分化和再生,具有免疫调节、抗氧化、抗炎作用[5],但其确切的抗炎作用机制仍不清楚。因此,本研究旨在探讨复方脑肽节苷脂注射液对急性脑梗死患者的疗效及其炎症反应的影响,为复方脑肽节苷脂注射液改善炎性介质的作用机制的深入研究提供了依据。
急性脑梗死的治疗目标是尽早恢复闭塞血管的血流,促进脑梗死区侧枝血管开放,进而恢复脑组织的血流,改善脑组织营养代谢和恢复神经细胞功能,因而保护受损神经细胞、减少进一步损伤变得尤为重要,急性脑梗死缺血部位脑组织早期损伤的致病机制为脑细胞内外酸中毒及诱导形成自由基和脂质过氧化物生成,导致线粒体电子呼吸链损害,使得ATP合成障碍,由于细胞离子失衡,大量Na+、C1-、Ca2+内流,导致细胞酸中毒加剧,进而出现细胞水肿及兴奋性氨基酸释放,并激活NO合成酶产生大量NO,产生神经毒性,并激发炎症反应导致微循环障碍,最终导致脑组织坏死、神经细胞死亡[6]。血小板活化因子Lp-PLA2是巨噬细胞合成并分泌的一种炎症反应物,Lp-PLA2在炎症级联反应中可以形成不稳定斑块,阻塞动脉血管诱发脑梗死。血清CRP是一种肝脏产生的急性期反应蛋白,其作为炎性因子,一方面可通过血液补体系统激活泡沫细胞,促进血栓形成,另一方面还可诱发血管内膜增厚和斑块破裂[7]。NSE是一种神经内分泌型的可溶性蛋白酶,受损的脑组织可释放NSE,是脑损伤和坏死的特异性指标,通过检测外周血清NSE水平可判断病情严重程度,且与预后密切相关。
复方脑肽节苷脂注射液是一复方制剂,其主要成分为多肽、多种神经节苷脂、次黄嘌呤等,其中次黄嘌呤能够改善脑细胞的物质与能量代谢,对受损的脑细胞起修复功能。神经节苷脂可参与细胞的识别、粘着、生长、分化以及细胞信息传递等过程,并且具有参与神经组织的分化、再生、修复作用,能加速损伤的神经组织的再生修复,促进神经支配功能恢复,减低兴奋性氨基酸的释放,研究发现其作用机制可能是通过激活线粒体自噬功能发挥的[8]。大量研究证实急性脑梗死患者的血清Lp-PLA2、hs-CRP、NSE多高于正常水平,与脑梗死严重程度及预后有关[2]。本研究发现,两组患者治疗后Lp-PLA2、hs-CRP、NSE均明显下降,但治疗组明显低于对照组,提示复方脑肽节苷脂注射液作用机制可能是降低血清Lp-PLA2、hs-CRP、NSE水平,从而起到保护脑细胞作用。
本研究表明急性脑梗死患者即使不在溶栓或者介入治疗时间窗内,早期予以复方脑肽节苷脂注射液治疗,能够有效改善神经功能缺损症状,改善患者生活质,且能显著降低血清中Lp-PLA2、hs-CRP、NSE炎性因子水平,保护缺血的脑细胞,可作为预防急性脑梗死的潜在靶点,且无肝肾损害及其它不良反应,临床应用安全,值得临床应用及推广。
