煤直接液化制油技术研究现状及展望
2020-03-19胡发亭王学云毛学锋李军芳
胡发亭,王学云,毛学锋,李军芳,赵 鹏
(1. 煤炭科学技术研究院有限公司 煤化工分院,北京 100013;2. 煤炭资源开采与洁净利用国家重点实验室,北京 100013;3. 国家能源煤炭高效利用与节能减排技术装备重点实验室,北京 100013)
0 引 言
化石能源是宝贵的不可再生能源和一次能源,我国化石能源总的特点是富煤贫油少气。我国煤炭探明可采储量达1 145亿t,居世界第3位[1]。2018年,我国煤炭产量达到36.8亿t,煤炭消费量在我国能源消费总量中占比59%,我国已经成为世界上最大的煤炭生产国和消费国[2-3]。煤炭价格低廉、来源可靠、可清洁利用,因此在未来相当长时期内,煤炭仍将是我国最丰富、可靠、经济的主体基础能源和重要原料。我国煤炭资源丰富,分布较广,煤种齐全,且大部分是中低变质、宜于加氢液化转化的煤种,对发展煤直接液化制燃料油及化学品是非常重要的资源保障。
近年来,由于我国工业发展迅速,石油、天然气进口量和消费量逐年大幅增加。目前,我国已成为世界上石油和天然气最大的进口国,石油和天然气对外依存度分别达到70.8%和43.2%,而且我国石油剩余使用年限为18 a左右,远低于全球50 a的平均水平,严重影响了我国的能源安全[4]。
煤炭直接液化制油技术是在高温高压条件下,煤炭在氢气、供氢溶剂和催化剂共同作用下,于反应器中经过热萃取、溶解、分解和加氢等物理化学过程,脱除S、N、O等杂原子,最终将固体煤转化成液态的油,生产洁净的液体燃料和化工原料的工艺技术,煤炭直接液化也被称为煤炭加氢液化。煤直接液化制油技术是促进煤炭清洁高效利用的有效途径,已成为保障我国能源供应安全、促进经济可持续发展的战略举措,对充分利用国内资源、解决石油安全具有重要的战略和现实意义。本文总结了一个世纪以来煤直接加氢液化技术的发展历程和技术进展,阐述了国内外在煤加氢液化反应机理、反应动力学、催化剂及液化工艺方面的发展状况,并对未来煤直接液化技术的研究重点和发展趋势进行展望,旨在为煤直接液化制油技术的关键技术开发和工业化推广提供理论基础与技术指导。
1 煤直接液化反应机理
1913年,德国Bergius发明了煤炭加氢液化技术,自此,许多学者开始对煤液化过程中的加氢液化反应机理以及氢转移机理进行研究。Zielke等[5]首先提出了煤加氢液化自由基反应机理,目前自由基反应机理得到了众多学者的一致认可。该机理认为,煤的直接加氢液化过程就是通过加热使煤分子结构之间的桥键断裂而分解生成自由基碎片,自由基在氢气、催化剂、溶剂存在的条件下与活性氢自由基结合,生成低分子的气体、水、油、沥青质等产物。因此,煤加氢液化自由基反应过程一般可分为煤的热解、氢传递和加氢反应3个步骤。
1.1 煤热解
煤炭升温到一定温度(250~300 ℃),煤中键能最弱的部位开始断裂,生成自由基碎片,温度进一步升高,煤中一些键能较低和较高的部位也相继断裂,产生自由基碎片。煤的热解是煤自身化学反应,主要由温度决定,受物理作用如搅拌、震荡等的影响比较小,因此选择适宜的加氢液化温度非常重要。
吴爱坪等[6]研究了胜利煤和新疆煤热解过程中的自由基变化,发现这2种煤在300~500 ℃热解时主要发生裂解反应,煤中芳环和桥键断裂,产生大量自由基,550 ℃以上,以缩聚反应为主;原煤与溶剂混合后升温,会快速热解释放出自由基,自由基浓度在10 min左右就会达到最大值,热解生成的自由基会与溶剂中的氢或小分子自由基结合,活性氢的数量直接决定了煤转化率和油收率。
1.2 氢传递
煤热解产生的自由基碎片不稳定,且反应活性很高,易与活性氢结合稳定下来,生成低分子量的沥青烯、油、气等初级加氢产物。煤液化过程中的活性氢主要来源于氢气、供氢溶剂、煤本身分子结构中的氢。供氢体不同,自由基反应中的氢传递路径不同。清晰认识煤直接液化过程中的氢传递途径和氢传递机理对于降低氢耗、提高煤转化率、改善液化油品质量具有非常重要的意义。
学者在氢传递路径和机理等方面进行了大量研究,对煤的加氢液化自由基反应机理达成了共识,认为采用强供氢能力溶剂、提高氢气压力、使用高活性催化剂等是促进活性氢产生的重要途径,另外反应温度和反应时间也会影响自由基反应中的氢传递[7-11]。Neavel等[7]以黄铁矿为催化剂,在管式反应器中对低阶煤进行液化试验,发现煤通过热解能为加氢液化反应提供部分活性氢,也能向自由基传递自身裂解产生的活性氢。史士东[10]研究了神东煤在铁系催化剂下的加氢反应行为,发现煤转化率小于57%时,稳定自由基的活性氢主要来源于供氢溶剂和煤自身;转化率大于57%时,反应活性氢主要来源于氢气,这时,氢气消耗量增加很快。赵鹏等[11]利用铁系复合型催化剂,研究了淖毛湖煤在四氢萘溶剂下的加氢液化反应行为,发现溶剂对液化反应的活性氢贡献更大,是气相氢的2倍左右。
近年来,随着科学技术的进步,同位素示踪技术开始成功应用于化学工程中,学者采用2H、3H、14C、35S等同位素示踪方法开展了煤液化过程中的氢转递途径及机理的研究,取得了大量的研究成果[12-13]。
Kabe等[14-15]利用14C和3H元素示踪法研究了煤加氢液化过程中的氢传递机理及加氢反应机理,发现不加催化剂的条件下,液化反应初期,稳定自由基碎片的活性氢基本来自供氢溶剂;当以甲苯作为溶剂并添加载体镍钼类催化剂时,即使在反应初始阶段,氢气与煤之间的交换也非常迅速。当添加催化剂并用萘作溶剂时,发现自由基的加氢反应也是通过萘作为媒介实现的,说明萘先被催化加氢生成了四氢萘,四氢萘再释放活性氢与自由基发生反应;无论使用哪种溶剂,3H在液化产物油、前沥青烯、沥青烯、残渣中的浓度依次升高。Wilson等[16-17]利用示踪方法研究了烟煤的加氢液化行为,发现氢首先进入芳香环的α脂肪碳上而不是远离芳香环的β和γ脂肪碳上。Ishihara等[18]对煤、水混合物和氢气的交换规律及机理进行研究,发现氢气产生的活性氢没有经过溶剂的传递,直接和煤热解自由基碎片发生了反应。
牛犇[19]利用纳米铁催化剂和同位素示踪法研究了溶剂的作用及氢传递机理,研究表明,液化升温阶段未加催化剂时,氢耗的80%来自溶剂,加催化剂后氢耗的50%来自溶剂。液化反应60 min时,未加催化剂时,氢耗的65%来自溶剂,加催化剂时,氢耗的35%来自溶剂。
1.3 加氢反应
加氢反应就是自由基或中间产物与活性氢结合发生加氢反应的过程,加氢反应的类型主要有芳烃加氢饱和、加氢脱氧、加氢脱氮、加氢脱硫和加氢裂化等几种。加氢催化剂的活性不同或加氢条件的苛刻度不同,加氢反应的深度也不相同。当加氢液化过程中温度过高或供氢不足时,有些自由基碎片就会相互结合缩聚成分子量更大的物质。
综上所述,煤液化反应是一个自由基反应过程,分为自由基加成过程和自由基传递过程。自由基反应的关键是氢传递,不同的氢传递路径之间相互竞争,溶剂中芳烃含量高和反应温度低则倾向于通过氢自由基传递过程,而溶剂中芳烃含量低时则更倾向于通过氢自由基加成过程[19]。供氢性溶剂确实具有氢传递的作用,但供氢溶剂是否为氢传递的主要路径还需要进一步证实。催化剂的存在促进了气相氢到溶剂的传递,同时促进了溶剂氢到煤的传递。在不同煤种、溶剂、催化剂或工艺条件下,煤液化过程中氢的传递途径和传递机理不完全相同。阐明不同条件下供氢体被活化的控制步骤以及活性氢与自由基碎片的结合路径是今后需要研究的重点方向。
由于煤的分子结构复杂,在煤直接液化反应器中,煤、供氢溶剂、氢气以及催化剂共存,热解和加氢反应多种多样,产物也是多种多样。由于产物定量分析困难和试验手段的限制,目前,人们尚未完全准确认识煤的加氢液化反应机理、反应历程以及氢在液化过程中的传递规律。
2 煤直接液化反应动力学
由于煤的加氢液化反应路径十分复杂,不同的反应条件、煤种以及不同的反应阶段煤的加氢液化反应类型及控制因素不同,无法用统一的反应动力学模型来描述。国内外学者对煤加氢反应动力学进行了详细研究,建立了不同煤种、不同催化剂、不同工艺等条件下的煤加氢液化反应动力学模型。
2.1 单组分和多组分动力学模型
1951年,Weller等[20]最早提出了煤加氢液化反应动力学理论,认为煤加氢液化反应过程是一个以沥青烯为中间产物的串联反应过程:煤—沥青烯—油。1978年,Cronauer[21]提出了具有影响力的液化反应并联动力学模型,将煤假设为单一活性组分,可以同时转化为前沥青烯、沥青烯、油、气,且为一级不可逆平行反应。Shah[22]利用固定床反应器对次烟煤进行了动力学研究,建立的单组分动力学模型将气体分为有机气体、副产气体及水,同时将油分为石脑油、燃料油及重油,增加了动力学模型的合理性。
有研究者发现煤的不同组分参与液化反应表现的活性不同,镜质组和壳质组为易反应组分,能在较低温度下进行加氢液化反应;惰质组是难反应组分,在较高的温度下才能发生液化反应,很难直接生成油或气体,而且其中的丝质体更加难以发生反应,为多组分动力学模型的建立奠定了基础。Szladow等[23]将煤假定为由不同性质的2种组分组成,并建立了相应的动力学模型,得到2种组分的反应活化能分别为131.2和167.2 kJ/mol。刘铭[24]利用高压釜对内蒙褐煤进行了动力学研究,根据集总理论,将煤划分为易反应组分、难反应组分以及不反应组分,并将液化产物分为油气、沥青质和残渣3个集总组分,建立了多组分一级不可逆反应动力学模型,发现煤向沥青质转化是主反应。
2.2 恒温和非恒温动力学模型
利用间歇式高压釜反应器进行液化动力学研究时,无法避免较长的升温和降温时间,而且加热过程有大量的液化反应发生,加热阶段的反应与恒温阶段的反应行为区别比较大。因此根据加氢液化过程中的温度变化情况,学者进行了恒温动力学和非恒温动力学的研究,建立了各种不同的动力学模型。
Mohan[25]以四氢萘为溶剂,研究了Illinois煤温度330~450 ℃、时间5~60 min的升温反应动力学,建立了考虑可逆反应的动力学模型;试验验证时发现,基于液相色谱的产物分离方法而建立的动力学模型对低温反应的拟合效果较好,基于溶剂萃取的产物分离方法而建立的动力学模型对高温反应拟合效果较好。李显[26]以神华煤液化重质油为供氢溶剂考察了神华煤在铁基催化剂条件下370~430 ℃的非恒温动力学,建立了三组分的一级反应动力学模型,发现升温阶段主要反应途径是煤转变为沥青质和煤转变为油、气。
恒温阶段是煤炭加氢液化反应的主要阶段,许多学者在不同的催化剂、不同的反应温度下对各种煤的恒温液化动力学进行了详细系统的研究。单贤根等[27-28]利用小型连续试验装置研究了恒温阶段的反应动力学,建立了11个集总动力学模型,动力学参数计算结果表明,恒温阶段主要是难反应组分进行液化反应,与沥青质生成速率以及重质油向轻质油转化速率相比,沥青质向油转化速率较小,是液化反应后期的控制步骤。Ding等[29]以黄铁矿为催化剂,考察了DECS-6煤在450 ℃条件下的恒温液化动力学,建立了包含6个速率常数的单组分网络反应动力学模型,没有考虑逆反应,动力学拟合曲线与试验数据吻合度比较高。梁江朋等[30]对新疆艾丁褐煤进行了恒温加氢液化动力学研究,通过Origin软件回归出各反应速率常数及活化能数据,发现反应组分生成各产物的反应速率顺序为:非酚油>沥青质>酚>气体。
2.3 多段反应动力学模型
随着液化动力学研究的不断深入,发现在煤液化反应的初期和后期表现出完全不同的反应模式,即存在前期煤的快速热解加氢和后期慢速加氢转化等多个反应阶段,很难用一个反应模型对整个加氢液化反应过程进行描述,因此采用多段反应的方式对煤液化动力学进行研究比较符合煤直接液化反应的真实特点。
Ikeda等[31]在由预热器和3个串联反应器组成的PSU中试装置上进行了动力学研究,认为预热器中反应模型为一级并联反应模型,第一反应器反应模型为一级不可逆串联反应模型,第三反应器反应模型为可逆的串联反应模型,三段反应模型如图1所示(Cf为快反应煤,Cs为慢反应煤,PA为前沥青烯,A为沥青烯,O和G分别为油和气体,k1、k2、k3、k1f、k2f、k3f、k1b、k2b、k3b分别为不同反应的动力学常数)。试验结果表明,预热器中主要反应为Cf煤迅速转化为沥青质、油和气,反应中期快反应煤通过沥青质转化为油和气,反应后期存在逆反应。
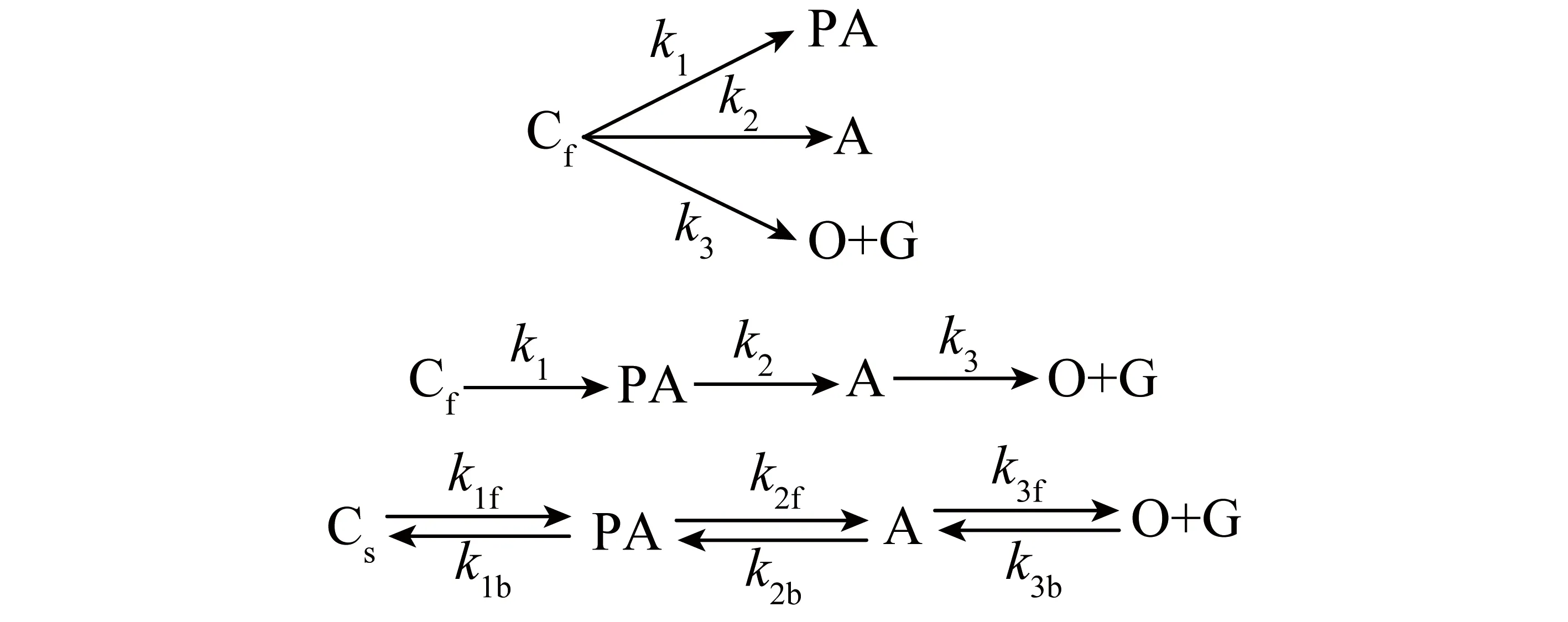
图1 Ikeda的三段液化反应动力学模型
Xu等[32]利用连续装置研究了Argonne煤的加氢液化动力学,发现加氢液化反应过程分为2个阶段,这2个阶段是平行、独立、一级不可逆反应,两段反应的活化能分别为35~80和124~238 kJ/mol。Itoh等[33]在150 t/d的PP试验装置上对Tanitoharum煤进行了反应动力学研究,分别为预热器和反应器建立了两段不同的动力学模型,预热器反应模型没有考虑沥青质向油的转化。李刚等[34]依据煤分子结构中官能团的表观活化能的突跃性变化,将煤加氢液化反应划分为初始高反应活性、慢速加氢和缩聚反应3个动力学阶段,并且根据初始阶段快速反应的特点,提出了高温快速液化的假设,进而提出了“理想液化”的理论设想。
煤加氢液化反应动力学研究成果可以计算煤浆预热炉出口的转化率,计算反应器温度分布和出口各产物产率,为液化工艺优化和工程设计提供理论指导。由于原料煤的结构复杂性、液化反应过程等诸多因素的不确定性,目前对于煤加氢液化的反应机理和动力学认识还没有达成共识,还有待学者们进行深入的反应机理和动力学研究。通过精馏将液化产物分为不同的窄馏分,进行液化反应动力学研究,是今后攻关的方向。
3 煤直接液化催化剂
在煤直接液化过程中,催化剂能有效促进液化反应中的自由基加氢、裂化以及S、N、O等杂原子的脱除反应,因此能提高煤液化效率,降低液化反应苛刻度,进而降低煤液化企业投资和运营成本,提高企业经济效益。经过催化剂筛选和活性比较发现Fe、Ni、Co和Mo等过渡金属对加氢液化反应具有活性。
煤直接液化催化剂种类很多,从其发展历史来看,加氢液化催化剂的研究和应用主要分为3类:第1类是以含铁的矿物、废弃物、合成物质为代表的廉价可弃型铁基催化剂;第2类是以加氢活性高的钼、钴、镍等有色金属元素催化剂,有色金属催化剂因资源有限、价格高,所以添加量要少;第3类是以SnCl2、ZnCl2为代表的强酸性金属卤化物催化剂,因强酸的严重腐蚀作用和回收困难,很难实现工业化。价格低廉、无毒性的铁系可弃型催化剂已经在神华百万吨级装置上实现了工业化应用,活性高的有色金属元素催化剂也具有工业化应用前景。
目前加氢液化催化剂的研究热点是优化催化剂制备工艺,提高催化剂活性。随着煤直接液化工艺的工业化,如何在提高催化剂活性的同时,选用价格低廉的原料和制备方法,降低催化剂生产成本,逐渐引起重视。提高催化剂活性的途径主要有:① 继续减小催化剂粒径,提高催化剂表面积,强化催化剂裂化功能;② 增强催化剂的酸性,提高催化剂的裂化性能;③ 提高催化剂的加氢功能,加入高活性物质。
3.1 超细高分散催化剂
提高催化剂分散度,制备超细高分散催化剂的方法主要有物理分散法(机械研磨、激光裂解等)、化学合成法以及非常规方法(火焰燃烧、气溶胶、等离子体溅射等)。
Sato等[35]通过研磨氧化铁催化剂,将其平均粒径从4.3 μm降至0.8 μm,进行长焰煤液化试验,发现萃取油产率由38%提高至46%,说明降低催化剂粒径能提高催化剂活性。由于物理研磨方法的局限性,催化剂粒径达到微米级已是极限,为了使催化剂的粒度更小,国内外学者使用新的制备方法研发出了纳米级的高分散催化剂。
Khadzhiev等[36]首次利用由表面活性剂、油和助剂制成的微乳液,利用反胶束方法制备出了粒径均匀可控的超细粒径液化催化剂,此后,微乳液法引起广泛重视。Li等[37-38]在乙醇和甲苯溶剂体系中,以FeCl3和油酸钠为原料,通过化学方法合成出了纳米氧化铁,并通过高温晶化方法,使纳米氧化铁的粒径达到了15 nm左右,以此作为催化剂进行液化试验,煤转化率和油收率分别达到97.2%和66.5%,表现出很好的加氢液化活性。李永伦等[39]以二乙胺和Fe/NaY为原料,采用化学气相沉积法制备得到氮掺杂碳纳米管铁基催化剂,粒径为50~100 nm,催化剂添加量仅为0.3%时,液化油产率就达到了55.55%。
近年来,其他非常规制备方法如火焰燃烧法、等离子体溅射法、气溶胶法等也逐渐在超细高分散催化剂制备中得到应用[40-41]。纳米材料的优异性能和纳米技术的兴起,促使广大学者开发出很多种制备纳米材料的方法,纳米材料也表现出了优异的催化性能。目前,这些纳米材料在煤加氢液化中的应用非常少,因此利用纳米合成技术成果来优化液化催化剂的制备方法,提高液化催化剂的加氢活性值得深入研究和探讨。
铁系催化剂性价比高,进入液化残渣对环境没有污染,是直接液化催化剂开发的重点方向,铁系催化剂粒径越细,液化反应器中生成的活性组分γ-Fe相越多,因此铁系催化剂正向着高分散的方向发展。降低超细催化剂制备成本是工业化应用的关键,物理分散和化学合成法是具有优势的超细高分散催化剂制备方法。
3.2 酸性催化剂

酸根离子一方面能改变液化催化剂的表面性质,有效改善催化剂分散度;另一方面能改变催化剂在反应中活性相的转变历程。由于煤加氢液化反应条件高温高压,缺乏先进的催化剂在线分析表征手段,目前对酸性离子作用本质的了解还比较浅薄,有待进一步加强离子改性液化催化剂的机理研究。
3.3 复合型催化剂
由于单一非贵金属元素催化剂活性低,通过添加高加氢活性金属元素或普通金属元素,利用多种金属/非金属催化剂的复合/协同效应来制备双金属或多金属催化剂,是提高煤加氢液化催化剂的活性的有效方法,也是近年来液化催化剂的研究和开发热点。
Sharma等[45]采用气溶胶技术制备出了一系列多金属催化剂,并评价了这些催化剂的液化效果,发现多金属复合催化剂比单独的Fe催化剂活性高,制备的纳米Fe-Al-S复合催化剂的煤转化率能提高8%,说明Fe和Al两种金属有协同作用。Kaneko等[46]以不同的褐铁矿作为液化催化剂时,发现印尼褐铁矿由于含有较高的Al、Ni和Cr等元素,在液化反应中表现出的催化活性高于其他种类的褐铁矿。
王勇等[47]在铁系矿物中加入少量的Ni、Mo元素,再经过细化干燥处理制备出了多金属复合型催化剂,研究发现复合型催化剂的转化率和油产率高于超细高分散铁系催化剂。谢晶等[48]采用共沉淀法添加金属元素对FeOOH进行改性,发现Si、Al、Ca、Ni、Co能改善催化剂分散度和比表面积,能提高液化油收率0.7%~2.7%,Mg没有促进作用。杨德山[49]研究发现复合型催化剂中,Al、Ca、Zr是通过改善催化剂的织构性质来提高催化剂的活性,Ni、Mo元素通过强化对氢气的活化,起到类似于电子型助剂的作用,添加的Si量小于5%时,由于能显著改善催化剂分散度和比表面积,明显提高了液化油收率。
从经济角度考虑,复合型催化剂需要高度分散,以减少添加量。为了达到高度分散的目的,一般选用油溶性的原料,如羰基化物、环烷酸盐、有机金属化合物等。制备复合型催化剂,添加价格高的贵金属元素时,要考虑催化剂的回收问题。催化剂的回收利用方式主要有液化中间产物的循环、化学法处理等,目前对复合型催化剂回收方法的研究不够深入,需要加强。
4 煤直接液化工艺
4.1 发展历程
煤炭直接液化工艺是根据煤液化反应机理,通过一系列设备的组合,达到液化反应的操作条件,使煤炭直接液化反应能连续稳定地进行。无论哪种煤直接液化工艺技术,基本都包括备煤、煤浆制备、催化剂制备、煤液化反应、固液分离及产物精制等部分[11]。
自20世纪初诞生煤直接液化技术以来,煤直接液化工艺经历了一百余年的发展和进步。到目前煤直接液化工艺发展经历了4个阶段的革命性进步,主要特征表现在催化剂、循环溶剂、溶剂加氢和固液分离技术方面[50-53]。
第1阶段是1913年到第二次世界大战结束,煤液化技术的发展主要集中在德国,代表性工艺是德国老IG液化工艺,催化剂采用赤泥催化剂,循环溶剂未预加氢,固液分离采用过滤方式,反应条件比较苛刻(压力70 MPa,温度470 ℃)。第2阶段是二次大战结束到1973年,由于20世纪50年代中东地区大量廉价石油的开发,煤直接液化技术陷于低谷,只有美国等少数国家进行基础研究,开发出了黄铁矿、赤铁矿等催化剂,其他方面的研究基本停滞。第3阶段是1973—2000年,由于20世纪70年代的2次石油危机,促使煤液化技术的研究开发形成了一个新的高潮,美国、德国、日本等发达国家从基础理论、反应机理到工艺开发、工程化放大等方面进行了深入研究,相继开发出了多种煤直接液化新工艺,代表性的工艺主要是德国的IGOR工艺、美国的HTI工艺和日本的NEDOL工艺;这一阶段的工艺特点是循环溶剂采用预加氢,固液分离采用减压蒸馏方式,催化剂采用研磨后的小粒径铁系催化剂或钼、镍等有色金属催化剂。第4阶段是2000年至今,进入21世纪,我国政府根据以煤为主的能源结构特点,大力支持国内企业和科研机构开展煤直接液化技术的研发工作,研发的代表性工艺技术有神华煤液化工艺和煤科院的CDCL液化工艺,工艺特点是催化剂采用超细高分散铁系催化剂,循环溶剂加氢采用高活性加氢催化剂。这一阶段,国外相关的开发研究工作基本上处于停滞状态。
煤直接液化工艺中,溶剂具有将煤粉成浆、溶解煤和氢气、供氢和传递氢、传热、直接参与煤液化反应等多种功能。早期的液化工艺用加压过滤和离心分离得到的部分液相产物作为溶剂,溶剂中含有未反应煤和难分解的沥青质,使得液化反应条件较为苛刻。后来对减压蒸馏的馏分油进行一定深度加氢处理后作为溶剂,具有供氢性好、油收率高等优点。随着溶剂制备技术的不断进步,煤直接液化工艺的反应条件越来越缓和,油收率越来越高。
煤直接液化装置的连续运转过程中,实际使用的溶剂是煤直接液化自身产生的中质油和重质油的混合油,通过催化加氢处理进行循环使用,称作循环溶剂,其主要组成是2~4环的芳烃和氢化芳烃。当煤液化反应条件过于苛刻或温和、溶剂加氢深度不合适或溶剂中直链烷烃积累过多时,符合成浆性和供氢性要求的循环溶剂数量就会减少,从而造成溶剂损耗。这时就需要采取相应调整措施,保持循环溶剂性质和数量的稳定,保障煤液化装置的连续稳定长周期运转。
传统的煤直接液化工艺通常在高温、高压下进行,导致设备投资和操作费用高,因此研发煤的温和液化工艺成为目前的开发热点[52-53]。目前煤直接液化产品以汽油和柴油为主,附加值不高,今后应开发高附加值的航煤、芳烃等产品,并对液化残渣进行深加工和资源化利用。未来的煤直接液化技术开发应立足于核心工艺优化和催化剂创新,重视液化主副产品的优化利用、反应器的大型化以及液化系统的高度集成,加强液化煤的分级转化以及开发直接液化-间接液化耦合工艺技术。
4.2 国内外典型液化工艺
4.2.1德国IGOR工艺
德国矿业研究院(DMT)、鲁尔煤炭公司和菲巴石油公司在20世纪90年代初改进了原德国老IG工艺,形成了新的IGOR(integrated gross oil refining)工艺。该工艺液化反应采用赤泥作催化剂,液化油加氢精制使用商业化的Ni-Mo-Al2O3催化剂。IGOR工艺流程如图2所示。
图2 德国IGOR工艺流程示意
IGOR工艺的操作条件在现代液化工艺中最为苛刻,适合于烟煤的液化,其工艺特点是:① 煤浆固体浓度大于50%,煤处理能力大,反应器空速可达0.5 h-1(其他煤液化工艺反应器空速为0.2~0.4 h-1);② 该工艺将循环溶剂加氢和液化油提质加工与煤直接液化串联在一套高压系统中,避免了其他工艺流程物料降温降压又升温升压带来的能量损失,节约投资和运营成本;③ 循环溶剂由老工艺中的重油改为中油与催化加氢重油混合油,不含固体,煤浆黏度大大降低,溶剂的供氢能力增强。
4.2.2日本NEDOL工艺
1980年,日本成立了新能源产业技术综合开发机构(NEDO),NEDO集中煤直接液化技术工艺的特点优化组合形成了日本烟煤液化工艺(称为NEDOL工艺),其液化对象主要是次烟煤和低品质烟煤,NEDOL工艺的工艺流程如图3所示。
日本NEDOL工艺的特点是:① 催化剂使用合成硫化铁或天然硫铁矿,价格低廉,降低了煤直接液化反应成本;② 配煤浆用的循环溶剂单独加氢,提高了溶剂的供氢能力,循环溶剂加氢技术来自于美国EDS工艺;③ 固液分离采用减压蒸馏的方式;④ 该工艺适用于从次烟煤至煤化程度低的烟煤等。
NEDOL在1983年建立了0.1 t/d BSU(bench scale unit)装置并进行试验运转。1988年在日本新日铁建成1 t/d工艺支持装置(process suport unit),1989年开始运转。1991年10月开始了150 t/d的NEDOL工艺工业性试验装置(pilot plant)的建设,1996年初完成建设并开始运转,至1999年150 t/d PP装置完成预定的试验计划,2000年装置全部拆除。
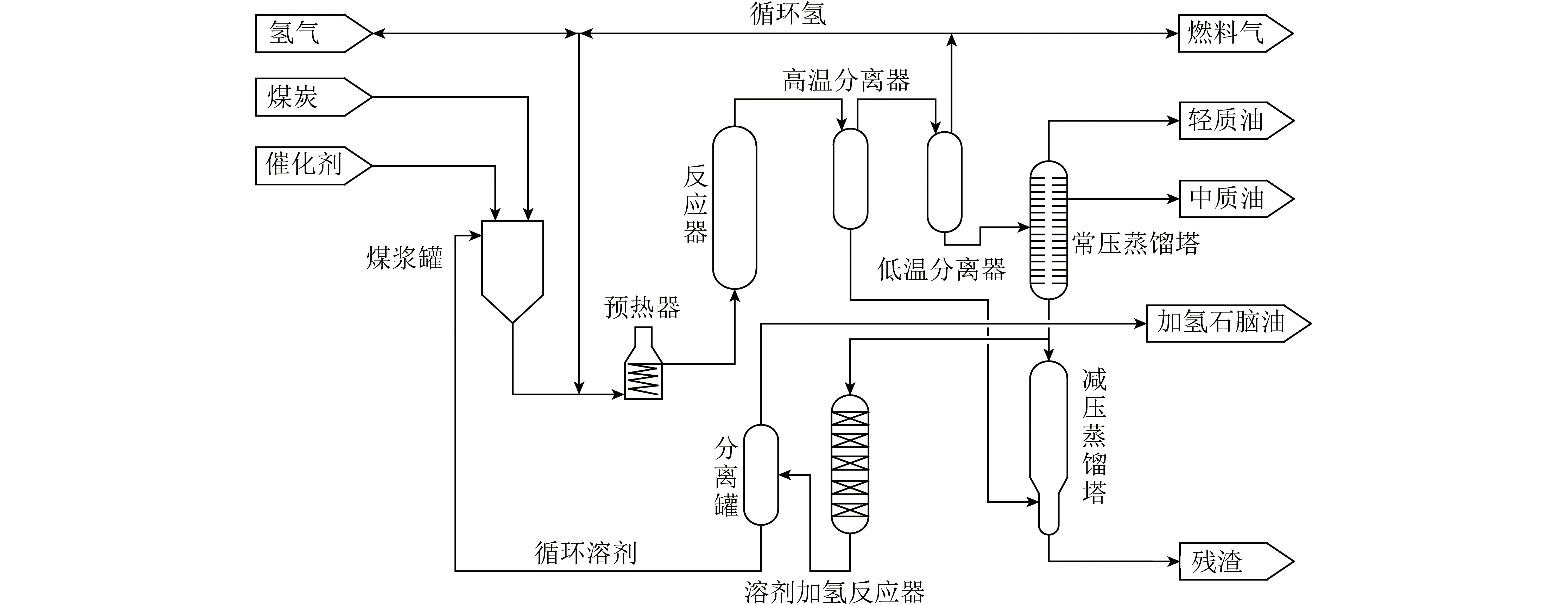
图3 日本NEDOL工艺流程示意
4.2.3中国神华煤直接液化工艺
2000年左右,我国神华集团在充分消化吸收国外现有煤直接液化工艺的基础上,利用先进工程技术,经过工艺开发创新,依靠自身技术力量,形成了具有自主知识产权的神华煤直接液化工艺。神华液化工艺流程如图4所示。
图4 中国神华煤直接液化工艺流程示意
神华煤直接液化工艺主要特点是:① 采用超细水合氧化铁(FeOOH)作为液化催化剂,该催化剂以部分液化原料煤为载体,粒径小、催化活性高;② 采用预加氢的供氢溶剂作为循环溶剂,供氢性能强;③ 液化反应器采用强制循环悬浮床反应器,反应器轴向温度分布均匀,反应温度容易控制,反应器气体滞留系数低,液相利用率高,而且物料在液化反应器中有较高的液速,能有效阻止固体物料的沉积。
神华煤直接液化工艺是世界上第一个完成了从实验室小试(BSU)、中试(PDU)直至百万吨级工业示范装置完整开发过程的煤液化技术。2008年,神华建成了单系列处理干煤量为6 000 t/d的百万吨级煤直接液化示范装置,并于同年12月,进行了第一次投煤试车试验,打通了全部生产流程,顺利实现油渣成型,产出合格的柴油和石脑油。这标志着我国成为世界上唯一实现百万吨级煤直接液化关键技术工业化的国家。
5 结语及展望
开展煤直接液化技术研究和发展煤直接液化产业适于我国化石能源的赋存状况及能源消费结构。一百多年来,国内外在煤直接加氢液化反应机理、反应动力学、催化剂及催化机理、工艺技术等方面取得了显著成果和重要进展,我国还首次实现了百万吨级的煤直接液化技术工业示范。但由于煤直接加氢液化反应条件苛刻、反应机理复杂、工艺单元繁多以及现有技术手段有限等,煤直接液化技术还存在煤液化化学反应工程认识不足、工艺复杂、催化剂活性低、投资高等诸多问题,需要不断加强基础理论、关键技术、工程放大等方面的研究,提高煤直接液化技术的核心竞争力。
1)煤的加氢液化反应是自由基反应机理,化学反应行为很复杂,包含煤的热解、自由基加氢、脱杂原子和缩合反应等,是一系列顺序反应和平行反应的综合结果,总体上以顺序反应为主。借助同位素示踪、原位实时检测、等离子体技术以及微波快速加热技术等现代分析方法和试验手段,重点研究自由基的产生速率、活性氢产生速率及定量传递机理,有助于深入认识和精准阐明煤加氢液化反应机理。
2)煤直接加氢液化反应动力学的研究经历了从单组分到双组分和多组分、从连续反应和平行反应到复杂的网络反应、从最初的一步反应到后来较为合理的多段反应的发展历程。根据反应阶段不同进行分段处理的多组分“集总”反应动力学模型将是今后煤加氢液化反应动力学发展的主要方向。从分子水平研究液化反应机理,借助先进分析手段及科学的处理方法,建立真正揭示不同条件下煤液化动力学规律的通用型动力学模型是未来的发展趋势。
3)催化剂在煤直接液化过中具有重要作用,煤液化催化剂能提高煤转化率、油收率以及液化产物的组成和质量,降低液化反应条件和装置操作难度,从而提高液化工艺先进性和经济效益。目前,煤直接液化催化剂的研究取得了一定进展,开发出多种高活性的催化剂,对催化剂作用机理和提高催化剂活性的方法都有了一定的认识,但液化催化剂的研究仍存在许多不足之处。发展高温高压条件的原位检测手段,揭示催化剂在加氢液化中的形态变迁规律及作用机理是未来的基础研究方向。借助纳米合成等高新技术,通过调控组分配伍、优化制备方法、控制结构特性等手段研发高活性、价格低廉、节能环保、易于回收利用的催化剂是开发新型煤直接液化催化剂的重要途径。
4)煤直接液化工艺经历了百余年的发展历程,中国、德国、美国、日本等许多国家都独自开发出了拥有自主知识产权的加氢液化工艺技术,在催化剂、溶剂加氢、固液分离、反应器、油品精制等方面都取得了显著的进展,操作条件进一步缓和,油收率大幅提高,热利用效率明显改善,产品成本明显降低。煤直接液化技术的研究方向和发展趋势是寻求更为廉价和活性更高的催化剂促进煤的温和液化和分级转化,通过系统合理配置和优化集成实现总体效率的最优化,延伸产品链和优化利用副产品进而提高产品附加值,促进煤直接液化和间接液化技术的融合发展。
