普萘洛尔联合32P敷贴治疗儿童脉管畸形疗效分析
2020-03-17任娟葛维媛成超
任娟 葛维媛 成超


[摘要]目的:研究普萘洛爾联合磷32(32P)敷贴治疗儿童脉管畸形的临床效果。方法:选取2016年1月-2018年1月笔者医院收治的86例脉管畸形患儿,按照治疗方法不同分为单纯组与联合组,每组43例。单纯组:使用普萘洛尔治疗;联合组:使用普萘洛尔联合32P敷贴治疗,连续治疗3个月,并对患者进行为期1年的随访。治疗期间密切观察患儿血压、心率、睡眠及病变部位的变化情况,并在治疗结束后对患儿家属进行护理指导。观察两组患儿的治疗效果、不良反应发生率及治疗满意度。结果:单纯性血管瘤的治疗效果高于静脉畸形与混合型血管瘤。静脉畸形与混合型血管瘤疗效比较差异无统计学意义(P>0.05);联合组的疗效优于单纯组(P<0.05),联合组的治疗总有效率亦显著高于单纯组(P<0.05);联合组患儿治疗后湿性皮炎、干性皮炎及色素脱失的发生率均高于单纯组,组间比较差异无统计学意义(P>0.05);联合组患儿色素沉着的发生率低于单纯组,组间比较差异也无统计学意义(P>0.05);联合组患儿的治疗满意度显著高于单纯组(P<0.05)。结论:普萘洛尔联合32P敷贴治疗儿童脉管畸形效果明显,可显著提高有效率,且患儿家属对治疗满意,为临床治疗与护理提供了依据。
[关键词]血管瘤;普萘洛尔;32P敷贴;静脉畸形;混合型血管瘤
[中图分类号]R732.2 [文献标志码]A [文章编号]1008-6455(2020)01-0029-03
Efficacy of Propranolol Combined with 32P Application in the Treatment of Vascular Diseases in Children
REN Juan1,GE Wei-yuan2,CHENG Chao1
(1.Department of Nuclear Medicine; 2.Blood Collection Department of Laboratory, Qingdao Municipal Hospital,Shandong Province,Qingdao 266000,Shandong,China)
Abstract: Objective To study the clinical effect of propranolol combined with Phosphorus 32 (32P) application in the treatment of children's hemangioma. Methods 86 cases of cutaneous hemangioma in our hospital from January 2016 to January 2018 were selected. According to the treatment method, they were divided into simple group and combined group, 43 cases each. The simple group was treated with propranolol, and the combined group was treated with propranolol combined with 32P dressing for 3 months, the patients were followed up for one year. During the treatment, the changes of blood pressure, heart rate, sleep and the lesion site of hemangioma were closely observed, and the family members of the children were given nursing guidance after the treatment. The therapeutic effect, incidence of adverse reactions and treatment satisfaction of children with hemangioma were observed and compared between the two groups. Results The treatment effect of simple hemangioma is higher than that of Venous malformations and mixed hemangioma. There was no significant difference in the therapeutic effect between Venous malformations and mixed hemangioma (P>0.05). The therapeutic effect of combined group was better than that of simple group (P<0.05). The total effective rate of combined group was also significantly higher than that of simple group (P<0.05). After treatment, children in combined group had wet dermatitis, dry dermatitis and depigmentation. The incidence of pigmentation in the combined group was lower than that in the simple group, and there was no significant difference between the two groups (P>0.05). The treatment satisfaction in the combined group was significantly higher than that in the simple group (P<0.05). Conclusion Propranolol combined with 32P dressing in the treatment of children's hemangioma has obvious effect, the effective rate is significantly improved, and the treatment satisfaction of children's family members is better, it provides a basis for clinical treatment and nursing.
Key words: hemangioma; propranolol; 32P application; venous malformations; mixed hemangioma
儿童血管瘤(infantile hemangioma,IH)是儿童体表软组织常见的良性肿瘤,来源于血管内皮细胞[1],儿童发病率5%~10%,出生时体重极低的早产儿的发病率可达20%~30%[2-4]。随着患儿年龄增长,多数患儿瘤体的面积及增长趋势可能会发生自发性退化。但部分血管瘤影响美观,且可导致皮肤破损、局部组织溃疡、呼吸道梗阻及视力障碍,甚至危及生命[5-6]。磷32(32P)敷贴是一种低辐射强度的局部短距离治疗方法,因其放射强度小,局部反应和毒副作用轻微,目前多用于治疗儿童型血管瘤[7]。普萘洛尔是目前治疗儿童血管瘤的一线药物[8],但其具有易复发性,且用药时间较长,为增加患儿的治疗效果,减少治疗时间,本研究尝试使用普萘洛尔联合32P敷贴治疗儿童血管瘤,现将结果报道如下。
1 资料和方法
1.1 一般资料:选取2016年1月-2018年1月在笔者医院皮肤科就诊的86例脉管畸形患儿,按照治疗方法不同分为单纯组与联合组,每组43例。单纯组:男23例,女20例,年龄4~26个月,平均(8.03±1.34)个月;体重5.29~12.51kg,头颈部20例,胸背部14例,下腹及下肢部9例。单纯性血管瘤31例,静脉畸形7例,混合型血管瘤5例;联合组:男22例,女21例,年龄6~25个月,平均(7.79±1.62)个月;体重5.12~12.07kg;头颈部19例,胸背部13例,下腹及下肢部11例。单纯性血管瘤32例,静脉畸形7例,混合型血管瘤4例。两组患儿在性别、年龄、体重、血管瘤部位及类型等方面比较差异无统计学意义。本次研究经笔者医院伦理委员会批准。
1.2 纳入和排除标准:纳入标准:①经皮肤科医师及超声检查确诊为脉管畸形;②年龄1个月~3岁;③未接受过其他治疗;④患儿家属均知情同意,并签署知情同意书。排除标准:①合并严重心、肺、肝等疾病;②伴有其他类型皮肤病;③易过敏体质;④深部血管瘤;⑤伴有支气管哮喘、过敏性支气管炎及肺气肿等患者;⑥甲状腺功能低下者。
1.3 方法:单纯组:治疗前检查患儿身体,并记录各项生命体征如呼吸、心率、血压等。向患儿家属解释治疗的方法及注意事项,说明可能出现的副作用及表现,征得患儿家属同意后,方可给患儿用药。按照患儿体质量使用普萘洛尔片,剂量为0.5~1.5mg/kg·d,分3次口服。联合组:在单纯组基础上使用32P敷贴敷于患处。具体方法为:将32P溶液配制为20cm×20cm的公用敷贴器,再按照患者血管瘤的形状及面积大小进行裁剪,制成个人专用的敷贴器。治疗的剂量为1.2Gy/(cm·d),敷贴的使用时间根据32P的衰变系数以及患者的年龄进行调整[9],1次/2d。所有患儿治疗后均要求住院1周,确认无不良反应后方可出院,嘱患儿每周复诊1次,记录瘤体的大小、颜色及质地变化。两组患者均连续治疗3个月,并在治疗结束后叮嘱患者每月至医院门诊复诊或由护士对患者进行电话回访,为期1年。
1.4 观察指标与疗效评价:①对两组患者血管瘤的治疗效果、不良反应及治疗满意度进行对比分析;②疗效判断标准[10]:治愈:血管瘤完全消失,患处肤色恢复正常或存在色素沉着;好转:血管瘤瘤体面积缩小1/3以上,患处皮肤颜色苍白暗淡;无效:治疗前后血管瘤瘤体面积没有明显变化,瘤体面积缩小<1/3;加重:患儿血管瘤变大,瘤体面积较治疗前扩大1/3以上。有效率=(治愈+好转)例数/总例数×100%;③治疗满意度评价标准:治疗效果达到治愈和好转为满意,无效和加重为不满意。
1.5 统计学分析:使用SPSS 19.0统计软件对数据进行统计分析,计数资料采用率(%)表示,用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组疗效比较:两组单纯性血管瘤的治疗效果均高于静脉畸形与混合型血管瘤,差异有统计学意义(P<0.05),两组静脉畸形与混合型血管瘤疗效比较,差异无统计学意义(P>0.05);联合组单纯性血管瘤、静脉畸形及混合型血管瘤的疗效均优于单纯组(P<0.05),联合组的治疗总有效率亦显著高于单纯组,差异有统计学意义(P<0.05),见表1。
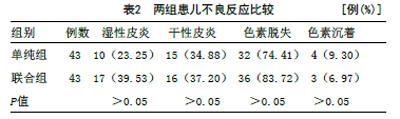
2.2 两组患儿不良反应比较:联合组患儿治疗后湿性皮炎、干性皮炎及色素脱失的发生率均高于单纯组,组间比较差异无统计学意义;联合组患儿色素沉着的发生率低于单纯组,组间比较差异无统计学意义,见表2。
3 讨论
脉管畸形起源于中胚叶的血管内皮细胞,发病机制目前仍不明确,以儿童多见[11]。可发生于身体任何部位,主要好发于头面部,前6个月增长异常迅速,且可能出现出血、破溃、感染、畸形或经久不愈等,故早期积极治疗对儿童血管瘤非常有利。目前常用的治疗与干预方法有:冷冻、手术、激光、放射及放射性核素治疗等[12],其中同位素敷贴因辐射强度低且具有安全、简便、无痛及高治愈率、低复发率的特点,受到众多患者与家属的青睐[8]。但同位素敷贴具有放射性,且用后患处易出现色素沉着及色素脱落,故不宜用于颜面部,且不宜长时间使用。而普萘洛尔是目前治疗儿童血管瘤的一线药物,众多文献报道证实,普萘洛尔治疗儿童血管瘤安全有效,且美国食品药品监督管理局与欧洲药品管理局均已批准普萘洛尔用于儿童血管瘤的治疗[13-14]。但普萘洛尔停药后常会出现复发的问题,其复发率最低为6%,最高可达25%[15],且疗程较长。故本研究将普萘洛尔与32P敷贴联合使用,观察其疗效。
结果显示两组单纯性血管瘤的治疗效果均高于静脉畸形与混合型血管瘤,差异有统计学意义,两组静脉畸形与混合型血管瘤间治疗效果比较差异无统计学意义。说明单纯性血管瘤对普萘洛尔与32P敷贴的敏感度更高,用于治疗单纯性血管瘤的效果更好,而静脉畸形与混合型血管瘤有待于进一步研究更好的治疗方法,目前有学者认为,超声32P胶体导入能更好地提高静脉畸形的治疗有效率[16]。普萘洛尔治疗血管瘤一般用药时间较长,且易导致心率减慢等不良反应[17],造成治疗依从性降低。本次研究结果显示,联合组单纯性血管瘤、静脉畸形及混合型血管瘤的治疗效果均优于单纯组,治疗总有效率亦显著高于单纯组,差异有统计学意义,说明联合用药的治疗效果更佳。虽然联合组患儿治疗后湿性皮炎、干性皮炎及色素脱失等不良反应的发生率均高于单纯组,但组间比较差异无统计学意义。本研究结果还显示,联合組患儿的治疗满意度显著高于单纯组,且差异有统计学意义。造成这一结果的原因可能是由于两种方法联合使用,缩短了治疗时间,增加了患儿对治疗的依从性,且联合组色素沉着的发生率显著降低,故而增加了患者对治疗的满意度。
治疗前后的护理及健康教育亦非常重要,由于联合治疗,故治疗过程中的不良反应较多,尤其需要加强护理及对患儿家长的健康教育。护士应随时与患儿家属沟通,向患儿家属详细介绍治疗方法、作用及不良反应,并对患儿家属治疗后护理措施进行指导。普萘洛尔的不良反应较多,主要有乏力、嗜睡、心动过缓、腹泻、低血压等,而32P敷贴对皮肤组织具有一定的刺激性,患儿在治疗过程中病变部位亦红肿,甚至破溃,故在使用过程中应密切监测患儿心率、血压及皮肤组织的变化,保持患儿治疗部位皮肤组织清爽、干燥。段永强等研究发现,3岁以内及3岁以上血管瘤患儿使用普萘洛尔联合32P敷贴的治疗效果相当。本研究所有对象均为1~3岁以下患儿,未对1岁以内及1~3岁患儿的治疗结果进行对比,故研究结果可能存在一定偏差,有待后续加大样本量,进一步研究。
综上所述,普萘洛尔联合32P敷贴治疗儿童脉管畸形效果显著,且患儿家属满意度较高,为临床治疗与护理提供了新的方法,但需密切注意不良反应的发生并及时给予处理。
[参考文献]
[1]吕文强,王亮,徐兵,等.普萘洛尔和聚桂醇分别治疗小儿血管瘤的临床效果比较[J].安徽医药,2017,21(12):2270-2273.
[2]Shah S,Frieden IJ.Treatment of infantile hemangiomas with beta-blockers:a review[J].Skin Therapy Lett,2013,18(6):5-7.
[3]Chandran S,Ari D,Jose J.Use of propanolol for treatment of large infantile haemangiomas-a report of two cases and review of the literature[J].Ann Acad Med Singapore,2013,42(5):253-256.
[4]Léauté-Labrèze C,Harper JI,Hoeger PH.Infantile haemangioma[J].Lancet,2017,390(10089):85-94.
[5]陈远征,白南,李雪晴,等.口服不同剂量普萘洛尔治疗儿童血管瘤的前瞻性随机对照研究[J].中华整形外科杂志,2018,34(5):337-342.
[6]张莉,陈涌,依光叫.口服普萘洛尔治疗40例面颈部儿童血管瘤的临床观察[J].中国美容医学,2014,23(14):1177-1180.
[7]张兰平,李宗良.32P敷贴治疗儿童血管瘤1619例疗效分析[J].海南医学,2013,24(11):1607-1608.
[8]Drolet BA,Frommelt PC,Chamlin SL,et al.Initiation and use of propranolol for infantile hemangioma:report of a consensus conference[J].Pediatrics,2013,131(1):128-140.
[9]潘中允.实用核医学[M].北京:人民卫生出版社,2014:1128-1129.
[10]李倩,李俊,杨涛.外用普萘洛尔和噻吗洛尔治疗儿童颜面部血管瘤疗效比较观察[J].中国美容医学,2014,23(3):221-223.
[11]彭慧子,周林,杨壮群.口服普萘洛尔治疗儿童体表血管瘤的临床研究[J].中国美容医学,2018,27(4):64-67.
[12]Hermans DJ,Bauland CG,Zweegers J,et al.Propranolol in a case series of 174 patients with complicated infantile haemangioma:indications,safety and future directions[J].Br J Dermatol,2013,168(4):837-843.
[13]Hoeger PH,Harper JI,Baselga E,et al.Treatment of infantile haemangiomas:recommendations of a european expert group[J].Eur J Pediatr,2015,174(7):855-865.
[14]Qi M,Chen X,Xie HF,et al.Effectiveness of external propranolol gel for treatment of superficial infantile hemangioma[J].Zhongguo Dang Dai Er Ke Za Zhi,2014,16(8):860-862.
[15]Sagi L,Zvulunov A,Lapidoth M,et al.Efficacy and safety of propranolol for the treatment of infantile hemangioma:a presentation of ninety-nine cases[J].Dermatology,2014,228(2):136-144.
[16]肖欢,陈鸿颜,严娟娟,等.32P胶体在超声引导下治疗儿童静脉畸形的临床价值[J].海南医学,2016,27(5):798-800.
[17]段永强,吴振夫,邱煊,等.32P敷贴联合普萘洛尔治疗儿童大面积皮肤毛细血管瘤[J].标记免疫分析与临床,2016,23(6):685-687,712.
[收稿日期]2018-12-25
本文引用格式:任娟,葛維媛,成超.普萘洛尔联合32P敷贴治疗儿童脉管畸形疗效分析[J].中国美容医学,2020,29(1):29-32.
