血液透析自体动静脉内瘘失功患者血浆Lp-PLA2水平变化及意义
2020-03-14程艺王卉刘辉张艺陈文莉
程艺 王卉 刘辉 张艺 陈文莉
430056 武汉,江汉大学(程艺);430014 武汉,华中科技大学同济医学院附属武汉市中心医院检验科(王卉),肾内科(刘辉,陈文莉),超声科(张艺)
慢性肾脏疾病(CKD)作为全球主要的公共卫生问题受到越来越多的关注[1]。当病情进展为终末期肾病时,则需要肾脏替代治疗。根据NKF-K/DOQI指南,自体动静脉内瘘(arteriovenous fistula,AVF)是终末期肾脏患者进行血液透析的首选。然而,AVF的持久性还远远不够理想,而且通畅率也很低[2]。AVF失功最常见的原因是狭窄和血栓形成[3-4]。一般来说,血管狭窄是新内膜增生的结果,虽然目前还不清楚新内膜增生的确切机制,但在多个实验和临床研究中已证明炎症在AVF狭窄的发展中起着重要的作用[5-7]。
脂蛋白相关磷脂酶A2(lipoprotein-associated phospholipase A2,Lp-PLA2)是一种促炎酶,多位学者已证实与动脉粥样硬化独立相关[7-8],Lp-PLA2在血管壁中积累,促进斑块形成,斑块又在细胞因子和蛋白酶的作用下溃疡或破裂,导致血栓形成和心血管事件的发生[9]。本研究旨在探讨血液透析患者Lp-PLA2与AVF狭窄的关系。
资料与方法
一、研究对象
选择2018年11月至2019年4月武汉市中心医院收治的尿毒症患者40例,男23例,女17例,年龄28~84岁,平均年龄(54.9±13.6)岁。
纳入标准:(1)AVF是患者的唯一血管通路,并规律使用此通路透析;(2)年龄大于18岁;(3)内瘘处震颤变小或消失;(4)透析时血流量小于200 mL/min,无法完成透析;(5)经彩超证实内瘘吻合口处、静脉端或动脉端有狭窄,伴或不伴血栓形成;(6)患者同意采用超声引导下经皮血管腔内成形术(percutaneous transluminal angio-plasty,PTA)治疗;(7)患者临床资料完整。
排除标准:(1)AVF不是患者的唯一血管通路;(2)年龄小于或等于18岁;(3)既往患有冠心病、脑梗死、恶性肿瘤、风湿结缔组织病病史者;(4)合并局部或全身严重感染,凝血功能障碍者;(5)妊娠或哺乳期妇女;(6)患者依从性差,临床资料不完整者。
本研究经武汉市中心医院医学伦理委员会批准,患者均签署知情同意书。
二、研究方法
1.AVF失功的定义 透析时血流量降低(≤200 mL/min),或血流量减少导致透析不充分。
2.分组 将内瘘失功并在超声下检查发现有血栓形成或血管狭窄的患者定为失功组,共19例,其中血管狭窄且血栓形成6例、血管狭窄13例;超声下见内瘘通畅的患者定为通畅组,共21例。
3.内瘘失功处理 内瘘失功者均予PTA治疗。具体方法:患者平卧,内瘘肢外展,常规消毒铺巾,2%利多卡因局麻穿刺点及狭窄部位,超声辅助下穿刺针穿刺前臂内瘘血管,置入6Fr血管鞘,超声引导下将0.035 inch超滑导丝经过狭窄处进入静脉,选取直径均为6 mm,长度均为40 mm的球囊进行扩张,扩张压力不超过最大爆破压24 atm(术中压力再根据患者动静脉内瘘狭窄程度调整)直至球囊完全打开无切迹,连续扩张2次,每次持续30~90 s。若有血栓,则向血管鞘缓慢注入尿激酶30万单位,分3次注入,保留15 min,并用球囊反复打碎血栓,狭窄解除后予超声检查全程示血流恢复良好,残余狭窄<30%。退出导丝、球囊,拔出鞘管,局部缝扎加压止血。经治疗,16例AVF通畅,3例仍未通畅。
4.相关指标观察 失功组患者术前及术后1个月、通畅组患者均于透析前隔夜禁食后清晨采空腹静脉血,用乙二胺四乙酸抗凝,1 000 r离心15 min,分离血清立即冷冻,保存在-80 ℃处,待检测。采用特异性酶联免疫吸附试验测定Lp-PLA2的质量浓度。血常规、血生化等指标采用全自动分析仪测定。本研究还收集患者一般资料,包括年龄、性别、透析龄、是否存在高血压、糖尿病。
5.透析治疗方案 所有患者均使用AVF行血液透析治疗,累积透析时间为1~84个月,其中失功组11例患者,透析频率为3次/周、4 h/次,8例患者透析频率为2次/周、4 h/次;通畅组12例患者透析频率为3次/周、4 h/次,9例患者透析频率为2次/周、4 h/次。所有患者均行1次/周血液透析滤过(hemodiafiltration,HDF)模式透析,剩余均为血液透析(hemodialysis,HD)模式;均给予促红细胞生成素。
三、统计学处理
结 果
一、两组患者一般资料
两组患者年龄、性别、高血压病史、糖尿病病史差异无统计学意义(P>0.05),具有可比性。(表1)
二、两组患者临床指标比较
失功组与通畅组纤维蛋白原(fibrinogen,FIB)、血红蛋白(Hb)、白细胞计数(white blood cell count,WBC)、中性粒细胞/淋巴细胞比值(neutrophil-lymphocyte ratio,N/L)、血肌酐、血尿酸(uric acid,UA)、K、Ca、P、白蛋白、甲状旁腺素(parathyroid hormone,PTH)水平的差异无统计学意义(P>0.05)。失功组Lp-PLA2、N/L水平均高于通畅组,差异具有统计学意义(P<0.05)。(表2)
三、失功组治疗成功者治疗前后炎症因子水平比较
失功组内瘘PTA治疗成功者治疗后血浆Lp-PLA2、FIB水平均较治疗前明显降低(P<0.05),治疗前后血浆N/L比较差异无统计学意义(P>0.05)。(表3)
四、Lp-PLA2与FIB、WBC、N/L的相关性分析
Spearman相关分析结果显示,Lp-PLA2与N/L正相关(P<0.05),Lp-PLA2与FIB、WBC均无相关(P>0.05)。(表4)

表1 2组患者一般资料比较
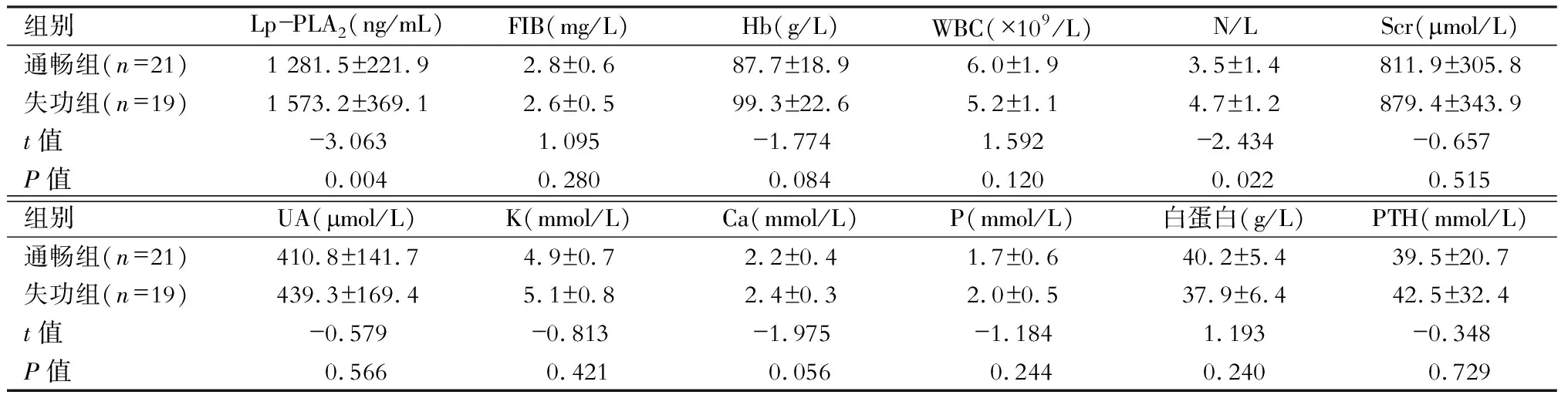
表2 2组患者临床指标比较
注:Lp-PLA2为脂蛋白相关磷脂酶A2,FIB为纤维蛋白原,Hb为血红蛋白,WBC为白细胞计数,N/L为中性粒细胞/淋巴细胞比值,Scr为肌酐,UA为尿酸,K为血钾,Ca为血钙,P为血磷,PTH为甲状旁腺激素
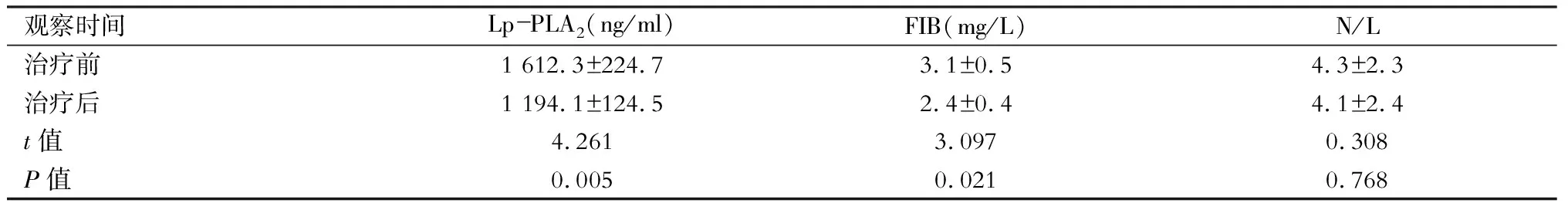
表3 失功组治疗成功者治疗前后血浆Lp-PLA2、FIB及N/L水平比较(n=17)
注:Lp-PLA2为脂蛋白相关磷脂酶A2,FIB为纤维蛋白原,N/L为中性粒细胞/淋巴细胞比值
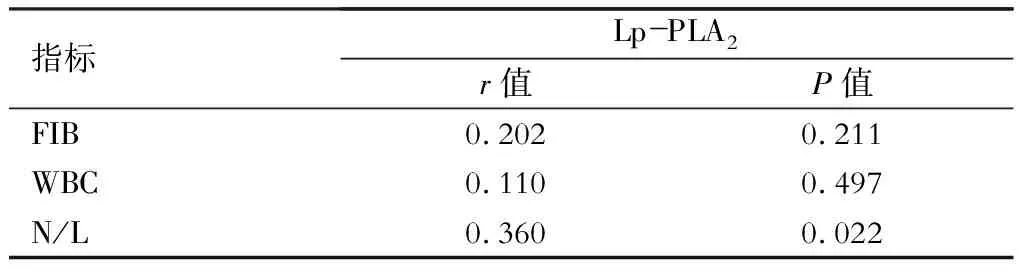
表4 Lp-PLA2水平与FIB、WBC、N/L指标的相关分析
注:Lp-PLA2为脂蛋白相关磷脂酶A2,FIB为纤维蛋白原,WBC为白细胞计数,N/L为中性粒细胞/淋巴细胞比值
讨 论
虽然AVF仍然是首选的血管通路,但原发性AVF失功的频率为40%[10],AVF术后1年的基本通畅率不超过60%[11]。AVF失功可能受到很多因素影响:如低血压、糖尿病、低蛋白血症、抗心磷脂抗体、移植物使用、炎症、尿毒症、缺氧、剪切力等[5,12]。早期AVF失功常发生在术后24 h内或术后1~8周,其主要原因为患者自身血管条件较差或为手术者技术不足,而临床上更常见的晚期AVF失功的原因主要是血栓形成[13]。
尿毒症患者体内代谢紊乱,炎性蛋白及炎性细胞因子产生增加,而血液透析通路的慢性隐匿性感染、透析膜的生物相容性、透析液质量、透析通量的大小、透析器使用技术和次数等加重了炎性反应的发展[14],李立等[15]研究也表明AVF的失功与微炎症状态有关。FIB、WBC、N/L是反映炎症状态的传统经典指标,而Lp-PLA2是新近发现的一种血管壁炎症的标志物[8]。Lp-PLA2可以水解氧化磷酸卵磷脂(主要来源于氧化低密度脂蛋白或者泡沫细胞的凋亡和坏死),生成促炎因子溶血磷脂胆碱和游离氧化脂肪酸,上述促炎因子可促进氧化应激,损害内皮功能和活力,影响血管平滑肌细胞的增殖和存活,并有助于巨噬细胞在组织积累,导致新内膜形成和狭窄[16]。由于AVF中静脉长期受到高流量动脉血冲击,致使静脉动脉化,因此我们推测Lp-PLA2也可预测AVF失功。
已有多项研究表明Lp-PLA2在糖尿病血管病、冠状动脉粥样硬化、颈动脉狭窄、冠状动脉PCI术后血管再通等多种血管病变中起着重要作用。多项研究表明Lp-PLA2参与组织炎症的正反馈回路,其可能原因为促炎因子溶血磷脂酰胆碱等趋化性使单核/巨噬细胞在组织聚集,单核/巨噬细胞既可吞噬氧化低密度脂蛋白形成泡沫细胞从而参与斑块形成,又可再分泌Lp-PLA2,从而形成恶性循环[17-18]。本研究发现血液透析患者AVF狭窄及血栓病变中的Lp-PLA2也明显升高。另外,失功组N/L的水平明显高于通畅组,与Yilmaz等[19]研究的AVF狭窄与N/L增高有关的结论相符。另外,我们发现AVF失功的Lp-PLA2与N/L呈正相关(P<0.05),可能这两个炎症因子在致AVF失功的机制方面有相同部分,需要我们进一步探究。而我们研究发现失功组内瘘治疗成功者治疗后血浆FIB水平较治疗前明显降低,与沈燕等[20]研究的AVF失功组经内瘘介入治疗前后血浆FIB水平比较无差异(P>0.05)的结果不同,可能是由于我们所纳入的患者较少,也可能与研究治疗AVF失功的手术方式有关。
故动态观察Lp-PLA2水平变化可能有助于监测血管通路状态,AVF术前血浆Lp-PLA2水平显著升高、AVF彩超检查发现血管条件不佳者,可考虑其他血管通路,如长期导管置入或者人造血管内瘘。我们研究发现内瘘再通后血浆Lp-PLA2水平明显下降,与朱慎慎等[21]研究的经皮冠状动脉介入治疗术后支架内无再狭窄组6~18个月复查的Lp-PLA2水平较术前明显下降的结论相符。可能因为PTA术后血管内膜损伤,血管外膜成纤维细胞可能参与重塑过程,损伤修复成纤维细胞增殖活化,转化为肌成纤维细胞,合成大量的胶原,而胶原含量通常被认为是斑块稳定性的标志[16,22]。有研究对猪的冠状动脉球囊损伤研究中提出外膜成纤维细胞在血管损伤后表型改变,获得肌细胞分化,增殖并迁移至新生内膜,同时胶原合成增加,导致血管重塑[22]。然而,我们的研究与Finn等[23]研究PCI术中撕裂及挤压斑块、球囊扩张、支架释放等导致局部血管壁损伤、血管炎症反应更重,诱发或加快了支架表面的内膜增生的结论相悖,可能原因是由于我们的实验方法并不完全相同,也可能是我们的研究样本量较少,需要更大样本量的研究去证实。
本研究证实Lp-PLA2与终末期肾病血液透析患者AVF失功有关,这种关系是独立于传统的引起AVF失功的危险因素,Lp-PLA2可能是氧化应激与炎症之间的积极联系,成为低密度脂蛋白修饰和氧化应激的介质,促进内膜生长,从而导致狭窄和血栓,但这一观点值得进一步研究。
综上所述,尿毒症AVF失功者血浆Lp-PLA2水平升高,该指标可能参与内瘘失功的形成,介导炎症反应、促进血管斑块形成,进而斑块破裂形成血栓。针对AVF术的患者,于内瘘术前、术后定期监测血浆Lp-PLA2水平,可以帮助临床医师及早发现和诊断AVF失功,进一步提高采取预防措施。但由于本研究为单中心小样本,有一定的局限性,研究结果还有待多中心大样本量的前瞻性研究进一步验证。
