替诺福韦酯与替比夫定在乙型肝炎病毒母婴阻断中的疗效对比
2020-03-13徐贤丽劳晓洁张春兰王佳洁罗淑铭陈茂伟
徐贤丽 劳晓洁 张春兰 王佳洁 罗淑铭 陈茂伟
1广西医科大学附属武鸣医院感染性疾病科(南宁530199);2广西医科大学第一附属医院感染性疾病科(南宁530021)
乙肝是全球重要公共卫生问题之一,全球的HBV感染1/3源自母婴传播,我国属于HBV中流行区,母婴传播导致30% ~ 50%HBV流行[1-2],为达到2030年“消灭肝炎”目标,阻断HBV母婴传播显得尤为重要[3-4],其中妊娠期抗病毒治疗、降低母体血清病毒载量则是母婴阻断一项重要措施。替比夫定(telbivudine,LdT)在中国上市已久,属于美国FDA药物妊娠安全性分类的B类药物,相关学者就LdT阻断母婴传播疗效的研究结果表明LdT可有效降低HBV母婴传播发生率、安全性良好[5]。替诺福韦酯(tenofovir disoproxil fumarate,TDF)是一种新型核苷酸逆转录酶抑制剂,具备抗病毒效力强、耐药屏障高、安全性强、FDA妊娠药物危险分级B级、药物费用低等各项特点,是目前国内外慢乙肝防治指南共同推荐的一线抗病毒药物[2,6-7]。研究证实 Aspen Port Elizabeth(Pty)Ltd 生产的TDF抗HBV疗效良好[8-9],但因其价格昂贵在国内应用受限,2017年国产TDF上市扩大了其应用,LIANG等[10]研究指出国产TDF 48周的疗效和安全性与原研药相当。目前少有针对国产TDF用于母婴阻断的疗效研究。本研究通过对2017年11月至2019年6月在广西医科大学第一附属医院就诊的HBV感染孕妇的临床资料进行分析,旨在对比国产TDF与LdT在妊娠期妇女中的HBV母婴阻断疗效。
1 资料与方法
1.1 一般资料 选取2017年11月至2019年6月在广西医科大学第一附属医院就诊的127例孕妇,分为预防性抗病毒组与治疗性抗病毒组,组内分为TDF观察组和LdT对照组。纳入标准:(1)诊断符合《慢性乙型肝炎防治指南》(2015年更新版)[11]临床诊断标准;(2)预防性抗病毒组:妊娠中晚期血清HBV DNA水平>106IU/mL,丙氨酸氨基转移酶(alanine amino transferase,ALT)正常者;治疗性抗病毒组:妊娠期间乙型肝炎病毒脱氧核糖核酸(hepatitis B virus Deoxidation Nucleic Acid,HBV DNA)可测并且ALT持续或反复异常者(其中HBeAg阳性者,HBV DNA>105IU/mL;HBeAg阴性者:HBV DNA>104IU/mL);(3)对该研究过程、方法了解并签署知情同意书。排除标准:(1)合并其他病毒感染,如甲型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、人类免疫缺陷病毒、巨细胞病毒、梅毒螺旋体、疱疹病毒等;(2)既往曾应用干扰素或其他核苷类似物治疗;(3)中断抗病毒治疗者;(4)肝硬化、肝癌、肝衰竭患者。本研究符合人体试验伦理学标准,已获医院伦理委员会批准(编号:伦审2019(KY-E-113)号)。
1.2 方法 以孕妇及家属自愿为原则,根据用药方案分为观察组与对照组。观察组给予口服富马酸替诺福韦二吡呋酯片(正大天晴药业集团股份有限公司,国药准字H20173303)300 mg每日1次,对照组给予口服LdT片(北京诺华制药有限公司,国药准字H20070028)0.6 g,每日1次。预防性抗病毒孕妇在第22~28孕周开始服药,治疗性抗病毒孕妇在第8~35孕周开始服药。观察组及对照组均分别在抗病毒治疗4周时、分娩前检测孕妇的HBV DNA(采用荧光定量聚合酶链式反应法检测)、HBeAg与HBeAb(采用酶联免疫吸附试验检测)、ALT(采用日立7600型全自动生化分析仪检测)等指标。
1.3 观察指标 以HBV DNA<5.0×102IU/mL作为HBV DNA转阴;以HBeAg<0.50 IU/mL作为HBeAg转阴;以HBeAg转阴并且HBeAg转阳(HBeAb>0.20 PEIu/mL)作为HBeAg血清学转换;ALT正常值范围为7~45 U/L,当测量值小于45 U/L即为复常。以肌酐> 84 μmol/L、血清磷<0.900 mmol/L、血清钙<2.080 mmol/L、肌酸激酶>140 U/L作为出现药物不良反应。
1.4 统计学方法 采用SPSS 23.0统计学软件进行分析。正态分布的计量资料采用均数±标准差表示,采用独立t检验进行组间比较。计数资料采用率(%)表示,采用Pearson χ2、Fisher确切概率法进行检验。以P<0.05作为差异有统计学意义。
2 结果
2.1 一般资料及基线治疗 启动抗病毒治疗前TDF、LdT药物组的孕妇基线血清HBV DNA差异无统计学意义(P>0.05),具有可比性(表1、2)。
表1 预防性应用TDF、LdT抗病毒治疗的妊娠期妇女的基线资料Tab.1 Baseline data of pregnant women on prophylactic TDF and LdT antiviral therapy ±s

表1 预防性应用TDF、LdT抗病毒治疗的妊娠期妇女的基线资料Tab.1 Baseline data of pregnant women on prophylactic TDF and LdT antiviral therapy ±s
TDF LdT t值P值例数37 28年龄(岁)30.16±4.02 30.11±3.80 0.056 0.956开始服药孕周(周)24.76±1.38 25.07±1.46-0.886 0.379服药至分娩的时长(周)12.55±2.03 12.29±2.13 0.514 0.609 HBV DNA(lg IU/mL)7.27±0.65 7.18±0.72 0.536 0.594 ALT水平(U/L)21.35±10.03 24.89±13.14-1.233 0.222
表2 治疗性应用TDF、LdT抗病毒治疗的妊娠期妇女的基线资料Tab.2 Baseline data of pregnant women on prophylactic TDF and LdT antiviral therapy ±s

表2 治疗性应用TDF、LdT抗病毒治疗的妊娠期妇女的基线资料Tab.2 Baseline data of pregnant women on prophylactic TDF and LdT antiviral therapy ±s
TDF LdT t值P值例数39 23年龄(岁)31.59±4.08 29.30±5.22 1.918 0.060开始服药孕周(周)21.85±7.70 17.22±6.77 2.387 0.020服药至分娩的时长(周)17.42±7.91 21.37±6.97-1.983 0.052 HBV DNA(lg IU/mL)6.62±1.07 6.91±1.00-1.087 0.281 ALT水平(U/L)178.85±143.48 194.74±103.18-0.464 0.644
2.2 抗病毒治疗后孕妇的血清HBV DNA情况TDF、LdT抗病毒治疗至分娩前,大部分妊娠期妇女的血清HBV DNA水平可降至105IU/mL以下,TDF组70/76例(92.11%),LdT组47/51例(92.16%),差异无统计学意义(P>0.05)。
TDF预防性、治疗性抗病毒4周时及分娩前孕妇的血清HBV DNA较基线下降幅度、HBV DNA转阴率与LdT组相当(P>0.05,表3、表4)。
2.3 HBeAg转阴及血清学转换情况 TDF、LdT预防性抗病毒治疗4周时,孕妇的HBeAg转阴率及发生血清学转换率均为0%;预防性抗病毒治疗至分娩前,TDF组出现2例(5.41%)孕妇的HBeAg转阴并发生血清学转换,LdT组孕妇的HBeAg未见转阴。
表3 妊娠期妇女预防性应用TDF、LdT抗病毒治疗后病毒学应答情况Tab.3 Virological response of pregnant women after prophylactic application of TDF and LdT antiviral therapy ±s
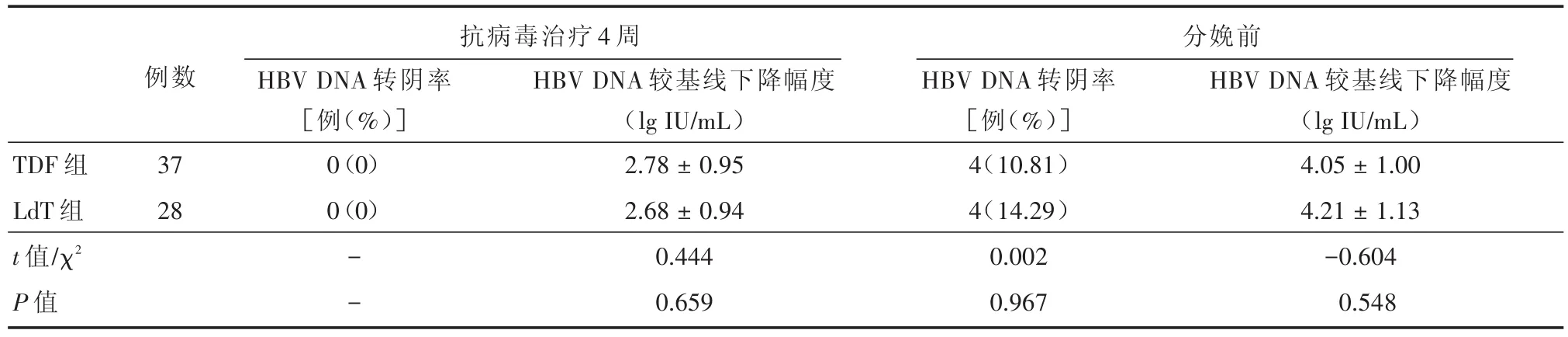
表3 妊娠期妇女预防性应用TDF、LdT抗病毒治疗后病毒学应答情况Tab.3 Virological response of pregnant women after prophylactic application of TDF and LdT antiviral therapy ±s
抗病毒治疗4周 分娩前例数TDF组LdT组t值/χ2 P值37 28 HBV DNA转阴率[例(%)]0(0)0(0)--HBV DNA较基线下降幅度(lg IU/mL)2.78±0.95 2.68±0.94 0.444 0.659 HBV DNA转阴率[例(%)]4(10.81)4(14.29)0.002 0.967 HBV DNA较基线下降幅度(lg IU/mL)4.05±1.00 4.21±1.13-0.604 0.548
表4 妊娠期妇女治疗应用TDF、LdT抗病毒治疗后病毒学应答情况Tab.4 Virological response of pregnant women after treatment with TDF and LdT antiviral therapy ±s

表4 妊娠期妇女治疗应用TDF、LdT抗病毒治疗后病毒学应答情况Tab.4 Virological response of pregnant women after treatment with TDF and LdT antiviral therapy ±s
抗病毒治疗4周 分娩前例数TDF组LdT组t值/χ2 P值39 23 HBV DNA转阴率[例(%)]1(3.45%)0(0)5.991 0.629 HBV DNA较基线下降幅度(lg IU/mL)3.28±1.00 3.10±1.07 0.620 0.538 HBV DNA转阴率[例(%)]23(58.97%)10(43.48%)1.395 0.237 HBV DNA较基线下降幅度(lg IU/mL)4.23±1.09 4.70±0.97-1.689 0.096
抗病毒治疗至分娩前,TDF预防性抗病毒组、治疗性抗病毒组孕妇的HBeAg转阴率、HBeAg血清学转换率与LdT预防性抗病毒组、治疗性抗病毒组比较差异均无统计学意义(P>0.05)。见表5。
2.4 ALT复常情况 TDF、LdT抗病毒治疗后,大部分妊娠合并CHB的患者可在分娩前达到ALT复常(TDF:79.49%vs.LdT:86.96%,P>0.05)。见表6。

表5 TDF、LdT治疗性抗病毒后妊娠期妇女的HBeAg情况Tab.5 The HBeAg condition of pregnant women after TDF and LdT therapeutic antiviral treatment 例(%)

表6 妊娠期妇女治疗应用TDF、LdT抗病毒治疗后ALT复常率情况Tab.6 ALT normalization rate after treatment of pregnant women with TDF and LdT antiviral therapy 例(%)
2.5 妊娠期间抗病毒治疗的安全性 127例孕妇应用TDF、LdT抗病毒治疗至分娩前,孕妇的血肌酐、血磷、血钙、血肌酸激酶均在正常范围内,均未出现不良事件。
3 讨论
HBV感染多呈慢性化,可发展为肝硬化、肝癌、肝衰竭等,严重威胁着人类的健康,母婴传播是导致HBV慢性感染的主要原因之一,全球约1/3的HBV感染源自于母婴垂直传播[12-14]。相关统计数据显示,我育龄期妇女HBsAg流行率约6.2%[15],新生儿接受乙肝疫苗联合乙型肝炎免疫球蛋白后,母婴传播发生率为6%,其中HBeAg阳性高病毒载量孕妇所生婴儿HBsAg阳性率高达11%[2]。中国二胎政策开放后,妊娠妇女的人数明显增加,HBV母婴阻断显得尤为重要。乙型肝炎母婴阻断临床管理流程[16]推荐高病毒载量的妊娠中晚期孕妇应用TDF、LdT预防母婴传播。对于血清HBV DNA载量>2×106IU/mL的免疫耐受期妊娠妇女,在充分的知情同意后,可在第24~28孕周时开始TDF预防性抗病毒,产后12周停药;对于免疫清除期妊娠妇女应在知情同意后应尽早启动TDF抗病毒,用药疗程同慢性乙型病毒性肝炎患者[2,17]。
本研究发现妊娠期应用TDF、LdT抗病毒治疗均可明显降低孕妇的血清HBV DNA,抗病毒治疗4周时血清HBV DNA水平下降显著,但大部分孕妇在分娩前的血清仍可检测出HBV DNA。国外学者研究[5,18-20]表明,妊娠期应用 TDF、LdT抗病毒治疗可以有效抑制乙肝病毒复制,但分娩前大多数孕妇的血清HBV DNA仍阳性,尤其是免疫耐受期的孕妇,本研究结果与国外学者的研究结果大致相同,说明产前孕妇血清HBV DNA处于低载量时HBV母婴传播几率小。
国内外文献[6,21-22]指出,HBV的宫内感染发生率与妊娠期间的HBV DNA水平呈正相关关系,当妊娠中晚期孕妇HBV DNA水平低于2×105IU/mL时,孕妇所生婴儿HBV感染率为0。本研究中92.11%的妊娠期妇女经TDF治疗后,分娩前血清HBV DNA可降至低于105IU/mL,应可降低HBV的母婴传播发生率。有报道指出应用TDF进行母婴阻断妊娠期妇女在停药3个月后出现HBV DNA反弹,少部分人出现ALT升高[18,23]。本研究中免疫耐受期妊娠妇女应用TDF、LdT抗病毒治疗4周时,其血清HBV DNA可较基线水平分别下降(2.78±0.95)、(2.68±0.94)lg IU/mL,据此可推断血清HBV DNA基线水平低于108IU/mL的孕妇抗病毒治疗4周时,其乙肝病毒载量可降至低于105IU/mL,可减少HBV母婴垂直传播事件发生。CYNTHUJA等[24]研究表明当母体病毒载量≥6 log10 IU/mL,在孕32周时开始抗病毒治疗,几乎完全阻断母婴传播。因此,HBV DNA低于108IU/mL的免疫耐受期孕妇也可考虑在孕32周左右开始启动预防性抗病毒治疗,相关文献指出替比夫定容易产生耐药性[25],未见TDF耐药病例报道,故而抗病毒药物建议选择TDF,减少药物对孕妇及胎儿的影响。
本研究对127例HBV感染孕妇进行分组治疗比较,发现TDF、替比夫定对HBV感染孕妇妊娠期的抗病毒治疗效果、安全性均良好,对于ALT正常、HBV DNA低于108IU/mL的HBV感染孕妇也可考虑在孕32周左右开始启动预防性抗病毒治疗,应可有效预防HBV母婴传播。
由于研究的样本量偏少,随访时间较短,未观察到新生儿出生后7、12月龄的HBsAg情况,也未对国产TDF与进口TDF药物的疗效进行对比,本研究存在一定的局限性,有待进行扩大样本深入研究。
