甲羟戊酸途径的代谢支路调控策略的研究进展
2020-03-12徐镇祥李美洁陈国强王纪明张海波
徐镇祥,李美洁,门 潇,陈国强,王纪明,咸 漠,张海波
(1.中国科学院青岛生物能源与过程研究所生物基材料重点实验室,山东青岛266101;2.齐鲁工业大学(山东省科学院)生物工程学院,山东济南250300;3.青岛农业大学生命科学学院光合固碳产能中心,山东青岛266109)
种类繁多的萜类化合物是广泛存在于自然界的一大类以异戊二烯为结构单元的聚合体及其衍生物。萜类化合物根据异戊二烯结构单元(C5H8)的数目可分为半萜(C5)、单萜(C10)、倍半萜(C15)、二萜(C20)、二倍半萜(C25)、三萜(C30)、四萜(C40)和多萜(>C40)[1]。目前发现的萜类化合物超过5万多种,常见的有单萜(薄荷醇、松油醇和芳樟醇),倍半萜(青蒿素、法尼烯和红没药烯),二萜(紫杉醇、维生素A),三萜(人参皂苷、灵芝酸),四萜(类胡萝卜素化合物)等[2]。萜类化合物在制药、香料、食品添加剂、着色剂、橡胶和高级生物燃料等行业中有着重要的应用。目前,萜类化合物主要从植物中提取或通过化学法合成。植物提取过程易受杂质干扰、纯化分离困难,而且部分植物对生长环境要求严格、生长缓慢,导致此方法产量低、成本高、不可持续[3]。化学合成法则面临着缺乏高效合成途径、原料不可再生以及环境污染等问题[4-5]。因此,寻找新型、高效、可持续的萜类化合物合成方法尤为重要。
近年来,随着代谢工程与合成生物学的发展,以可再生糖为原料,利用高效的微生物代谢工程合成萜类物质是当前生物化工领域的研究重点[6]。已经发现的萜类化合物的生物合成途径有两种:甲羟戊酸途径(MVA)和2-C-甲基-D-赤藻糖醇-4-磷酸途径(MEP)[7-9],前者主要存在于动植物中,后者主要存在于古生菌与原核生物中[10]。目前以微生物作为底盘细胞,利用底盘自身或外源的MEP或者MVA途径,合成目标萜类化合物是研究的热点。其中,MVA途径由于具有高效性、较好调控性和辅因子需求低等优点,是目前利用代谢调控方法提升效率的研究重点,当前研究主要集中在对其主路径的代谢调控策略上,而支路径,具体包括前体物质和辅助因子的供应、竞争途径的干扰等,对于提升萜类化合物的合成效率也是至关重要的。
本文中,笔者首先对甲羟戊酸(MVA)途径进行简单介绍,然后从前体供应的加强和辅助因子的协调、竞争途径的调控以及间接对代谢调控产生影响的生物宿主的进化三个方面,综述萜类化合物甲羟戊酸途径的代谢途径支路调控策略研究进展并进行了部分总结(表1),最后展望其进一步精确调控的发展方向。
1 MVA途径的简介
MVA途径可分为上游途径与下游途径(图1),该途径通过7步催化反应将前体物质乙酰辅酶A(Ac-CoA)转化为萜类化合物共同的前体物质异戊烯焦磷酸(IPP)和二甲基烯丙基焦磷酸酯(DMAPP)。在上游途径中,Ac-CoA在乙酰辅酶A硫解酶(AACT)和β-羟基-β甲基戊二酰-CoA合成酶(HMGS)的催化作用下生成HMG-CoA。然后,在下游途径中,甲羟戊酸在甲羟戊酸激酶(MK)的催化作用下生成5-磷酸-甲羟戊酸(5-MVAP),并消耗1个ATP;5-磷酸-甲羟戊酸在甲羟戊酸磷酸激酶(PMK)作用下生成甲羟戊酸-5-二磷酸(MVAPP),消耗1个ATP;甲羟戊酸-5-二磷酸在甲羟戊酸-5-焦磷酸脱羧酶(MDD)的催化作用下生成异戊烯基焦磷酸(IPP),消耗1个ATP;在异戊烯基焦磷酸异构酶(IDI)作用下,DMAPP和IPP可以相互转化。在糖酵解途径中,从1分子葡萄糖合成2分子前体物质乙酰辅酶A产生2分子ATP和4分子NADH,而1分子NADH在酶的催化作用下合成1分子NAD(P)H。综上,以葡萄糖作为碳源,通过MVA途径合成1分子IPP/DMAPP时,需要消耗1.5分子葡萄糖,产生4分子NAD(P)H;乙酰辅酶A是甲羟戊酸途径最主要的前体;ATP和NAD(P)H是MVA途径代谢过程中主要涉及到的辅因子。因此,利用代谢工程策略保证前体物质乙酰辅酶A的供应和协调辅因子的是提高MVA途径代谢流,从而进一步提高萜类化合物产量的前提条件。
2 前体供应的加强与辅因子的协调
MVA途径的前体乙酰辅酶A是其上游过程中细胞中心碳代谢的关键因子,参与多种代谢过程,并在合成和分解代谢中发挥重要作用。因此,在不影响细胞生长的前提下加强上游途径中流向MVA途径的乙酰辅酶A是一种提升MVA途径效率的代谢工程策略。乙酰辅酶A通过糖酵解途径合成(图2)。常用的提高乙酰辅酶A合成的代谢策略包括提高乙酰辅酶A合成效率和减弱或者抑制消耗乙酰辅酶A的支路途径两种。
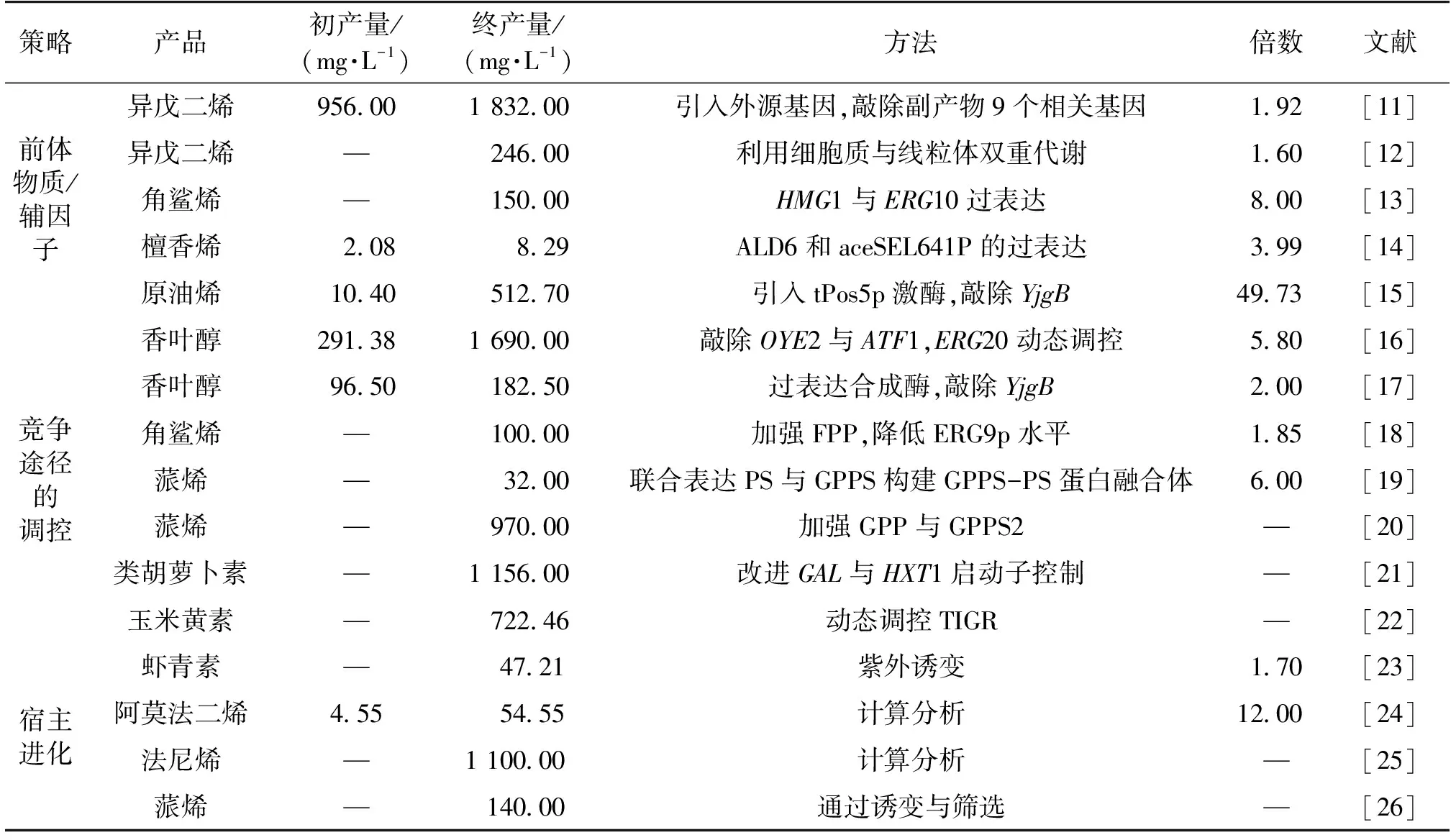
表1 三种调控策略对萜类化合物产量的影响
注:—文献中未说明。
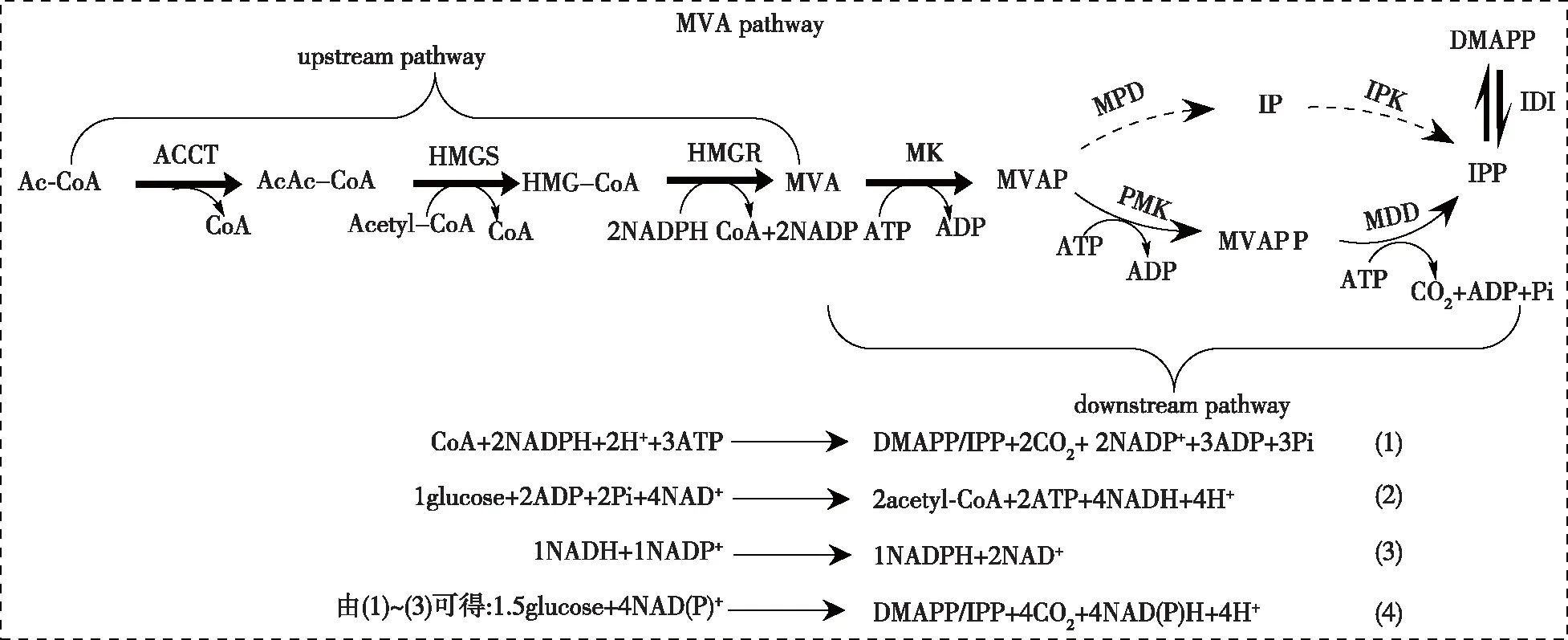
AcAc-CoA—acetoacetyl-CoA;IP—isopentenyl phosphate;ACCT—acetoacetyl-CoA;HMGR—HMG-CoA reductase;MPD—MVAP decarboxylase;IPK—IP kinaes图1 萜类物质的MVA途径和MVA途径转化为IPP/DMAPP的化学计量Fig.1 MVA pathway of terpenoids biosynthesis and stoichiometries of the conversion of glucose to IPP/DMAPP through the central carbon pathway and the MVA pathway
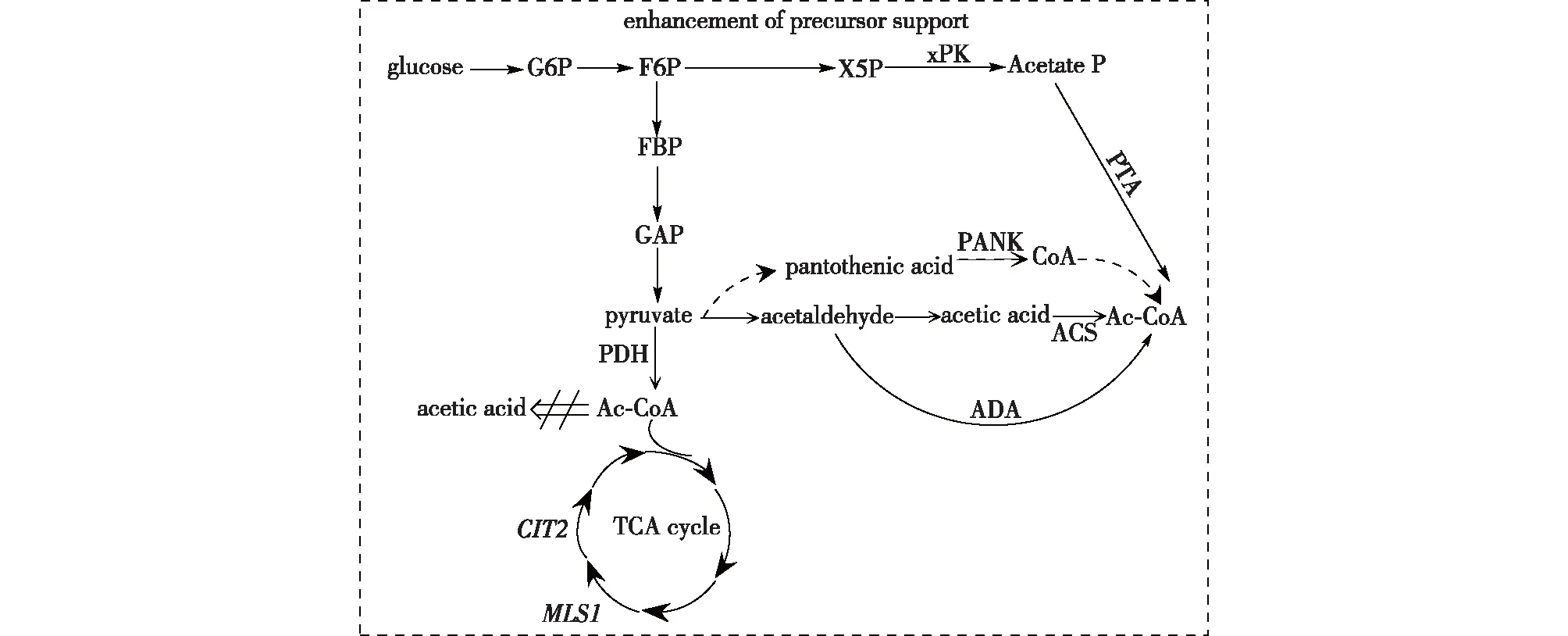
图2 前体物质的加强Fig.2 Enhancement of precursor support
过表达关键酶基因是提高乙酰辅酶A合成效率的常见策略。直接过表达乙酰辅酶A合成酶可显著减少副产物醋酸酯的产生,同时减少碳的消耗,使碳通量流向MVA途径是常用提高乙酰辅酶A合成酶(ACS)合成效率的方法[27]。过表达上游关键酶泛酸激酶(PANK)和丙酮酸脱氢酶(PDH),也可提高细胞内乙酰辅酶A水平[28-29]。另外,外源引入新的乙酰辅酶A合成途径也是提高乙酰辅酶A合成效率的一种策略。在酿酒酵母中,通过过表达木酮糖-5-磷酸特异性磷脂酶(xPK)、磷酸转乙酰酶(PTA)和乙醛脱氢酶(ADA)这3个外源酶,以新的路径合成乙酰辅酶A,这个新型路径减弱了碳的流失和ATP的需求,提高了乙酰辅酶A的合成效率[30]。
通过敲除支路途径基因或者过表达反向基因,从而抑制乙酰辅酶A的流失也是一种优化策略。在酵母中,Chen等[14]为了尽量减少流向三羧酸循环(TCA)的乙酰辅酶A,分别敲除三羧酸循环中关键酶基因CIT2和MLS1,确保形成可以运输到线粒体中进行氧化的C4有机酸。Kim等[11]在改造大肠杆菌生产异戊二烯时,为了减少乙酰辅酶A副产物的生成,通过敲除9个相关基因形成大肠杆菌AceCo(大肠杆菌MG1655ΔackA-pta、poxB、ldhA、dld、adhE、pps和atoDA),结果发现,AceCo菌株在发酵培养过程中副产物积累减少,异戊二烯产量明显增加,其产量由956 mg/L增至1 832 mg/L。乙醇和乙酸盐是常见的乙酰辅酶A产物,除了通过敲除基因抑制其生成,还可以通过过表达反向合成酶挽救其代谢流。其中,ADH2的过表达使碳通量流向从乙醇转向乙酰辅酶A,而ALD6和aceSEL641P的过表达使乙酸盐流向乙酰辅酶A,其檀香烯产量由2.08 mg/L提高到8.29 mg/L,最终产量提高近4倍[14]。
综上所述,通过提高合成和减弱消耗的策略加强前体乙酰辅酶A的供应,从而加强MVA途径代谢流,最终可以提高萜类化合物的合成。通过对宿主细胞正常生长代谢的发酵条件等因素进行分析,仅靠提高乙酰辅酶A的浓度并不一定能够达到提高生产效率的目的,如何更好地平衡乙酰辅酶A在细胞的合成代谢和MVA途径的关系,保证细胞生长的同时将足够的通量引入萜类化合物合成代谢途径是以后研究的重要方向。
调控辅因子NAD(P)H的浓度也是利用支路代谢调控甲羟戊酸途径代谢的一种方法。根据计算,葡萄糖通过MVA途径产1分子IPP/DMAPP需要消耗2分子NADPH,而其上游糖酵解途径能够合成6分子NADH。通过加强或者敲除相关基因,可以实现从NADH到NADPH的高效转化,进而能够有效提升MVA途径合成效率[31]。例如,将酿酒酵母中NADH激酶(tPos5p)转入大肠杆菌中,催化NADH合成NAD(P)H,同时敲除yjgB基因(图3),使得原油烯的产量由10.4 mg/L提高到512.7 mg/L[15]。

图3 辅助因子的协调Fig.3 Coordination of cofactors
总体来说,辅因子的协调策略主要集中在MEP途径。根据MVA与MEP途径的化学计量分析,在产萜类化合物的过程中,1.5分子的葡萄糖经过MVA途径会产生4分子的NAD(P)H,而1分子葡萄糖经过MEP途径需要消耗2分子NAD(P)H。
鉴于目前多数代谢工程菌株大多是同时利用MVA途径和MEP途径生产萜类化合物,如何利用NAD(P)H的转化和调控协调好微生物体内MVA途径与MEP途径的效率,是以后研究的重要方向。
3 竞争途径的调控
甲羟戊酸下游途径与微生物的生长代谢途径密切相关,两者对碳源存在依赖与竞争关系。为了提高萜类化合物的产量,需从支路途径和竞争途径重新定向碳通量。阻断竞争途径是重新定向碳通量的常用方法,具体控制策略具体包括:a. 敲除其中关键酶基因[16-17]。b. 选择较弱的启动子或执行RNA干扰[18,21]。c. 动态控制竞争酶的表达[21]。d. 酶抑制剂的利用[32]。e. 基因振荡器的应用[33](图4)。
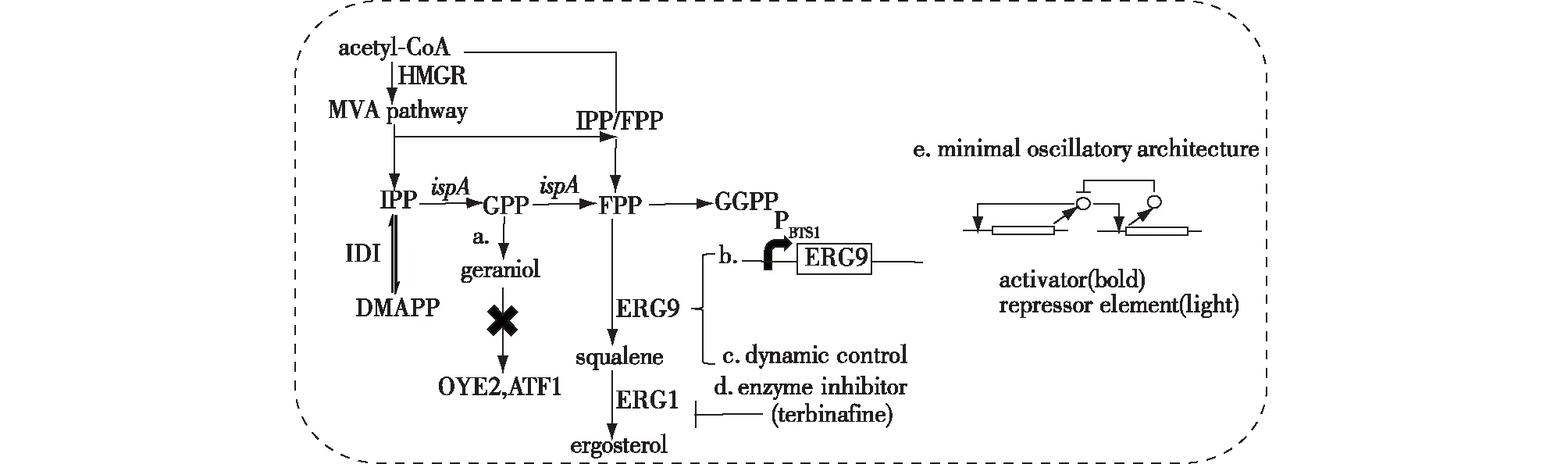
图4 阻断竞争途径Fig.4 Blocking the competitive pathway
敲除竞争途径的关键酶基因是常见的代谢工程策略。敲除参与香叶醇向其他萜类化合物内源性转化的OYE2(编码NAD(P)H氧化还原酶)与ATF1(编码乙醇乙酰转移酶)基因,使更多的碳通量流向到香叶醇的生产:OYE2基因的敲除使其产量为285.9 mg/L,比对照提高了1.7倍;ATF1基因的敲除使其产量达到了259.8 mg/L,比对照提高了1.6倍[16]。敲除关键基因的优点是在阻止中间产物扩散或者代谢流向竞争途径时稳定性高,可以有效增加主路径代谢流。如果竞争途径参与了细胞生长代谢,那么敲除关键酶基因会影响细胞生长,而通过选择较弱的启动子或执行RNA干扰可以避免这个问题。法尼基焦磷酸(FPP)是合成倍半萜类化合物与鲨烯共同的前体,而鲨烯是合成细胞膜组分麦角固醇的前体,为了积累更多的FPP用于倍半萜类化合物的合成,可使用弱启动子PBTS1代替鲨烯合成酶基因ERG9原本的启动子[21]。RNA开关为天然核开关,是一类位于mRNA3’或5’-UTR上的能够结合小分子代谢物以调控基因的转录和翻译的mRNA元件。它与小分子代谢物的结合不依赖于任何蛋白质,从而使构象发生改变,并在转录或翻译水平调控基因的表达[34-36]。对于一些关键的支路途径,通过采用1个较弱的启动子或执行RNA干扰,既保证了宿主的正常生长又减少了支路途径的竞争,然而这种策略不能根据代谢过程中的需求做出实时调控。利用调控元件可以实现对竞争途径代谢流的实时动态调控。例如,Xie等[21]将受葡萄糖抑制的改良GAL启动子调控合成类胡萝卜素主路径基因的表达,将受葡萄糖诱导的HXT1启动子调控竞争路径ERG9基因的表达,实现根据葡萄糖浓度进行动态调控。动态调控策略虽然能够有效提高微生物发酵的生产强度和效率,但是由于调控元件的特异性,这类元件很难广泛应用到其他产品中,而且针对特定的化合物,研究者还需要花费大量时间和精力去开发、寻找新的调控元件[37-39]。利用酶抑制剂是一种比较简单、容易操作的代谢工程策略。Peng等[18]建立了一种序列依赖内质网相关蛋白降解(ERAD)机制(富含Pro、Glu/Asp、Ser和Thr),降低ERG9p的水平,使倍半萜(nerolidol)产量达到100 mg/L,提高了86%。尽管酶抑制剂方法简单易操作,但是也具有抑制剂选择难度大等局限性,限制了其广谱性的应用。基因振荡器装置也是目前采用的一种新型策略,作为一种基因调控装置,通过基因振荡器的幅度和周期来决定基因表达的时间[33]。这种对基因表达时间的控制,可以用在大规模基因网络中,同时仅利用少量的调控因子即可调控相对较多的基因,从而实现对复杂细胞行为的调控。此外,动态调控策略还需要综合考虑转录水平和翻译水平后进一步完善。由此可见,调控策略各有利弊,并且已经成功应用于目标萜类化合物的生产中,但是如何根据具体需求选择最佳调控方法将效率调控至最佳依然是目前的研究难点。
4 宿主的进化
通过前体物质供应和辅助因子的协调、竞争途径的调控直接作用于甲羟戊酸路径的支路,对菌株萜类化合物的生产产生了较大影响。然而,也可通过其他策略间接影响代谢途径的效率,例如随机诱变、定向驯化和系统分析等策略对底盘细胞进行优化,改造菌株,从而影响代谢途径的效率。底盘细胞为萜类化合物的合成提供所需要的合成场所,而且萜类化合物的合成途径与底盘细胞的代谢网络之间具有非常复杂的关联。因此,可以采用随机诱变、定向驯化和系统分析等策略优化底盘细胞,间接影响甲羟戊酸路径的代谢效率,以此提高菌株自身的优势(图5)。
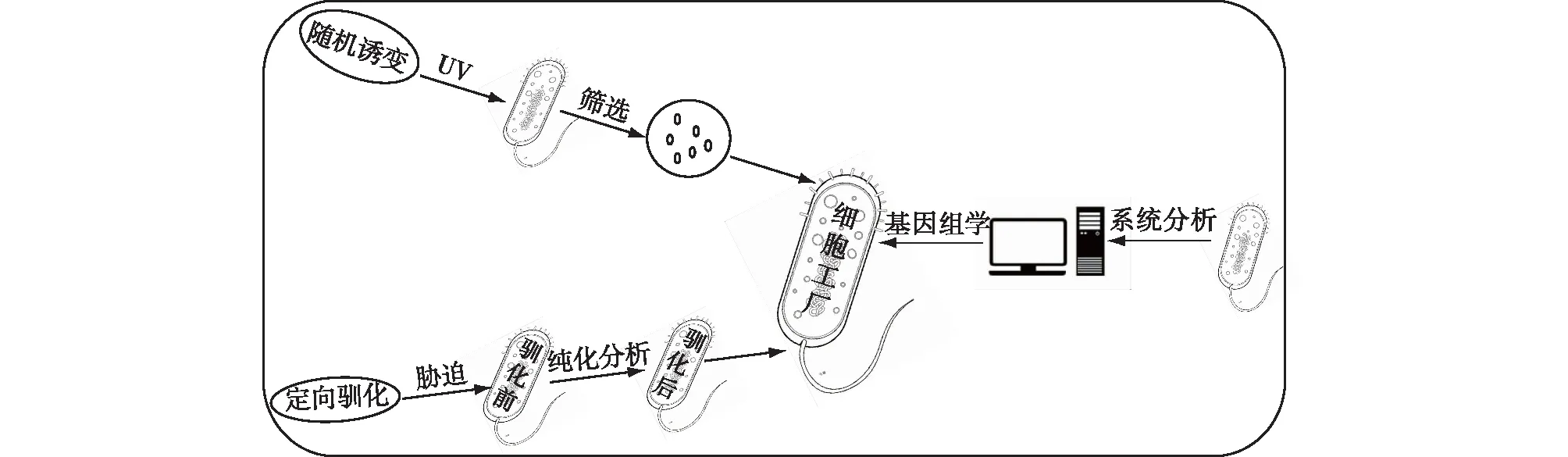
图5 宿主细胞的进化Fig.5 Microbial host evolution
随机诱变是最常见、操作简易的进化方法。Wang等[23]通过紫外照射突变体UV11-4使细胞干质量增加,然后采用抑制剂二苯胺(DPA)来筛选高产虾青素的产生菌株。突变体DPA12-2经逆变培养、增殖和转化,虾青素产量是野生型的1.7倍,达到(47.21±3.30) mg/g。然而,随机诱变需要大量的后期筛选工作,通过采用高通量筛选方法可大大提高工作效率[40]。
对于很多化合物的合成,无法建立高通量筛选方法,而定向驯化[41-42]可以解决这个问题。与随机诱变相比,定向驯化目的性更强,是一种可以富集、筛选微生物和改变微生物生理性状的一种有效方法,在菌种选育工作中已有广泛的应用。随着萜类化合物生产水平的不断提高,一些终端产品(如蒎烯、桧烯[43]和某些生物燃料)对细胞的毒性限制了其进一步改进可能。Brennan等[44]通过定向驯化,以提高宿主对柠檬烯的耐受性,筛选出优势菌株,宿主对柠檬烯耐受性提高了9倍,蒎烯与月桂烯分别提高了11与8倍;通过测序分析发现,Tcb2p和Tcb3p基因属于突变基因,但是与其代谢途径并无直接关联,主要通过间接代谢调控改变对有毒物质的耐受性。这与大肠杆菌对乙醇[45]和异丁醇[46]的耐受性以及酿酒酵母对木糖[47]和半乳糖[48]的利用率,在作用机制上有着相似的情况,都是通过间接方式对代谢调控来提高产物的积累。
随机诱变与定向驯化的作用机制不可控制,属于非理性策略,在实验后期有大量的筛选鉴定工作。因此采用计算机进行系统分析,寻找目标基因是一种优化替代策略。为了促进萜类化合物的合成,Zhu等[25]对宿主酿酒酵母的代谢网络进行计算分析,确定了具有促进萜类化合物产生潜力的敲除位点,构建了相应的单突变体。Sun等[24]最终获得的突变株产生的阿莫法二烯产量达到54.55 mg/L,是野生型的12倍。相对来说,随机诱变、定向驯化和系统分析,这三种针对宿主细胞进行优化的代谢策略都是比较耗时的,并且对甲羟戊酸途径的的作用机制尚不明确,但是,通过这3种策略获得的用于生产改良的突变体和突变基因通常具有创造性和原创性。因此,下一步需要提高筛选工作效率来筛选阳性突变体和基因,并加大对突变后作用机制的研究。
5 结论与展望
针对甲羟戊酸途径的代谢支路调控,从前体物质供应和辅助因子的协调、竞争途径的调控以及间接对代谢调控产生影响的宿主的进化这三个方面阐述了其调控策略的研究进展。这些调控策略结合主路径的代谢调控,使得萜类化合物生产水平不断提高,但是想要进一步提升合成效率达到工业化水平,仍有很多问题需要考虑:①在保证细胞生长不受影响的基础上,将上游充足的前体物质通量引入甲羟戊酸途径是以后研究的重要方向。②随着合成生物学的发展,在下游支路调控中采用动态代谢调控受到越来越多的关注。但是在实际应用中,动态调控还需要综合考虑转录后水平、翻译水平和发酵水平的影响,对于动态代谢调控系统在实验设计时,应该做进一步的优化。③甲羟戊酸途径的代谢主路径调控与支路径调控对于萜类化合物生产同等重要,如何对主路径与支路径优化结合,为更好提高萜类化合的产量是以后研究重点。
综上所述,随着新技术的发展与调控方法的日益成熟,对于微生物细胞工厂的构建将逐步完善,萜类化合物生产能力将会得到大幅提高,其生物合成萜类化合物生产成本降低,为萜类化合物的绿色生产奠定基础。
