乙状结肠造口皮肤黏膜深度分离影响因素的探究
2020-03-11云红张怡于洪霞张梦怡
云红 张怡 于洪霞 张梦怡
皮肤黏膜分离是指肠造口黏膜与腹壁缝合处愈合不良,使皮肤与黏膜分离造成的伤口,是肠造口术后常见的并发症之一[1]。国外文献报道,乙状结肠造口术后皮肤黏膜分离的发病率为4%~24%[2],我国万淑琴等[3]的研究报道为16.33%。但针对皮肤黏膜深度分离的发生率及发生的相关因素尚无文献报道。表浅的皮肤黏膜分离通过专业的护理能够较快恢复,对患者影响较小。皮肤黏膜的深度分离延长患者住院时间、增加治疗费用,如果伤口愈合速度较慢还会影响患者下一步的综合治疗。因此皮肤黏膜的深度分离不但会增加患者的经济负担,同时也加重了患者的心理压力。本项研究回顾性分析了450例低位直肠癌行腹会阴联合切除、乙状结肠造口术患者的临床资料,探讨皮肤黏膜深度分离发生的相关因素,对存在这些因素的患者加强护理观察,积极采取预防措施,防止皮肤黏膜分离的发生。对发生皮肤黏膜分离的患者做到早期发现、早期治疗,减轻组织损伤的程度,缩短伤口愈合时间,从而减轻患者痛苦、心理压力和经济负担。现将研究分析报道如下。
资料与方法
一、研究资料
回顾性分析2016年3月至2019年5月期间中国医学科学院肿瘤医院结直肠外科收治的450例低位直肠癌行腹会阴联合切除、乙状结肠造口术患者的临床资料。其中,男性264例,女性186例。年龄32~75岁。纳入标准:①年龄≤75岁;②术前无腹部手术史;③术前无肠梗阻;④术前无严重的心肺疾病;⑤术前经造口治疗师行造口定位;⑥术后皮肤黏膜深度分离:皮肤与肠黏膜缝合处未愈合,损伤深度达到脂肪层[2];⑦患者知情同意并签署知情同意书。排除标准:①术后出现肠梗阻、出血等并发症;②皮肤黏膜分离表浅,损伤止于真皮层。
二、资料收集方法
所有资料收集均由造口治疗师通过查阅病历、造口并发症处理记录和造口患者随访记录的方式完成资料收集。
一般资料包括:性别、年龄、BMI指数、术前有无合并糖尿病、术前白蛋白指标、术前是否接受新辅助治疗、术后是否发生肠造口黏膜坏死及造口局部组织脂肪液化等。
三、统计学分析
应用SPSS 19.0统计软件对所录入的资料进行统计学分析,计数资料采用频数、百分比表示,组间比较采用χ2检验或者Fisher精确检验。将皮肤黏膜深度分离有统计学意义的单因素纳入Logistic二元逻辑回归模型中进行分析,得到影响皮肤黏膜发生的独立因素。以P<0.05为差异有统计学意义。
结 果
一、研究对象的一般资料
本研究共纳入450例乙状结肠造口患者,男性264例,女性186例;发生皮肤黏膜深度分离为36例,发生率为8%,在发生皮肤黏膜深度分离的人群中:男性21例,女性15例;年龄>60岁25例,≤60岁11例;BMI正常12例、低于正常6例、高于正常18例;术前接受过新辅助治疗21例、未接受新辅助治疗15例;白蛋白指标正常12例、低于正常24例;合并糖尿病26例、无合并糖尿病10例;肠黏膜坏死31例、无肠黏膜坏死5例;肠造口局部组织脂肪液化31例、无脂肪液化5例,见表1。
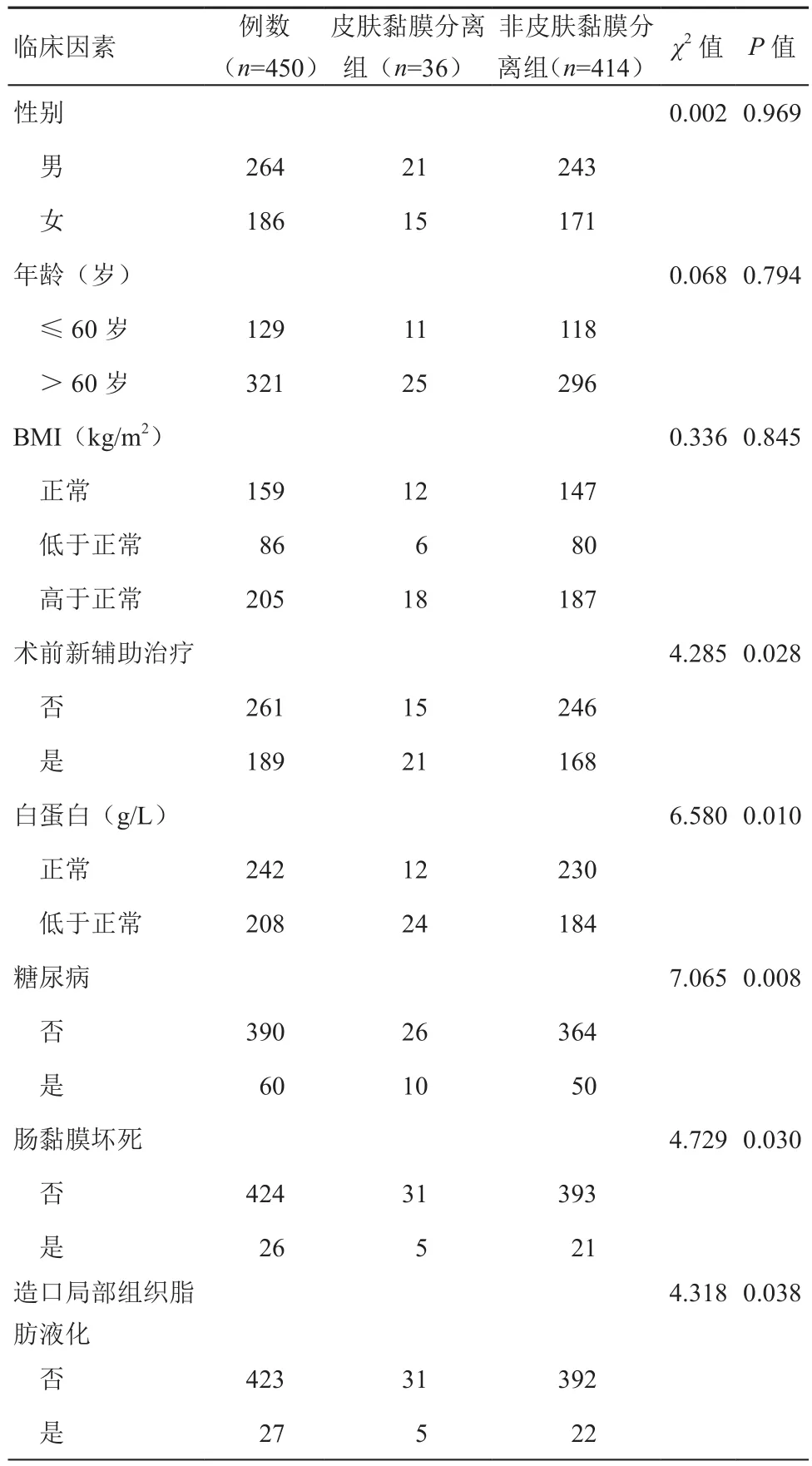
表1 乙状结肠造口皮肤黏膜深度分离的单因素分析(例)
二、皮肤黏膜深度分离影响因素的单因素分析
研究数据显示:性别(χ2=0.002,P=0.969)、年龄(χ2=0.068,P=0.794)、BMI 指 数(χ2=0.336,P=0.845)与乙状结肠造口皮肤黏膜深度分离无关。术前行新辅助治疗(χ2=4.285,P=0.028)、低白蛋白(χ2=6.580,P=0.010)、合并糖尿病(χ2=7.065,P=0.008)、术后肠黏膜坏死(χ2=4.729,P=0.030)、造口局部组织脂肪液化(χ2=4.318,P=0.038)是皮肤黏膜深度分离的影响因素,见表1。
三、皮肤黏膜深度分离影响因素的多因素分析
将单因素分析有统计学意义的因素,纳入多因素Logistic回归分析。结果显示:白蛋白低于正常(OR=2.514,95%CI:1.217~5.134;P=0.01)、合并糖尿病(OR=3.014,95%CI:1.287~7.057;P=0.011)、肠黏膜坏死(OR=3.155,95%CI:1.036~9.610,P=0.043)、伤口局部组织脂肪液化(OR=5.467,95%CI:1.754~17.038;P=0.003)是皮肤黏膜深度分离的独立影响因素,见表2。
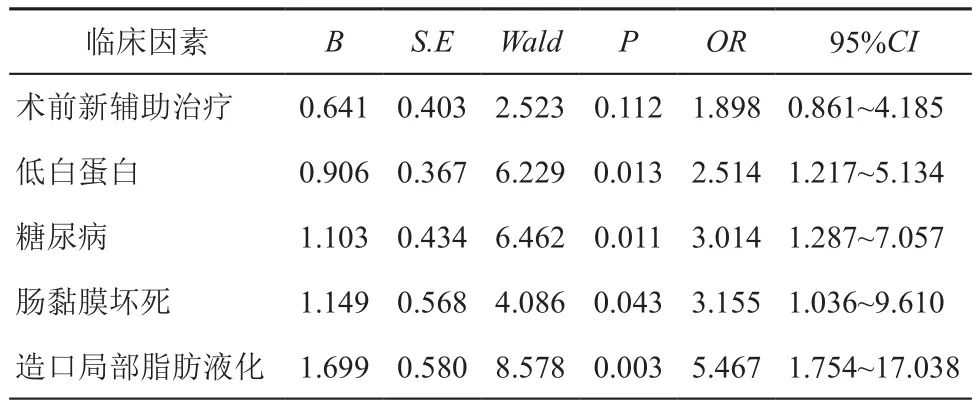
表2 乙状结肠造口皮肤黏膜深度分离的logistic回归分析
讨 论
一、术前新辅助治疗对皮肤黏膜愈合情况的影响
直肠癌术前新辅助治疗能够提高完全缓解率、降低局部复发率,提高中低位直肠癌的保肛概率,成为目前中低位直肠癌综合治疗的重要手段之一。放射治疗对肠道的损伤分为急、慢性直肠炎。慢性放射性损伤致肠壁内小血管损伤,组织纤维化,发生概率为2%~20%[4]。在直肠镜下放射性直肠炎表现为直肠黏膜充血-水肿-溃疡[5]。由于肠壁血管损伤、微循环障碍和肠道黏膜水肿增加了皮肤黏膜愈合不良的危险。本项研究结果显示术前行新辅助治疗的患者皮肤黏膜深度分离的发生率占总发生人数的58.3%,是皮肤黏膜深度分离的影响因素。
二、术前营养状况与皮肤黏膜愈合的关系
血清白蛋白水平是衡量营养状况的重要指标。营养不良会导致术后切口感染风险增加,切口愈合能力下降。其机制可能为营养不良会延长炎性反应,或影响胶原蛋白的合成[6-7]。一项Meta分析报道,当白蛋白水平<35 g/L时,术后手术部位感染的风险将增加2.5倍[8]。本研究数据显示,术前白蛋白指标低于正常是皮肤黏膜深度分离的独立影响因素。乙状结肠造口术后,肠道功能恢复后自肠造口排大便。粪便中含有大量细菌,皮肤与黏膜缝线处极易被粪便污染,感染的机会大大增加,因此术前补充营养纠正蛋白水平,术后选择适合肠造口外观的底盘和辅助的造口用品管理好粪便,防止粪水自底盘剪孔处渗到皮肤黏膜缝线部位,降低感染发生的机会,促进皮肤黏膜愈合。
三、糖尿病对皮肤黏膜深度分离的影响
糖尿病患者糖代谢紊乱以及糖酵解功能明显降低,中性粒细胞吞噬功能差,且患者体内蛋白质代谢异常,免疫性蛋白合成不足致使患者免疫能力下降[11]。另外糖尿病患者皮肤黏膜防御机能明显降低,体内的高糖环境利于细菌生长繁殖,易发生软组织感染性疾病,导致伤口感染率增加[9-10]。肠造口的功能就是排便,因此皮肤黏膜缝合处不可避免的会被细菌污染。糖尿病患者的免疫力差和体内的高糖环境给细菌增殖提供了条件,发生皮肤黏膜愈合不良的危险增加。本研究结果显示糖尿病是皮肤黏膜深度分离的独立影响因素。因此对合并糖尿病患者在围手术期加强血糖监测并将血糖控制在正常范围对于预防术后伤口感染,促进伤口愈合非常重要。
四、肠黏膜缺血坏死是皮肤黏膜深度分离的独立影响因素
伤口愈合需要有良好的血运提供营养。肠黏膜缺血坏死时,肠黏膜和皮肤缝合处的伤口不能愈合而发生深度的皮肤黏膜分离。导致肠黏膜缺血坏死的原因包括手术意外损伤或结扎供应肠造口的血管、提拉肠管时张力过大、扭曲压迫肠管或缝合时误伤肠系膜血管、腹壁开口过小或缝合过紧、肠系膜血栓形成等[11]。因此医生在做肠造口手术时要观察肠管的血运情况,注意操作细节,防止人为因素造成肠黏膜坏死。术后护士要加强观察肠黏膜颜色,及时发现肠黏膜血运不良的情况,及早处理。防止皮肤黏膜分离的创面进展而增加伤口处理难度。
五、造口局部组织脂肪液化是皮肤黏膜愈合不良发生深度分离的独立影响因素
腹部手术脂肪液化的原因包括患者肥胖;高频电刀的高温致使脂肪细胞热损伤发生变性,脂肪组织内的毛细血管热凝固栓塞,进而导致脂肪组织血运障碍发生液化;以及术者的缝合技术等[12]。伤口脂肪液化是脂肪组织发生的无菌性坏死,形成较多渗液[13]。肠造口部位的皮下脂肪发生液化未及时引流,渗液积存在皮下组织并形成腔隙,进一步导致皮肤黏膜缝合部位无法愈合。在更换造口底盘时按压肠造口周围组织,观察是否有伤口渗液自皮肤黏膜缝合处溢出,及时与医生沟通,适当拆除无效的缝线,充分引流并积极换药处理,促进伤口愈合。
综上所述,直肠癌腹会阴联合切除、乙状结肠造口术患者,术前行新辅助治疗、白蛋白指标低于正常可以引起影响术后肠造口皮肤黏膜深度分离的发生。肠造口黏膜坏死、合并糖尿病以及造口局部组织脂肪液化是皮肤黏膜深度分离发生的独立影响因素。临床工作中对存在以上因素的患者应给予充分重视,提早预防,及时发现皮肤黏膜愈合不良,早期处理,减轻患者的经济负担和心理压力。
