动物双歧杆菌A6 体内外安全性评价
2020-02-28周晓娟桑跃刘治麟葛绍阳
周晓娟,桑跃,刘治麟,葛绍阳
(1.中国农业大学食品科学与营养工程学院,北京 100083;2.河北省畜产食品技术创新中心,廊坊 065201;3.北京和益源生物技术有限公司,北京 100089)
益生菌是一类对宿主有益的活性微生物,是定植于人体肠道、生殖系统内,能产生确切健康功效从而改善宿主微生态平衡、发挥有益作用的活性有益微生物的总称[1]。近年来,随着研究的深入,人们对益生菌在人类健康及疾病中的作用有了更加全面及深入的认识,多种益生功能和作用机制得到了深入的研究,包括改善肠道炎症[2]、免疫调节[3,4]、预防过敏性疾病[5]等。
益生菌主要应用于益生菌制剂、益生菌饮品和膳食添加剂等产品中, 如乳制品、饮料和益生菌胶囊等。调查表明, 益生菌在我国食品中得到广泛应用,其中80%应用于发酵乳制品[1]。随着益生菌产业的飞速发展,与其相关的功能和安全性研究也得到了越来越多的重视。人们提出一些能够反映肠道细菌活性的指标,来评价乳酸菌的安全性,对产生的生物胺、耐药性及毒性因子等潜在安全性风险进行研究,成为评价益生菌安全性的重要部分[6]。
本试验对动物双歧杆菌A6进行安全性评价,其中体外安全性主要通过研究抗生素抗性、分析有毒代谢物等方面进行评价[6];体内安全性主要从菌株的毒理学、移位可能性等方面进行评价[7]。
1 材料和方法
1.1 菌株与培养基
动物双歧杆菌A6,由中国农业大学功能乳品实验室提供,中国普通微生物保藏管理中心保藏,菌株号CGMCC No.9273。培养基组成同文献[8]。
1.2 试验方法
抗生素敏感性检测、生物胺检测、动物试验设计、血生化和血常规指标检测、细菌移位能力评价方法均与文献[8]相同。
1.3 统计分析
2 结果与讨论
2.1 抗生素敏感性
氨基糖苷类、喹诺酮类抗生素及氨多作用于革兰氏阴性菌,对革兰氏阳性菌效果普遍较差。试验结果表明,A6对氨基糖苷类、喹诺酮类、糖肽类部分抗生素及胺/氨的敏感性为R或者I(表1),与文献报道相符。已有多篇文献报道干酪乳杆菌、鼠李糖乳杆菌以及植物乳杆菌等乳酸菌天然对糖肽类抗生素如万古霉素具有普遍耐受性。从检测范围分析,菌株A6不存在种属保守耐性以外的抗生素耐受性。菌株的这种固有耐性多为菌株纵向遗传获得,而非基因横向转移,耐性的转移风险小。
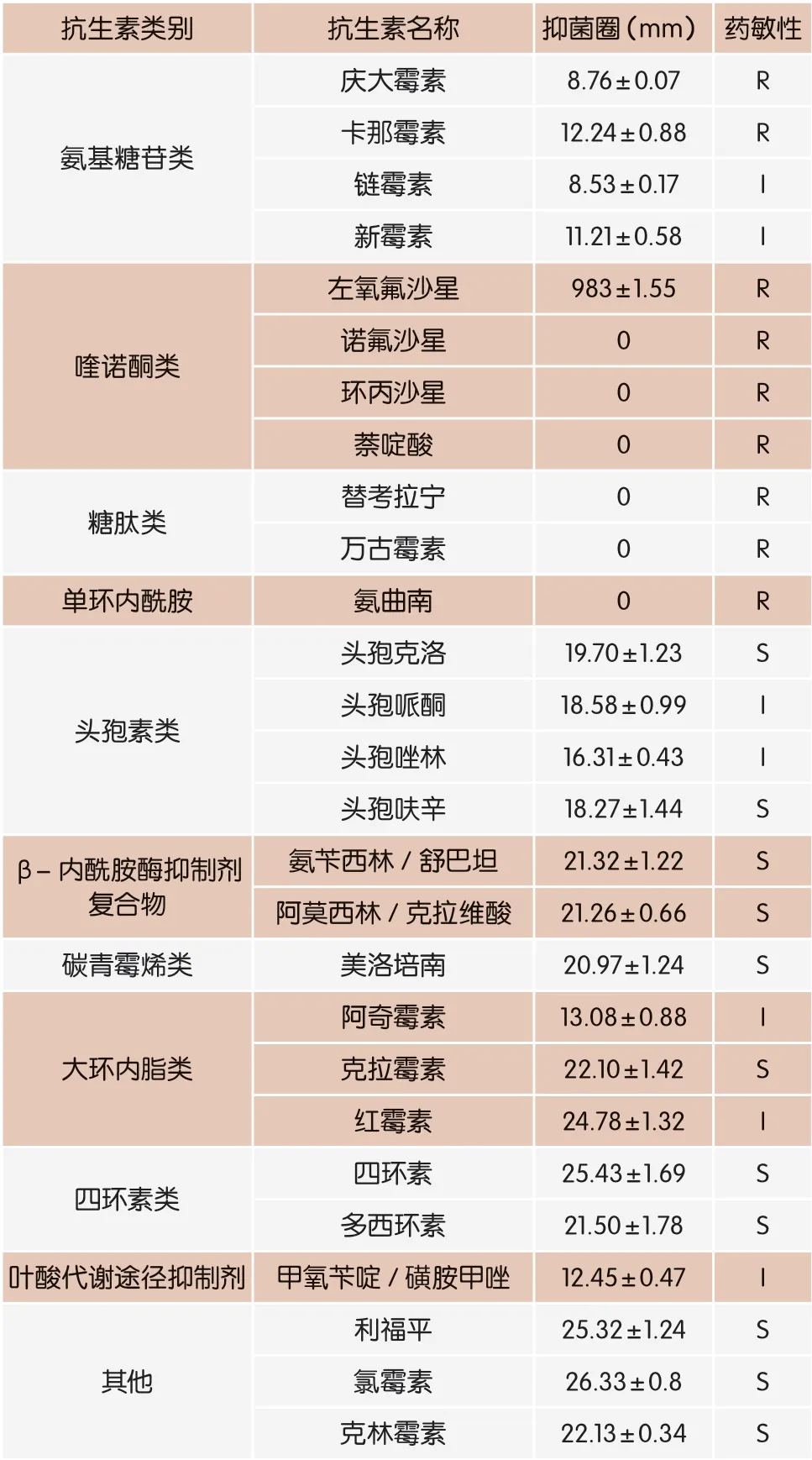
表1 试验菌株药物敏感性能
2.2 生物胺检测
脱羧酶培养基中的溴甲酚紫的有效指示范围为pH 5.2~6.8,pH值在5.5时呈黄色,稍大于5.5就会出现颜色变化,呈现紫色或紫红色。A6在改良脱羧酶液体培养基培养4d,相对于空白对照培养基,添加了鸟氨酸、组氨酸、酪氨酸、精氨酸四种不同氨基酸的液体培养基均呈现浑浊状态,表明乳酸菌在其中可以正常生长,而各培养基均呈黄色,表明菌株生长并未使培养液pH值升高,初步判断菌株未产生胺类物质。
2.3 口服A6 急性毒性试验
血常规指标可反映试验菌株在血液中的副作用,血生化指标反映营养不足及代谢失衡的状况。这些指标的变化通常早于其他的临床症状。本试验中试验组和对照组血常规和血生化指标未发生任何显著变化(表2),说明试验菌株对试验动物无不利影响。
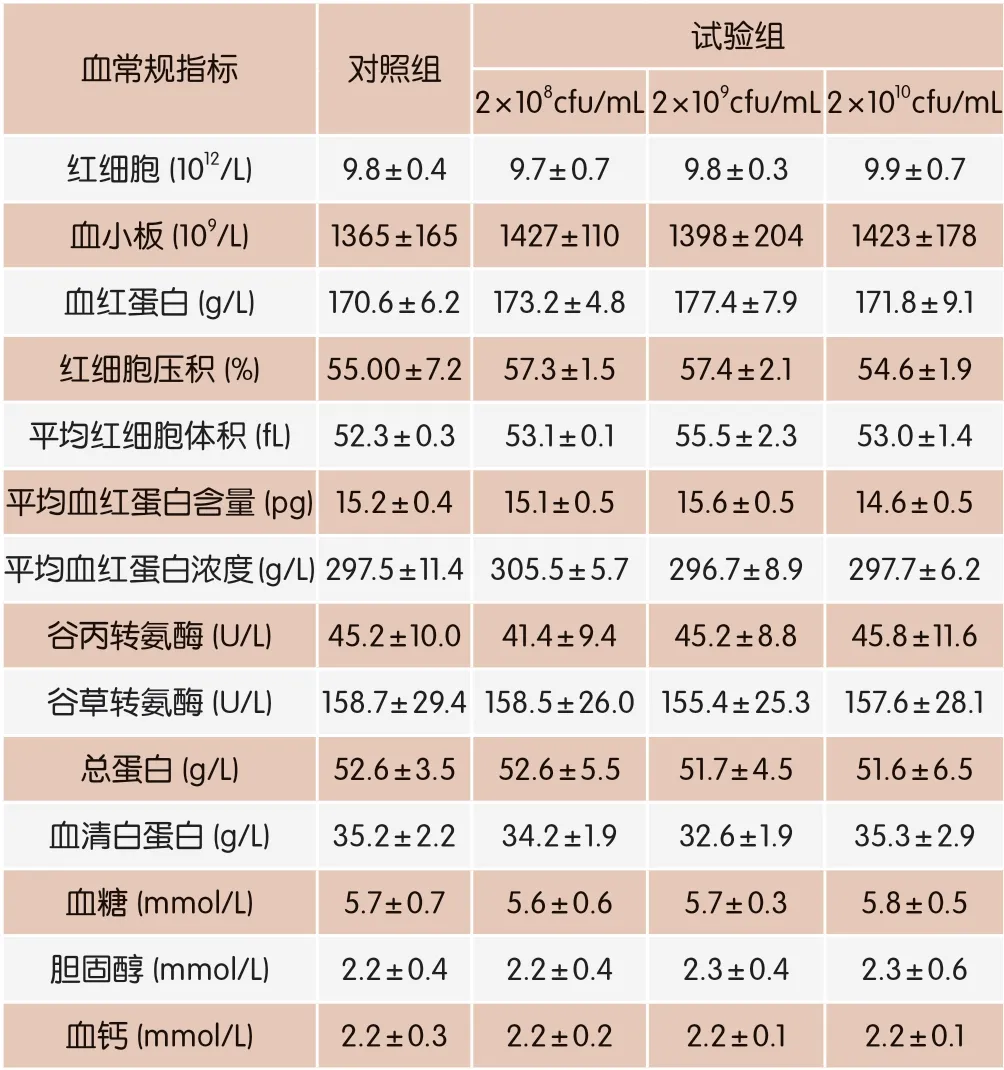
表2 试验小鼠的血常规和血生化指标(n=10)
2.4 细菌移位检测
细菌移位是益生菌安全性的最严重问题之一。益生菌移位可引发感染,包括菌血症、败血症或心内膜炎[9,10]。因此,评价益生菌的移位能力是十分重要的。本试验结果表明,对照组和试验组的组织和血液样本经过培养后,各培养基上均无菌落生长(表3),表明试验动物的组织和血液未受到污染,菌株没有从肠道转移到组织和血液中,未发生移位现象。

表3 试验小鼠被试菌转移到肝、脾、肾和血液的移位率
3 结论
动物双歧杆菌A6不存在种属特有耐性以外的抗生素耐受性,不存在抗生素转移的风险;产胺试验未发现生物胺的产生。以2×108cfu/mL、2×109cfu/mL、2×1010cfu/mL三种菌剂量灌胃小鼠28d,均未发生不良反应,未发生血液、肝脏、脾脏和肾脏的移位;表现为较高的移位安全性。动物双歧杆菌A6安全性评价未发现菌株的不安全因素。
