降脂理肝汤对高脂饮食诱导的非酒精性脂肪肝病大鼠非经典的细胞焦亡途径的影响①
2020-02-20尹抗抗湖南中医药大学医学院长沙410028
唐 标 尹抗抗 (湖南中医药大学医学院,长沙 410028)
非酒精性脂肪肝病(nonalcoholic fatty liver disease,NAFLD)是全球激增的健康问题,是肝脏疾病和心血管代谢疾病死亡的关键危险因素[1]。部分NAFLD患者会进展为肝炎、肝纤维化和肝硬化,最终发展为肝癌、肝衰竭,NAFLD的发病机制与脂质代谢紊乱、脂质蓄积、胰岛素抵抗、内质网应激以及炎症等多种因素有关[2,3]。
细胞焦亡是一种炎症相关的可调控性细胞死亡方式,gasdermin D(GSDMD)蛋白是细胞焦亡的执行分子,GSDMD被活化剪切生成的GSDMD的N端(GSDMD-N)会形成聚合物并与细胞膜上的脂质分子形成孔道,导致细胞肿胀破裂,释放大量促炎因子,加重炎症反应[4]。GSDMD的活化由Caspase-1/4/5/11介导,Caspase-4/5为大鼠和小鼠种属Caspase-11在人体中的同源蛋白,由Caspase-1活化介导的细胞焦亡,为经典的细胞焦亡途径;而由脂多糖(LPS)诱导的Caspase-4/5/11活化而诱导的细胞焦亡为非经典的细胞焦亡途径[5,6]。已有研究揭示细胞焦亡介导了NAFLD中肝细胞的死亡以及加重炎症反应和纤维化的进程,成为NAFLD干预的重要靶点[7,8]。
降脂理肝汤由泽泻、丹参、决明子、郁金、海藻和荷叶6味中药组成。临床观察和实验研究表明,降脂理肝汤能有效干预NAFLD[9]。前期实验研究表明,降脂理肝汤能调节高脂饮食诱导的NAFLD大鼠脂代谢,抑制炎症反应,减轻肝脏病理损伤,并且能抑制NLRP3炎症小体的活化[10-12]。但是降脂理肝汤在NAFLD中的抗炎机制以及非经典的细胞焦亡途径是否介导其抗炎机制还不明确,因此本研究观察降脂理肝汤对NAFLD中非经典的细胞焦亡途径的影响,探讨降脂理肝汤干预NAFLD的机制。
1 材料与方法
1.1材料
1.1.1实验药物 降脂理肝汤由泽泻10 g,决明子30 g,丹参10 g,郁金10 g,海藻30 g,荷叶10 g组成,中药饮片均购自湖南中医药大学第一附属医院药房,经湖南中医药大学陈晓阳教授鉴定为治疗标准复合要求的药材。上述药物加8倍量水浸泡30 min 后,沸后煎煮1 h后过滤,再加6倍量水沸后煎煮1 h过滤,两次药液混合,于65℃减压旋蒸浓缩,浓缩成2 g/ml的浓缩液,于4℃冷藏储存,临用前用生理盐水稀释成所需浓度。
1.1.2动物 健康SPF级SD雄性大鼠,体质量(150±10)g,由湖南斯莱克景达实验动物有限公司提供,生产许可证号为SYXK(湘)2017-0003。实验前,在动物房适应性饲养1周,饲养室温度(22±2)℃,自然昼夜节律光照,自由进水摄食。整个动物实验方案获得湖南中医药大学伦理委员会的批准,实验过程中对动物的处置符合2006年国家科技部发布的《关于善待实验动物的指导性意见》。
1.1.3试剂 水合氯醛(批号:8MQ20-CC)购自梯希爱化成工业发展有限公司;Western及IP细胞裂解液(批号:P0013)购自碧云天;蛋白酶抑制剂Cocktail (不含EDTA,100 × DMSO储液,批号:B14002),磷酸酶抑制剂Cocktail (100×B15002,批号:B15002)购自Bimake;大鼠IL-1β ELISA试剂盒(批号:GN-R30172)、大鼠L-18 ELISA试剂盒(批号:GN-R30168)、大鼠TNF-α ELISA试剂盒(批号:GN-R31092)、大鼠IL-6 ELISA试剂盒(批号:GN-R30201)购自盖宁生物;LPS检测试剂盒(批号:H178)购自南京建成生物工程研究所;GSDMD鼠单克隆抗体(批号:sc-393581)、Caspase-11(批号:sc-374615)鼠单克隆抗体购自Santa Cruz Biotechno-logy;GSDMD-N兔单克隆抗体(批号:93709)购自Cell Signaling Technology;β-actin鼠抗单克隆抗体(批号:A5316)购自Sigma;山羊抗兔二抗(批号:AP132P)、山羊抗鼠二抗(批号:AP124P)购自Merck。
1.1.4仪器 酶标仪、电泳仪、转膜仪和凝胶成像系统(美国Bio-Rad公司)。
1.2方法
1.2.1NAFLD大鼠模型的建立 参照前期研究[13],采用高脂饲料喂养12周的方法建立NAFLD大鼠模型,高脂饲料配方:脂肪10%、胆固醇2%、胆盐0.5%、蛋黄粉5%,标准大鼠饲料82.5%,高脂饲料由湖南斯莱克景达实验动物有限公司提供。
1.2.2动物分组和药物干预 SD大鼠随机分为正常组、模型组、降脂理肝汤组,其中降脂理肝汤给药剂量参照前期研究,按照动物与人体间的等效剂量换算,设3个剂量,分别为降脂理肝汤低剂量组(2.3 g/kg)、降脂理肝汤中剂量组(4.6 g/kg)和降脂理肝汤高剂量组(9.2 g/kg)。正常组标准饲料喂养,模型组和降脂理肝汤高脂饲料喂养,喂养12周后,每组随机抽取3只,取肝组织苏木精-伊红染色(HE染色),观察组织病理学变化,观察到高脂饲料肝脏出现不同程度的脂肪变性和空泡样变,验证模型成功后,进行药物干预,降脂理肝汤采用灌胃给药的方式,均1次/d。连续6周,每周称重1次,按体质量调整给药量。正常组和模型组每天灌胃给予等量的生理盐水,药物干预期间,喂养方式同前。干预结束后,取各组大鼠肝门静脉和腹主动脉血液和肝脏待检测。
1.2.3Western blot检测蛋白表达量 每组5只大鼠,取大鼠同部位肝脏组织100 mg,加入含蛋白酶和磷酸酶抑制剂的裂解液1 ml于冰上匀浆30 min,提取组织总蛋白,BCA法测定蛋白浓度,调平各样品蛋白浓度。取40 μg蛋白进行SDS-PAGE电泳分离后,转移到硝酸纤维素膜上,5%脱脂奶粉封闭1 h,用抗GSDMD(1∶1 000)、GSDMD-N(1∶1 000)、Caspase-11(1∶500)和β-actin(1∶5 000)一抗抗体4℃孵育过夜,洗涤后加HRP标记的二抗(1∶10 000),室温孵育1 h,洗涤后ECL显色曝光,用Quantity One灰度分析软件进行图像定量分析,测定目的蛋白的相对光密度值(IOD),以β-actin为内参蛋白,计算目的蛋白IOD与内参蛋白IOD的比值,以此表示蛋白表达量。
1.2.4门静脉血清LPS水平检测 门静脉血液静置离心后提取血清,按照检测试剂盒说明书检测,首先向预先包被了抗体的酶标孔中加入样本,再加入生物标记的识别抗原,于37℃孵育1 h,PBST洗涤3次,加入亲和素HRP,于37℃孵育1 h,在450 nm波长下测吸光值,以标准孔吸光值及其对应浓度绘制出标准曲线,计算各组血清中LPS的浓度。
1.2.5血清IL-1β、IL-18、TNF-α和IL-6水平检测 大鼠腹主动脉血液静置离心后提取血清,按照试剂盒说明书进行检测,试剂盒于室温下平衡20 min后,将稀释好的样品或不同浓度标准品按照100 μl/孔加入相应孔中,每孔设置1复孔,同时设置本底校正孔,即空白孔,设置方法为该孔只加TMB溶液和终止液,用封板膜封住反应孔,室温孵育120 min后,洗板5次,且最后一次置于厚吸水纸上拍干,加入生物素化抗体100 μl/孔,封孔后室温孵育60 min,洗板5次,加入辣根过氧化物酶标记100 μl/孔,室温避光孵育20 min,洗板5次,加入显色剂TMB溶液100 μl/孔,室温避光孵育20 min,加入终止液50 μl/孔,混匀后立即测量A450值。根据标准品浓度和吸光度值绘制标准曲线,通过样品吸光度值和标准曲线计算样品浓度。

2 结果
2.1降脂理肝汤对NAFLD大鼠肝组织GSDMD蛋白表达的影响 Western blot结果显示,与正常组相比,高脂饮食诱导的模型组大鼠肝组织GSDMD和GSDMD-N蛋白表达量显著增加(P<0.01);降脂理肝汤药物干预后,大鼠肝组GSDMD和GSDMD-N蛋白表达量显著降低(P<0.05或P<0.01),结果见图1。
2.2降脂理肝汤对NAFLD大鼠肝组织Caspase-11蛋白表达的影响 Western blot结果显示,与正常组相比,模型组大鼠肝组织Caspase-11蛋白表达量显著增加(P<0.01);与模型组相比,降脂理肝汤药物组肝组织Caspase-11蛋白表达量显著降低(P<0.01),结果见图2。
2.3降脂理肝汤对NAFLD大鼠肝门静脉血清中LPS水平的影响 与正常组相比,高脂饮食诱导的模型组大鼠肝门静脉血清LPS水平显著升高(P<0.01);与模型组相比,降脂理肝汤药物的干预均能显著降低大鼠肝门静脉血清LPS水平,并呈剂量依赖性(P<0.01),结果见图3。
2.3降脂理肝汤对NAFLD大鼠血清中IL-1β、IL-18、TNF-α和IL-6水平的影响 检测结果显示,与正常组相比,模型组大鼠血清IL-1β、IL-18、TNF-α和IL-6水平显著升高(P<0.01);与模型组相比,降脂理肝汤药物组大鼠血清IL-1β、IL-18、TNF-α和IL-6水平显著降低(P<0.05或P<0.01)。结果见图4。
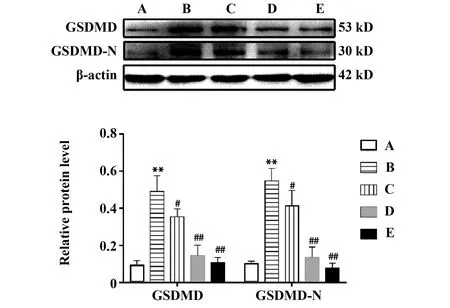
图1 降脂理肝汤对大鼠肝组织GSDMD蛋白表达的影响
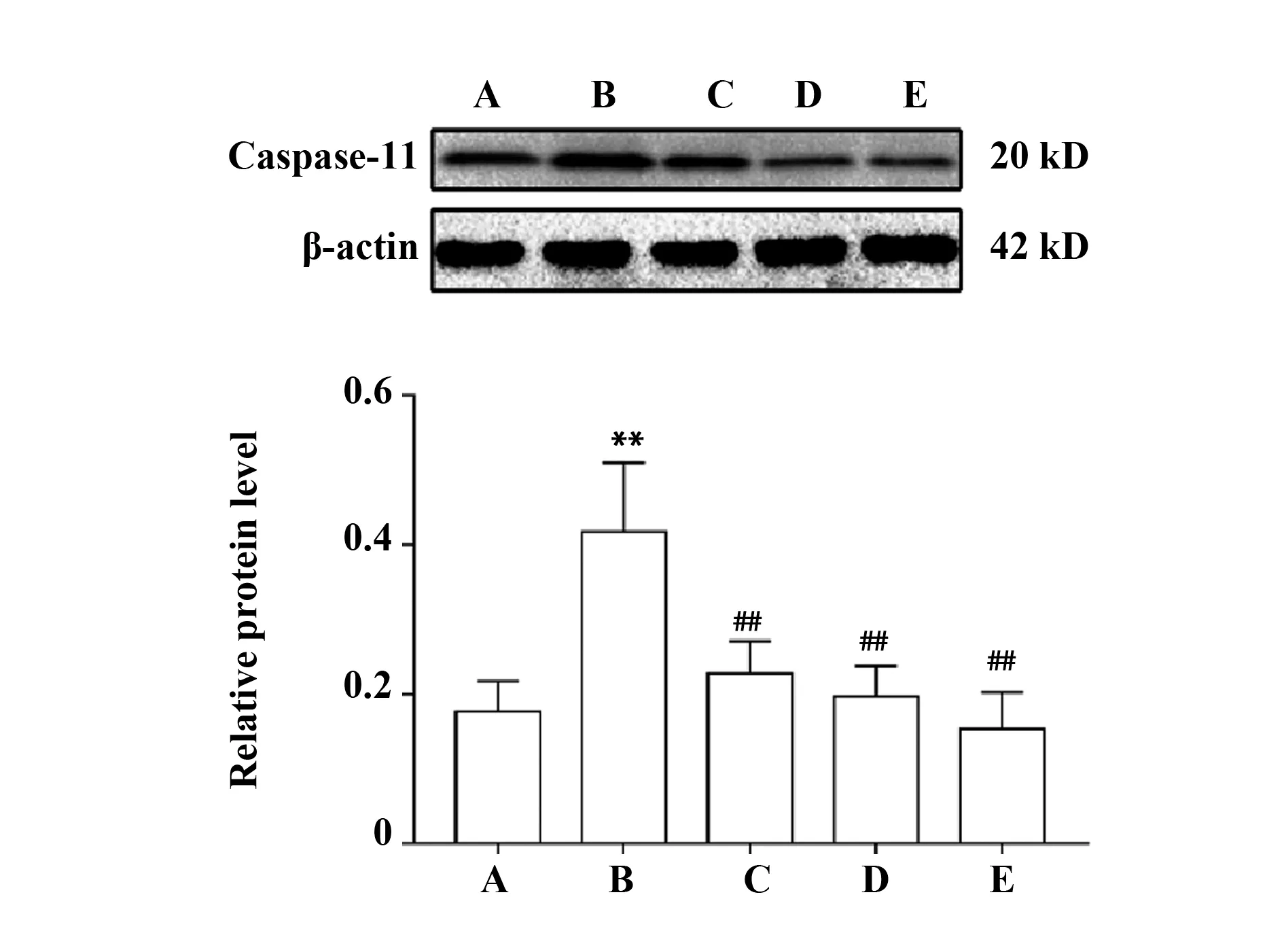
图2 降脂理肝汤对大鼠肝组织Caspase-11蛋白表达的影响
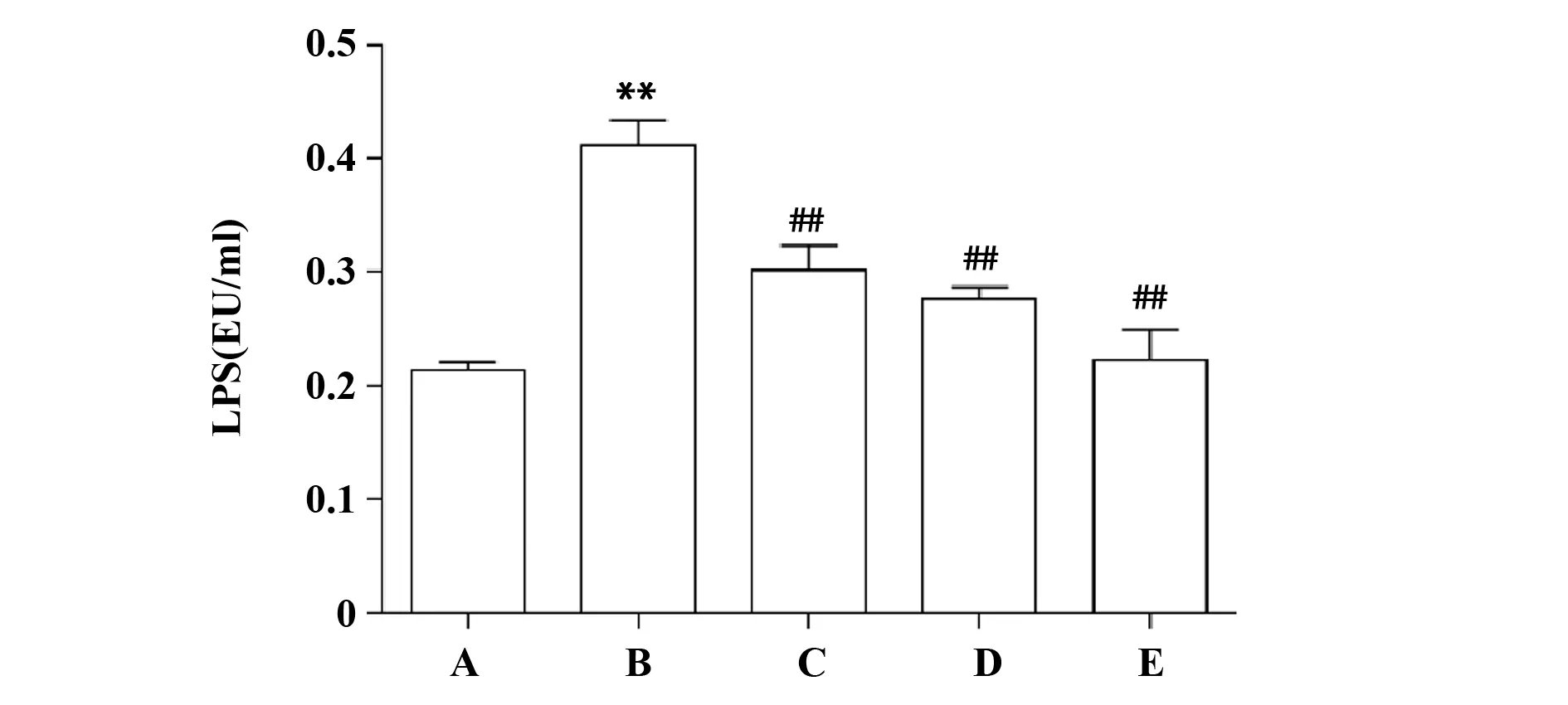
图3 降脂理肝汤对大鼠肝门静脉血清LPS的影响
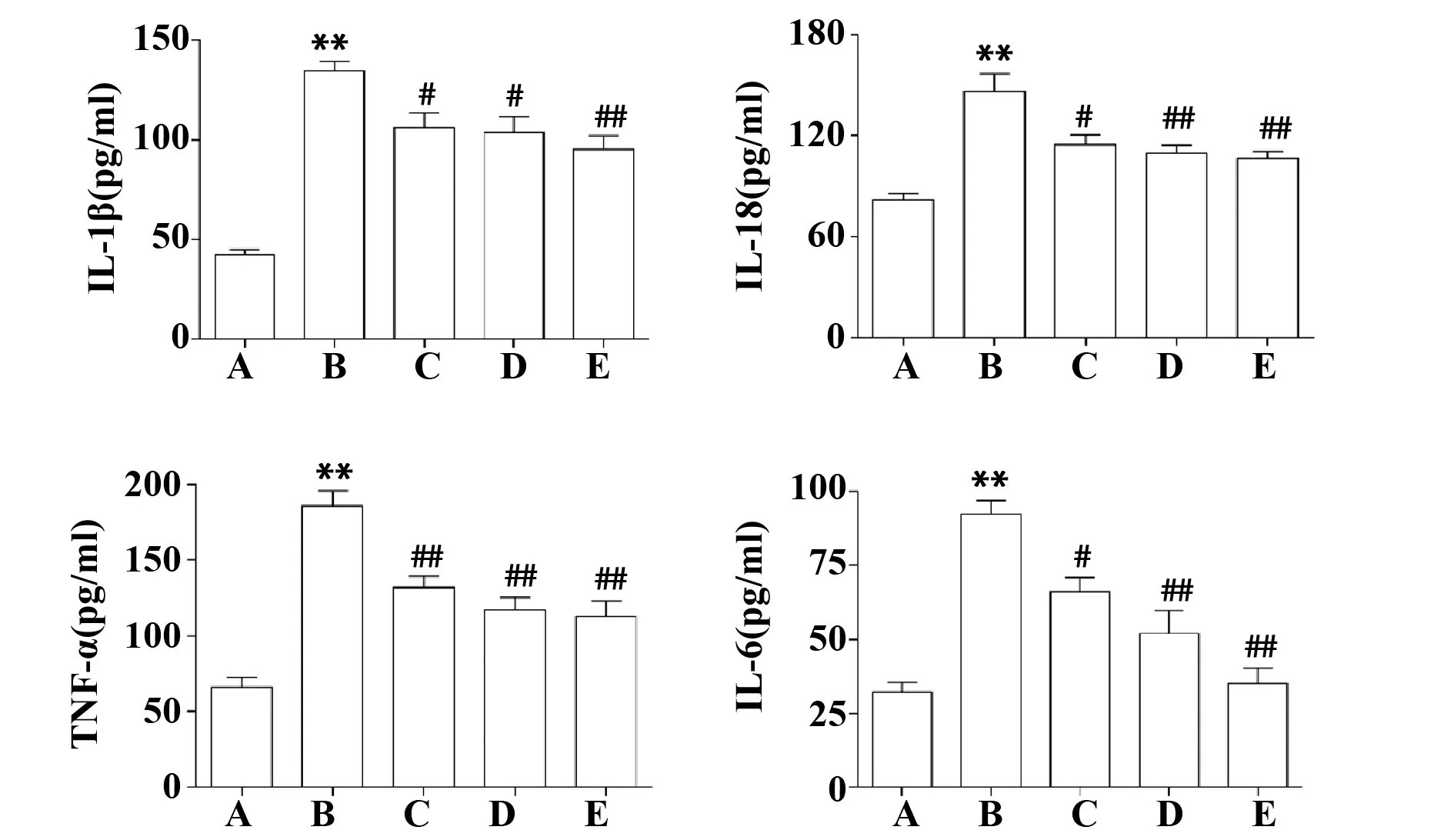
图4 降脂理肝汤对大鼠血清中IL-1β、IL-18、TNF-α和IL-6水平的影响
3 讨论
前期的实验研究揭示,降脂理肝汤可降低高脂饮食诱导的NAFLD大鼠体重、肝重和肝指数,调节脂代谢,改善脂质过氧化,改善肝功能和肝脏病理损伤,其机制与抑制炎症反应、调控肠道菌群有关[10-14]。
炎症反应作为NAFLD发病机制的核心环节在NALFD的发生发展中发挥了重要作用,细胞焦亡介导了NAFLD中的炎症反应,成为NAFLD干预的重要靶点[8]。已有的研究揭示,GDSMD蛋白作为细胞焦亡的执行蛋白,介导了NAFLD进展过程,GSDMD蛋白被剪切活化后生成GSDMD-N,GDDMD-N导致细胞穿孔肿胀破裂,释放大量促炎因子,加重炎症反应,抑制GDSMD的活化能阻断NAFLD疾病的进展[15]。本研究结果显示,高脂饮食诱导的NAFLD大鼠,GSDMD蛋白及其活化后的GSDMD-N表达明显增加,而降脂理肝汤的干预能降低GSDMD和GSDMD-N的水平,表明降脂理肝汤能调控GSDMD的活化。
在非经典的细胞焦亡途径中,LPS可直接活化的Caspase-4/5/11,活化Caspase-4/5/11剪切GDSMD诱导细胞焦亡。本研究结果显示,高脂饮食诱导的NAFLD大鼠肝脏组织中,Caspase-11的水平明显升高,而降脂理肝汤的干预能降低能显著降低Caspase-11的水平,提示降脂理肝汤可能通过Caspase-11来调控GSDMD蛋白的活化。已有研究表明在NAFLD中肠道菌群的紊乱以及肠道黏膜的受损可导致肠道内革兰氏阴性杆菌溶解释放的LPS进入门静脉血液加重NAFLD肝脏炎症和加快疾病进展[16-18]。本研究结果显示,高脂饮食诱导的NAFLD大鼠肝门静脉血清中LPS含量显著升高,而降脂理肝汤的干预能显著降低大鼠肝门静脉血清中LPS含量,我们前期实验研究揭示,降脂理肝汤能调控NAFLD大鼠肠道菌群,修复肠黏膜损伤,减少LPS入血[13,19],提示降脂理肝汤可能通过降低NAFLD大鼠门静脉血清中LPS含量,调控Caspase-11和GSDMD的活化。
细胞焦亡的发生会导致IL-1β和IL-18等促炎因子的释放,而促炎因子会加重NAFLD中的炎症反应[20,21]。因此我们进一步观察了降脂理肝对血清中促炎因子的影响,实验结果显示,高脂饮食的NAFLD大鼠血清中IL-1β、IL-18、TNF-α和IL-6水平明显升高,而降脂理肝汤的干预能显著降低血清中IL-1β、IL-18、TNF-α和IL-6的水平,这提示降脂理肝汤能降低NAFLD大鼠促炎因子的水平。
本研究结果显示高脂饮食诱导的NAFLD大鼠,存在非经典的细胞焦亡途径的活化,IL-1β和IL-18等促炎因子水平明显升高,而降脂理肝汤能抑制NAFLD大鼠中非经典细胞焦亡途径的活化,降低促炎因子的水平,近期有研究揭示抑制细胞焦亡能有效减轻NAFLD损伤以及抑制非经典的细胞焦亡途径能有效干预酒精性肝炎的进展[22,23],提示降脂理肝汤可能通过调控非经典的细胞焦亡途径干预NAFLD。
综上所述,降脂理肝干预NAFLD的机制可能与抑制非经典的细胞焦亡途径,降低促炎因子的水平有关。
