农林废弃物基生物炭对重金属铅和镉的吸附特性
2020-02-07嵇梦圆胡逸文桑文静李登新
嵇梦圆,胡逸文,梁 程,桑文静①,李登新
(1.东华大学环境科学与工程学院国家环境保护纺织工业污染防治工程技术中心,上海 201620;2.上海市大气颗粒物污染防治重点实验室,上海 200433)
近年来,随着经济的快速发展,我国环境中的重金属污染问题日益突出。我国2014年公布的《全国土壤污染状况调查公报》显示,全国土壤环境状况总体不容乐观,土壤重金属总的点位超标率为16.1%,其中铅、镉污染物点位超标率达到1.5%和7.0%。铅、镉重金属是继汞之后会对生态环境和人类健康造成重大威胁的第2、3大重金属元素[1]。原位钝化修复被认为是修复重金属污染土壤经济有效的处理方法之一。目前,常用于钝化重金属的材料主要有活性炭、石墨烯、碳纳米管、铁氧化物、粉煤灰和膨润土等[2],但是这些吸附材料制备复杂,价格昂贵,加上可能会产生二次污染,限制了其大规模应用[3]。因此,原料广泛、成本低且具有较高环境稳定性的生物炭作为污染物吸附与钝化的材料越来越受到学者的青睐[4]。
目前,生物炭修复重金属污染环境研究以采用单一生物炭并针对单一重金属的研究为较多,如王震宇等[5]研究表明高温生物炭(≥500 ℃)具有更完备的π共轭芳香结构,促进了生物炭对Cd2+的吸附作用;JIANG等[6]研究发现生物炭吸附Pb2+的过程中,静电作用与非静电作用共存,且生物炭表面官能团与Pb2+形成络合物是吸附的主要机制。而土壤污染多为重金属复合污染,有关生物炭对复合重金属吸附特性的研究还较薄弱。戴静等[7]研究指出溶液中Cd2+和Pb2+是通过与生物炭中 CO32-、PO43-和SiO44-发生沉淀反应而被去除。李瑞月等[8]研究发现,玉米秸秆炭的有机碳和官能团含量较高,孔隙结构较好,比表面积大,可能主要通过表面吸附和官能团的络合作用去除溶液中Pb2+和Cd2+。此外,不同材料制备的生物炭具有不同特性,从而表现出不同的吸附效果。JIANG等[9]研究也发现与软质生物炭(Qmax=1.47 mg·g-1)相比,硬质生物炭(Qmax=2.31 mg·g-1)对铜和锌具有更高的吸附性能。
分别以玉米、水稻和沙柳3种秸秆为原料,在500 ℃条件下限氧热解获得玉米生物炭、稻草生物炭和沙柳生物炭,并对其形貌特征和元素组成等一系列理化特性进行表征和分析,研究了不同影响因素条件下不同生物质来源的生物炭对土壤中铅和镉的吸附效果,并运用经典吸附动力学模型和吸附等温模型对实验数据进行拟合,初步探讨其吸附机制,以期为农业废弃物资源化利用及生物炭治理土壤重金属污染提供理论指导。
1 材料与方法
1.1 生物炭的制备
以玉米秸秆、水稻秸秆和沙柳秸秆(均购自安徽星美秸秆循环利用科技有限公司)为原料,在自然条件下风干1周后粉碎至粒径小于0.85 mm。装满已清洗的石英舟后轻微压实置于管式炉中,采用高温限氧热解法,在500 ℃缺氧环境下热解炭化2 h(升温速率为5 ℃·min-1),冷却至室温后,取出过0.15 mm孔径筛并用去离子水洗涤至中性,烘箱中烘干保存备用。热解制备的玉米生物炭、水稻生物炭和沙柳生物炭分别标记为CB、SB和SWB。
1.2 生物炭的表征
用pH计(PHSJ-4A,上海精密科学仪器有限公司)测定生物炭样品的pH值〔m(固)∶V(液)为1∶20〕,用灼烧法测定样品灰分含量。3种生物炭中 C、H 和 N 含量采用元素分析仪(TCH-600,LECO USA)测定,在此基础上,计算H/C比值。采用带能谱的扫描电镜(SEM-EDS)观察CB、SB和SWB样品形状、骨架结构和表面孔隙结构。生物炭比表面积和孔径采用比表面及孔径分析仪(Micromeritics ASAP 2010,美国)测定。采用溴化钾压片法对生物炭样品进行傅里叶变换红外光谱仪(FTIR)表征(Nicolet 5700,美国Thermo Nicolet公司),定性分析生物炭表面官能团。
1.3 吸附试验
将一定量3种生物炭分别加入PbCl2和CdCl2溶液中,于25 ℃条件下避光,按200 r·min-1恒温振荡。吸附动力学试验中ρ(Pb2+)和ρ(Cd2+)初始值分别为200和50 mg·L-1,称取0.08 g生物炭用作吸附剂,向溶液中添加0.01 mol·L-1NaNO3作为背景电解质,进行吸附振荡试验,定时取样。准一级动力学方程[10]和准二级动力学方程[11]分别为
Qt=Qe(1-e-K1t/2.303),
(1)
t/Qt=(1/K2Qe2)+(1/Qe)t,
(2)
h0=K2Qe2。
(3)
式(1)~(3)中,Qe为平衡吸附量,mg·g-1;Qt为t时刻吸附量,mg·g-1;K1为准一级动力学方程反应速率常数,h-1;K2为准二级动力学方程的反应速率常数,mg·g-1·h-1;h0为初始吸附速率,mg·g-1·h-1。
等温吸附试验中ρ(Pb2+)分别为10、20、50、100、200、400、600和800 mg·L-1,ρ(Cd2+)分别为5、10、15、25、50、80、100和150 mg·L-1,生物炭投加量为1.6 g·L-1,于25 ℃条件下振荡24 h后过滤,测定滤液中 Pb2+和Cd2+浓度。采用Langmuir方程[12]和Freundlich方程[12]进行等温吸附模拟,其表达式分别为
(4)
(5)
(6)
式(4)~(6)中,Qm为完全单层覆盖时对应的最大吸附容量,mg·g-1;KL为Langmuir平衡常数,L·mg-1;Ce为平衡吸附质量浓度,mg·L-1;C0为重金属离子初始质量浓度,mg·L-1;Qe为平衡吸附容量,mg·g-1;KF为Freundlich常数,它是与吸附容量相关的常数;n为表示吸附程度的常数;RL为分离因子。
1.4 影响因素试验
以0.01 mol·L-1NaNO3作为背景电解质,混合液污染物ρ(Pb2+)和ρ(Cd2+)初始值分别为200和50 mg·L-1,分别考察pH值、共存离子强度和生物炭投加量对吸附效果的影响。不同pH值:将40 mL混合液加入50 mL分别装有80 mg SWB、SB和CB的离心管中,调节初始pH分别为3、4、5和6,离子强度为10 mmol·L-1,生物炭添加量为2 g·L-1。不同离子强度:设置初始离子(Na+和Ca2+)强度分别为10、20、50、100、150和200 mmol·L-1,pH控制为6,生物炭添加量为2 g·L-1;探究不同价态共存阳离子(Na+、Ca2+)对生物炭吸附Pb2+和Cd2+的影响。不同生物炭投加量:设置初始生物炭投加量分别为0.08、0.16、0.40、0.80、1.20、1.60、2.40、3.20和4.80 g·L-1,pH控制为6,离子强度为10 mmol·L-1。
以上试验均重复3次,样品测定前需用0.45 μm孔径滤膜过滤,之后用电感耦合等离子体光谱仪(ICP-Prodigy-space,美国LEEMAN LABS公司)测定滤液中Pb2+和Cd2+浓度。生物炭对重金属离子的吸附量(Qt)和吸附效率(E)计算公式为
(7)
E=(Ci-Ct)/Ci×100%。
(8)
式(7)~(8)中,Qt为吸附t时刻吸附剂吸附重金属的吸附量,mg·g-1;E为去除率,%;Ci和Ct分别为溶液中重金属离子初始质量浓度和t时刻溶液中重金属离子质量浓度,mg·L-1;V为加入重金属溶液的体积,mL;m为投加的吸附剂质量,mg。
2 结果与讨论
2.1 生物炭性质
玉米、水稻和沙柳秸秆3类生物质在500 ℃条件下热解所制备的生物炭pH值、灰分和主要元素含量等基本理化性质见表1。由表1可知,SWB碱性最强,CB次之,SB最小,说明SWB和CB表面含有更丰富的碱性阳离子(K+、Ca2+、Na+和Mg2+等)。此外,与CB和SB相比,SWB灰分含量也更高,灰分含有的如碳酸钙等水溶性碱性矿物质也会导致生物炭具有较强碱性。
H/C(摩尔比)可用来表征生物炭的芳香性[13]。表1中3种生物质来源的生物炭C、H和N元素含量差别不大,CB、SB和SWB的H/C分别为0.46、0.48和0.46,属于从“硬质碳”向“软质炭”之间过渡的阶段,具有较为适中的芳香性,也说明热解产生的生物炭较好地保留了秸秆生物质中的有机成分,表面官能团丰富。
表1 3种生物炭的基本理化性质
Table 1 Basic physical and chemical properties of three biochars

生物炭pH平均粒径/nmw(H)/%w(C)/%w(N)/%H/C(摩尔比)w(灰分)/%玉米(CB)7.452 6432.1255.740.950.4611.36水稻(SB)7.292 6432.2556.701.120.4810.21 沙柳(SWB)7.552 6432.4363.521.520.4615.46
2.2 FTIR红外分析


CB为玉米生物炭,SWB为沙柳生物炭,SB为水稻生物炭。
2.3 表面结构与比表面积分析
CB、SB和SWB的扫描电镜图像见图2。3种生物炭在扫描前均经过研磨和筛分,但从扫描电镜图中仍能看出其保留了一定的秸秆骨架结构,生物炭碎片均呈条形片状,轮廓清晰,具有丰富的孔隙结构。生物炭颗粒表面不平整,可能是因为在制备过程中生物质中的矿物质积聚在生物炭表面。扫描图中生物炭颗粒粒径基本在1~50 μm之间。对比发现SWB和CB表面孔隙更加丰富,可能具有更大的比表面积。比表面积分析仪(BET)测试结果显示,CB、SB和SWB比表面积分别为18.07、16.98和40.06 m2·g-1,其中,SWB比表面积最大,CB次之,SB最小,因此推测在物理吸附性能上3种生物炭由强到弱依次为SWB、CB和SB。与常见商业生物炭相比,笔者实验中制备的CB、SB和SWB比表面积均较小(表2[15-19]),可能是由于农林废弃物生物质在500 ℃热解条件下生物炭内层的中孔和内孔还没有完全打开[20]。
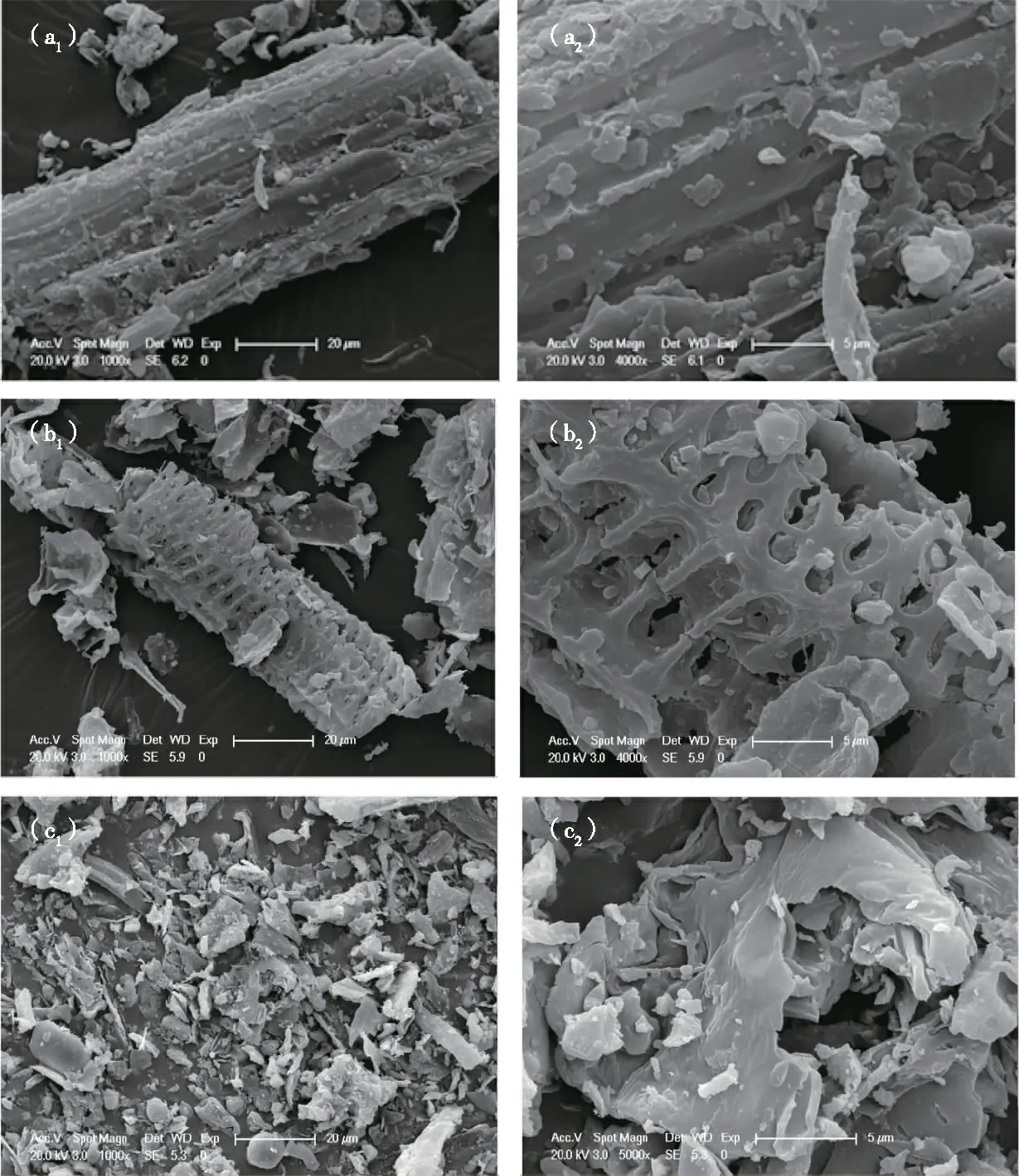
a1和a2分别为SWB放大1 000和5 000倍的SEM图;b1和b2分别为CB放大1 000和5 000倍的SEM图; c1和c2分别为SB放大1 000和5 000倍的SEM图。
表2 各种生物炭比表面积比较
Table 2 Specific surface area of biochars

生物炭类型裂解温度/℃比表面积/(m2·g-1)竹炭[15-16] 1 000517.28米糠等[17]70073.40~255.65鸡粪[18]500~75048.79~246.10木炭[19]700247玉米生物炭(CB)50016.98水稻生物炭(SB)50018.07沙柳生物炭(SWB)50040.06
2.4 吸附动力学
CB、SB和SWB对Pb2+和Cd2+的吸附量随时间的变化曲线见图3,可据此判断吸附剂对吸附质的吸附速度,进而得出吸附剂的吸附效率[6]。由图3可知,在吸附前8 h,3种生物炭对Pb2+和Cd2+吸附量均迅速增加,此后,随着吸附时间的增加,生物炭对Pb2+和Cd2+的吸附量增加,但吸附速率降低(如CB、SB和SWB在8 h时对Pb2+吸附量分别占其总吸附量的96.32%、94.26%和98.76%,对Cd2+的吸附量分别占总吸附量的91.31%、96.51%和91.35%),并且在24 h内均达到吸附平衡状态,说明生物炭对Pb2+和Cd2+的吸附过程出现“先快后慢”现象。这可能是由于吸附开始时吸附剂表面吸附位点较多(如生物炭表面含氧官能团—COOH、—OH等与重金属离子相互作用的吸附),不存在重金属离子之间的竞争作用;而吸附剂的吸附位点是有限的,随着吸附位点逐渐达到饱和,有效吸附位点逐渐减少,同时污染物浓度也在大幅降低,Pb2+和Cd2+需要扩散达到多孔介质内部,传质速率减慢,且竞争吸附作用越来越明显,此时,吸附速率取决于重金属离子从吸附剂外部进入内部位点的速度[21]。

图3 3种生物炭对Pb2+、Cd2+的吸附动力学拟合曲线Fig.3 Adsorption kinetic data and modeling of Pb2+ and Cd2+ on SWB, CB and SB
分别采用准一级动力学和准二级动力学模型对吸附动力学数据进行拟合,结果见表3。由表3可知,CB、SB和SWB对Pb2+、Cd2+的准二级吸附动力学方程模拟获得的决定系数R2均大于准一级动力学方程模拟获得的决定系数,且根据准一级动力学方程计算Pb2+和Cd2+的理论平衡吸附量Qe都与实际平衡吸附量相差较远,说明准二级动力学方程能够更好地描述3种生物炭对Pb2+、Cd2+的吸附过程,表明3种农林废弃物基生物炭对Pb2+和Cd2+的吸附过程主要受化学吸附的控制[22]。
表3 3种生物炭对Pb2+、Cd2+的吸附动力学参数
Table 3 Fitness of dynamics models for Pb2+and Cd2+sorption on biochar
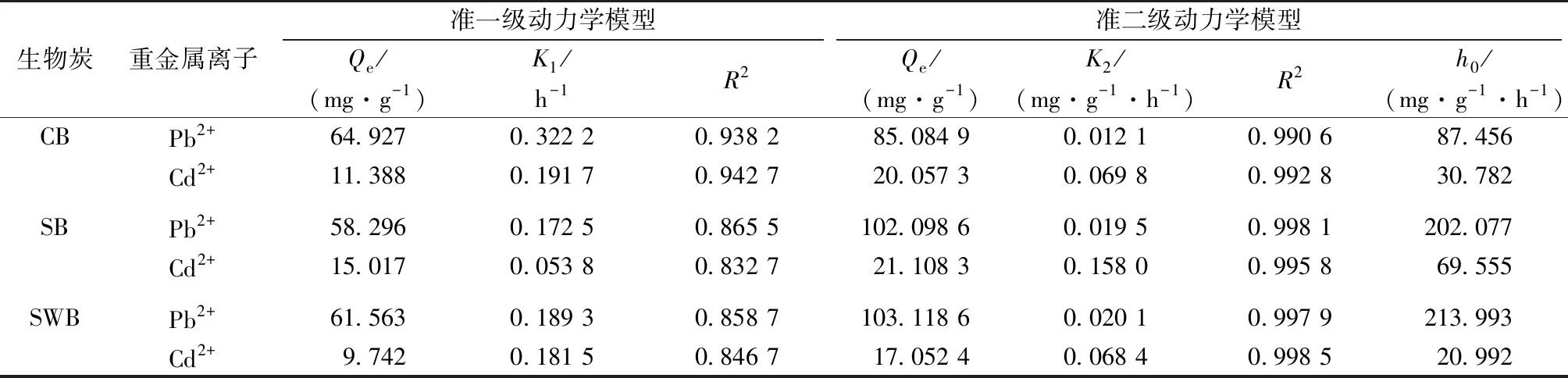
生物炭重金属离子准一级动力学模型准二级动力学模型Qe/(mg·g-1)K1/h-1R2Qe/(mg·g-1)K2/(mg·g-1·h-1)R2h0/(mg·g-1·h-1)CBPb2+64.9270.322 20.938 285.084 90.012 10.990 687.456Cd2+11.3880.191 70.942 720.057 30.069 80.992 830.782SBPb2+58.2960.172 50.865 5102.098 60.019 50.998 1202.077Cd2+15.0170.053 80.832 721.108 30.158 00.995 869.555SWBPb2+61.5630.189 30.858 7103.118 60.020 10.997 9213.993Cd2+9.7420.181 50.846 717.052 40.068 40.998 520.992
SB、CB和SWB分别为水稻生物炭、玉米生物炭和沙柳生物炭。Qe为平衡吸附量,K1为准一级速率常数,R2为决定系数,K2为准二级速率常数,h0为吸附的初始速率。
采用准二级动力学模型拟合得到的吸附速率常数K2可以反映吸附过程的快慢。动力学速率常数越大,表明吸附过程越快,达到平衡所需时间越短[8]。由表3可知,SWB对Pb2+的吸附速率(0.020 1 mg·g-1·h-1)比SB(0.019 5 mg·g-1·h-1)和CB(0.012 1 mg·g-1·h-1)快,而SB对Cd2+的吸附速率(0.158 0 mg·g-1·h-1)远高于SWB(0.068 4 mg · g-1· h-1)和CB(0.069 8 mg · g-1· h-1)。
2.5 吸附等温线
采用Langmuir和Freundlich等温吸附模型模拟生物炭对Pb2+和Cd2+的吸附等温线(图4),拟合参数见表4。就Pb2+而言,Langmuir等温吸附模型的R2明显高于Freundlich等温吸附模型,可以得出,Langmuir等温吸附模型能够更好地描述3种生物炭对Pb2+的等温吸附过程。同时,采用Langmuir模型计算出的饱和吸附量与实验得出的最大吸附量相近,表明生物炭对Pb2+的吸附近似单分子层吸附。而就Cd2+而言,Langmuir 等温吸附模型和Freundlich 等温吸附模型的R2均较高,说明其既符合Langmuir 等温吸附,又符合 Freundlich 等温吸附,Freundlich 模型描述的是多层吸附,在高浓度条件下吸附容量持续增加,常用于描述物理吸附[7]。笔者试验中,当ρ(Cd2+)初始值大于100 mg·L-1时,CB、SB和SWB对Cd2+的吸附量增加均趋于平缓,且Qe值大于Langmuir等温吸附模型拟合所得的Qm值,表明在高浓度条件下,3种生物炭对Cd2+的吸附存在多分子层吸附[5]。
由图4可知,这3种生物炭对Pb2+的吸附去除率显著高于Cd2+,这可能是由于Pb2+的水化热低于Cd2+的水化热[23],具有低水化热的Pb2+更易脱去络合水而成为暴露的Pb2+,易与生物炭内部阳离子发生交换反应而被吸附。另外,Pb(OH)2溶度积常数要低于Cd(OH)2,更容易形成沉淀,通过静电作用被生物炭吸附,从而降低溶液中剩余Pb2+浓度。同时,由于Pb2+电负性大于Cd2+,一般情况下电负性越大,重金属元素与生物炭表面或内部氧原子形成的共价键就越强[7]。由表4可知,就Langmuir模型而言,3种生物炭对Pb2+和Cd2+吸附的RL值(RL为无量纲参数分离因子:RL>1时,为不利吸附;0 图4 3种生物炭对Pb2+和Cd2+的吸附等温线Fig.4 Adsorption isotherms of Pb2+ and Cd2+ adsorption on biochars 表4 3种生物炭对Pb2+和Cd2+的等温吸附模型拟合参数 Table 4 Fitness of isotherm models for Pb2+and Cd2+sorption on biochar 吸附材料重金属离子Langmuir模型Freundlich模型Qm/(mg·g-1)KL/(L·mg-1)R2RLKF/(mg1-n·g-1·L-n)nR2玉米生物炭(CB)Pb2+85.7350.5740.964 20.008 6~0.148 429.2145.2570.871 2Cd2+20.5230.1160.951 30.041 3~0.462 94.9873.1890.987 1水稻生物炭(SB)Pb2+110.5120.6210.976 60.007 9~0.138 738.9545.2470.814 0Cd2+15.8870.1240.979 40.038 7~0.446 43.6253.3020.973 8沙柳生物炭(SWB)Pb2+105.0530.5860.970 40.008 5~0.145 835.1965.1840.895 2Cd2+29.4500.1010.959 50.047 2~0.497 55.2162.5440.975 2 Qm为最大吸附容量;KL为Langmuir平衡常数;R2为决定系数;RL为分离因子;KF为Freundlich常数;n为吸附程度常数。 在工业废水中存在浓度较高的Na+和Ca2+,这些阳离子的存在可能会对吸附材料吸附Pb2+、Cd2+产生影响[25]。图5显示,3种生物炭吸附Pb2+的效果随着溶液中离子强度的增强而降低,造成该现象的原因是Na+或Ca2+会和Pb2+发生竞争吸附作用,竞争吸附剂表面活性位点。此外,生物炭表面吸附Na+或Ca2+后会形成致密的水合壳进而阻碍Pb2+进入生物炭表面,导致生物炭对Pb2+吸附量降低,该结果也与XIAO等[26]的研究结果相符,即干扰离子强度的增加降低了生物炭对Pb2吸附量。 对Cd2+的吸附情况与Pb2+略有不同,由图5可知,虽然SWB对Pb2+的吸附效果随着离子强度的增强而降低,但对于Cd2+的吸附效果则是随着离子强度的增强而增大。由BET测试结果可知,SWB比表面积显著大于CB和SB,随着共存阳离子强度的增加,在其表面能够富集比CB和SB更多的正电荷,与Cd(OH)2形成络合物[27],使得络合作用强于离子交换[28],从而减小由竞争作用产生的吸附抑制效果,并增加Cd2+吸附量[24,29]。 图5 不同离子强度对3种生物炭吸附Pb2+和Cd2+的影响Fig.5 Effects of ionic strength on the sorption of Pb2+ and Cd2+ pH值对生物炭吸附Pb2+和Cd2+的影响见图6。由图6可知,溶液pH由3升至6时,生物炭对Pb2+和Cd2+的吸附效果随pH值的增加而升高。这主要是因为pH升高降低了溶液中H+浓度,而H+浓度过高时易与生物炭表面的含氧官能团结合,与重金属离子竞争吸附点位,降低其吸附效果,升高pH会提供更多的活性位点而提高生物炭吸附性能。此外,pH对生物炭的影响还表现在会导致生物炭表面ζ-电位的改变和酸性官能团的解离[30],且当pH较低时,生物炭表面带正电荷,会与重金属离子产生静电排斥,从而降低吸附效果。这与JIANG等[31]和PARK等[32]的研究结果类似。 (2)吸附动力学与吸附等温线模拟结果表明SB、CB和SWB对Pb2+和Cd2+的吸附更符合准二级动力学方程,说明3种生物炭对Pb2+和Cd2+的吸附速率主要由化学机制控制。对于Pb2+,Langmuir等温吸附模型的R2明显高于Freundlich等温吸附模型,表明生物炭对Pb2+的吸附近似单分子层吸附;而对于Cd2+,2种模型均能较好地模拟,随着Cd2+初始浓度的增大,出现Qe值大于Langmuir等温吸附模型拟合所得Qm值现象,说明在较高浓度条件下,Cd2+在生物炭上存在多分子层吸附。3种生物炭对Pb2+的吸附量显著高于Cd2+,可能是由于Pb2+水化热低于Cd2+水化热,并且Pb2+的电负性大于Cd2+。 图6 pH对3种生物炭吸附Pb2+和Cd2+的影响Fig.6 Effects of solution pH on the sorption of Pb2+ and Cd2+ (3)影响因素试验结果表明pH为5~6时,SB、CB和SWB对水溶液中Pb2+和Cd2+的吸附效果较好。随着背景溶液中离子强度的增大,3种生物炭对Pb2+的吸附效果减小,SB、CB对Cd2+的吸附受离子强度的影响效果类似。而SWB对Cd2+的吸附则随着离子强度增大而增大,这是由于离子强度增大改变了SWB表面电荷,使得络合吸附作用强于离子交换吸附作用,从而促进SWB对Cd2+的吸附。可见,500 ℃条件下制备的SWB对Cd2+具有较强的吸附能力,可作为吸附复合重金属Pb2+和Cd2+的优势材料之一。

2.6 共存阳离子对吸附效果的影响

2.7 pH对吸附效果的影响
3 结论


