以樟树籽仁油、油茶籽油、全氢化棕榈油为原料的起酥油基料油的表征
2020-01-16毛锦远马晓雨胡振瀛余宁翔朱雪梅
毛锦远,马晓雨,胡振瀛,余宁翔,朱雪梅,熊 华
(南昌大学 食品科学与技术国家重点实验室,南昌 330047)
起酥油作为一种可食用油部分替代猪油和奶油,加入到焙烤食品(馅饼皮和面包等)和其他预制食品中,能获得理想的口感和保质期的延长。在20世纪初,为了缓解起酥油基料油供不应求的现状,油脂氢化技术得到了大规模应用并同时促进了部分氢化植物油的使用[1]。然而,部分氢化技术可能导致反式脂肪酸(TFA)的形成。据报道,TFA的摄入可能对人类血脂有不良影响,最明显的是LDL和HDL比率的改变[2]。此外,起酥油带来脂肪的过量摄入,是造成超重和肥胖的主要原因[3],一种有效策略是用中链脂肪酸(MCFA)代替部分常规膳食中的长链脂肪酸(LCFA),因为其与普通植物油脂中LCFA的代谢途径不同,可以大幅减少人体脂肪沉积[4]。
樟树(Cinnamomumcamphora(L.)Presl)又名香樟、乌樟、芳樟、樟木等,是樟科(Lauraceae)樟属常绿高大乔木,产于我国东南及西南各地,江西是樟树资源总量最多的省份[5]。樟树籽仁油癸酸和月桂酸含量占90%以上,均匀分布在甘油三酯sn-1,2和3位上,不仅食用安全、无毒副作用,还具有抗动脉粥样硬化的功能[6],是天然的中碳链油脂资源。目前对樟树籽仁油的研究利用较少[7-9],将樟树籽仁油应用于起酥油的制备,可以拓宽樟树籽仁油的应用范围。
油茶籽油不饱和脂肪酸(USFA)含量高,在我国传统用于胃痛和烧伤的辅助治疗药物和高档烹饪油,在降低心血管疾病风险、增强免疫力、降低胆固醇水平、预防和治疗高血压以及预防某些癌症方面也具有显著效果[10]。全氢化棕榈油则具有高棕榈酸含量,其具有的天然β′结晶形式不仅提供了良好的通气能力,而且还有利于某些脂肪产品的熔融和结晶,因而被广泛应用于食品加工的各个领域[11]。
本研究采用樟树籽仁油、油茶籽油、全氢化棕榈油为原料,以不同的比例混合后在专一性脂肪酶Lipozyme TL IM的催化下进行sn-1,3位随机酯交换制备起酥油基料油,以物理混合物(PB)为对照,分析酯交换后产品(IP)的脂肪酸组成及熔点、多晶形式、微观结构、甘油三酯(TAG)组成等,以期获得带有能被快速吸收的中链脂肪酸(MCFA)的起酥油基料油,并为商业起酥油提供一定的理论和实践支持。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
樟树籽取自南昌大学校园,采用有机溶剂浸提得到樟树籽仁油(CCSO);油茶籽油(COO)、全氢化棕榈油(FHPO)分别购于江西天玉油脂有限公司和浙江望园科技有限公司;GLC-463脂肪酸甲酯混标(标准品)购于美国Sigma公司;正己烷(色谱纯)购于美国Tedia公司;其他试剂均为分析纯。
1.1.2 仪器与设备
Agilent6890B气相色谱仪、Agilent 1260高效液相色谱仪,美国Agilent公司;DSC1差示扫描量热仪,瑞士Mettler toledo集团;D1 system型多功能X射线衍射仪,英国BEDE公司;RHB1 S25型磁力搅拌器,德国IKA公司。
1.2 实验方法
1.2.1 起酥油基料油的制备
参考Zhao等[12]的方法,并做少量修改。按照一定的质量比(2∶2∶4, 2∶2∶5, 2∶2∶6, 2∶2∶7)分别称取CCSO、COO、FHPO于50 mL具塞锥形瓶中,反应体系油脂总质量为20 g。向反应体系加入2 g专一性脂肪酶Lipozyme TL IM,并在65℃下水浴磁力搅拌反应 8 h,搅拌转速为300 r/min。反应完成后,在4 200 r/min下离心4 min,除去酶并收集反应产物。向产物中加入正己烷、酚酞,用0.5 mol/L KOH的乙醇溶液滴定,待溶液粉红色30 s不褪色,加入温水洗涤至粉红色消失,静置,分层,将有机层通过无水硫酸钠除去水分,40℃下氮吹至正己烷完全挥发。
1.2.2 滑动熔点(SMP)的测定
根据 AOCS Official Method Cc 3-25方法测定滑动熔点。
1.2.3 脂肪酸组成的测定
甲酯化:取2 mg油样,加入1.5 mL正己烷、40 μL乙酸甲酯和100 μL NaOCH3/CH3OH溶液,37℃甲酯化20 min,然后在-18℃冷冻10 min,取出后迅速加入60 μL草酸,离心除去沉淀,过无水硫酸钠柱子,过0.44 μm滤膜,氮气吹干,加入1 mL正己烷,进行GC分析。GC分析条件:CP-Sil88熔融石英毛细管色谱柱;载气为H2,燃烧气为N2、H2和空气;进样口温度250℃;检测器温度250℃;柱内流速1.8 mL/min;程序升温过程为45℃保持4 min,以13℃/min升至175℃,保持27 min,再以4℃/min升至215℃,保持35 min,总测定时间86 min;进样量1 μL,不分流。通过与脂肪酸甲酯标准品对照进行定性,采用面积归一化法确定各脂肪酸的相对含量。
1.2.4 X射线衍射光谱分析
样品在70℃完全熔化后置于矩形塑料模具上,并在25℃下放置24 h,通过D1 system型多功能X射线衍射仪分析样品的晶型,在 25℃条件下,仪器配置铜靶管射线源(波长=1.541 8 Å),管压40 kV,管流40 mA,扫描角度2θ为32°~60°,扫描速度为2(°)/min。
1.2.5 油脂微观结构分析
将油样在70℃下熔化以破坏原有的晶体结构。向60℃预热的载玻片上滴加10 μL的油液,用经过同样预热处理的盖玻片小心地覆盖,保证玻片内不存在气泡且油脂厚度均匀。4℃下恒温放置24 h。油脂微观结构的观察采用尼康ECLIPSE Ti-U多端口倒置显微镜中配备的微分干涉(DIC)显微镜,放大倍数为400倍。
1.2.6 差示扫描热量分析及固体脂肪含量(SFC)计算
利用差示扫描热量仪分析样品的熔融曲线。称取6~10 mg样品置于铝盘中,盖上铝盖后置于DSC内,以空铝盘作为对照,进行分析。加热样品至80℃,保持10 min,再以10℃/min冷却至-60℃,保持10 min,后以5℃/min升温至80℃,得到样品的熔融曲线。每个样品做一次平行实验。通过熔融曲线分析得到油脂的SFC。
1.2.7 TAG组成测定
精确称取10 mg样品溶解在2 mL二氯甲烷中,经0.22 μm有机过滤膜过滤后,取10 μL滤液进行高效液相色谱检测,通过比较保留时间和碳当量数(ECN)鉴定TAG。液相色谱条件为:Nova-Pak C18色谱柱(150 mm×3.9 mm),70℃下操作的蒸发光散射检测器(Alltech 3300,USA),气体流速1.8 L/min,洗脱溶剂是正己烷-异丙醇(体积比1∶1)(溶剂A)和乙腈(溶剂B)的二元溶剂系统,洗脱液流速0.8 mL/ min,洗脱程序为0~10 min, 60% A; 20~50 min, 56% A; 50~60 min, 60% A; 60~70 min, 60% A。
1.2.8 统计分析
采用Origin 8.0软件绘图,所有数据结果均以“平均值±标准偏差”表示。使用IBM SPSS Statistics 19软件进行单因素方差分析(ANOVA)以确定差值的显著性。
2 结果与分析
2.1 样品的脂肪酸组成及滑动熔点(见表1、表2)

表1 CCSO、COO、FHPO、PB和IP的脂肪酸组成 %
由表1可知,所有样品中均未检测到TFA。CCSO中含有较多的MCFA(癸酸C10∶0, 46.56%;月桂酸C12∶0, 43.70%),高于椰子油中的MCFA(约为61.4%)[13],这与赵曼丽等[14]的研究结果一致。CCSO含有98.98%饱和脂肪酸(SFA),而COO中的不饱和(UFA)含量高达88.51%,主要为油酸(79.92%)。FHPO中含有99.99%的SFA,主要是棕榈酸(C16∶0, 60.58%)和硬脂酸(C18∶0, 37.22%)。IP中含有36.69%~45.35%的棕榈酸、21.79%~26.07%的硬脂酸、13.94%~21.82%的油酸,特别是IP中仍有12.21%~16.91%的MCFA(主要是癸酸和月桂酸)被保留。总体而言,IP在满足了所需合成目的的前提下,既保留了MCFA含量,利于吸收,又保证了LCFA提供的能量。对比相同混合比例条件下的PB,IP的C12∶0均存在显著性差异(p<0.05,p<0.01),MCFA含量无显著性差异,混合比例2∶2∶6和2∶2∶7的SFA和UFA含量存在显著性差异(p<0.05,p<0.01)。由表2可知,IP和PB的滑动熔点均随混合比例中FHPO的增大而升高,且相同混合比例下IP高于PB。

表2 PB和IP的滑动熔点 ℃
2.2 油脂的多晶形式和微观结构
图1为PB和IP的X射线衍射图谱。衍射强度在4.6 Å,表示β晶型;衍射强度在3.8、4.2 Å或者4.3 Å,表示β′晶型;衍射强度在4.15 Å,表示α晶型[15]。由图1可看出,4.02 Å仅在PB中出现,而IP则表现为单一的β′晶型,这可能归因于PB油脂结晶顺序不同,高熔点的FHPO先结晶,使油脂有利于形成β′晶型,但由于FHPO中脂肪酸链非常对称,比较稳定,在结晶时又倾向于β晶型,造成了4.02 Å峰型的存在,而酯交换反应则避免了这一问题。
从油脂的微观结构(图2)可以看出,PB的结构具有密集的不规则叶状晶体,并且许多团簇被拉伸(约55 μm),而在IP中观察到小的球状晶体(约20 μm),这些球状晶体可以在乳化阶段围绕在气泡周围且稳定气泡,并使其成为焙烤产品中的“小孔”,为烘焙产品提供光滑细腻的口感[16]。

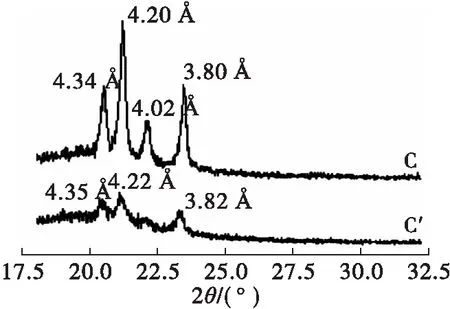

图2 PB(B)和IP(B′)的晶体微观结构
2.3 DSC熔融曲线(见图3)
从图3可以看出,PB出现的第一个熔化峰在12.6℃,这可能是物理混合的CCSO和COO协同作用的结果,在54.8℃出现了一个强峰,很明显这是底物FHPO的高熔点导致的。但是IP只在37.7℃产生了一个响应值相对较弱的峰,结合图2的微观结构可以说明已经合成了符合条件的起酥油。
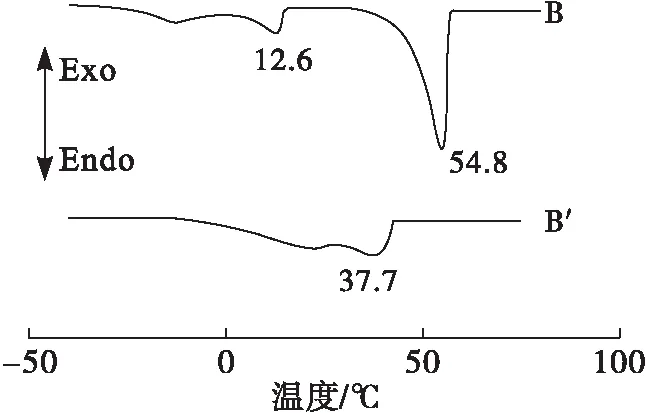
图3 PB(B)和IP(B′)的DSC熔融曲线
2.4 SFC曲线(见图4)
从图4可以看出,PB的SFC曲线在0~15℃下降,15~40℃趋于平缓,之后急剧下降,然而,IP显示的SFC曲线则一直呈现陡峭下降的趋势,具有狭窄的塑性范围,类似于商业烘焙起酥油中的高稳定性起酥油。此外,优质的起酥油在40℃需具备一定的SFC(6.97%~10.84%)以维持产品的塑性,使产品有一定的疏松度;而在55℃左右则需要完全熔化[17]。从图4可以看到,相较于PB,IP在40℃左右,3个比例(2∶2∶4, 2∶2∶5, 2∶2∶6)的SFC分别为5.2%、4.0%、7.7%,极大地降低了油脂的粗糙感和砂粒感。且4个比例的IP中在50℃就已经为0,与PB差异明显,是理想的高稳定起酥油基料油。
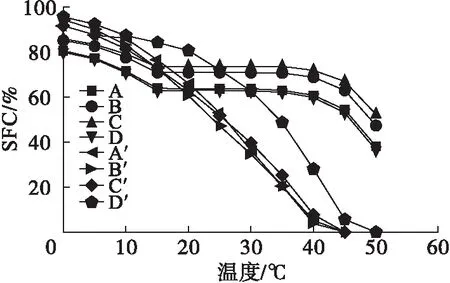
图4 不同比例PB和IP的SFC曲线
2.5 甘油三酯(TAG)组成(见表3)
从表3可以看出,PB中的PPO、PPP和PPS分别为21.83%、21.83%和30.54%,然而在IP中大幅减少到7.18%、ND和10.17%,值得一提的是,LaCC/CLaC在PB中高达19.48%,而在IP中未检测到,可能是TAG在酯交换反应过程中生成了新种类的TAG造成的,并且这些新产生的TAG会引起PB和IP之间一些物理特性(SMP,SFC等)的差异。酯交换之后,产生的不同且多种结构类型的TAG实现了一定理化特性(SMP,SFC等)和营养功能(MCFA,UFA)的起酥油的用途。
3 结 论
通过表征物理混合物(PB)和酯交换后产品(IP)的脂肪酸组成、熔点变化、多晶形式、TAG的组成发现,IP在满足了所需合成目的的前提下,既保留了MCFA (12.21%~16.91%)含量,利于吸收,又保证了LCFA提供的能量。微观结构上也表现为更小(约20 μm)的球状晶体形式,适合于起酥油的应用;从DSC熔融曲线发现,IP在37.7℃只产生了一个响应值较弱的峰形,SFC曲线则表现一直陡峭下降的趋势,具有狭窄的塑性范围,是理想的高稳定起酥油基料油。这些物理性质的变化,都是因为酯交换反应后甘油三酯结构发生了改变。
