牙型低磷酸酯酶症1例
2020-01-16赵增波王惠敏李晓娜李聪聪杨运田
赵增波 王惠敏 李晓娜 李聪聪 杨运田
低磷酸酯酶症(hypophosphatasia)为常染色体隐性遗传,发病率约为十万分之一[1]。牙型低磷酸酯酶症患者,临床多表现为乳牙提前脱落或严重龋坏,牙根牙骨质形成不全或发育不良,牙本质钙化不规则或牙髓腔扩大以及边缘牙槽骨的改变,其中牙根牙骨质形成不全或发育不良被认为是其主要表现,通常不伴有骨骼系统异常[2]。
一、病例资料
患儿,男,9 周岁,因乳牙较早脱落,恒牙长时间未萌来我科就诊。身体发育未见其他异常。足月顺产,母乳喂养,生长发育正常。否认家族史。体格检查:患儿营养发育正常,智力正常,语言及运动功能未见异常,未发现其他器质性病变。全身皮肤无过角化现象。专科检查发现:颜面部无畸形,颌骨发育正常,唇腭正常;口腔卫生良好,口腔粘膜及牙龈无异常,舌体活动自如;牙齿检查: 乳牙早失,15,16,21,25,31,32,34,35,36,41,42,45,46 萌出,釉质发育不全;21,31,32,41,42 切1/3 釉质明显的水平沟带,可探及牙本质层;15,25,34,35,36,45,46 牙冠缺少釉质覆盖,残留釉质坚硬粗糙,色泽棕黄色;16 牙面牙色充填物;余牙未萌出,21 反颌(图1)。实验室检查:生化检查ALP:12.0U/L(参考值86.00~315.00U/L);血清钙:2.69mmol/L(参考值2.11~2.52mmol/L);血清磷:2.12mmol/L(参考值0.85 ~1.51mmol / L); 甲状旁腺激素(PTH):15.40pg/ml(参考值15.00~68.30pg/ml);25-羟基维生素D(VitD-T):13.56ng/ml(参考值15-100ng/ml)。基因检测:NGS 基因检测报告为低碱性磷酸酶症相关基因ALPL 存在两处杂合突变(ALPLc.30dupA 杂合突变、ALPLc.931T>C 杂合突变)。影像学检查:全口曲面断层片显示恒牙及牙胚数目正常(16 髓腔及根管内高密度根充材料影像,26 近中倾斜阻生),釉质缺损影像,髓室及根管扩大,髓壁薄,牙根短,牙槽骨出现萎缩现象(图2)。股骨及胫腓骨片显示:未见特殊骨质改变。临床诊断:牙型低磷酸酯酶症。
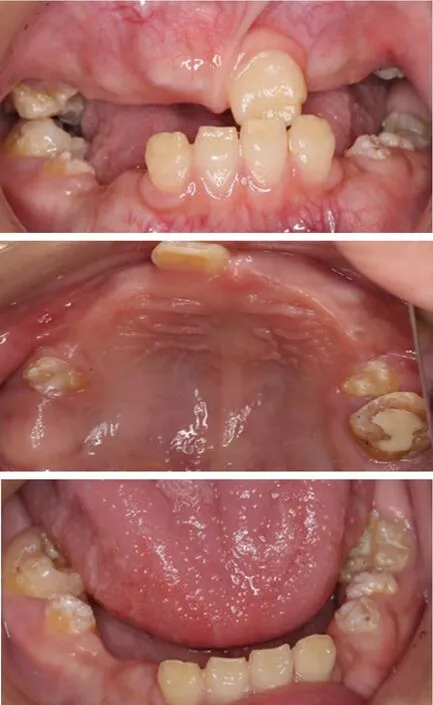
图1 初诊时口内照
二、讨论
基因分子检测表明,低磷酸酯酶症是一种常染色体隐性遗传病,其与组织非特异性碱性磷酸酶(TNAP)基因突变有关,如果位于1 号染色体短臂上的碱性磷酸酯酶基因(ALPL)中的一个核苷酸发生突变,就可能引发低磷酸酯酶症[3]。
根据该病发病年龄和有无涉及骨骼系统的变化,目前可以分为六型:围产型(先天型)、婴幼儿型、儿童型、成年型、牙型及假性低磷酸酶血症[4]。牙型低磷酸酯酶症只是该病的一种分型,本病例报道患儿未见骨骼系统异常,仅表现为牙齿早失,牙齿矿化受阻,牙釉质严重发育不全,冠髓腔及根管腔扩大,牙槽骨吸收萎缩。与以往报道不同的是该名患者牙釉质严重发育不全,可能与该病的基因位点突变后釉质矿化受阻有关,需要进一步检测。
目前对于该病无法根治多采用对症治疗,口腔的对症治疗包括口腔卫生指导,拔除松动严重的牙齿,牙周治疗等。全身治疗可以补充生长激素、维生素D 和钙剂或可减轻临床症状。另外移植有免疫应答能力的骨髓和间充质干细胞,可能对此类疾病有所帮助[5]。随着科学技术的发展,基因治疗在该病的治疗上也有了新进展,Seiko Yamamoto 等[6]通过基因治疗的方法明显改善了此病的临床症状,基因治疗为该病的彻底治疗提供了新方法。
