胃神经内分泌癌23例临床病理特点和诊治分析
2020-01-10张同方徐皓方心安
张同方,徐皓,方心安
作者单位:六安市人民医院(安徽医科大学附属六安医院)普外科,安徽 六安237005
胃神经内分泌癌(G-NEC)作为一种临床预后较差的少见病,是胃肠道神经内分泌肿瘤中恶性程度较高的一种[1],国内相关的大样本研究较少,因此临床上对G-NEC的认识不够,由于临床无特异性表现而容易被误诊,目前对G-NEC的诊断、临床病理特点、治疗、预后等尚没有统一的共识,本研究对23例G-NEC病人的临床表现、病理特征、免疫组织化学特征、治疗方式及其预后进行回顾形分析,探讨G-NEC的诊治经验,以期促进G-NEC的临床诊治规范,提高对该疾病的认识以及旨为G-NEC的诊治提供参考。
1 资料与方法
1.1 一般资料 调阅安徽医科大学附属六安医院普外科2011年3月至2018年3月收治的23例G-NEC病人的临床病理资料进行回顾性分析,其占我科同期收治胃癌病人的1.2%,其中男性16例,女性7例,年龄范围为42~79岁,中位年龄64岁,23例G-NEC术前均行电子胃镜检查,电子胃镜检查病理学检查结果提示:胃上部癌10例,胃中部癌6例,胃下部癌7例。
1.2 诊断和治疗 手术标本经10%中性福尔马林固定,主要途径是通过光镜观察形态特点以及免疫组织化学特异的神经内分泌标记,免疫组化采用EnVision法,使用标记的抗体CD56(神经细胞粘连分子)、Syn(突触素)和CgA(嗜铬蛋白),根治性切除被定义为无残留肿瘤状态(R0切除+R1切除),宏观残余肿瘤被定义为姑息性切除(R2切除)。
1.3 随访及分析方式 采用电话和门诊复查的方式对病人术后进行定期随访,生存时间是自手术时间至随访数据库截止时间(2018年3月),根据随访结果统计生存时间,病人生存时间按月计算。
1.4 统计学方法 数据处理应用SPSS 16.0软件,采用Kaplan-Meier法进行生存曲线绘制。
2 结果
2.1 临床特点 23例胃神经内分泌癌病人主要临床症状无特异性表现,和胃癌相似,伴有上腹隐痛不适者l3例(56.5%),吞咽困难5例(21.7%),反酸、嗳气2例(8.6%),贫血6例(26.1%),恶心、呕吐1例(4.3%),其他症状还包括纳差、乏力和消瘦等非特异性症状。查体可触及腹部肿块1例,余无明显腹部阳性体征,入院常规检查时发现11例病人合并有不同程度的低蛋白血症和贫血。CT影像学表现:其中2例表现病灶处胃壁呈不均匀增厚,伴有胃周及腹膜后淋巴结肿大,增强CT表现动脉期胃壁可见强化,行上消化道钡餐造影检查14例,提示局部病灶可伴有黏膜不同程度改变,病灶明显处有充盈缺损或龛影。
2.2 病理类型及特征 光镜下表现:肿瘤细胞大小不等、形态不一,具有明显的核异型性,核分裂数较高,核浆比例增大,肿瘤细胞排列呈巢片状,细胞小,细胞核深染,核分裂象多见(见图1),有的肿瘤细胞排列呈梁索状,细胞小,细胞核深染,核分裂象多见。23例G-NEC中,Syn阳性表达率82.6%(19例)(见图2),CgA阳性表达率65.2%(15例)(见图3),CD56阳性表达率73.9%(17例)(见图4),Syn、CgA和CD56三者联合检测阳性表达率100%;其中病灶:溃疡浸润型18例,肿块型5例,T分期:T1(1例),T2(2例),T3(2例)T4a(11例),T4b(7例),平均清扫淋巴结数目(17.5±1.9)个,其中14例合并有局部或淋巴结转移。
2.3 治疗情况 23例胃神经内分泌癌病人均行手术治疗,根据病人具体情况,病灶位于胃上部及中部者16例行全胃切除+食管空肠Roux-EN-Y术;病灶位于胃下部者7例行远端胃癌根治术,其中行全胃切除术+脾脏切除者1例,全胃切除术+胰体尾切除者1例,腹腔镜辅助胃癌根治术3例。其中R0切除者19例,R1切除者2例,姑息性切除者2例。有2例病人出现术后并发症,其中十二指肠残端瘘l例,肺部感染l例。根据病人术后病理分期及对化疗的耐受程度制定个体化化疗方案,术后有21例行常规化疗,方案为奥沙利铂(或多西他赛)联合氟尿嘧啶辅助化疗,疗程为6~8个周期,2例因个人原因未行化疗。
2.4 生存结果 至随访截止日,本组病人均获得随访,至随访结束存活9例,死亡14例,死因为肿瘤复发或广泛转移导致多脏器功能衰竭,随访生存时间为7~84个月,中位生存期为28个月,1、3、5年生存率分别为86.5%、37.9%、9.5%(见图5)。
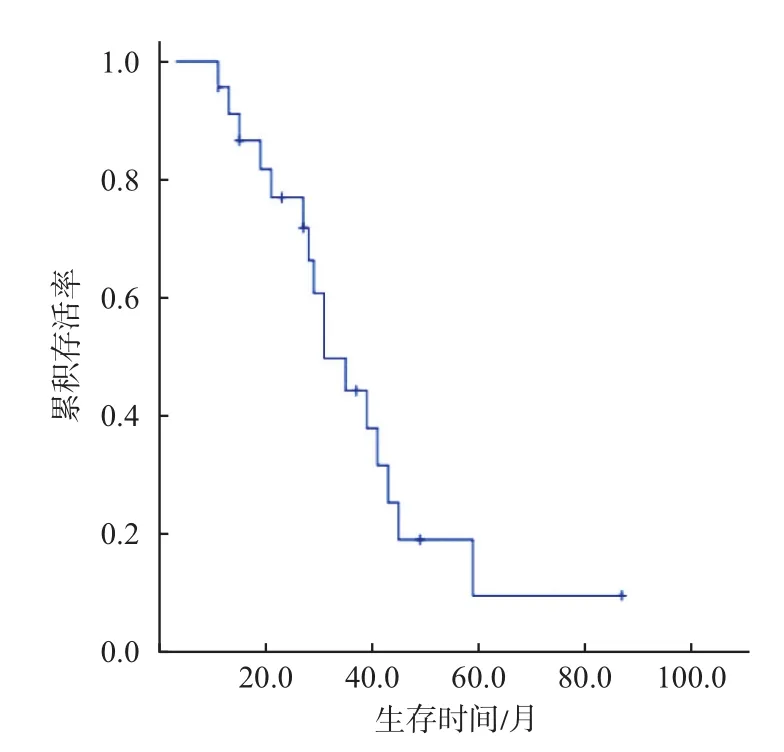
图5 胃神经内分泌癌23例的总生存曲线
3 讨论
神经内分泌肿瘤是以消化系统内分泌肿瘤最常见,其中0.6%~0.9%为胃神经内分癌[2-3],约占所有胃肿瘤的0.1%~0.6%[4],G-NEC是胃神经内分泌肿瘤中侵袭性强、预后较差的一种特殊病理分型[5],早期容易发生淋巴结和远处转移。本研究发现,我院G-NEC占同期胃癌发病率的1.2%,G-NEC发病率呈上升趋势[7],但由于缺乏特异性的临床表现,术前诊断率较低,目前我国乃至全球仍缺乏大样本G-NEC分析[8]。本组23例G-NEC病人中中位年龄64岁,其中男16例,女7例,在发病年龄、性别等结构构成上与报道的结果一致[9];有学者提出病人性别、年龄与病人预后无关[10-12],但有国内学者[6]提出性别是影响病人预后的独立因素,有研究显示肿瘤T分期越晚预后越差[13]。
G-NEC的临床表现复杂且缺乏特异性,G-NEC病人常见的临床表现为和胃癌常见临床类似,其临床表现与肿瘤的位置、大小等因素有关。本组23例G-NEC病人主要表现为上腹疼痛不适者l3例(56.5%),吞咽困难5例(21.7%),反酸、嗳气2例(8.6%),贫血1例,恶心、呕吐1例,其他症状还包括黑便和消瘦等非特异性症状。G-NEC术前常用的检查方法有电子胃镜、上消化道造影、CT等检查。电子胃镜是术前诊断的重要手段,上消化道造影检查可了解肿瘤的形态及位置,CT检查可判断肿瘤位置、大小、淋巴结转移、浸润等情况,对于判断肿瘤分期,确定手术方式和综合判断预后有很大的帮助,本组病人均行电子胃镜检查,术前诊断均为癌,但均未确诊为G-NEC,确诊最终需要术后病理形态学表现及免疫组化检查,本研究中Syn、CgA和CD56三者联合检测阳性率100%,联合检测将有助于提高确诊率,与报道[10,14-15]数据无明显差异。与胃腺癌相比,G-NEC淋巴结转移率更高,G-NEC根治术后的长期预后比胃腺癌更差[16],因此,足够的淋巴结清扫数目是G-NEC手术根治程度的重要指标之一,有超过半数的G-NEC病人伴有周围淋巴结或远处转移[17],本研究中有14例合并淋巴结转移,有研究提示脉管神经是否受累与G-NEC病人生存率及预后有关[10]。
外科根治性切除是G-NEC首选的治疗方法,一般遵循胃癌的治疗原则[18]。对G-NEC来说,手术是唯一可能治愈的手段[19]。手术方式与胃腺癌要求及标准相同,术中要仔细探查是否存在多发病灶。本研究中按照国内外相关指南和规约要求,所有病例均行手术治疗:根据病人具体情况,病灶位于胃上部及中部者16例行全胃切除+食管空肠Roux-ENY术;病灶位于胃下部者7例行远端胃癌根治术,2例行联合脏器切除,其中R0切除者19例,R1切除者2例,姑息性切除者2例。对于无法行根治性手术者或对于初诊已有远处转移的晚期G-NEC病人,不推荐行姑息性手术切除、减瘤术或细胞减灭术[20-21]。化疗是胃神经内分泌癌病人的重要治疗方法,文献报道对中晚期G-NEC病人行化疗可使病人获益的[15,22],但目前尚无统一标准的化疗治疗方案[23],本人认为可以根据病人术后病理分期、身体一般状况,家庭经济情况以及对化疗的耐受程度等制定个体化治疗方案,包括化疗、放疗、中医中药治疗、生物治疗及靶向治疗等。
综上所述,G-NEC是胃的一种特殊类型的恶性肿瘤,临床表现缺乏特异性,发病率及术前诊断率较低,术后病理学及分子学检查是G-NEC诊断的重要方法,G-NEC侵袭性强、分化差、恶性程度高,较易发生转移,且确诊时多进展期,故G-NEC总体预后较差[24-26],根治性切除手术切除是治疗的关键,术后应根据病人具体情况制定个体化治疗方案及进行多学科综合治疗。外科手术可使病人生存获益,手术是首选治疗方案,综合治疗在其治疗中起到重要作用[27-28]。
(本文图1~4见插图1-3)
