维持性血液透析患者发生心脑血管疾病的相关分析
2020-01-09孟美娟蔡婷孙铸兴
孟美娟 蔡婷 孙铸兴
慢性肾脏病的(chronic kidney disease,CKD)发病率逐步升高,已成为威胁国人健康的重要的公共卫生难题,王海燕教授发现我国普通人群中每十个人中就有一个人患者有肾脏病[1]。随着患者肾脏功能的进行性恶化,患者心脑血管事件的发生率逐步升高。心脑血管事件的死亡率占CKD 总死亡率的44%~51%,是CKD患者主要的死亡原因,更是MHD 患者首位死亡原因。维持性血液透析同时存在传统和非传统心血管危险因素,心脑血管事件的患病率远高于一般人群,维持性血液透析(maintain hemodialysis,MHD)患者血脑管事件的防治一直是临床医生治疗的重中之重。本研究分析MHD 患者心脑血管事件患病的现状,并探讨患者发生心脑血管疾病(cardio-cerebrovascular diseases,CVD)的危险因素。
1 资料与方法
1.1 一般资料
研究从2016年3月—2016年4月共纳入了42 名MHD 患者参加本研究,并对参加研究的患者持续三年的临床观察。文章主要对参与者基线的横截面数据进行分析,根据患者是否发生心脑血管意外分为两组,发生心脑血管意外的CVD组及未发生心脑血管意外的non-CVD组。在本研究中心脑血管事件包括心血管事件及脑血管意外。心血管事件主要包括急性心肌梗死、急性冠脉综合征,脑血管意外包括脑出血、脑梗死、短暂性脑缺血发作。CVD组包括6例患者,其中4 人发生心血管事件,2 人发生脑血管事件,其中男性4 名,患者的平均年龄为(63.67±7.53)岁;non-CVD组36 人,其中包括男性20 名,女性16 名,患者的平年龄为(53.44±12.83)岁;所有患者的平均年龄(54.90±12.67)岁,其中男性24 名,患者的平均透析年龄为(65.71±36.23)月;cfPWV 的平均值为(11.19±4.27)cm/s;血清总钙平均值为(2.35±0.24)mmol/L,血清无机磷平均值为(1.75±0.45)mmol/L,全段甲状旁腺素(iPTH)426.15(199.05~766.10)pg/ml。
纳入标准:(1)年龄为18~80 岁;(2)透析的时间超过三个月;(3)透析方案为4 h HD,一周三次;(4)临床评估患者达到干体重;(5)签署相关书面知情同意书。
排除标准为:(1)存在恶性高血压,SBP >180 mmHg,或者DBP >110 mmHg;(2)急性感染期;(3)急性心力衰竭;(4)中风的急性期;(5)失代偿肝硬化或恶性肿瘤;(6)淀粉样变性或扩张型心肌病;(7)颈内静脉置管患者等存在影响患者cfPWV 测定影响因素。
1.2 研究方法
参加本研究的所有患者详细记录病史及用药史,病史包括患者是否存在心脑血管意外、糖尿病及高血压病史;服药史主要包括他汀类药物、ACEI/ARB、EPO 等使用情况。
在本研究中,所有患者在一周中的非透析日完成cfPWV 测定;我们采用Complier(Aerotech Medical;Maris,France)分析仪完成cfPWV 检测,所有的操作均按照检测仪的使用说明书进行。因为MHD 患者存在血液透析这个规律的医疗行为,患者的透析时的血压并不能代表透析间期血压情况,动态血压更能真实准确地反应患者血压情况[2],因此在本项研究中我们同时记录了患者的24 h动态血压,本研究采用SpaceLabs 90217(SpaceLabs Medical Inc,Redmond,Washington,USA)来完成动态血压的监测,所有患者动态血压监测的时间相对固定,均在PWV 检测结束后开始,在下次透析开始前结束。动态血压监测仪器在白天(06:00—22:00)会每20 分钟测量一次血压,夜间(22:00—06:00)每半小时测量一次血压。
所有受试者在拆除动态血压后,我们在血液透析前自动静脉内瘘处采血完成相关实验室数据的监测,具体的监测项目包括血脂、白蛋白、血色素、快速反应蛋白、矿物质代谢的指标(血清总钙Ca、血清无机磷P、iPTH),由无锡市人民医院检验科完成所有数据检测。
1.3 评价方法
比较CVD 及non-CVD 两组患者患者组间区别,并探讨MHD患者发生CVD 的危险因素。
4 统计分析
我们采用SPSS 19 软件进行统计处理,正态分布的数值数据使用(平均数±标准差)表示,当数值变量变异性较大时使用中位数(四分位距)表示;组间差异通过t 检验或卡方检验完成,我们通过二元logistic 多因素回归分析研究患者发生CVD 的危险因素,P <0.05 具有统计学差异。
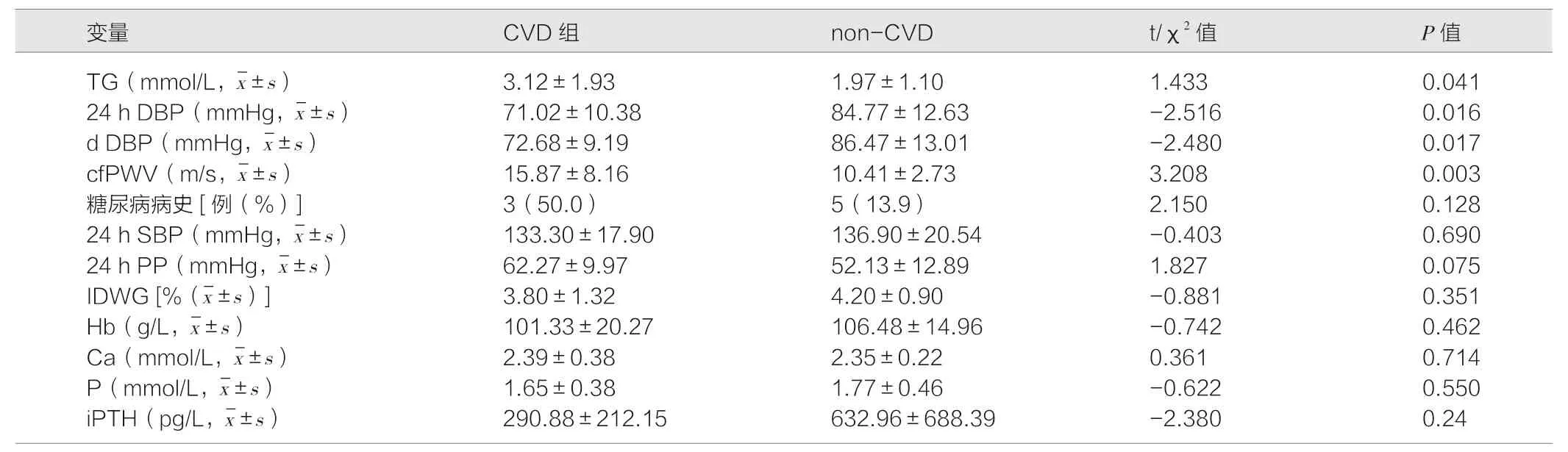
表1 比较CVD 及non-CVD 两组的组间区别
2 结果。
2.1 维持性血液透析患者心脑血管意外的现状
本研究中MHD 患者心脑血管事件的患病率14.29%,其中心血管事件的患病率为9.52%,脑血管事件的患病率为4.76%;均远高于一般人群。
2.2 比较CVD组及non-CVD组患者的临床数据的实验室检查的区别
本研究中,CVD组患者血脂(triglyceride,TG)、cfPWV 高于non-CVD组,而24 h 动态血压的舒张压(24 h DBP)、白天动态血压的舒张压(d DBP)低于non-CVD组,差异具有统计学意义(具体见表1),而两组患者糖尿病病史、收缩压、脉压差、高密度脂蛋白、低密度脂蛋白、胆固醇等传统危险因素无明显差异,ACEI/ARB、EPO 等药物服用情况无明显差异,透析间期体重增长(interdialysis weight gain,IDWG)等透析相关因素无差异。
2.3 MHD 患者发生CVD 危险因素
通过二元logistic 回归分析,我们将是否发生CVD 作为因变量,结合本研究中两组间差异及相关文献阅读,我们将TG、24 h SBP、24 h DBP、cfPWV、糖尿病病史、Ca、P、iPTH、24 h PP作为自变量,发现24 h DBP(B=-0.201,P=0.024)与MHD 患者CVD病史呈现负相关,而cfPWV(B=0.412,P=0.026)呈现正相关(详见表2),这提示过低舒张压及过高的cfPWV 可能会促进患者心脑血管事件的发生。
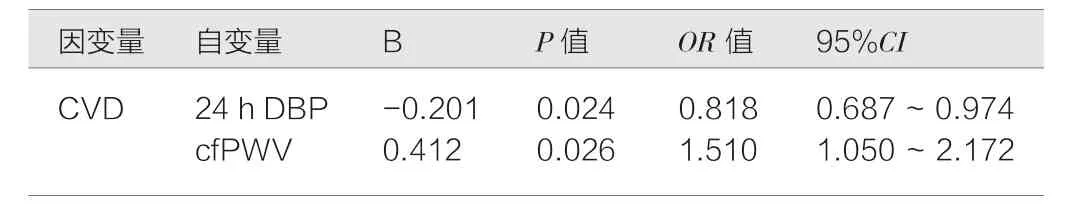
表2 MHD 患者发生CVD 危险因素
3 结论
心血管疾病发病率增高显著增加了慢性肾脏病患者的死亡率,且慢性肾脏病患心脑血管事件的患病率随肾功能减退进行性升高。除了传统危险因素外,MHD 患者存在矿物质代谢紊乱,IDWG 等特有的危险因素,多种因素共同作用于透析患者,导致MHD 患者CVD 事件发生率显著升高。MHD 患者发生CVD 事件的危险因素一直是研究热点。
MHD 患者血压波动较大,且受到血液透析活动的影响,透析间期血压与透析日血压水平存在差异,透析日血压不能取代ABPM 用于评估MHD 患者透析间期的血压水平[2]。近些年,多项高血压指南推荐使用动态血压监测作为诊断MHD 患者高血压的金标准[3-4]。然而在既往研究中,ABPM 与MHD 患者CVD 事件相关性研究很少,且结论差异较大[5-7]。本研究发现MHD 患者中发生CVD 患者的24 h DBP 及d DBP 均低于未发生CVD 患者,且多因素回归分析发现24 h DBP 与MHD 患者发生CVD 为负相关,这与ISAR 研究部分相符合[8],ISAR 研究发现SBP 和PP 与全因死亡率呈U 型非线性相关,SBP 是独立的风险预测因素,DBP 与患者全因死亡率呈负相关;但本研究中两组患者SBP及PP无明显差异。在本研究中,CVD组及non-CVD组的收缩压的平均值分别为(133.30±17.90)mmHg、(136.90±20.54)mmHg,患者血压控制在较合理范围,可能处于U 型非线性相关的平台处,因此未得到阳性结果。SBP及PP 与MHD 患者CVD 事件的相关性有待于进一步研究。
除24 h DBP 外,本研究同时发现cfPWV 与MHD 患者发生CVD 呈现正相关,这与既往研究相符合,在慢性肾脏病患者中,PWV 可以作为心脑血管事件发生的独立预测因子[9-10]。目前认为PWV 是检测患者发生动脉硬化的金标准;cfPWV 的测定是通过测量脉搏波在劲动脉及股动脉的传导时间和两个点间的距离求得。早在1999年Blacher 就研究发现动脉硬化其独立于年龄、病程、脉压、血脂等传统因素是MHD 患者致死性CVD 事件的独立危险因素[11]。本研究同时证明血管钙化是MHD 患者发生非致死性CVD 事件的独立危险因素。
矿物质代谢紊乱可造成血管钙化[12],从而导致MHD 患者CVD 发病率升高[13-14],高磷、高钙血症会显著增加MHD 患者致死性及非致死性CVD 发生,是患者死亡率的危险因素[15-18],然而在本研究中我们暂未发现MHD 患者CVD 与Ca、P、iPTH 的相关性的阳性结果,需考虑到本研究为横截面研究,排除了出现了致死性CVD 患者,且样本量较小,参加本研究患者的Ca、P、iPTH平均值在较合理范围,研究具有一定偏倚,有待于进一步随访观察矿物质代谢紊乱与MHD 患者心脑血管意外的相关性。
综上所述,本研究发现维持性血液透析患者CVD 的患病率高于一般人群,过低的舒张压及过高的cfPWV 促进患者心脑血管事件的发生。
