C.I. 荧光增白剂263的毒理学数据及其使用安全性(二)
2020-01-02董仲生
董仲生
(沈阳化工研究院,辽宁沈阳,110021)
(上接《中国洗涤用品工业》第10期第73页)
4.5 急性毒性-腹腔注射
(1)1972年用FWA 263进行了一项非-GLP研究[4],用剂量为100、250、500、1000mg/kg bw的FWA 263商品制剂(纯度约45%),每个剂量组15只雄性Wistar大鼠进行了腹腔注射实验,观察期14天。
结果:剂量mg/kg/死亡大鼠数量/ 有症状大鼠数量/大鼠数量

症状:给药30 min~7 days,全身状况明显降低。LD50>2500 mg/kg bw。
(2)1972年用FWA 263还进行了一项非-GLP研究[4],用剂量为100、250、500、 1000、1250、1500、1600、1700、1750、2000、2500 mg/kg bw的 FWA 263工业级(纯度100%),每个剂量组15只雄性Wistar大鼠进行了腹腔注射实验,观察期14天。
结果:剂量mg/kg/死亡大鼠数量/ 有症状大鼠数量/大鼠数量

症状:给药1~3天后有死亡发生。全身状况明显降低,镇静、呼吸困难。LD50>1725 mg/kg bw。
4.6 眼睛刺激
(1)兔子(性别和品系不详) 被施用50mg三种不同剂型的FWA 263:钠/钾盐的液状剂型,大约28%的无水酸工业品;(纯度100%)工业品;大约45%的FWA 263四钠盐。FWA 263被用于兔子眼睛,使用方式不详。只有FWA 263液状剂型的引起眼结膜的轻微变红。
结果:在该实验中FWA 263四钠盐对兔子的眼睛没有刺激[5]。
(2)Kimmerle、Thyssen和Bayer公司分别于1972年、1974年和1975年,用 FWA 263(100%的FWA 263及含有切削剂和液体配方的制品)对兔子眼睛的刺激性进行了实验[3],结果:FWA 263对兔子眼睛没有刺激作用。
(3)1972年用FWA 263进行了一项非-GLP 研究[4],用2只兔子,单一剂量的 FWA 263为50mg/kg bw。结果:FWA 263对兔子眼睛无刺激性。
(4)1975年用FWA 263进行了一项非-GLP 研究[4],用没有稀释的 FWA 263液体制剂处理2只兔子的眼睛。结果:在施用1h后兔子眼睛轻微变红。
(5)1986年根据OECD准则405 (急性眼刺激性/腐蚀性)和GLP,用雌、雄性新西兰白兔各3只,将FWA 263 0.1g放入兔子的右眼睛中,左眼不处理用于对照。在1、24、48和72h对眼刺激进行了评估[1]。
结果:在处理1h后,观察到一只被处理的眼睛角膜表面的正常光泽消光,随后没有观察到这只眼睛的角膜混浊。在整个研究阶段其他被处理的眼睛角膜表现正常。
在处理1h后两只处理的眼睛发现虹膜炎,同时其他被处理的眼睛虹膜表现正常。在24、48和72h没有观察到虹膜炎症,结果见表4。
在处理后的1和24h观察到所有处理的眼睛出现结膜炎,在48和72h正常。
结论:在施用FWA 263后,在24、48和72h计算得分平均值,所有动物角膜不透明性<1分,虹膜炎<1分,结膜变红和水肿<2。该物质不满足被分类为眼睛刺激的标准
因此,根据CLP法规(EC 1272/2008), 该物质可以被分类为无刺激。
4.7 皮肤刺激/致敏
(1)1972年拜耳公司对14只豚鼠进行的皮内实验[4]表明,FWA 263(100%纯度)不是致敏剂。
(2)1972年进行了一项非-GLP研究[4],用FWA 263含量约为45%的商品制剂,用2只兔子的内耳分别进行了24h的半封闭斑贴实验。结果显示:对兔子的皮肤无刺激。
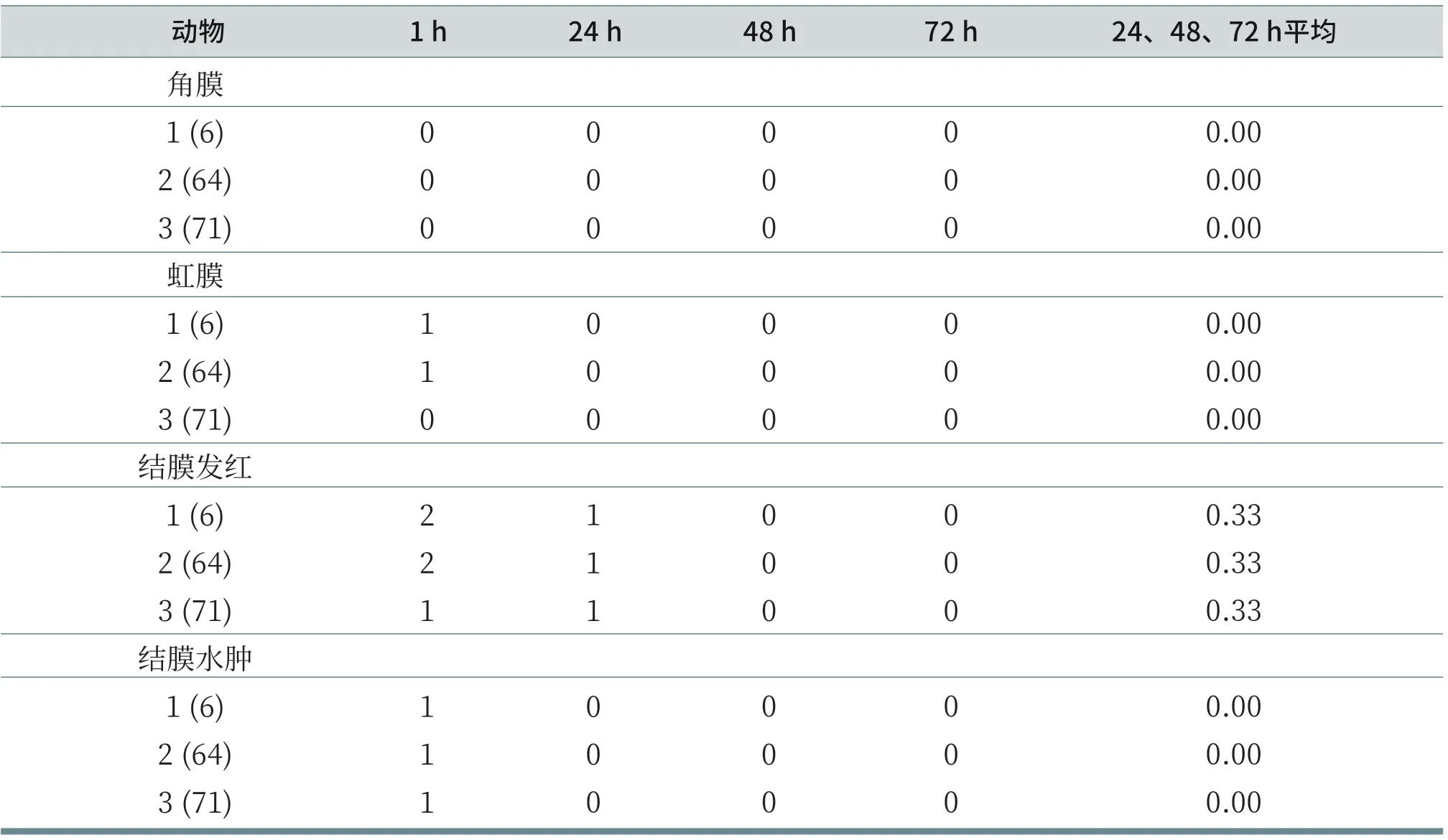
表4 兔子眼睛给药后的反应和评估得分
(3)1975年进行了一项非-GLP 研究[4],用FWA 263的液体制剂,对4只兔子的内耳分别进行了4~24h的半封闭斑贴实验。结果显示:对兔子的皮肤无刺激。
(4)用豚鼠(5只雄性、9只雌性,品系不详)经最初皮内注射0.05mL0.1%的FWA 263四钠盐生理盐水悬浮液之后,进行9次附加的0.1mL悬浮液诱导注射,观察FWA 263四钠盐的致敏情况。在最后诱导注射14天以后,用0.5mL的悬浮液激发。结果显示:没有发现不良反应。在该实验中FWA 263四钠盐对豚鼠不致敏[5]。
4.8 经口-重复剂量毒性
(1)1972年拜耳公司进行了一项亚慢性重复剂量毒性实验[5],Wistar大鼠 (15只/性别/剂量) 经口灌胃剂量为30、100和300 mg/kg-bw/day 的FWA 263四钠盐(纯度100%)13周。
结果显示:没有发现死亡和临床症状。与对照相比,在体重、组织病理学参数、临床化学或尿分析上没有差别。尸检显示没有肉眼可见的不良发现,器官重量也无改变。无可见有害作用水平NOAEL = 300 mg/kg-bw/day (最高实验剂量)。
(2)1991年根据OECD指南407(啮齿动物重复-剂量28-天经口毒性)和欧洲方法B.7重复-剂量(28-天)毒性(口服)以及GLP,用标称剂量0,50,200,1000 mg/kg-bw/day 的FWA 263口服灌胃 Wistar 大鼠(0、1000剂量组雌、雄性各10只;50、200剂量组雌、雄性各5只)每天一次,共计28天,然后给予14天无给药的恢复期[1],同时进行对照实验。
结果显示:在研究期和恢复期均未观察到与处理相关的临床表现。在尸检前无过早死亡发生。在食物消费量(绝对/相对)和器官重量(相对)方面观察到的各种统计差异(增加/减少)被认为与毒理学无相关性,因此,没有任何证据证明FWA 263在任何剂量水平上的毒性,NOAEL=1000mg/kg bw/day (标称)。
4.9 遗传毒性
4.9.1 基因突变
(1)1982年根据Green等人的平板渗入方法并按照GLP,使用大肠杆菌E. coli WP2 uvrA测定了FWA 263的潜在基因突变活性。在有和无肝脏微粒体活化(S9-混合物)的情况下,以8种浓度1.58、5、15.8、50、158、500、1580和5000μg/plate对FWA 263进行了3平行实验,同时进行对照实验。
结果显示:在所述细菌诱变性实验中,在有或无S9-混合物的情况下,未观察到实验物质的毒性作用,FWA 263没有显示潜在基因突变活性的迹象。
(2)1989年根据OECD 准则 471(细菌回复突变实验)和GLP,用菌株:S. typhimurium(鼠伤寒沙门氏菌)TA 1535、TA 1537、TA 1538,TA 98和TA 100 在有和无代谢活化作用下,以FWA 263浓度0、40、200、1000、5000 μg/plate进行了实验。同时进行对照实验。
结果:鼠伤寒沙门氏菌在有和无代谢活化作用下其遗传毒性均为阴性。
(3)1991年的一份报告介绍,根据OECD准则471 (细菌回复突变实验)和GLP,用菌株:TA 1535、TA 1537、TA 1538、TA 98和TA 100在有和无代谢活化系统存在下,FWA 263以浓度实验.I:10.0、100.0、333.3、1000.0和5000.0 μg/plate和实验II:100.0、333.3、1000.0、2500.0和5000.0 μg/plate进行细菌体外基因突变研究,同时进行对照实验。
结果显示:菌株有和无新陈代谢活化作用下均无遗传毒性。在所述诱变性实验期间以及在所报告的实验条件下,FWA 263并未通过所用菌株基因组中的碱基对变化或移码来诱导点突变。
(4)1998年根据OECD 准则 471(细菌回复突变实验)和GLP,用菌株:S. typhimurium TA 1535、TA 1537、TA 98和TA 100和菌株:E. coli WP2 uvr A进行了一项细菌体外基因突变研究。代谢活化系统为苯巴比妥和β-萘酚黄酮诱导的大鼠肝微粒体(S9)。FWA 263浓度为33、100、333、1000、2500和5000 μg/plate。同时进行对照实验[1]。
结果显示:鼠伤寒沙门氏菌以及菌株以及大肠杆菌株在有和无新陈代谢活化作用下,其遗传毒性都为阴性。
4.9.2 染色体畸变
4.9.2.1 体外
(1)1989年根据OECD准则475(哺乳动物骨髓染色体畸变)、OECD准则473 (体外哺乳动物染色体畸变实验)以及GLP,中国地鼠卵巢细胞(CHO)在有和无代谢活化作用下,使用FWA 263浓度:1000、2000、3000、4000和5000 μg/mL(无代谢活化物)和2000、3000、4000和5000μg/mL(有代谢活化物)进行了体外细胞染色体畸变实验,同时进行对照实验[1]。
结果显示:FWA 263在中国仓鼠卵巢细胞中没有引起染色体畸变,对中国仓鼠卵巢细胞在有和无新陈代谢活化作用下均无遗传毒性。
(2)1991年的一份报告显示,根据OECD准则473和GLP,中国仓鼠肺成纤维细胞(V79)在有和无代谢活化作用下,使用FWA 263浓度:10 μg/mL (18h有和无S-9混合物);100 μg/ml (18h有和无S-9混合物);150 μg/mL (7、18和28h 有和无S-9 混合物)进行了哺乳动物细胞的体外细胞遗传性/染色体畸变研究,同时进行对照实验。
结果显示:在实验条件下,FWA 263在V79中国仓鼠细胞系中没有引起结构染色体畸变,对中国仓鼠肺成纤维细胞(V79)在有和无新陈代谢活化作用均无遗传毒性。
(3)1991年的另一项实验介绍,根据OECD准则473和EU方法B.10 (体外哺乳动物染色体畸变实验)以及GLP,中国仓鼠肺成纤维细胞(V79)在有和无代谢活化作用下,使用FWA 263浓度:
实验 I (有和无S9 混合物)

实验 II (有 S9 混合物)

进行了哺乳动物细胞的体外细胞遗传性/染色体畸变研究。同时进行对照实验。
结果显示:FWA 263在V79中国仓鼠细胞系中没有引起结构染色体畸变,FWA 263对中国仓鼠肺成纤维细胞(V79)在有和无新陈代谢活化作用下均无遗传毒性。
4.9.2.2 体内
(1)1977年根据OECD准则478 (遗传毒性: 啮齿动物显性致死实验),用NMRI小鼠,FWA 263单一剂量为5000mg/kg bw,50只雄性一次口服灌胃处理,250只雌性未处理。同时进行对照实验,研究染色体畸变。
结果显示:没有动物死亡。雄性动物的繁殖力未受FWA 263影响。无与物质相关的植入后损失,也未发现FWA 263对每个雌性植入率、活植入率和死植入率产生影响。FWA 263不会诱发生殖细胞染色体畸变所致胚胎或胎儿死亡的遗传毒性。
(2)为了研究FWA 263在小鼠骨髓细胞中的嗜多染红细胞诱导(引起)微核的潜能,1990年根据OECD 准则474(哺乳动物红血细胞微核实验)和GLP,用FWA 263单一剂量5000 mg/kg bw对雌、雄性NMRI小鼠各5只口服灌胃进行了实验[1],同时进行对照实验。施药后的24h、48h和72h采集骨髓细胞用于微核分析。
结果显示:施用FWA 263处理后,与阴性对照相比嗜多染红细胞(PCEs)和正染红细胞(NCEs)的比值不受影响,这表明无细胞毒性作用。与阴性对照比较,在施用FWA 263后的任何制备间隔,检测到的微核发生率都没有明显的增加。表明FWA 263不能引起(诱导)微核,结果见表5。
(3)1995年根据OECD 准则478和GLP,用50只NMRI雄性小鼠,口服FWA 263剂量2500和5000 mg/kg,同时进行对照实验,研究了FWA 263的毒性[1]。
结果显示:雄性小鼠急性经口给药后没有症状,它们的外观和身体活动未受影响,表现正常。给药后的雄性受精率没有影响,因此FWA 263不会引起植入前损失增加。此外,结果显示:FWA 263对植入后损失没有影响,没有诱导致死性,致突变作用的迹象,遗传毒性为阴性。
4.10 致癌性
(1) 1979的一份报告介绍,用FWA 263剂量0.5μg/cm2对雌雄性各50只Skh无毛小鼠皮肤2cm×3cm的面积进行致癌性实验。暴露时间为320天,每周3次(1、3、5),在施用FWA 263 1h后开始紫外光照射。同时进行对照实验。
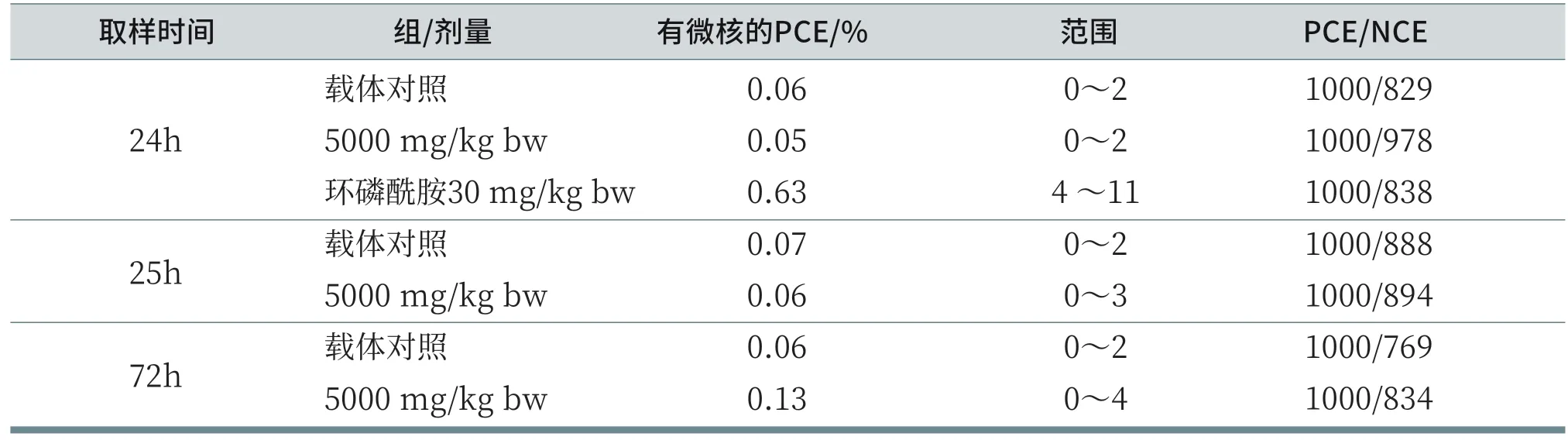
表5 小鼠骨髓细胞微核实验
结果显示:所有动物的体重变化正常。死亡率在各组间无显著性差异,所有组均发现红斑和坏死。皮肤肿瘤各组间无显著性差异。
结论:紫外线诱导,FWA 263不会引起致癌性。
4.11 生殖毒性
(1)2000年根据美国环境保护署(EPA)的EPA OPPTS 870.3800(繁殖和生育率影响)实验方法,Crj: CD(SD)大鼠(26只/性别/组)经口灌胃剂量为0、100、300、1000 mg/kg bw/day的FWA 263。双亲(P)代在交配前10周直到安乐死。F1和F2代后代在子宫中和在哺乳期与FWA 263接触。选择组成F1亲本组的F1后代在交配前(开始于年龄≥28天)暴露于FWA 263≥70天,直到安乐死。暴露频率为每日一次。同时进行对照实验[1]。
结果显示:在双亲大鼠中,唯一与处理相关的影响是雌性大鼠的绝对和相对肾重量的增加。双亲中的雄性在1000 mg/kg bw/day没有发现与处理相关的影响。在P或F1双亲中没有发现生育参数受到与处理相关的影响。在F1和F2 后代的发育或成长中没有发现不良的、与处理相关的改变。


(2)1999-2000年根据OECD准则421(繁殖/发育毒性筛选实验)和GLP,用Sprague-Oawley大鼠进行了一-代生殖毒性研究。在该项研究中,评估了FWA 263对大鼠的繁殖毒性剂量水平。5组,每组每个性别10只动物经口灌胃,FWA 263剂量水平为0、30、100、300和1000 mg/kg/day。同时进行对照实验。
暴露持续时间:在交配前给雄性和雌性大鼠施用FWA 263至少28天,雄性继续给药直到交配期结束(直到尸检前一天)。雌性在交配期和妊娠期继续接受给药,直到哺乳期的第3天。
结果显示:成年大鼠在交配前、交配后、怀孕期或哺乳期,所有的亲本动物存活到预计的安乐死,而且没有观察到与FWA 263相关的临床发现。
与对照比较,来自于处理组的成年动物在体重、体重增加、或食物消耗没有观察到具有统计学意义或与FWA 263相关的变化。在亲本动物尸检时没有发现异常。施用FWA 263对死亡率没有影响。
处理组和对照组比较,交配、死亡率和繁殖力指标相似。
雌性生育窝仔和活胎或死胎数量、怀孕期、或怀孕指数没有与FWA 263相关的变化。在第0天幼崽/窝仔、活胎和死胎和存活到第4天的数量,在对照和处理组之间是相似的。
与对照组相比,没有观察到FWA 263对幼崽成长(体重增加)或外部发现相关的影响。

4.12 发育毒性
(1)1998-1999年根据EPA OPPTS 870.3700(产前发育毒性研究)和GLP,用新西兰白兔和剂量为100、400和 800mg/kg bw的FWA 263,对它的发育毒性包括致畸性进行了评价[1]。给药持续时间从孕第7天到第28天。每个剂量每组25只雌性,每日给药一次。雌性兔子按照时间接受交配。同时进行对照实验。
结果显示:在800mg/kg/day观察到死亡,在体重增加和食物消耗的统计学意义上的明显降低以及流产增加作为过度的母体毒性的证据。因此,该组在研究进行完之前被终止。在400mg/kg/day观察到较轻的母体毒性。
来自于800 mg/kg/day组的共8只兔子在孕期死亡,并且另一高剂量组母兔在极端情况下被安乐死。研究期间来自于高剂量组的另7只母兔流产。在100或400mg/kg/day组没有观察到与处理相关的死亡。
在400mg/kg/day观察到的与处理相关的临床发现,包括软便和变色的粪便。在100或400mg/kg/day没有观察到体重、体重增加或食物消耗的变化。
来自于800mg/kg/day组的母兔尸检结果发现,包括肝变色、胃水肿/或变色、肠子变红和/或水肿、肠子中血红的和/或黏液状的内容物。在尸检时,在400mg/kg/day组流产的兔子有胃水肿和液体的、血红色的肠子内容物,也被认为是与处理相关。从800mg/kg/day组处理以前的三窝仔收集的胎儿检查数据像是在各自的表格中,但是在该报告中没有被总结、统计分析或讨论。在100或400mg/kg/day组没有观察到对子宫参数的影响。
黄体、着床、活和死胎以及在吸收数量在载体对照和100和400mg/kg/day组之间是相似的。
当与载体对照组比较时,400mg/kg/day组的胎儿体重在统计学上是较低的。
基于母兔在400mg/kg/day组与处理相关的临床观察和时间发现,在该研究中母体影响的无观察效应水平(NOEL)是100mg/kg/day,是最低的实验剂量。在400mg/kg/day组胎儿体重有统计学意义上的降低。这些变化可能是从属于在该研究中观察到的母体毒性,被认为不是发育毒性的迹象。

胎儿: 胚胎毒性/ 致畸形性影响:无影响。
(2)1999年根据EPA OPPTS 870.3700 (产前发育毒性影响)和GLP,用大鼠和剂量为100、400和1000mg/kg bw的FWA 263,对FWA 263的发育毒性包括致畸性进行了评价。经口给药持续时间从孕第6天到第19天。每个剂量每组动物数30只雌性。每日给药一次。同时进行对照实验。
结果显示:由于在妊娠第6天至第19天期间大鼠给药未观察到对母体或胎儿的不良影响,因此,本研究的结果表明:FWA 263对大鼠无致畸作用。
NOEL(母体毒性)=1000mg/kg bw;
NOEL(发育毒性)=1000mg/kg bw。
4.13 人类致敏实验
(1)1972年进行了一项由10名志愿者参与的人类重复伤害斑贴实验[3],目的是测试FWA 263(工业品,纯度100%)对人类皮肤致敏性,给药路径是经皮封闭斑贴。每周暴露两次,共5周,暴露时间为24小时,在周六用相同的浓度在另一应用区域激发。
结果显示:10名志愿者都不致敏。
(2)1972年8名志愿者用FWA 263商品含量约45%的钠盐进行半封闭实验,暴露期为7天。结果无刺激[3]。
(3)1973年进行了一项由78名男女性志愿者参与的人类重复伤害斑贴实验[10]。目的是测试FWA 263对人类皮肤致敏性,给药路径是经皮封闭斑贴。0.35%洗涤剂混合物水溶液中含有24%的该FWA 263,以及分别含有0.7%和16%的其他荧光增白剂。
结果显示:所有78名志愿者的结果都是阴性。
5人接触FWA 263的途径及其衍生无影响水平
工人和普通人群有可能接触FWA 263的途径和其衍生无影响水平(DNEL)[1]见下表6。FWA 263的衍生无影响水平是这样一种暴露(接触)水平,人类不应暴露在此水平之上。换句话说,在DNEL以下人类接触FWA 263是安全的。
由于人们对健康和环保意识的加强,从目前的FWA 263生产和应用情况看,工人和普通人群不可能长期接触到DNEL这样高浓度或剂量的FWA 263,因此,人们不必担心FWA 263会带来健康危害。
6 FWA 263安全性评价——持久性、生物累积性和毒性评估结论[1]
6.1 持久性或高持久性(即P或vP)的证据及评估
筛选标准基于REACH 的附录XIII(为确认持久性、生物累积性和毒性物质及高持久性和高生物累积性物质的标准)和在淡水或河口水中的半衰期T1/2≤ 40天[1]。
在标准的生物降解实验中,该物质既不易也非固有的可生物降解。然而,该物质可直接光解,在自然光下湖泊和河流的透光层中光降解速度快。在晴朗的夏天,在接近于天然水的表面FWA 263的半衰期大约为4~5h。其他过程如生物降解和水解不能使该物质以良好的速度降解。吸附将把FWA 263部分地带到悬浮颗粒的表面,而且也将有助于物质吸附到沉积物里。因此,认为FWA 263为潜在的持久性物质,结论为持久性而非高持久性物质(即P 而非vP)。
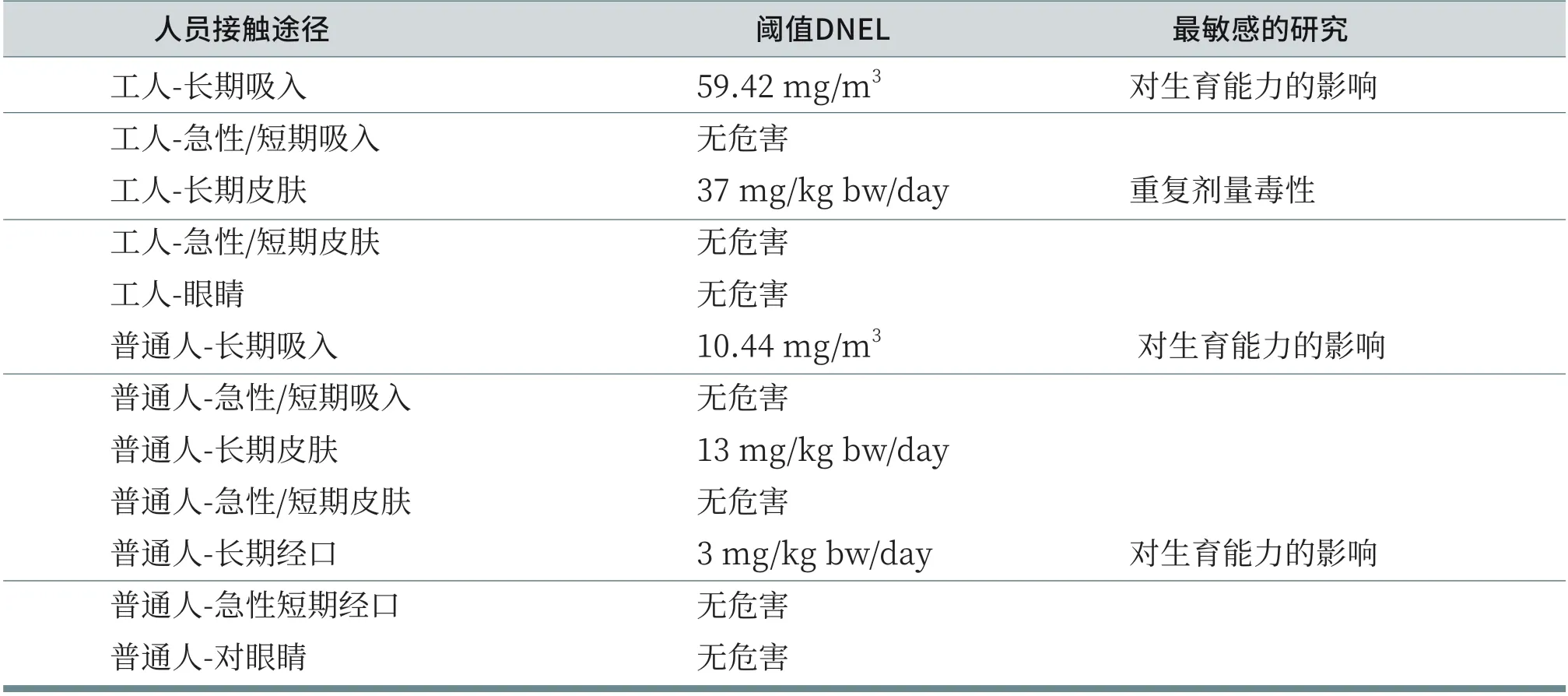
表6 人接触FWA 263的途径以及DNEL
6.2 生物累积(B或vB)的证据及评估
由于该物质的辛醇-水分配系数log Kow为-13.14~-1.58,所以,它没有生物累积潜能。而且实验测试了FWA 263以及类似的荧光增白剂CAS 16090-02-1在鱼体中的生物累积[6],在暴露水平高达1mg/L的所有鱼毒性实验中,只有微量浓度(小于0.05mg/kg)的FWA 263存在于鱼中,在大多数情况下,没有发现可测量的FWA 263。
又基于筛选标准辛醇-水分配系数log Kow≤4.5为非累积性和非高累积性物质(非B和非 vB),而该物质的log Kow=-13.14~-1.58,比筛选标准B的阈值低很多。因此,认为FWA 263为非累积性和非高累积性物质(即非B 和非vB)。
另据REACH法规附件XIII中标准BCF≤2000L/kg为非B和非vB。根据该物质的BCF[11]=3.16L/kg wet-wt,认为FWA 263是非B和非vB。
6.3 毒性证据以及评估
标准基于REACH的附录XIII,非毒性物质(即非-T)基于:对于海洋/淡水有机物(长期毒性)EC10 或 NOEC≥0.01mg/L。FWA 263的NOEC(21d)大型蚤=6.59mg/L,所以FWA 263为非毒性物质(即非-T)。
又根据指令67/548/EEC(危险品分类和标签),该物质没有被归类为致癌物(1或2类)、致突变物(1或2类)或生殖毒物(1、2或3类)。或根据法规EC No1272/2008(物质和混合物分类、标签和包装的法规)该物质没有被分类为致癌物(1A或1B类)、生殖细胞诱变物(1A 或1B类)或生殖毒物(1A、1B或2类)。所以FWA 263既没有被分类为有环境毒性也没被分类为致癌、致畸、致生殖毒性物质(即CMR)。

又根据指令67/548/EEC,该物质没有其他的慢性毒性证据被分类为T、R48或Xn、R48(即T-有毒物质, 或Xn-有害物质、R48-长期接触有严重损害健康的危险);或根据EC No 1272/2008,该物质没有其他的证据存在重复暴露之后特殊的靶器官毒性(1或2类)。所以,FWA 263既没有被分类为有环境毒性也没被分类为T、R48或 Xn、R48。
由此可见,FWA 263对哺乳动物和水生生物没有毒性。该物质既不能被分类为环境毒物也不能被分类为CMR(致癌、致畸、致生殖毒性物质)或T(有毒物质), R48(长期接触有严重损害健康的危险)或Xn(有害物质)。由此可得出结论:FWA 263没有毒性。
总之,FWA 263不是PBT/vPvB物质。
(全文完)
