单侧颈动脉支架置入术后支架对侧颈动脉供血区微栓塞的危险因素研究
2019-12-16陈学丛孔文婷张跃其朱晓龙张淑云时宝林
陈学丛,孔文婷,张跃其,朱晓龙,张淑云,时宝林*
迄今为止公布的数据显示颈动脉支架置入术(CAS)在长期预防卒中效果方面与颈动脉内膜剥脱术(CEA)之间并无明显差别[1-2],前者由于创伤小、恢复快,成为越来越多颈动脉狭窄患者的重要选择。尽管有远端抗栓塞保护装置的应用,但CAS后患者仍有较高的脑梗死发生率,尤其是磁共振弥散加权成像(DWI)阳性的无症状微栓塞[3]。有研究发现,CAS后微栓塞发生率为50%,而CEA后微栓塞发生率仅为17%[4]。CAS后微栓塞不仅发生在支架同侧颈动脉供血区,也常见于支架对侧颈动脉供血区以及椎基底动脉供血区,显然所有病变不能仅用已经被支架覆盖的颈动脉斑块解释。目前CAS后发生支架同侧颈动脉供血区微栓塞的机制如高龄、颈动脉溃疡斑块已相对明确[5],但CAS后支架对侧颈动脉供血区微栓塞的发生机制国内鲜有文献提及,目前推测可能与主动脉弓斑块等诸多因素密切相关。本研究旨在初步探讨单侧CAS后支架对侧颈动脉供血区微栓塞的发生率及其高危因素,以期为今后对CAS高风险患者进行初步筛选提供借鉴。
1 对象与方法
1.1 研究对象 连续选取2013年12月—2018年8月在潍坊市人民医院神经内科就诊的拟行单侧CAS的颈动脉狭窄患者164例为研究对象。纳入标准:(1)症状性颈动脉狭窄≥50%,非症状性颈动脉狭窄≥70%;(2)术前未进行脑血管造影;(3)可行颅脑MRI检查;(4)知情同意并签字。排除标准:(1)同时处理两侧颈动脉病变;(2)合并椎动脉、基底动脉严重狭窄或其他颅内、外血管严重狭窄;(3)其他特殊原因导致血管狭窄:如血管夹层、创伤等;(4)严重疾病不能承受手术;(5)严重肾功能损害不能承受造影剂。本研究已经过本院伦理委员会审批通过。
1.2 研究方法
1.2.1 一般资料收集 收集患者性别、年龄、高血压发生情况、糖尿病发生情况、高脂血症发生情况、冠心病发生情况、心房颤动发生情况、吸烟(每天吸烟1支以上,连续吸烟≥6个月定义为吸烟)情况、卒中史、术前颈动脉狭窄程度。
1.2.2 术前检查 颈动脉狭窄经头颈部磁共振血管成像(MRA)/CT血管造影(CTA)证实,狭窄程度根据北美症状性颈动脉内膜剥脱术试验(NASCET)标准进行评估[6];常规行胸部X线检查,术前1周内常规行颅脑MRI平扫检查,进行CAM评分(见表1)。
1.2.3 CAS 完善术前检查,术前常规口服拜阿司匹林100 mg/d、氯吡格雷(波立维)75 mg/d 至少 3 d。局部麻醉下行脑血管造影,直接或者配合4/5 F多功能导管(MPA)将长鞘或指引导管输送到位,通过狭窄处后打开远端抗栓塞保护装置(波士顿科学FilterWier EZ或强生公司Angioguard),视狭窄程度选择是否预扩,支架(波士顿科学Wallstent支架或强生公司Precise支架)到位后释放支架,视残余狭窄情况选择球囊后扩。术后继续口服拜阿司匹林100 mg/d以及氯吡格雷75 mg/d至少3个月,后改口服拜阿司匹林100 mg/d。
1.2.4 术后评估 CAS后3 d内进行颅脑MRI平扫检查,确定微栓塞发生情况及部位(分为支架同侧颈动脉供血区微栓塞、支架对侧颈动脉供血区微栓塞、支架两侧颈动脉供血区微栓塞、后循环供血区微栓塞)。记录术后颈动脉狭窄程度、术后支架对侧颈动脉狭窄程度、支架对侧颈动脉闭塞发生情况、左侧颈动脉病变发生情况、Ⅱ/Ⅲ型主动脉弓发生情况、CAM评分≥3分情况、闭环支架使用情况、平均增加导管和/或导丝数量、手术时间。
1.2.5 分组 根据CAS后3 d内的颅脑MRI平扫检查结果,剔除后循环供血区微栓塞患者,将剩余患者分为同侧组(支架同侧颈动脉供血区微栓塞)和对侧组(支架对侧颈动脉供血区微栓塞或支架两侧颈动脉供血区微栓塞)。
1.3 统计学方法 采用SPSS 18.0软件进行统计分析。采用单样本K-S检验进行数据的正态性检验,正态分布计量资料以(x ±s)表示,两组间比较采用两独立样本t检验;计数资料以相对数表示,组间比较采用χ2检验,理论频数(T)<5但≥1采用连续校正χ2检验,20%以上格子的T<5采用似然比χ2检验,T<1采用Fisher's确切概率法;支架对侧颈动脉供血区微栓塞影响因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 164例患者中有163例完成CAS,CAS后即刻造影示血流正常,远端无大血管闭塞,CAS后3 d内颅脑MRI平扫检查发现72例(44.2%)新发微栓塞(其中支架同侧颈动脉供血区微栓塞39例,支架对侧颈动脉供血区微栓塞5例,支架两侧颈动脉供血区微栓塞13例,后循环供血区微栓塞15例)。剔除发生后循环供血区微栓塞患者,剩余57例,将其分为同侧组(39例)和对侧组(18例)。
2.2 两组一般资料及术后评估指标比较 两组性别、年龄、高血压发生率、糖尿病发生率、高脂血症发生率、冠心病发生率、心房颤动发生率、吸烟率、卒中史发生率、术前颈动脉狭窄程度、术后颈动脉狭窄程度、术后支架对侧颈动脉狭窄程度、支架对侧颈动脉闭塞发生率、Ⅱ/Ⅲ型主动脉弓发生率、闭环支架使用率、平均增加导管和/或导丝数量、手术时间比较,差异无统计学意义(P>0.05);对侧组左侧颈动脉病变发生率、CAM评分≥3分发生率高于同侧组,差异有统计学意义(P<0.05,见表2)。
2.3 支架对侧颈动脉供血区微栓塞影响因素的多因素Logistic回归分析 以支架对侧颈动脉闭塞发生情况(赋值:发生=1,未发生=0)、左侧颈动脉病变发生情况(赋值:发生=1,未发生=0)、Ⅱ/Ⅲ型主动脉弓发生情况(赋值:发生=1,未发生=0)、CAM评分≥3分情况(赋值:发生=1,未发生=0)、闭环支架使用情况(赋值:使用=1,未使用=0)为自变量,以CAS后支架对侧颈动脉供血区微栓塞发生情况为因变量(赋值:发生=1,未发生=0),进行多因素Logistic回归分析,结果显示,左侧颈动脉病变、CAM评分≥3分是颈动脉狭窄患者CAS后发生支架对侧颈动脉供血区微栓塞的影响因素(P<0.05,见表3)。

表1 CAM评分标准Table 1 CAM scoring criteria
3 讨论
BÜSING等[7]研究发现,在心血管造影过程中,约有15%~22%的患者发生DWI阳性的亚临床颅内微栓塞事件。而颅内微栓塞也是CAS后最常见的并发症之一,相较于CEA后24%~34%的微栓塞发生率,CAS后微栓塞发生率为26%~78%[8]。大部分的术后微栓塞看似无临床症状,但有研究表明,术后微栓塞可能与术后一过性认知功能减退有关,尤其是注意力、计算力等方面减退明显[9]。GENSICKE等[10]认为CAS后微栓塞预示着6个月内有更高的卒中复发概率。因此,识别CAS后微栓塞高危患者,尽量避免栓塞事件的发生尤其重要。GRÖSCHEL等[5]总结CAS后发生微栓塞的危险因素包括高龄、颈动脉溃疡斑块、吸烟、颈动脉斑块钙化、复杂的主动脉弓解剖以及颈总动脉、颈内动脉迂曲。但CAS后支架对侧颈动脉供血区微栓塞的发生机制鲜有文献提及,因此本研究对此进行初步探讨。
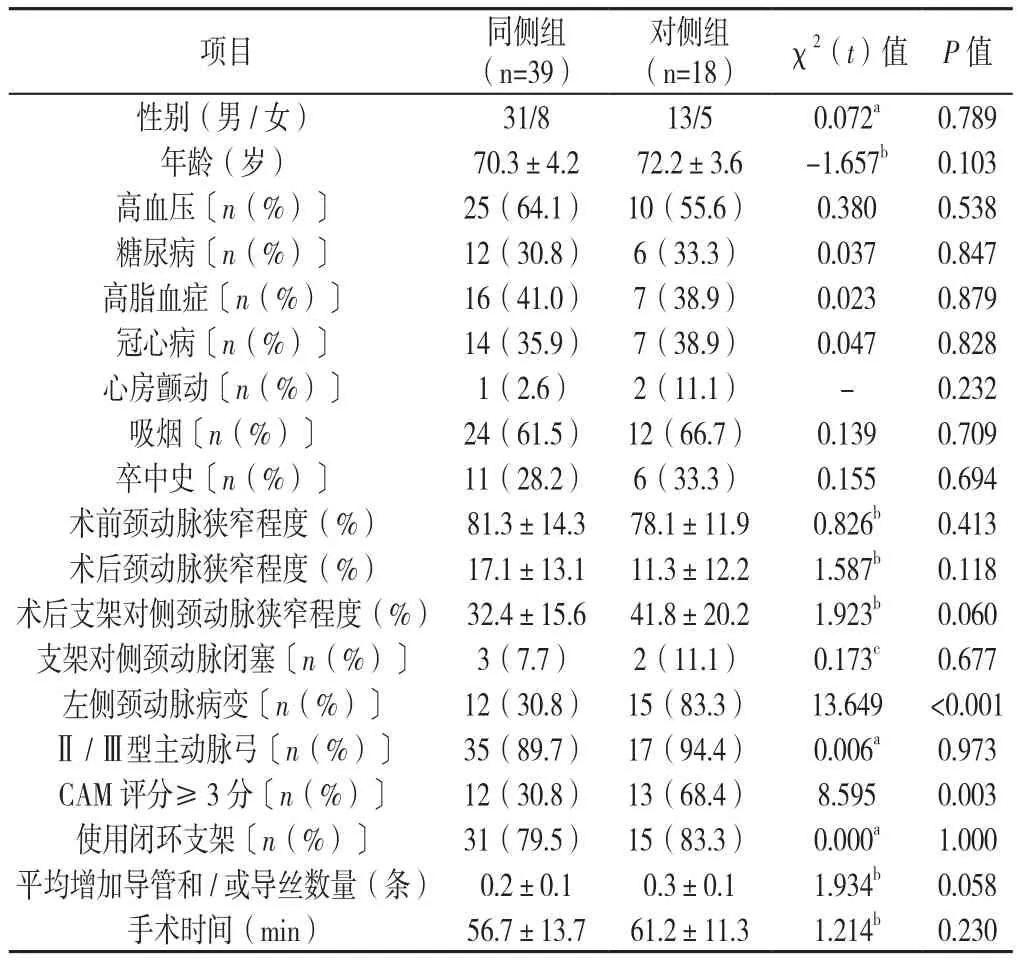
表2 两组一般资料及术后评估指标比较Table 2 Comparison of general data and postoperative evaluation indices between the two groups

表3 CAS后发生支架对侧颈动脉供血区微栓塞影响因素的多因素Logistic回归分析Table 3 Multivariate Logistic regression analysis of influencing factors of microembolism in the supply blood area of the contralateral carotid artery
本研究发现CAS后微栓塞发生率为44.2%(72/163),其中分别有5、13例发生在支架对侧颈动脉供血区和支架两侧颈动脉供血区。基于胸部X线检查钙化分级的CAM评分越高,表示主动脉弓存在斑块的概率越大,一般CAM评分≥3分提示主动脉弓存在斑块[11]。本研究应用CAM评分来预估主动脉弓斑块的严重程度,而本研究发现,CAM评分≥3分是颈动脉狭窄患者CAS后发生支架对侧颈动脉供血区微栓塞的影响因素之一。有研究提示行CAS的患者在主动脉弓没有斑块的情况下,非手术侧未见新发梗死灶[12]。KIM等[13]研究发现,主动脉弓上导丝导管的操作对于CAS后非同侧颈动脉供血区及后循环供血区新发微栓塞有关。这些研究均提示CAS后支架对侧颈动脉供血区新发微栓塞可能与主动脉弓斑块有关,本研究结果与之一致。主动脉弓斑块包括软斑、活动性斑块、溃疡斑块,其本身具有产生栓子的潜力,虽然抗栓塞保护装置可以预防手术侧严重栓塞事件的发生,但显然不能保护支架对侧颈动脉供血区,而目前在造影或者主动脉弓操作期间更没有任何装置能够保护支架对侧颈动脉供血区,因此在主动脉弓进行复杂操作时可能已经造成主动脉弓斑块脱落导致远端颅内的微栓塞。
本研究结果显示,左侧颈动脉病变也是颈动脉狭窄患者CAS后发生支架对侧颈动脉供血区微栓塞的影响因素。2011年NAGGARA等[14]研究发现,左侧CAS后发生微栓塞的概率更大,在经股动脉入路时,导管在进入主动脉弓开口朝右、同主动脉夹角小的左颈总动脉时相对困难,常规造影导管常不能提供足够的支撑力,甚至需要更换Simmon导管以及长硬导丝,即使应用望远镜技术或交换技术,指引导管或长鞘常需多次操作才能成功到位,如此反复操作容易损伤主动脉弓。GENSICKE等[15]则认为CAS后支架对侧颈动脉供血区微栓塞的发生不仅与支架对侧颈动脉狭窄程度>50%有关,而且更可能与复杂的路径(Ⅱ/Ⅲ型主动脉弓)有关。
有研究提示操作时间短、较少更换导丝导管的患者术后微栓塞发生率低于操作时间长、多次更换导丝导管的患者[16]。本研究结果则提示同侧组手术时间短于对侧组,平均增加导管和/或导丝数量少于对侧组,虽然差异无统计学意义,但提示快速短时操作显然并不增加术后微栓塞发生率。KIM等[13]研究还发现,相较于直接指引导管到位,应用同轴技术指引导管到位术后微栓塞发生率更低,提示在手术操作过程中,尤其是在复杂路径中尽量选用合适的技术,减少不必要的操作,以尽可能减少对所有行进路径中斑块的接触,从而减少颅内微栓塞的发生。
尽管在术中除造影外进入锁骨下动脉的操作并不多,但本研究发现后循环供血区微栓塞发生率并不低,为9.2%,提示在主动脉弓、头臂干、左侧锁骨下动脉的操作均有可能导致后循环供血区微栓塞,而颈动脉脱落的栓子也可随开放的后交通动脉到达后循环供血区发生脑微栓塞。
综上所述,左侧颈动脉病变以及CAM评分≥3分是CAS后支架对侧颈动脉供血区微栓塞的影响因素,提示复杂的路径以及严重的主动脉弓斑块可能导致CAS后支架对侧颈动脉供血区微栓塞的发生概率增加。因此在CAS前,术者应充分预估手术风险,制定详细手术方案,同时配合熟练的短时操作、合理的技术应用以及合适的器械选择,以减少在主动脉弓的操作,同时减少术后微栓塞的发生。最后,由于本研究纳入患者例数较少,今后的研究中有待增加样本量;另外,本研究还发现CAS后后循环供血区微栓塞的发生率并不低,但并未深入探讨其发生机制及其危险因素,有待今后进一步研究。
作者贡献:陈学丛进行文章的构思与设计、可行性分析,撰写论文;孔文婷、朱晓龙进行文献/资料的收集、整理;张跃其进行统计学分析,文章、英文的修订;张淑云、时宝林负责文章的质量控制及审校;时宝林对文章整体负责、监督管理。
本文无利益冲突。
