原发性开角型青光眼视盘周围血管密度变化的研究
2019-12-09曾洪波
刘 勇,郭 毅,曾洪波
0引言
青光眼是一种常见的不可逆性致盲眼病,其患病率居于致盲性眼病中的第二位[1-2]。原发性开角型青光眼(primary open angle glaucoma,POAG)一旦出现视力、视野等视功能损害,便无法逆转。因此早诊断、早治疗是防止视功能损害的有效途径[3-4]。目前认为缺血学说是POAG发病的重要原因之一,由于局部血流自动调节障碍和局部血管痉挛等原因引起视乳头供血不足,最终导致视网膜神经节细胞损伤[5-6]。然而缺血学说尚未得到完全证实。近年光相干断层扫描血流成像(OCT angiography,OCTA)技术得以迅速发展,可定量测量视网膜血管密度(vessel density,VD)[7-9]。按照POAG缺血学说,理论上POAG患者视盘周围VD可能会低于正常人。因此,本研究旨在利用OCTA技术对POAG患者的视盘周围VD进行测量并分析视盘周围VD诊断POAG的价值。
表1 两组研究对象的基本特征比较

变量对照组(n=60)POAG组(n=60)t/χ2P年龄(x±s, 岁)57.55±6.8158.57±7.55-0.7740.440性别(男/女,例)32/2825/351.6370.201用药前眼压(x±s,mmHg)14.53±3.2528.75±3.73-22.243<0.001中央角膜厚度(x±s,μm)550.62±30.47543.40±29.211.3240.213等效球镜度(x±s,D)0.33±0.960.41±1.08-0.4230.673收缩压(x±s, mmHg)127.05±14.68130.98±17.94-1.3140.791舒张压(x±s,mmHg)75.95±7.8476.38±9.88-0.2660.683眼轴(x±s, mm)23.24±0.7623.39±0.54-1.2510.213杯盘比(x±s)0.29±0.090.78±0.16-20.959<0.001视野MD(x±s,dB)-1.41±1.05-16.57±4.8023.890<0.001视野PSD(x±s,dB)1.66±0.387.41±2.49-17.703<0.001
1对象和方法
1.1对象纳入2018-03/12期间在我院初诊的POAG患者60例,同时纳入60例性别、年龄、屈光度以及眼轴长度匹配的正常志愿者作为对照组。POAG诊断标准:(1)房角开放;(2)眼压高于21mmHg;(3)眼底视杯扩大,相应视盘盘沿组织丢失;(4)典型的青光眼视野缺损。POAG患者纳入标准:(1)确诊为POAG的患者;(2)年龄≥18岁;(3)屈光度-3 .00~+3.00D;(4)既往无糖尿病、高血压等病史;(5)研究眼无外伤、手术史,除POAG外无其它眼部病变病史;(6)屈光介质透明,可以获得清晰的图像。排除标准:(1)因配合欠佳或其他原因导致成像质量不好的患者;(2)视野检查中固视丢失率、假阳性率或假阴性率大于20%的患者;(3)孕妇或者哺乳期患者;(4)不能签署知情同意书的患者。对照组入选标准:(1)可获得清晰图像的无任何眼部疾病以及手术史的研究对象;(2)年龄≥18岁;(3)等效球镜度-3.00~+3.00D;(4)既往无糖尿病、高血压等系统疾病病史。病例组单眼患病的纳入患眼作为研究对象,双眼患病的患者以及对照组患者均纳入右眼作为研究对象。最终共纳入POAG患者60例60眼,正常对照组60例60眼。POAG组纳入女35例35眼,男25例25眼,对照组中女28例28眼,男32例32眼,两组眼压、杯盘比、视野MD、视野PSD的差异均有统计学意义(P<0.001),而年龄、性别、中央角膜厚度、等效球镜度、收缩压、舒张压、眼轴等参数两组之间差异均无统计学意义(P>0.05),见表1。本研究经本院伦理委员会批准,并遵循《赫尔辛基宣言》。所有研究对象均签署知情同意书。
1.2方法
1.2.1常规检查所有研究对象均接受全面的眼科检查:包括最佳矫正视力(best corrected visual acuity,BCVA)、非接触眼压计测量眼压(intraocular pressure,IOP)、裂隙灯检查、等效球镜度(球镜度数+1/2柱镜度数[6])、房角镜、眼底检查、眼底照相、Humphrey视野计检查视野、眼轴、IOL Master检查前房深度以及Orbscan II 眼前节分析系统检查角膜中央厚度。此外所有研究对象均接受基本检查:心率、血压、身高、体质量等。
1.2.2 OCTA检查方法所有OCTA检查均由同一个操作熟练的检查者采用RTVue-100 OCT血流成像系统完成。患者取坐位注视机器内视标,以视乳头为中心,选择4.5mm×4.5mm大小的扫描模式扫描(图1)。OCT扫描数据框扫描的OCT血流图为304×304像素[10]。采用分频幅去相关血流成像算法计算视网膜VD,视网膜非灌注区面积[10-11]。在扫描过程中研究对象因眼球扫视与固视改变会导致OCT出现运动伪迹,而运动校正技术可消除这些运动伪迹[11]。视盘周围VD计算采用OCT系统自带的软件自动测量,自动计算视盘周围上方、下方、鼻侧、颞侧视网膜VD,此外还提供上半部以及下半部的VD(图1)。R测量视盘周围RNFL厚度(包括视盘周围平均RNFL厚度,视盘周围上方、下方、鼻侧、颞侧以及上半部、下半部RNFL厚度)。OCTA的图像质量由两位研究者进行单独评价,如果两位研究者之间的评价存在差异则通过第三个人重新评估。如果图片的信号强度指数小于40,则定义为图像质量不好,不纳入本研究中。此外如果图像中有明显的运动伪迹,也不纳入本研究中。
统计学分析:采用SPSS 21.0软件进行数据分析,符合正态分布的计量资料采用独立样本t检验,分类变量则采用卡方检验。视盘周围VD与视盘周围RNFL的关系采用Pearson相关性分析。多元线性回归分析视盘周围VD及视盘周围RNFL厚度的独立相关因素。绘制受试者工作特征曲线(receiver operating characteristic curve,ROC)及计算ROC曲线下面积(area under curve,AUC);比较视盘周围VD及视盘周围RNFL厚度的诊断性能。以P< 0.05为差异有统计学意义。
2结果
2.1两组视盘周围VD比较POAG组视盘周围平均VD、视盘周围上、下方的VD明显低于对照组,差异均有统计学意义(P<0.001);POAG患者平均RNFL、上方、下方RNFL厚度明显薄于对照组,差异均有统计学意义(P<0.001),见表2。
2.2视盘周围VD与RNFL厚度相关性分析Pearson相关分析结果提示:所有研究对象视盘周围平均VD与视盘周围RNFL平均厚度呈显著正相关(r=0.339,P<0.001,图2)。
2.3多因素线性回归分析将所有变量逐一采用进入法进行一元线性回归分析,然后将一元回归分析有显著相关性的变量再纳入多因素模型中,采用逐步法进行多元线性回归分析。结果显示POAG诊断、视野PSD、视野MD以及等效球镜度是视盘周围平均RNFL厚度的独立相关因素。矫正了视野PSD、视野MD以及等效球镜度混杂因素后,POAG诊断仍然与视盘周围平均RNFL厚度存在显著相关性。而POAG诊断与杯盘比则是视盘周围平均VD的独立相关因素(表3)。
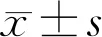

变量对照组(n=60)POAG组(n=60)tP视盘周围VD(%)平均58.40±3.9252.55±5.286.886<0.001上方58.43±4.1152.38±5.316.970<0.001下方58.36±3.4052.58±5.326.730<0.001视盘周围RNFL厚度(μm)平均143.41±11.13108.21±16.7213.573<0.001上方140.08±10.0196.87±16.3517.459<0.001下方146.60±18.82118.82±19.038.041<0.001
表3 多因素线性回归分析

因素OR(95%CI)标准误回归系数tP视盘周围平均RNFL厚度 诊断(对照vs POAG)-32.488(-46.582~-18.393)7.115-0.702-4.566<0.001 视野PSD-4.724(-5.594~-3.855)0.439-0.704-10.759<0.001 视野MD0.907(0.223~1.591)0.3450.3252.6280.010 等效球镜度2.660(0.482~4.837)1.0990.1222.4200.017视盘周围VD 诊断(对照vs POAG)-9.696(-13.282~-6.211)1.805-0.864-5.328<0.001 杯盘比7.718(1.330~14.106)3.2550.3782.3530.018

图1视盘周围VD的OCTA图A:浅层血流密度;B:彩色血管密度图(视盘周围毛细血管层)。

图2视盘周围平均VD与视盘周围平均RNFL厚度相关性分析。

图3视野MD、视盘周围平均VD、视盘周围平均RNFL厚度的ROC曲线。
2.4 ROC及ROC曲线下面积分析ROC及ROC曲线下面积分析结果显示:视盘周围平均VD、视盘周围平均RNFL厚度、视野MD、视野PSD以及杯盘比均能有效诊断POAG(表4)。视盘周围平均VD、视盘周围平均RNFL厚度、视野MD、视野PSD以及杯盘比参数的ROC曲线见图3、4。所有纳入的参数AUC值均有统计学意义(P<0.001)。其中视野MD以及杯盘比诊断效能最大,AUC值均为1.000,其余指标诊断效能由大到小依次为视野PSD、视盘周围平均RNFL厚度以及视盘周围平均VD。
3讨论
目前世界范围内总共大约有7000万人患有青光眼,其发病隐匿,大约一半患者即使视力损伤却没有意识到患病[3]。视网膜神经节细胞的损伤是青光眼的共同病理特征[12]。在疾病的早期,POAG的临床表现不典型,诊断困难。当出现特征性临床表现时,视功能已经出现不可逆转的损害。目前诊断青光眼的主要手段还是依赖观察视盘形态改变,视功能的改变包括特征性的视野变化以及通过OCT检查视盘周围RNFL厚度。然而对于早期青光眼,经常检测不到特征性的视野缺损,因为青光眼的形态学改变往往发生在功能学改变之前,出现了可检测到的视野异常时,RNFL已经出现明显的损害[13]。而杯盘比的改变,也存在假阳性的可能性,有部分患者本身就存在先天性大视杯。因此众多眼科医生一直在努力寻找相对敏感的诊断早期青光眼的方法。近年来随着OCTA技术的发展,青光眼诊断又多了一个可能的工具。OCTA可清晰地显示视网膜血管形态(包括浅层以及深层),并可定量计算出视网膜血流面积、VD以及非灌注区的面积[14-15]。有研究发现青光眼的视盘周围VD较正常人明显降低[16-17]。因此本研究利用视网膜血流成像技术测量POAG患者视盘周围VD,并开发它作为诊断POAG工具的可能性。由于VD的计算方法为一定区域内大血管和微血管所占的面积的百分比。视网膜VD分为浅层VD以及深层VD,其中浅层VD测量的是视网膜浅层毛细血管网的VD,深层VD测量的是视网膜深层毛细血管网的VD。在本研究中我们仅将视网膜内层VD作为评价指标。
表4 各参数诊断POAG的敏感性及特异性

变量敏感性(%)特异性(%)AUC(95%CI)P视盘周围平均VD91.765.00.808 (0.730~0.887)<0.001视盘周围平均RNFL厚度91.786.70.956 (0.919~0.993)<0.001视野MD96.71001.000(1.000~1.000)<0.001视野PSD96.798.30.989 (0.968~1.000)<0.001杯盘比91.71001.000 (1.000~1.000)<0.001

图4视野PSD、杯盘比的ROC曲线。
研究结果发现,POAG患者视盘周围VD与视盘周围RNFL厚度均较正常人低,差异有统计学意义。关于RNFL厚度,青光眼患者低于正常人已经成为共识并且作为青光眼诊断的指标之一。Yarmohammadi等[18]通过检测58例伴有视野受损的POAG患者以及28例正常人的视盘周围以及黄斑部的VD,发现POAG患者视盘周围以及黄斑VD明显低于正常人。并且发现降低的VD与视野受损存在相关性。VD降低有可能比视野诊断POAG的敏感性更高。Hou等[19]亦发现POAG患者VD明显低于正常人。与我们的研究结论类似。国内学者也做了类似研究同样也发现POAG患者视乳头周围VD明显下降。所有的研究结果趋势均与本研究一致,说明POAG患者视盘周围VD下降结果可靠。由于纳入本研究的POAG患者的眼压、杯盘比以及视野的相关参数与正常人存在显著差异。因此我们进一步做了多因素线性回归分析,结果提示在排除了这些混杂因素后,发现POAG患者视盘周围平均VD较对照组少9.7%。证明视盘周围VD降低与视盘周围RNFL厚度均是发生POAG的独立危险因素,是POAG患者独立而有特征性的改变,可作为诊断POAG的重要参数。我们进一步将视盘周围VD与视盘周围RNFL厚度做了相关性分析,结果提示视盘周围VD与视盘周围RNFL厚度具有高度相关性。这种相关性并不难解释:按照缺血理论,视神经受损是眼部血流障碍引起的RGC细胞轴突缺血的结局[6, 20]。反之,青光眼患者受损的神经组织会进一步导致视网膜微循环的改变,形成一个相辅相成的病理循环[21]。
多元线性回归提示:视盘周围VD与POAG的发生呈独立相关。我们进一步做了ROC曲线及AUC分析。AUC值在1.0和0.5之间。如果AUC值位于0.5~0.7时,该参数有较低准确性,AUC值位于0.7~0.9时该参数有一定准确性,AUC值位于0.9以上时该参数有较高准确性。分析结果显示:已经用于临床诊断青光眼的相关指标如:杯盘比、视野MD、PSD值以及视盘周围RNFL厚度均是诊断POAG的重要指标,AUC值均>0.95以上。而视盘周围VD参数的AUC值为0.808,说明用它来诊断POAG时有一定准确性,但是比目前常用诊断指标杯盘比、视野指标以及RNFL厚度等相比,诊断青光眼的效能略低。因此在临床工作中,我们认为视盘周围VD可作为其它常规诊断青光眼的补充手段。
本研究纳入的病例样本量相对比较大,共纳入了60例POAG患者,之前相关研究纳入的样本量低于本研究。其次本研究有严格的纳入、排除标准。同时为了减少混杂因素的影响,我们运用多因素线性回归模型对这些混杂因素进行校正,得出独立相关因素。虽然有不少研究证实POAG患者视盘周围VD明显低于正常人,但是本研究理由统计学方法层层递进,证实不仅POAG患者视盘周围VD明显低于正常人,而且是独立影响因素,更能作为诊断POAG的辅助指标。本研究仍存在不足之处和局限性。首先,研究表明降眼压药物可能会改变眼部血流[22-23],本研究尚不能排除降眼压药物引起的眼部血流变化。其次早期和晚期POAG在病理特征上有可能存在一些差异,眼部血流可能也存在一定差异,如果将研究对象按照早期和晚期POAG进行区分,研究所得出的结论将更精确。再次,由于本研究仅仅为一个横断面研究,我们无法评估视盘周围VD测量在评估青光眼进展方面的有效性。将来设计一个纵向队列研究则可评估青光眼视盘周围VD与进展的关系。
总之,POAG患者视盘周围VD明显变低,视盘周围RNFL厚度均明显变薄,视盘周围VD与视盘周围RNFL厚度均是POAG的独立相关因素。它们均有较好的POAG诊断价值,视盘周围VD可作为其它诊断青光眼的补充手段。值得一提的是,青光眼的早期诊断仍需要综合患者的视野、眼压、视盘、房角、神经纤维层以及血流等多种因素分析并动态观察来获得。
