地西他滨在骨髓增生异常综合征中的应用及疗效相关影响因素研究
2019-12-04郭莉吴志敏王继芳任荣香魏秀丽
郭莉,吴志敏,王继芳,任荣香,魏秀丽
(河南省新乡市第一人民医院 血液内科,河南 新乡 453000)
骨髓增生异常综合征(myelodysplastic syndrome,MDS)是造血干细胞增殖、分化异常导致的造血系统功能障碍性疾病,按照病因分析可分为原发性MDS 和继发性MDS,按照形态学可分为难治性贫血、难治性贫血伴原始细胞增多、难治性贫血伴环形铁粒细胞、难治性贫血伴原始细胞过多转变型及慢性粒单核细胞白血病五种类型[1]。MDS发病隐匿,有外周全血细胞减少、病态造血、骨髓细胞增生等表现,DNA 甲基化异常参与其发生、发展过程,患者总体表现为高度甲基化,去甲基化药物如地西他滨(decitabine, DAC)在MDS 治疗中占据重要地位,但有关地西他滨治疗MDS 的用药方案、影响因素等尚未有统一方案[2]。为探究地西他滨在MDS 治疗中的应用效果,探究其疗效影响因素,期望为临床治疗做出启示,现报道如下。
1 资料与方法
1.1 一般资料
收集2018 年2 月至2019 年 2 月本院收治的MDS 患者90 例为研究对象,纳入标准:符合世界卫生组织制定的MDS 诊断标准[3];于本院接受两个疗程以上的地西他滨指标;年龄18~70 岁;经本院伦理委员会批准同意;患者及其家属知情并同意。排除标准:合并多种血液系统疾病;同期服用可能影响研究结果药物;临床资料不全;地西他滨过敏或禁忌证;高度敏感体质。根据上述标准纳入90 例患者,其中男51 例,女39 例;年龄23~70(56.88±5.26)岁,骨髓细胞形态学检查中难治性贫血5 例,难治性贫血伴原始细胞增多1 型26 例,难治性贫血伴原始细胞增多2 型21 例,难治性血细胞减少伴多系发育异常38 例;危险度分级中低危、中危-1、中危-2、高危分别为10 例、39 例、29 例、12 例。
1.2 方法
①治疗方法:患者入院后均进行血常规、染色体核型分析等检查,根据危险度、病情等使用不同剂量地西他滨治疗,剂量约为12~25 mg/m2,1 次/d,静脉滴注,每次滴注时间约70 min,连续注射5~8 d,4 w 或6 w 为一疗程,理想情况下每一疗程之间间隔3 w,在实际情况中根据患者治疗情况调整。对所有患者进行追踪随访,观察90 例患者治疗后的疗效,疗效判定依据为国际MDS 工作组制定的MDS 疗效判定标准[4],疗效分为完全缓解(complete response, CR)、部分缓解(partial response,PR)、骨髓完全缓解(marrow CR,mCR)、血液学改善(hematology improve, HI)、疾病稳定(stable disease, SD)、治疗失败(failure, F)六类,其中重点关注前四位,前四位作为治疗总有效率(overall response rate, ORR),后两位为总无效率,并观察患者不良反应情况,不良反应的评估以世界卫生组织化疗药物不良反应分级标准[5]为依据。②影响因素分析方法:按照文献资料及临床经验,拟选择性别、年龄、初发病情况(有无重度贫血、有无粒细胞缺乏、有无血小板减少、有无多系细胞系减少等)、合并其他恶性肿瘤情况、药物剂量、治疗方案等作为影响患者疗效的可能因素,分别统计和分析不同疗效患者的上述资料,其中重度贫血是指红细胞<60 g/L,粒细胞缺乏是指中性粒细胞绝对值<0.5×109/L,血小板<30×109/L 为血小板减少,多系细胞系减少两系以上为多系细胞系减少。
1.3 统计学方法
数据均以IBM SPSS 19.0 分析,计量资料以均数±标准差()表示,计数资料以例或百分率(%)表示,计量资料及不同因素对疗效影响分析采用Fisher 精确概率法和χ2检验进行,P<0.05为差异有统计学意义。
2 结果
2.1 90例患者总体疗效分析
90 例患者中78 例患者应用地西他滨及其他药物联合治疗,12 例患者仅使用地西他滨治疗,其中疗效为完全缓解的患者10 例(11.11%),部分缓解的患者12 例(13.33%),骨髓完全缓解的患者 8 例(8.89%),血液学改善 17 例(18.89%);患者达到最佳疗效的疗程范围在2~5 个疗程,平均为(3.46±0.22)个疗程;治疗前的染色体分型结果显示,预后中间患者32 例,预后不良患者58 例,按照预后情况分组比较疗效发现,预后中间组患者完全缓解、部分缓解、骨髓完全缓解、血液学改变例数分别为6 例、7 例、4 例、7 例,预后不良组对应为4 例、5 例、4 例、10 例,两组完全缓解、部分缓解、骨髓完全缓解、血液学改变例数均差异无统计学意义(χ2=2.934, 3.135, 0.800,0.289;P=0.087,0.077,0.371,0.591)。
2.2 90例患者不良反应分析
大部分患者(81 例)接受地西他滨治疗后均出现不同程度骨髓抑制和由骨髓抑制而引发的感染,多数集中在中度骨髓抑制,大部分患者(80 例)出现3、4 级血液学不良反应(如粒细胞缺乏、红细胞减少等)。在输血、刺激骨髓造血、抗感染治疗、细胞集落刺激因子等的治疗后,所有患者均度过骨髓抑制期。
2.3 不同因素对疗效的影响分析
有无重度贫血、有无粒细胞缺乏、有无血小板减少、有无多系细胞系减少患者之间的治疗总有效率差异均具有统计学意义(P<0.05),性别、年龄、合并其他恶性肿瘤情况、药物剂量、治疗方案之间的疗效差异均无统计学意义(P>0.05),见表1。
2.4 影响地西他滨疗效的多因素分析
根据表1 结果,将治疗无效作为因变量,将重度贫血、粒细胞缺乏、血小板减少、多系细胞系减少作为自变量进行Logistics 回归分析,校正其他因素影响后上述自变量均进入回归方程。血细胞减少、多系细胞系减少是地西他滨治疗无效的危险因素,见表2。
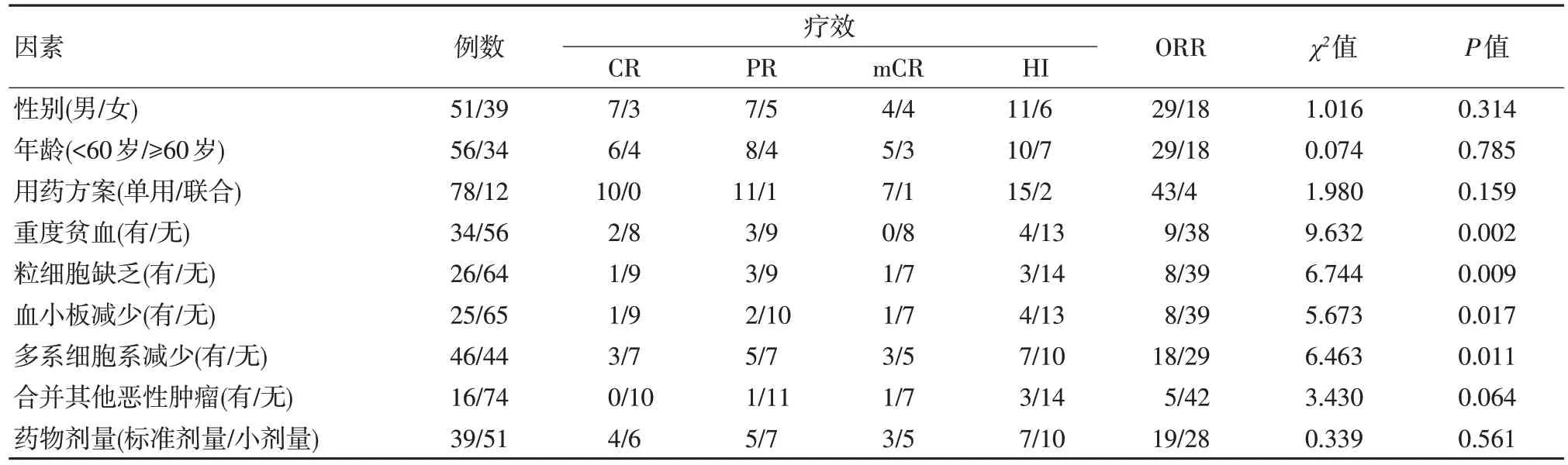
表1 不同因素对地西他滨疗效的影响分析 例

表2 影响地西他滨疗效的Logistics 回归分析
3 讨论
近年来的表观遗传学研究发现,DNA 去甲基化在MDS 发病、发展过程中发挥重要作用,同时去甲化也是恶性肿瘤表观遗传学修饰的主要方式之一,是指甲基转移至胞嘧啶碳5 位置上导致的转录因子改变,高度去甲基化可累及肿瘤抑制基因、细胞周期调控基因等多个基因,导致MDS 发生造血异常[6]。
本研究回顾性分析地西他滨在90 例MDS 患者中的应用效果发现,地西他滨治疗MDS 的ORR可达到52.22%(47/90),单独来看,完全缓解11.11%(10/90),部分缓解13.33%(12/90),骨髓完全缓解8.89%(8/90),血液学改善18.89%(17/90),与黄琴等[7]报道的地西他滨 66.7% 的ORR 相差不大,在纳入样本量上,本研究样本量高于黄琴等[7]研究,疗效的个体化差异可能是本文ORR 略低的重要原因,但仍在可接受范围内。不良反应的观察中发现,地西他滨作为一种化疗药物,骨髓抑制、血液系统影响等常见不良反应均存在,经过对应治疗有所改善,结合疗效认为地西他滨可作为治疗MDS 较好选择。地西他滨是DNA 聚合酶α 的良好替代物,在高浓度作用下,其进入机体后可促使尿嘧啶脱氨酶转化为对应的碱基半体,使DNA 甲基转移酶失活,直接作用于细胞周期,抑制DNA 的甲基化,达到去甲化作用,有细胞毒作用;同时,低浓度下的地西他滨能够逆转抗癌基因启动子的异常超甲基化,促进抗癌基因表达,阻断抑癌通路,达到抗癌作用[8],这一药理机制导致其疗效受到多种因素的影响,在剂量、治疗方案、疗程、应用方针上仍有争论。文中对比性别、年龄、发病情况、药物剂量、使用方案等临床资料进行疗效差异的分析发现,有无重度贫血、有无粒细胞缺乏、有无血小板减少、有无多系细胞系减少患者之间的治疗总有效率差异均具有统计学意义,提示这些因素是影响地西他滨疗效的重要因素。接下来的Logistics 回归分析显示,血细胞减少、多系细胞系减少是地西他滨治疗无效的危险因素,而陈祥云等[9]的类似研究同样发现这些因素对使用地西他滨治疗的MDS生存期产生影响,是判断患者预后的重要指标,其指出,地西他滨疗效并不能以低危或高危进行简单划分,地西他滨的疗效与反应持续时间有关,血细胞减少、多系细胞系减少可能对反应持续时间产生影响,故而初发病存在血细胞减少、多系细胞系减少的患者疗效较差,但由于条件所限,本文仍未了解其对地西他滨反应持续时间的影响机制,但临床治疗上仍需关注外周血血象情况,以对疗效进行预判[10],此外,其他未显示对疗效有影响的因素也不能忽视,MDS 作为一种复杂的血液系统疾病,其治疗和疗效影响因素仍有待更大样本量的研究探索。
综上所述,地西他滨在MDS 的应用中效果较好,发病时血细胞减少、多系细胞系减少或可对疗效产生影响,临床治疗上需对此类患者加大关注。
