椎体成形术联合调强放射治疗脊柱转移瘤疗效
2019-11-19孙建业伦俊杰胡效坤赵俊玲吴文亮殷好治
孙建业,伦俊杰*,胡效坤,赵俊玲,吴文亮,殷好治
(1.昌乐县人民医院肿瘤科,山东 潍坊 262400; 2.青岛大学附属医院介入医学中心,山东 青岛 266011)
脊柱转移瘤引起的顽固性疼痛、病理性骨折甚至瘫痪严重影响患者生活质量[1]。采用调强放射治疗(intensity modulated radiotherapy, IMRT)止痛效果明显,但起效时间长,椎体稳定性较难加强,且增加继发病理性骨折风险[2]。经皮椎体成形术(pereutaneous vertebroplasty, PVP)通过向病变椎体注入骨水泥而快速增强椎体强度,能有效减轻疼痛,但对抑制癌细胞生长的作用有限[3]。本研究探讨PVP联合IMRT治疗脊柱转移瘤的临床疗效,分析其影响因素。
1 资料与方法
1.1 一般资料 回顾性收集2011年1月—2016年3月106例昌乐县人民医院收治的椎体转移瘤患者(共164个患病椎体),其中38例接受PVP联合IMRT治疗(PVP+IMRT组),38例接受PVP治疗(PVP组),30例接受IMRT治疗(IMRT组),见表1。纳入标准:①有恶性肿瘤病史,影像学或病理学明确诊断为单个或多个脊柱转移瘤;②患椎Bilsky脊髓压迫程度分级为0~1C级,椎体后壁侵犯程度低;③治疗前患椎疼痛视觉模拟评分(visual analogue scale, VAS)>6分;④均为胸、腰段椎体患病;⑤均有疼痛及相应节段神经功能障碍;⑥预期生存期大于3个月。排除标准:①不能耐受俯卧体位或不配合;②已接受椎体转移瘤开放性手术;③术前已接受放射治疗;④严重凝血功能障碍。治疗前完善椎体CT/MR检查和颅脑、胸、腹部CT检查。本研究经本院伦理委员会审查通过;患者均知情同意并签字。
1.2 仪器与方法 采用Philips AIIura Xper FD20双板DSA、Siemens MAGnetom Veno 3.0T MR、Siemens System Somatom Definition AS+64排多层螺旋CT机,骨水泥穿刺针(Cook公司)、聚甲基丙烯酸甲酯骨水泥(天津合成材料工业研究所)、Varian Clinac CX-SN5348直线加速器。
嘱患者俯卧,消毒、铺巾,2%利多卡因局部麻醉,根据术前CT或MRI确定目标椎体和进针角度,治疗胸椎病灶通过胸椎关节入路,腰椎病灶通过椎弓根入路。于透视下穿刺目标椎体,使针尖位于椎体前中1/3交界处并达合适位置后,调配牙膏期骨水泥,透视下向椎体注入,回退套管后继续注入,直至骨水泥弥散适当或见明显渗漏时停止。PVP+IMRT组于PVP治疗后1周内行IMRT。IMRT:CT检查示大体肿瘤、硬膜外和椎旁侵犯病变,并参考MRI、增强CT等表现确定大体靶区(gross tumor volume, GTV),临床靶区(clinical target volume, CTV)一般将GTV外扩 5 mm,将CTV外扩 5 mm为计划靶区(planning target volume, PTV);采用6 MV X线对PTV行4野IMRT,处方剂量30~50 Gy,每日2 Gy,总疗程15~25次。
1.3 疗效评价与随访 记录PVP手术及放疗相关不良反应。于术后6个月,根据实体瘤疗效评价标准1.1版不可测量病灶疗效判断标准评估疗效。行门诊或电话随访,分别于术前及术后1、3、6、12个月记录VAS;术前及术后1、3个月记录脊柱不稳定评分(spinal instability neoplastic score, SINS)、 Karnofsky功能状态评分(Karnofsky performance score, KPS),随访期至患者死亡或末次随访。患者生存时间为治疗结束至死亡或末次随访时间。随访截止时间2018年6月。
1.4 统计学分析 采用SPSS 18.0统计分析软件。方差齐性检验采用Levene法,符合正态分布的计量资料以±s表示,以列联表χ2检验比较3组间和组内不同时间点疗效评价及KPS等计数资料,两两比较采用χ2分割法(P<0.016 7为差异有统计学意义);采用单因素方差分析比较3组间和组内不同时间VAS和SINS,两两比较采用Bonferroni校正法;生存时间采用Kaplan-Meier法,Cox模型分析各因素对患者预后的影响。P<0.05为差异有统计学意义。
2 结果
3组一般资料比较差异均无统计学意义(P均>0.05),见表1。PVP均顺利完成(图1、2),无重度椎管内骨水泥渗漏、肺栓塞等严重并发症,无感染及手术死亡病例。
2.1 疗效评价 治疗后6个月,PVP+IMRT组3例(3/38,7.89%)、PVP组11例(11/38,28.95%)、IMRT组7例(7/30,23.33%)局部进展,差异无统计学意义(χ2=5.890,P=0.061)。
2.2 VAS 3组治疗前VAS比较差异无统计学意义(P>0.05)。治疗后1、3、6、12个月3组VAS差异均有统计学意义,且PVP+IMRT组疼痛较IMRT组改善明显(P均<0.016 7);治疗后1、3个月PVP+IMRT组与PVP组差异无统计学意义(P=0.653、0.109),治疗后6、12个月差异有统计学意义(P均<0.016 7);治疗后1、3个月PVP组与IMRT组差异有统计学意义(P均<0.016 7),治疗后6、12个月差异无统计学意义(P=0.979、0.850)。组内比较,3组治疗前与治疗后总体差异有统计学意义(P均<0.001),PVP+IMRT组与PVP组组内治疗前与治疗后差异均有统计学意义(P均<0.001),但治疗后1、3、6、12个月两两比较差异均无统计学意义(P均>0.016 7);IMRT组治疗前与治疗后差异均有统计学意义(P均<0.016 7),治疗后1个月与3、6、12个月差异有统计学意义(P均<0.016 7),治疗后3、6、12个月差异无统计学意义(P均>0.016 7)。见表2。
2.3 KPS 3组KPS治疗前及治疗后1、3个月组间比较差异均无统计学意义(P均>0.05)。PVP+IMRT组及PVP组组内治疗前和治疗后总体差异有统计学意义(P=0.007、0.033),治疗前与治疗后3个月差异有统计学意义(P均<0.016 7),治疗后1、3个月间差异无统计学意义(P均>0.016 7)。见表3。

表1 患者一般临床资料(例)
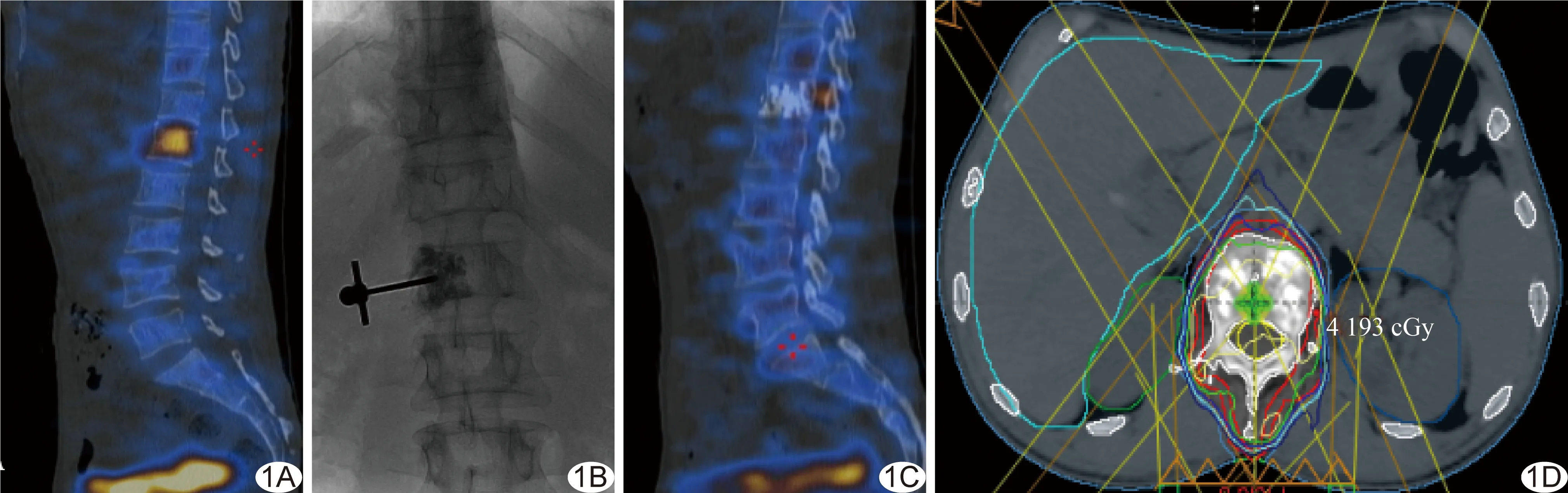
图1 患者男,56岁,肺癌脊柱转移瘤,行PVP+IMRT A.术前增强CT示L1椎体放射浓聚; B.PVP术中穿刺针到位后注射骨水泥; C.术后6个月增强CT见原病灶骨水泥填充良好,未见新发病灶及骨折; D.IMRT计划,为4野调强放疗,避开脊髓,包含上下各1个椎体

图2 患者女,66岁,肺癌多发脊柱转移瘤,行PVP A.术前MRI示T12、L1、L2椎体转移瘤,L1椎体压缩性骨折; B.PVP,骨水泥填充可,有骨水泥外溢; C.术后6个月复查CT,见原病灶骨水泥填充可,未见新发骨折
2.4 SINS 3组治疗前SINS比较差异无统计学意义(P>0.05);3组治疗后1、3个月SINS总体差异有统计学意义,治疗后1、3个月PVP+IMRT组与IMRT组差异均有统计学意义(P均<0.016 7),PVP+IMRT组与PVP组差异均无统计学意义(P=0.154、0.141),PVP组与IMRT组差异有统计学意义(P<0.016 7)。PVP+IMRT组及PVP组组内总体差异均有统计学意义(P均<0.001),PVP+IMRT组与PVP组治疗后1、3个月与治疗前差异均有统计学意义(P均<0.016 7),但治疗后1、3个月差异无统计学意义(P>0.016 7)。见表4。
表2 3组各时间点VAS比较(±s)

表2 3组各时间点VAS比较(±s)
组别治疗前治疗后1个月3个月6个月12个月F值P值PVP+IMRT组(n=38)7.03±1.153.02±0.782.94±0.752.80±0.752.75±0.89158.791<0.001PVP组(n=38)7.13±1.163.29±0.893.35±0.883.51±0.893.47±1.08105.269<0.001IMRT组(n=30)6.96±1.275.43±1.103.85±0.803.75±0.983.82±1.0148.822<0.001F值0.17065.8299.7797.8506.355——P值0.844<0.001<0.0010.0010.003——

表3 3组各时间点KPS比较[例(%)]
注:治疗后3个月时,PVP+IMRT组死亡2例,PVP组死亡1例,IMRT组死亡2例
表4 3组各时间点SINS比较(±s)
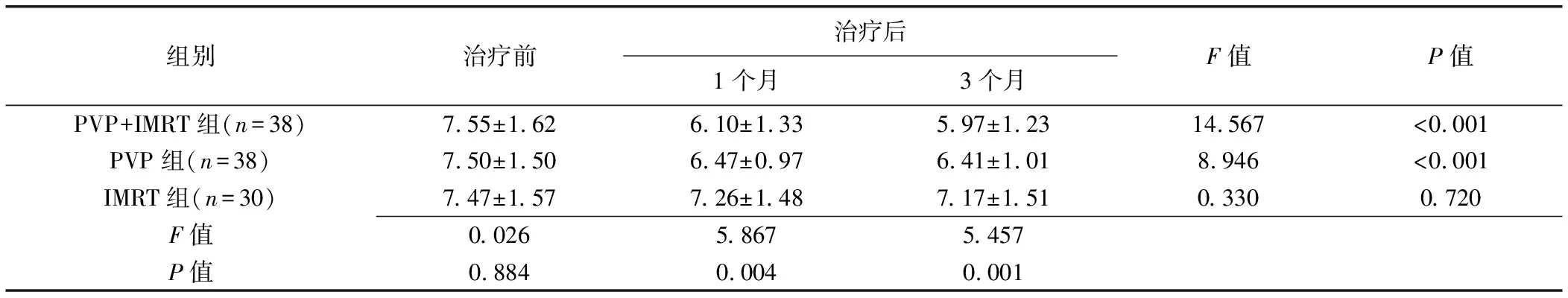
表4 3组各时间点SINS比较(±s)
组别治疗前治疗后1个月3个月F值P值PVP+IMRT组(n=38)7.55±1.626.10±1.335.97±1.2314.567<0.001PVP组(n=38)7.50±1.506.47±0.976.41±1.018.946<0.001IMRT组(n=30)7.47±1.577.26±1.487.17±1.510.3300.720F值0.0265.8675.457P值0.8840.0040.001
2.5 生存分析 截至随访结束,所有患者生存时间3~43个月,中位生存时间15个月[95%CI(13.25,16.74)]。PVP+IMRT组、PVP组、IMRT组中位生存时间分别为14个月[95%CI(11.93,16.07)]、15个月[95%CI(13.39,16.61)]、17个月[95%CI(14.54,19.46)],差异无统计学意义(P>0.05),见图3。椎体转移数目、脑或内脏转移、KPS、内科治疗均对生存期有显著影响(图4),脑或内脏转移、KPS、内科治疗分别为独立预后影响因素(表5)。
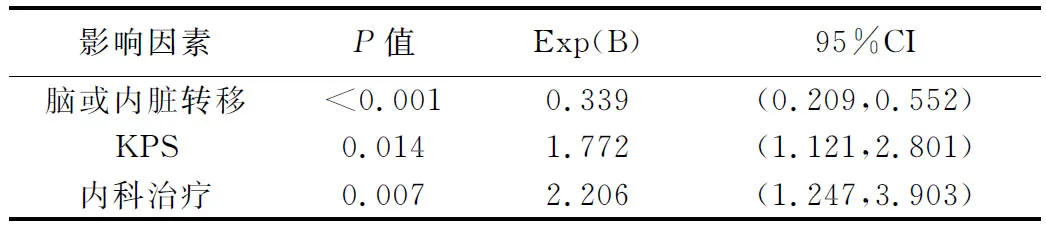
表5 Cox回归模型生存分析
2.6 不良反应 PVP+IMRT组骨水泥渗漏10例(10/38,26.32%),其中椎旁组织渗漏3例,椎间盘渗漏4例,椎弓根渗漏2例,1例发生轻度椎管渗漏,临床无神经系统损伤表现。PVP组骨水泥渗漏7例(7/38,18.42%),椎旁组织渗漏4例,椎间盘渗漏2例,椎旁静脉渗漏1例;2组渗漏率差异无统计学意义(χ2=0.680,P=0.410)。IMRT组放疗期间放射毒性主要为恶心、食欲减退,经对症处理均可耐受。
3 讨论
疼痛控制是治疗脊柱转移瘤的首要问题[4],其次是预防骨相关事件发生,目前56.0%~82.3%患者疼痛控制欠佳[5]。精确放射治疗(precision radiotherapy, PT)主要适用于脊柱尚稳定或未出现脊髓压迫症者,Miller等[6]报道,放射治疗脊柱肿瘤疼痛缓解中位时间为1个月,6个月和12个月局部有效率分别为63%和51%,疼痛进展中位时间为10个月;神经功能障碍[风险比(hazard ratio, HR)=2.48,P<0.01]和椎外骨转移(HR=2.83,P<0.01)与疼痛缓解相关。van der Velden等[7]认为SINS是影响疼痛缓解的主要因素,SINS越高疼痛缓解越差,单纯PT用于SINS<6分者。目前认为PVP主要通过维持椎体力学的稳定性缓解疼痛,其控制疼痛和改善椎体稳定性的有效率为71.8%~89.4%。Bao等[3,8]采用PVP治疗颈、胸椎转移瘤,止痛效果显著。Sun等[9]对43例脊柱转移瘤患者行PVP治疗,术后1、3、6、12个月的疼痛缓解率分别为89.7%、87.5%、86.9%及84.6%。本研究结果也表明,IMRT、PVP和两者联合均可有效止痛。
PT可有效控制局部肿瘤发展,但术后1~2周才达到最佳止痛效果,疼痛控制总有效率一般低于60%,约50%患者在6个月内出现疼痛复发,且不能减少骨相关事件发生。PVP可及时缓解疼痛、增加脊椎强度与稳定性,减少骨相关事件发生率[10],两者联合效果显著[5,11]。Huang等[4]对137例脊柱转移瘤患者分别行内放放射治疗(external radiotherapy, ERT)、PVP及ERT联合PVP治疗,疼痛缓解有效率分别为72.5%、76.3%及84.8%,ERT联合PVP改善神经压迫症状有效率为50%,ERT为18.2%,PVP为11.1%。本研究表明,PVP联合IMRT能更好地控制疼痛,且组内术后1、3、6、12个月VAS差异无统计学意义(P均>0.016 7),表明联合治疗止痛效果好。Yang等[11]认为PVP联合ERT治疗可提高局部抗肿瘤作用,而单纯ERT约需3周达到最好效果。本研究结果表明PVP联合IMRT可明显降低SINS,增加椎体稳定性,术后6个月3组局部进展率比较虽差异无统计学意义,而PVP+IMRT组病变进展率明显降低,提示PVP联合IMRT治疗脊柱转移瘤可在一定程度上控制肿瘤进展;但术后1、3个月组间KPS差异无统计学意义,提示在术后短期,联合治疗对维持功能、减轻疼痛仍起主要作用。

图33组Kaplan-Meier生存曲线图图4Log-rank分析显示内脏或脑转移情况(A),KPS(B),椎体转移数目(C)及内科治疗(D)对术后患者生存时间的影响
对于脊柱转移瘤患者,治疗前应首先评估其功能状态和预期寿命,其次应评价肿瘤负荷、肿瘤控制情况以及全身治疗是否有效,综合评价制定个体化治疗方案[5,12-13]。Petteys等[14]发现KPS是影响肾癌脊柱转移患者生存最重要的危险因素,其次是内脏转移和其他部位转移。Huang等[4]认为术前KPS及有无内脏或脑转移是影响患者生存期的重要因素。本研究Cox回归模型分析显示,脑或内脏转移、KPS、内科治疗分别为独立预后影响因素。
综上所述,PVP联合IMRT脊柱转移瘤疗效满意,可明显减轻患者疼痛,一定程度上提高局部控制率,改善患者生活质量。