水蒸气对甲烷燃烧影响的数值模拟研究
2019-11-18单天翔李自力
单天翔,崔 淦,李自力,王 顺
(中国石油大学(华东)储运与建筑工程学院,山东青岛266580)
随着中国经济的发展,天然气的开采量与进口量逐年增加。在工业生产与日常生活中所使用的甲烷气体难免会含有水蒸气,并且有时需要利用水蒸气对甲烷的燃烧进行抑制,所以水蒸气对于甲烷燃烧的影响值得研究。
水蒸气的加入会对甲烷燃烧的火焰温度、火焰传播速度等宏观表现产生影响,也会对燃烧的微观进程产生影响。S.Lee等[1]利用数值模拟研究了水蒸气对于甲烷-空气对冲火焰的火焰结构与熄火极限的影响,研究了压力对火焰最高温度的影响。A.Yoshida等[2,3]利用实验与数值模拟研究了水雾对于滞止流场中丙烷火焰的稳定性的影响,测量了流场中的火焰传播速度。H.H.Xu等[4]利用模拟和实验手段研究了水蒸气的化学效应、热效应、迁移效应和辐射效应对H-CO合成气燃烧火焰中OH自由基的影响,并对其进行了详细的动力学分析。朱清华等[5]利用数值模拟研究了水蒸气对甲烷燃烧中烟黑生成的影响,并从微观层面对影响机理进行了分析。J.P.C.Cano[6]等利用实验研究了不同压力下水蒸气对甲烷层流火焰传播速度的影响,并且利用Chemkin与Gri Mech 3.0机理分析了水蒸气对于甲烷燃烧的影响因素。R.E.Padilla等[7]利用实验与数值模拟研究了对冲火焰中燃料侧的水对燃烧的影响,研究结果表明,水主要影响O、H和OH自由基的产生和消耗过程,进而影响燃烧。M.Vicariotto等[8]利用预混火焰燃烧器研究了水蒸气对甲烷燃烧火焰的温度分布与熄火极限的影响,结果表明,随着水蒸气摩尔分数的升高,燃烧火焰峰值温度下降,当水蒸气摩尔分数在0.705~0.715时,火焰会熄灭。X.B.Shen等[9]研究了水蒸气对甲烷爆炸的影响,结果表明,在甲烷含量较高的情况下,水蒸气对爆炸过程有显著的抑制作用。在空气中含有饱和水蒸气时,甲烷的爆炸上限与爆炸下限分别为6%和14%,比普通甲烷/空气混合物的爆炸极限范围(5%~15%)略小。
在前人的研究中,未研究水蒸气对甲烷燃烧过程中不同自由基的作用规律,也未分析水蒸气对甲烷燃烧基元反应进程的影响,所以本研究利用数值模拟,研究了水蒸气对甲烷燃烧过程中基元反应的影响。利用Chemkin 17.0中的化学与相平衡反应模型计算不同水蒸气摩尔分数下甲烷燃烧的绝热火焰温度,并且利用预混层流火焰传播速度计算不同含水量下甲烷燃烧的预混火焰温度和预混火焰传播速度,分析水蒸气对于甲烷燃烧的宏观影响。然后利用预混层流火焰传播速度计算模型研究水蒸气对甲烷燃烧过程中的H、O、OH自由基浓度变化的作用规律,进而分析水蒸气对甲烷燃烧微观反应进程的影响。研究可为甲烷燃烧装置的设计、水蒸气对甲烷燃烧影响的实验研究提供帮助。
1 计算方法
在含水甲烷绝热火焰温度的模拟中,采用的模型是Chemkin 17.0中的化学与相平衡反应模型(Chemical and Phase Equilibrium Calculation),确定平衡的单元势能法[10]的基本理论是以吉布自由能的最小化为基础的,系统的吉布斯自由能为:


式中,gk为根据温度与压力计算出的单一物质k的吉布斯自由能,J/mol;T为温度,K;R为通用气体常数,J/(mol·K);Xk为k物质在系统中的摩尔分数。
在层流预混火焰的温度与传播速度的模拟中,采用的模型是Chemkin 17.0中的预混层流火焰传播速度计算模型(Premixed Laminar Flame Speed Calculation),该模型是用于模拟一维稳态等压层流预混火焰,其控制方程可简化为以下几个关系式:
连续性方程:

能量守恒方程:

组分守恒方程:

状态方程:

式中,x为坐标,m;M为质量流量,kg/s;Yk为物质k的质量分数;T为温度,K;u为混合物流速,m/s;Wk为物质k的摩尔质量,kg/mol;----W为混合物的平均摩尔质量,kg/mol;R为气体常数,J·/(mol·K);λ为导热系数,W/(m·K);cp为混合物定压比热容,J/(kg·K);ωk为物质k每单位体积的摩尔生成率,mol/(s·m3);hk为物质k的定焓,J/kg;υk为物质k的扩散速率,m/s;A为流管的截面积,m2。
对层流预混火焰模型进行简化分析[11],可推导出层流预混火焰传播速度公式:

式中,α为热扩散系数,m2/s,α=λ(ρucp)-1;υ为燃烧反应方程式中氧化剂的消耗量,kg;为燃料的平均反应速率,kg/(s·m3);ρu为未燃烧气体密度,kg/m3。该简化方法拟合了传热、传质理论,并且结合了化学动力学和热力学原理来分析层流火焰传播速度的影响因素。
通过查阅文献与燃烧学方面的资料,笔者最终在计算中选用Frenklach等学者编制的GRIMech3.0机理作为甲烷燃烧的详细化学反应机理[12],此机理包含53个组分,325个基元反应。
现有研究结果表明[13-15],在当量比为1.00~1.10时,甲烷-空气火焰的温度与火焰传播速度达到最大值,因此,在模拟计算中,选取当量比为1.05。在计算中,采用摩尔分数为0.79N2、0.21O2的混合气体模拟空气,忽略空气中的水蒸气与其他气体;甲烷的摩尔分数固定为0.10。在模拟计算中,选择压力为101.325 kPa、初始温度为298 K,分别计算绝热火焰温度、预混火焰温度和预混火焰燃烧速度,然后分析水蒸气的加入对于甲烷燃烧反应微观进程的影响。在本文的模拟中,水蒸气的摩尔分数选取0.10~0.30,具体配比见表1。

表1 甲烷/空气/水蒸气配比Table1 Configuration of methane/air/water vapor gas
2 计算结果
2.1 水蒸气对甲烷-空气火焰温度的影响
水蒸气对甲烷-空气燃烧的绝热火焰温度与预混火焰温度影响如图1所示。

图1 不同水蒸气摩尔分数下甲烷-空气火焰温度Fig.1 Methane-air flame temperature in different water mole fraction
从图1中可看出,在甲烷-空气混合气体中加入水蒸气后,其绝热火焰温度与预混火焰温度均有明显下降。随着水蒸气的摩尔分数增加,绝热火焰温度从2 189.7 K下降至1 821.1 K,预混火焰的温度从1 999.3 K下降至1 722.4 K。模拟结果表明,加入水蒸气后,绝热火焰温度与层流预混火焰温度出现不同程度地下降,水蒸气摩尔分数越大,对于甲烷-空气火焰的温度影响越大。在绝热火焰与预混火焰温度下降的同时,由于辐射以及对流所散失的热量也随之下降,导致二者的温度差变小。
2.2 水蒸气对甲烷-空气火焰燃烧速度的影响
在预混火焰燃烧过程中,通常定义了3种燃烧速度:
(1)层流火焰传播速度,是指层流火焰相对于静止燃烧壁面的运动速度。
(2)层流火焰膨胀速度,是指在封闭系统中,因燃烧产生的压力升高而引起燃烧产物膨胀的膨胀速度。
(3)层流火焰燃烧速度,是指反应区相对于未燃混合气的移动速度。
这3种速度中,层流火焰燃烧速度是研究燃烧机理的重要参数,是可燃预混合气的一种基本物理属性,是发展和验证燃料燃烧化学反应动力学机理的重要手段,它反映了预混燃料燃烧的基本特性,对化学反应动力学验证、燃烧模型建立、燃烧器设计和火灾研究有重要意义[16]。因此,在模拟计算中,采用层流火焰燃烧速度来分析水蒸气对于甲烷-空气火焰传播的影响。水蒸气对甲烷-空气燃烧的层流预混火焰燃烧速度影响见图2。

图2 不同水蒸气摩尔分数下甲烷-空气层流预混火焰燃烧速度Fig.2 Methane-air laminar flame speed in different water mole fraction
从2图可看出,在甲烷-空气混合气体中加入水蒸气后,其层流预混火焰燃烧速度明显下降,模拟结果与A.N.Mazas等[17]的实验规律一致。随着水蒸气的摩尔分数增加,预混火焰燃烧速度从36.999 cm/s下降至10.247 cm/s,下降率为72.3%。模拟结果表明,加入水蒸气后,层流预混火焰的燃烧速度被不同程度地减慢了,水蒸气摩尔分数越大,对于甲烷-空气层流预混火焰的燃烧速度影响越大。
3 化学动力学分析
3.1 水蒸气对OH、O、H自由基浓度的影响
在甲烷的燃烧过程中,其主线是从OH、O、H自由基撞击甲烷分子产生甲基自由基开始的[18],并且在其他反应中,这些自由基仍然会参与其中。因此,OH、O、H自由基的浓度是影响甲烷燃烧过程的重要因素。在燃烧过程中,不同含水量下的自由基浓度变化如图3所示。

图3 H2O对各种自由基的影响Fig.3 The influence of H2O on every free radical
从图3中可看出,随着水蒸气摩尔分数的增加,在层流预混火焰中生成的H、O、OH自由基的摩尔分数均显著下降,其中H自由基最高摩尔分数下降了76.8%,O自由基最高摩尔分数下降了84.4%,OH自由基最高摩尔分数下降了57.1%。水蒸气摩尔分数越大,H、O、OH自由基摩尔分数下降比例越大,这与李成兵等[19]对于水蒸汽对甲烷爆炸过程中自由基浓度影响的数值计算结果相同。然而,在各自由基摩尔分数下降的同时,OH自由基所占的比例随着水蒸气摩尔分数的增加而上升。
3.2 水蒸气对甲烷燃烧基元反应的影响
H、O、OH自由基摩尔分数的变化会影响甲烷燃烧的基元反应,因为OH自由基所占比例增加,所以OH自由基对于甲烷燃烧基元反应的影响上升。在分析水蒸气对于甲烷燃烧微观反应进程影响的模拟计算中,利用不含水蒸气的甲烷与CH4/H2O(g)(物质的量比为1∶3)的含水甲烷燃烧反应路径进行分析。模拟计算结果表明,甲烷燃烧中水蒸气主要消耗反应为[12]:
2OH↔O+H2O(R86)
在甲烷燃烧反应中,OH自由基主要生成反应为R38,随着水蒸气的增加,反应R86被强化,同时,甲烷中的水蒸气会降低氧气所占的比例,这会抑制反应R38的进行。
H+O2↔O+OH(R38)
图4所描述的是两种情况下甲烷燃烧反应中CH3自由基的生成与消耗速率,两种情况下,CH3主要的生成反应是R53与R98:
OH+CH4↔CH3+H2O(R98)
H+CH4↔CH3+H2(R53)
在无水甲烷的燃烧过程中,CH3自由基主要的消耗反应为R10:
O+CH3↔H+CH2O(R10)
从反应R86可看出,随着甲烷中水蒸气摩尔分数的增加,OH自由基所占的比例上升,致使反应R98在CH3生成的反应中所占比例显著上升。相应的,CH3自由基主要的消耗反应变为R97:
OH+CH3↔CH2(s)+H2O(R97)
对比图4可看出,相比无水甲烷的燃烧,含水甲烷燃烧过程中反应R119消耗的CH3所占比例有所提高,会有较多比例的CH3自由基转化成CH3O自由基。
HO2+CH3↔CH3O+OH(R119)
水蒸气对于CH3基团的消耗反应路径有较大影响:在无水甲烷燃烧过程中,CH3基团主要经过反应R10生成CH2O基团;在含水甲烷燃烧中,CH3基团主要生成CH2(s)基团,且生成较多的CH3O基团。计算结果表明,含水甲烷燃烧过程中生成的CH2(s)会进一步反应,主要经过反应R148生成CH2;生成的CH2会继续参与反应进程,主要经过反应R126生成CH。
H2O+CH2(s)↔H2O+CH2(R148)
H2+CH↔H+CH2(R126)

图4 不同条件下CH3自由基的生成速率Fig.4 CH3rate of production in different conditions
图5所描述的是两种情况下甲烷燃烧反应中CH自由基的生成与消耗速率,在两种情况甲烷燃烧过程中,CH的主要生成反应为R126。
H2+CH↔ CH2+H(R126)
在CH消耗过程中,水蒸气的加入会改变反应进程。当甲烷中没有水蒸气时,CH主要通过反应R125消耗,转化成HCO基团;当甲烷中加入水蒸气时,反应R127被强化,致使CH基团主要转化成CH2O基团。
O2+CH↔ CHO+O(R125)
H2O+CH↔ CH2O+H(R127)

图5 不同条件下CH自由基的生成速率Fig.5 CH rate of production in different conditions
图6所描述的是两种情况下甲烷燃烧反应中CH2O自由基的生成与消耗速率,在两种情况的甲烷燃烧过程中,CH2O主要生成反应为R10,在加入水蒸气后,反应R57所占比例明显上升,这是因为反应R119被强化,从而使较多比例的CH3转化成CH2O,使反应R57被增强。
O+CH3↔CH2O+H(R10)
H+CH2O↔CH3O(R57)
在两种情况下,CH2O自由基均生成了HCO自由基,对比图6可看出,在无水甲烷燃烧过程中,CH2O主要通过R58反应被消耗;在含水甲烷燃烧反应中,CH2O主要通过R101反应被消耗。这是因为当甲烷中加入水蒸气后,反应生成的O、H、OH自由基中OH自由基所占的比例增大,H自由基所占的比例减小,促进了反应R101的进行。
H+CH2O↔HCO+H2(R58)
OH+CH2O↔HCO+H2O(R101)
在甲烷燃烧过程中,HCO主要通过反应R166和R168氧化成CO。在无水甲烷燃烧过程中,反应R166与反应R168在HCO的消耗反应中所占比例相当;在含水甲烷燃烧过程中,因为水蒸气浓度的上升,反应R166被强化,同时,因为氧气所占的比例下降,反应R168在HCO消耗反应中所占比例下降。
HCO+H2O↔H+CO+HO2(R166)
HCO+O2↔HO2+CO(R168)
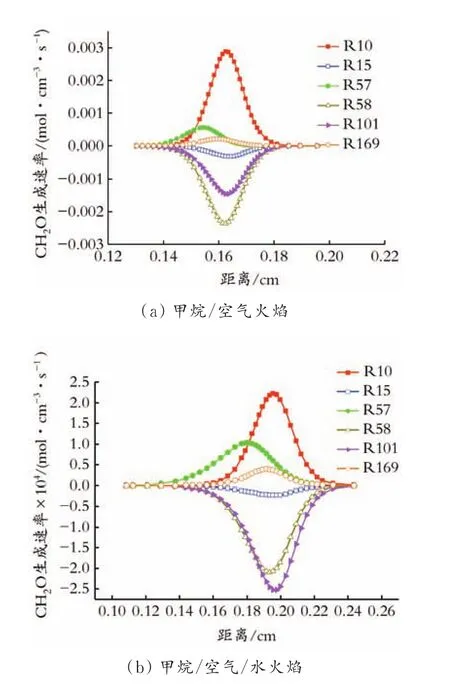
图6 不同条件下CH2O自由基的生成速率Fig.6 CH2O rate of production in different conditions
最后,CO经过反应R99被氧化成CO2,因为水蒸气的加入会降低OH自由基的浓度,所以,在含水甲烷中,R99的反应速率下降。
OH+CO↔H+CO2(R99)
从上述模拟结果中可看出,水蒸气的加入会改变甲烷燃烧过程中的微观反应进程。在无水蒸气加入时,甲烷燃烧的主要反应过程为CH4→CH3→CH2O→HCO→CO→CO2;加入水蒸气后,强化了CH3→CH2(s)→CH2→CH→CH2O 过程,同时强化了CH3→CH3O→CH2O过程。发生这些转变的原因是因为随着水蒸气的加入,OH自由基在所有自由基中所占的比例增加,强化了OH自由基传递的链式反应进程。
4 结 论
(1)随着甲烷中水蒸气摩尔分数的增加,甲烷燃烧的预混火焰温度与绝热火焰温度均有明显的下降,绝热火焰温度从2 189.7 K下降至1 821.1 K,预混火焰的温度从1 999.3 K下降至1 722.4 K。同时,预混火焰燃烧速度明显下降,从36.999 cm/s下降至10.247 cm/s。
(2)随着甲烷中水蒸气摩尔分数的增加,作为链传递者的O、H、OH自由基摩尔分数均下降,这导致链式反应速率的下降,从而导致其他自由基摩尔分数下降、甲烷燃烧的反应速率减小。但是,在3种自由基中,OH自由基所占比例随着水蒸气摩尔分数的上升而上升,导致因OH传递的链式反应所占的比例上升。
(3)随着甲烷中水蒸气摩尔分数的增加,OH自由基在链传递自由基中所占比例上升,强化了甲烷燃烧链式反应中CH3→CH2(s)→CH2→CH→CH2O过程,同时强化了CH3→CH3O→CH2O过程,提高了甲烷燃烧反应中以OH为载体所进行的基元反应比例。
