大鼠血浆中桑色素的浓度测定及其药动学研究
2019-11-05姚庆强邓志鹏
柳 佳,姚庆强,邓志鹏
(1.济南大学 山东省医学科学院 医学与生命科学学院,山东 济南250200;2.山东省医学科学院 药物研究所,山东 济南250062;3.国家卫生部生物技术药物重点实验室,山东 济南250062;4.山东省罕少见病重点实验室,山东 济南250062)
桑白皮为桑科植物桑(Morus albaL.)的干燥根皮,是一味传统中草药,主要分布于我国安徽、河南、河北、湖南、四川、广东等地,具有泻肺平喘,利水消肿的功效[1]。现研究表明,桑白皮具有镇咳平喘[2]、抗炎[3]、降血糖[4-5]和降血脂[6]的作用。桑白皮的化学成分繁多,主要包括黄酮类化合物、芪类化合物、Diels-Alder型加合物和多糖类化合物等[7]。桑色素(morin)是从桑白皮(Mori cortex)中分离得到的黄酮类化合物[8]。近年,实验发现桑色素具有抗癌、抗高尿酸血症和消炎作用[9],但尚未有关于桑色素的药动学研究。本文建立了一种快速、高灵敏度、高选择性的超高效液相色谱-质谱联用方法(UPLC-MS/MS)测定桑色素在大鼠血浆中的浓度,并将其应用于大鼠体内的药动学研究。
1 仪器与材料
1.1 仪器
Shimadzu Prominence 超高效液相色谱仪(日本岛津公司);AB SCIEX Q-TRAP 5500 型质谱仪,包括电喷雾离子源(ESI),Analyst®1.6.3数据采集和处理系统(美国 AB SCIEX 公司);EVA50A型多功能样品浓缩仪(北京普利泰科仪器公司);Sorvall Biofuge Stratos高速冷冻离心机(赛默飞世尔);EL204电子天平(梅特勒-托利多);IKA Vortex天才3旋涡混匀器(广州艾卡仪器设备公司)。
1.2 试剂
桑色素标准品(批号:HMO52276198,纯度:98.87 %,宝鸡辰光);芫花素标准品(内标物质,纯度:94.2 % ,中国食品药品检定研究院);丙二醇(分析纯,批号:20170901,南京威尔药业);甲醇(色谱纯,批号:18075174,美国TEDIA公司);乙腈(色谱纯,批号:164791,赛默飞世尔);甲酸为(色谱纯级别,天津科密欧);实验用水为娃哈哈纯净水,其他试剂均为分析纯。
1.3 实验动物
5只健康雄性Sprague-Dawley大鼠,体重200±20 g,购自济南朋悦动物繁育公司,许可证号为SCXK(鲁)20140007。实验期间大鼠在恒定环境下饲养,饲养温度为23±3 ℃,相对湿度为55 %±15 %,自由饮食饮水。
2 方法与结果
2.1 色谱条件及质谱条件
2.1.1 色谱条件 采用Thermo Hypersil GOLD-C18(50 mm×4.6 mm,3 μm)色谱柱对待测样品和内标化合物进行分离,流动相为0.1 % 甲酸水溶液(A)-乙腈(B),梯度洗脱,洗脱程序为:0~2.5 min,70 % B→90 % B;2.5~2.6 min,90 % B→7 %B;2.6~5.0 min,70 % B;流速设定为0.5 ml/min,柱温设为40 ℃,自动进样器温度为15 ℃,进样量2 μl。
2.1.2 质谱条件 采用电喷雾离子源,选用负离子检测方式,扫描方式为多反应监测(MRM)。气帘气(CUR)设定为35 psi,碰撞气设为medium,离子源喷雾电压(IS)设为-4500 V,离子源温度(TEM)设为 550 ℃,雾化气压力(Gas 1)设为 55 psi,加热气压力(Gas 2)设定为55 psi。通过切换阀的切换, 每次运行仅记录1.0~5.0 min 的MS/MS 数据。桑色素和内标的定量离子分别为m/z300.9→151.2和m/z283.1→268.2,同时将m/z300.9→125.1作为桑色素的定性离子对。桑色素和芫花素的二级MS图谱见图1。
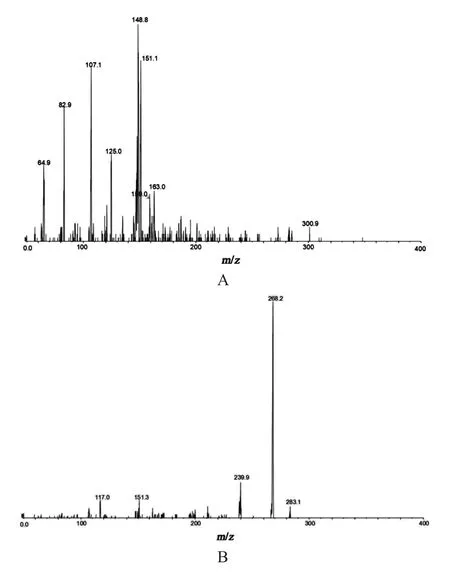
图1 桑色素和芫花素的MS图谱
2.2 溶液的制备
2.2.1 大鼠灌胃溶液的配制 精密称取桑色素标准品4.41 mg,加丙二醇10 ml,超声,然后边涡流边缓慢滴加10 ml水,得到桑色素单体的大鼠灌胃溶液(浓度为218.01 μg/ml)。
2.2.2 标准溶液的配制 精密称取桑色素标准品5.10 mg,用甲醇1 ml溶解,配制成5.10 mg/ml的储备溶液,-80 ℃贮存。临用前先超声,再用乙腈逐步稀释获得系列标准溶液后待用。精密称取芫花素标准品2.88 mg,加入甲醇6 ml,超声溶解,并用乙腈逐步稀释成浓度为50 ng/ml的内标工作溶液。
2.3 血浆样品的处理方法
取50 μl内标溶液,置入1.5 ml EP管,依次加入50 μl血浆样品和100 μl乙腈,涡旋振荡5 min,6 ℃条件下以13 000 r/min的转速离心5 min,取上清进样,进样量2 μl。
2.4 方法学验证
参照FDA[10]和中国药典2015版的指导原则[11],对本文建立的UPLC-MS/MS方法进行方法学验证,包括选择性、标准曲线、精密度和准确度、提取回收率、基质效应和稳定性等。
2.4.1 选择性 分别取6份来自不同批次的大鼠空白血浆样品、含桑色素和内标的标准血浆样品及给药10 min后的大鼠血浆样品进行 UPLC-MS/MS 分析。结果显示,空白血浆中无内源性杂质干扰,桑色素和内标化合物的峰形良好且互不干扰,保留时间分别为1.33,1.68 min。在高浓度样品之后测定大鼠空白血浆样品,其残留不影响桑色素和内标的含量测定。
2.4.2 标准曲线 将桑色素的储备溶液用乙腈逐步稀释成浓度为20.2,40.3,100.8,403.4,1008.4,4033.6,10084 ng/ml的系列对照品溶液。取对照品溶液10 μl,加入190 μl大鼠空白血浆,最终得到浓度分别为1.01,2.02,5.04,20.2,50.4,201.7,504.2 ng/ml的对照血浆样品溶液。按2.3项方法处理上述血浆样品后进行UPLC-MS/MS分析,连续测定3 d,记录峰面积。以桑色素的浓度(ng/ml)作为横坐标(x),桑色素峰面积和内标峰面积的比值作为纵坐标(y),权重因子采用1/X2进行线性回归分析,得到桑色素的线性回归方程,其回归方程为y=1.46×10-3x+2.82×10-3(r=0.9953),线性范围为1.01~504.2 ng/ml,定量下限为1.01 ng/ml,其精密度RSD≤7.24 %,RE≤-1.19 %,满足生物样品测定的方法学要求。
2.4.3 精密度与准确度 将桑色素的储备溶液用乙腈逐步稀释,得到低、中、高浓度的质控样品溶液,桑色素的浓度分别为40.4,606,8068 ng/ml。取10 μl质控样品溶液,加入190 μl大鼠空白血浆,涡旋振荡并离心,最终得到血浆浓度为2.02,30.3,403.4 ng/ml的质控血浆样品。将质控血浆样品按2.3项方法处理并进样分析(每个浓度进样5次,连续测定3 d),计算同一浓度下的精密度和准确度,得到日内精密度RSD≤9.04%,RE≤10.06 %;连续测定3 d,其日间精密度RSD≤6.10 %,RE≤10.40 %。
2.4.4 提取回收率和基质效应 取50 μl内标溶液,依次加入50 μl低、中、高3个浓度的质控血浆样品溶液和100 μl乙腈(重复6份),按2.3项方法处理,取上清进样分析,记录桑色素及内标的峰面积(Am,AIS);另取50 μl空白血浆,加入150 μl乙腈,涡流混合5 min,13 000 r/min离心5 min,取全部上清,氮气吹干,用 50 μl内标溶液和50 μl桑色素溶液(浓度分别为2.02,30.3,403.4 ng/ml)对其进行复溶(重复6份),涡流混合后进行UPLCMS/MS分析,记录桑色素及内标的峰面积(Bm,BIS)。桑色素和内标的回收率用峰面积之比A/B计算。桑色素的回收率为85.3 %~92.9 %,内标的回收率为91.2 %。另取50 μl纯水和150 μl乙腈,涡流混合后经氮气吹干,再加入50 μl内标溶液和50 μl桑色素溶液(浓度为2.02,30.3,403.4 ng/ml),按2.3项方法处理,平行测定6份,记录桑色素和内标的峰面积(Cm,CIS)。分别以峰面积的比值B/C计算桑色素和内标的基质效应。桑色素的基质效应为91.6 % ~ 105.9 %,内标为103.1 %。由结果可见,大鼠血浆中的基质对桑色素的离子作用很微弱,不影响结果的准确性,可忽略。
2.4.5 稳定性试验 桑色素分别于-80 ℃放置7 d、-80 ℃反复冻融3次、室温放置6 h、自动进样器(15℃)中放置12 h。按2.3项方法处理后进行UPLCMS/MS分析,平行测定3次。结果RSD≤15 %,RE≤15 %,表明桑色素在上述4种环境下均保持稳定。
2.5 大鼠药动学研究及结果
大鼠按2.186 mg/kg灌胃给药,给药前禁食12 h,自由饮水。分别在给药后0.083,0.167,0.5,0.75,1,1.5,2,3,5,8,12,24 h于眼底静脉丛取血约300 μl,置入肝素化的EP管,13 000 r/min离心3 min,取上层血浆,置-80 ℃保存待测。
按2.1项条件,采用UPLC-MS/MS测定大鼠血浆中桑色素的浓度,采用DAS2.1.1软件进行拟合,得到血药浓度-时间曲线(见图2)和主要的药动学参数(见表1)。大鼠灌胃给予桑色素单体后,药-时曲线下面积(AUC0-∞)为375.8±265.7 μg/L·h,消除半衰期(t1/2z)为3.27±1.26 h,达峰时间(Tmax)为0.167±0.00 h,药峰浓度(Cmax)为234.2±45.8 μg/L。

图2 大鼠体内桑色素的血药浓度-时间曲线(n=5)
3 讨论
本实验比较了桑色素在水-甲醇、水-乙腈、0.1 % 甲酸水溶液-乙腈及含10 mmol/L乙酸铵的0.1 % 甲酸水溶液-乙腈4种流动相条件下的分离效果,流动相为0.1 % 甲酸水溶液-乙腈时桑色素和内标的分离效果最好。通过比较桑色素在ESI下正、负两种离子的检测方式,发现桑色素在负离子模式下的响应明显高于正离子,所以本实验选择在负离子检测方式下进行。在负离子检测模式下,对桑色素进行二级MS分析,得到桑色素的主要碎片离子为m/z300.9→151.2和m/z300.9→125.1,内标的主要碎片离子为m/z283.1→268.2。分别将m/z300.9→151.2,m/z283.1→268.2作为桑色素和内标的定量离子,同时采用m/z300.9→125.1对桑色素进行定性分析。在负离子条件下对桑色素和内标的各质谱参数进行优化。结果如下:桑色素的去簇电压(DP)、射入电压(EP)、碰撞室射出电压(CXP)、碰撞能(CE)分别为50 V,15 V,15 V和 28 V,内标的去簇电压(DP)、射入电压(EP)、碰撞室射出电压(CXP)、碰撞能(CE)分别为65 V,15 V,50 V和32 V。
表1 桑色素的主要药动学参数(±s,n=5)
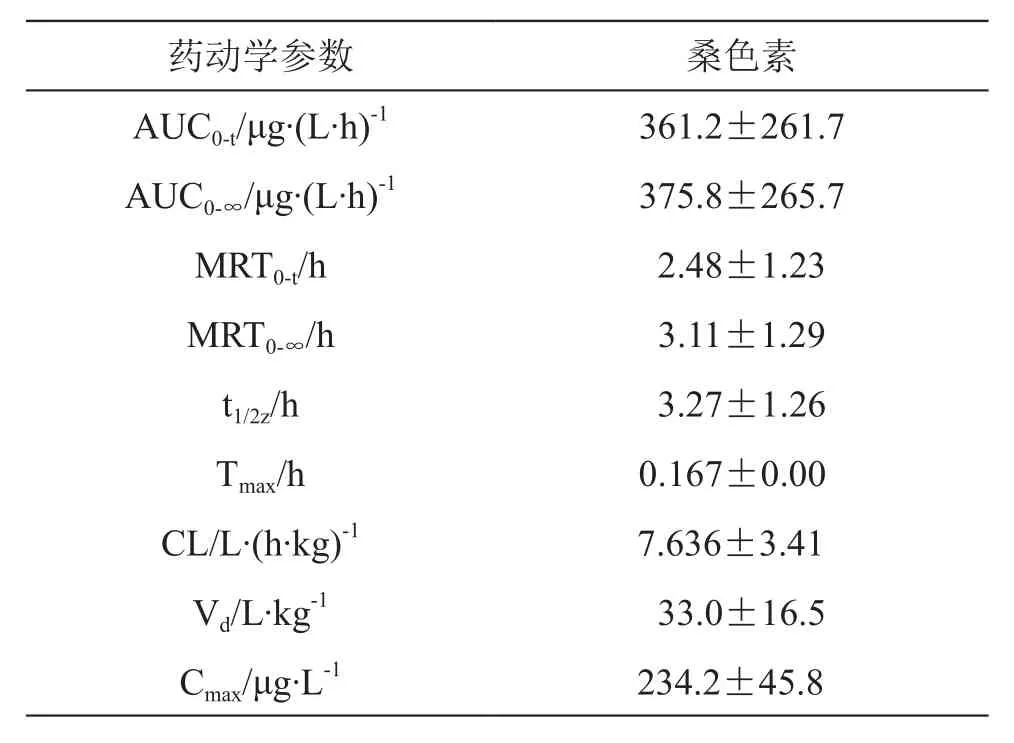
表1 桑色素的主要药动学参数(±s,n=5)
药动学参数桑色素AUC0-t/μg·(L·h)-1361.2±261.7 AUC0-∞/μg·(L·h)-1375.8±265.7 MRT0-t/h2.48±1.23 MRT0-∞/h3.11±1.29 t1/2z/h3.27±1.26 Tmax/h 0.167±0.00 CL/L·(h·kg)-1 7.636±3.41 Vd/L·kg-133.0±16.5 Cmax/μg·L-1 234.2±45.8
4 结论
本实验考察了SD大鼠灌胃给予桑色素单体后的药动学性质,结果表明,桑色素在大鼠体内呈非线性动力学特征,且其在大鼠体内吸收速度较快,大鼠灌胃给药0.167 h即达血药峰浓度(Cmax)。本文建立了一种测定大鼠血浆中桑色素浓度的UPLCMS/MS方法,该方法操作简便、前处理简单、稳定性良好且回收率较高,可用于生物样品中桑色素含量的测定,为桑色素的进一步研究提供帮助和支持。
