基于植酸锆/普鲁士蓝复合膜的电催化行为研究
2019-11-01黄新花董洁郭小玉文颖杨海峰
黄新花 董洁 郭小玉 文颖 杨海峰


摘 要: 通过层层自组装技术,构建植酸锆/普鲁士蓝(ZrIP6/PB)多层结构膜.基于普鲁士蓝(PB)对双氧水(H2O2)有很高的电催化性能,加之5层植酸锆/普鲁士蓝膜多孔结构有利于传质过程,该H2O2传感器具有高灵敏度和高选择性.实验结果显示:修饰电极对H2O2响应的物质的量浓度范围为2.00×10-5 ~1.76×10-3 mol·L-1,线性相关系数R=0.998 9.
关键词: 植酸锆; 普鲁士蓝(PB); 双氧水(H2O2)传感器; 自组装
中图分类号: O 647.3 文献标志码: A 文章编号: 10005137(2019)04041208
Abstract: The zirconium phytate/Prussian blue(ZrIP6/PB) multilayer structure film was constructed by layerbylayer selfassembly technology.Since Prussian blue(PB) has high electrocatalytic performance for H2O2,and the 5layer ZrIP6/PB membrane with porous structure is beneficial to the mass transfer process,the asprepared hydrogen peroxide sensor shows high sensitivity and selectivity.The result showed that the linear concentration response range of such modified electrode on H2O2 is from 2.00×10-5 to 1.76×10-3 mol·L-1,and the linear correlation coefficient (R) is 0.998 9.
Key words: zirconium phytate; Prussian blue(PB); H2O2 sensor; selfassembly
0 引 言
近年来,普鲁士蓝(PB)或铁氰化物以其独特的电化学、光学和电磁学等性质受到人们的广泛关注[1-2].由于PB对于双氧水(H2O2)的电催化具有高灵敏度和高选擇性[3-5],而被人们称为“人工过氧化物酶”[6],研究人员尝试通过不同的方法将其制备成修饰电极,用于制备各种电化学传感器.
其中,研究较多的方法是电化学沉积法,此方法虽然操作简单,但受操作方法的影响,所制备的修饰电极不具备很好的微观结构,从而影响了传感器的各项响应性能.RAMSDEN等[7]提出的聚合物静电自组装方法,主要原理是基于带不同电荷的聚电解质之间的静电力作用.这种方法具有制备简单、结构可控、较稳定等优点,在近年得到了广泛应用.基于此,研究人员利用Fe(CN)63-和Fe2+以及Fe(CN)64-和Fe3+之间的静电作用,研究了静电自组装PB膜的制备[8-9].
利用磷酸基团与金属离子之间的络合作用及静电作用,通过层层自组装的方法制备硫酸钛的工作已有报道[10].这种方法操作方便、厚度可控,而且制备的PB膜机械强度好.另外,将硫酸钛和PB结合到制备的复合物膜中,由于硫酸钛具有良好的离子交换和离子传递能力[11-13],阳离子容易在膜中扩散,因此,复合物膜具有比单纯PB膜更好的电荷转移能力;同时由于PB膜的导电能力,加速了复合物膜的电子转移能力[14].本文作者主要利用磷酸基团与金属离子的强络合作用及相反电荷离子间的静电作用,通过层层自组装的方法制备了植酸锆/普鲁士蓝(ZrIP6/PB)复合膜修饰电极,并与单纯PB膜进行比较,研究其电化学催化H2O2行为,考察传感器性能.
1 实验部分
1.1 实验试剂
ZrOCl2·8H2O(分析纯,国药集团化学试剂有限公司);植酸钠(IP6,分析纯,Aldrich公司);磷酸盐缓冲溶液(PBS)由KH2PO4和Na2HPO4调配而成,不同pH的缓冲溶液用0.1 mol·L-1的NaOH与H3PO4调节得到;FeCl3·6H2O和K4[Fe(CN)6]·3H2O(分析纯,国药集团化学试剂有限公司);所有实验用水均为超纯水(电阻率大于18 MΩ·cm).
1.2 实验仪器
CHI660d型电化学工作站(上海辰华仪器有限公司);H011B型恒温磁力搅拌器(山海梅颖浦仪器仪表制造有限公司);FE20型pH计(上海梅特勒-托利多仪器有限公司);SK2200H型超声清洗器(上海科导超声仪器有限公司).
1.3 ZrIP6/PB复合膜修饰电极的制备
玻碳电极(GCE)用金相砂纸打磨,超纯水超声清洗,然后用直径为0.3 μm的αAl2O3粉末在麂皮上将电极抛成镜面,分别用超纯水、乙醇、超纯水超声清洗后,用氮气(N2)吹干获得干净的电极表面.
将处理干净的GCE浸在用超纯水配制的聚二烯丙基二甲基氯化铵(PDDA)溶液中,组装20 min后取出,用水轻轻冲洗晾干后,得到表面带有正电荷的修饰电极.将PDDA修饰的GCE浸入到10 mmol·L-1的ZrOCl2 酸性溶液中,5 min后将其浸入1×10-2 mol·L-1的植酸钠(pH=4)溶液中,10 min后,洗净、晾干,即得到一层植酸锆修饰的GCE.将植酸锆修饰的GCE浸入10 mmol·L-1 FeCl3溶液中,5 min,去离子水冲洗,晾干后浸入10 mmol·L-1 K4[Fe(CN)6]溶液中,5 min,用去离子水冲洗、晾干,即得到一层ZrIP6/PB修饰的GCE.重复上述过程,即得到不同层数ZrIP6/PB修饰的GCE.制得的修饰电极记作(ZrIP6/PB)n/PDDA/GCE电极,n表示层数.
将修饰有PDDA的GCE分别在10 mmol·L-1 FeCl3溶液和10 mmol·L-1 K4[Fe(CN)6]溶液中各浸泡5 min,即得到单层PB膜修饰的GCE.重复此过程得到多层PB膜修饰的GCE,记作PBn/PDDA/GCE.
1.4 电化学测量方法
采用三电极系统,修饰电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极,循环伏安和计时电流测试前,向一定量的磷酸盐缓冲溶液中通入高纯N2 20 min,以除去溶液中的氧气(O2).
2 结果和讨论
2.1 ZrIP6/PB复合膜修饰电极的直接电化学
根据本课题组先前工作中对ZrIP6的扫描电镜表征结果[15],其在电极表面的形貌呈现三维多孔结构,有利于PB的修饰和在一定反应体系内反应物的传质.图1是不同扫速下,(ZrIP6/PB)5/PDDA/GCE修饰电极在0.1 mol·L-1 KCl 溶液中的循环伏安曲线.从图1中可以看出,修饰电极在KCl 溶液中有一对明显的氧化还原峰.由于植酸锆是电化学惰性的,这对峰来源于PB中Fe (Ⅲ/Ⅱ) 的氧化还原反应.随着扫速的增大,氧Symbol~A@50 mV·s-1范围内,氧化还原峰电流均与扫描速度平方根呈线性关系,结果如图1内插图所示,说明在该扫描速率范围内电极反应是一个扩散控制的过程.也进一步确定了PB已固定到电极上,并且发生了直接的电子传递反应.
2.2 峰电流与修饰层数的关系
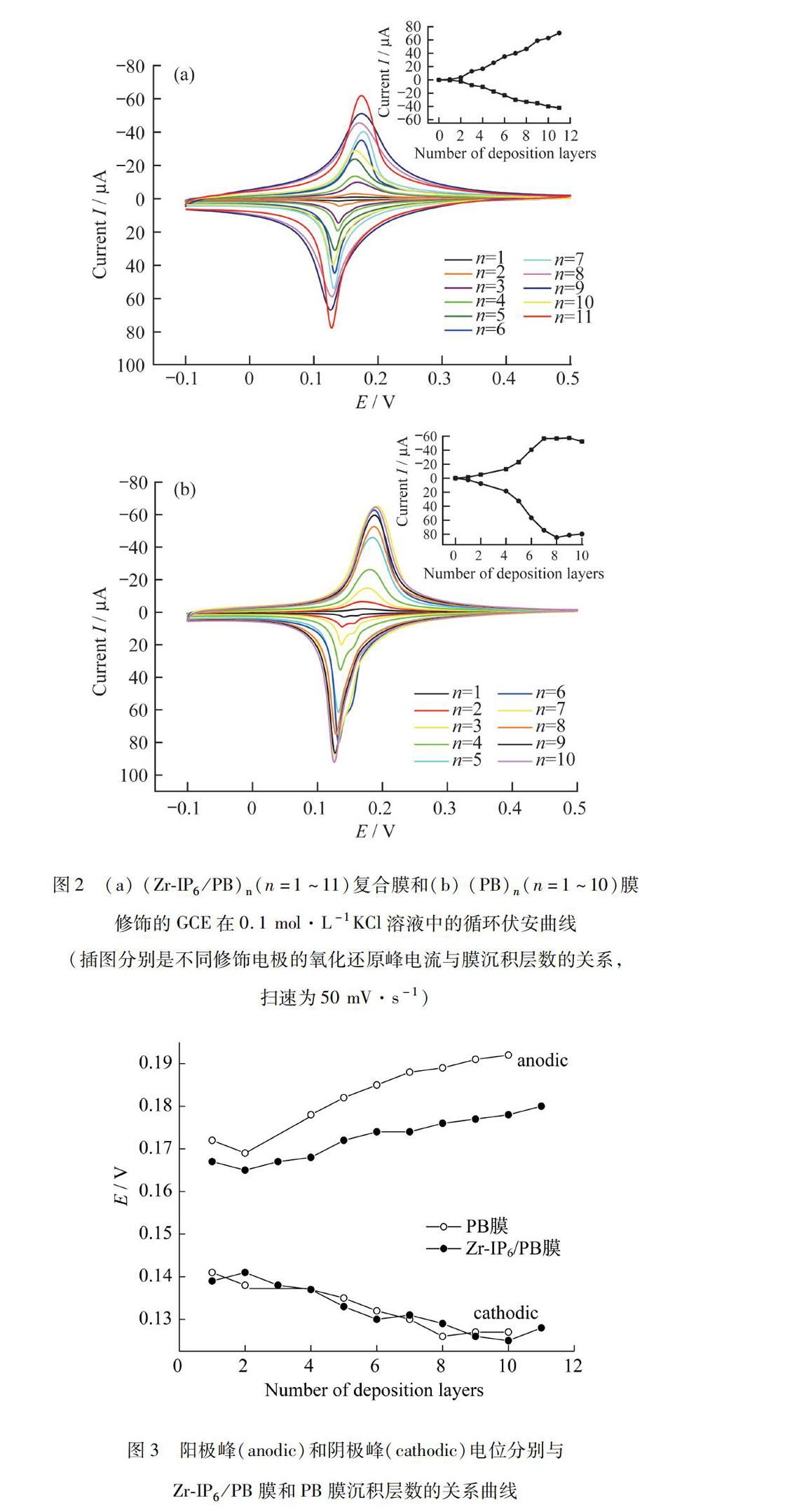
图2(a)是不同层数ZrIP6/PB复合膜修饰电极在0.1 mol·L-1 KCl溶液中的循环伏安曲线.在-0.1~0.5 V扫描电位内,只组装一层植酸锆的GCE没有氧化还原峰(数据未给出),证明植酸锆/PDDA在这个电位范围内是电化学惰性的.继续组装一层PB后,在163 mV和207 mV处可看到一对明显的氧化还原峰.同时,随着ZrIP6/PB膜沉积层数的增加,氧化还原峰电流不断增加,证明即使在ZrIP6/PB膜很厚的情况下,PB与电极间的直接电子转移依然较容易实现.修饰层数较多时,峰型及峰电位略微发生变化,其原因可能是植酸锆不导电,层数过多,不利于传质过程和电子传递.单纯PB膜修饰的GCE的氧化还原峰电流与沉积层数的关系如图2(b)所示.由图2(b)可见,氧化还原峰电流也随着PB膜层数的增加而增大,但当PB膜达到8层后,峰电流基本不变,甚至降低.以上结果表明:与单纯PB膜修饰的GCE相比,ZrIP6/PB复合膜修饰电极中的ZrIP6促进了PB与电极间的电子转移,这是由于ZrIP6膜能够促进PB电化学反应过程中的抗衡离子在ZrIP6/PB复合膜中的扩散.
2.3 峰电位与修饰层数的关系
图3是ZrIP6/PB膜和PB膜修饰电极上阴阳极峰电位与沉积层数的关系曲线.随着沉积层数的增加,2种膜修饰电极的阳极峰电位均增加,阴极峰电位降低.说明沉积层数的增加使电子转移变得困难,即电阻增大.主要有2个原因:1)沉积层数增加,使电极表面膜厚度增加,活性中心与电极间的距离增加;2)膜厚度增加,抗衡离子在修饰膜间的扩散受阻程度增大,所以峰间距增大.但是相同沉积层数下,ZrIP6/PB膜修饰电极的峰间距明显小于PB膜修饰电极,证明在ZrIP6/PB膜中PB能够更快地传递电子.
2.4 pH条件优化
由于PB易在中性和弱碱性溶液中溶解,研究了修饰电极(ZrIP6/PB)10/PDDA/GCE在不同pH的PBS溶液中的电化学行为,结果如图4所示.从图4中可以看出,在pH为4~8范围内,随着pH增加,氧化还原峰电流降低,且当pH为7时,峰电流降低明显,所以在接下来的电化学实验中,选择pH为6的PBS溶液作为电解质溶液.
2.5 (ZrIP6/PB)5/PDDA/GCE催化过氧化氢
图5为(ZrIP6/PB)5/PDDA/GCE修饰电极对H2O2的电催化还原行为的研究.在PBS中加入H2O2后,曲线峰形有很大的改变,与空白值0相比,随着加入H2O2物质的量浓度不断增大,曲线还原峰电流增大,氧化峰电流减小.由此可见,ZrIP6/PB复合膜修饰电极对H2O2有良好的电催化还原作用.
2.6 计时电流响应
图6是修饰电极(ZrIP6/PB)5/PDDA/GCE在工作电位为-210 mV下,向不断搅拌的PBS溶液(pH 6.0)中连续加入H2O2时的计时电流曲线.由图6可见,随着H2O2浓度的不断增加,还原电流逐渐增大.插图是修饰电极的响应电流与H2O2浓度的标准曲线.实验结果显示:修饰电极对H2O2响应的浓度范围为2.0×10-5~1.76×10-3 mol·L-1,线性相关系数R =0.9989,最低检測限为1.0×10-6 mol·L-1.
与其他文献报道的过氧化氢传感器性能比较结果如表1所示,构建的 (ZrIP6/PB)5/PDDA/GCE传感器具有更宽的动态浓度范围和更低的检出限,显示出良好的检测性能.OHALLORAN 等[3]曾报道PB修饰电极对抗坏血酸盐、尿酸盐和对乙酰氨基酚等常见干扰物质的响应小于基线噪声,表明对H2O2测定的专一性.PB被称为“人工过氧化物酶”[6],因此,PB对于H2O2的电催化具有高灵敏度和选择性,本工作构建的(ZrIP6/PB)5/PDDA/GCE电极对H2O2的快速检测具有广泛的实际应用前景.
2.7 实际样品的检测
为了探究修饰电极(ZrIP6/PB)5/PDDA/GCE电化学过氧化氢传感器能否在实际样品中检测,实验检测了3%的 H2O2医用消毒水中H2O2的实际含量,并用加标回收法检验了方法的可靠性,结果如表2所示.根据测定结果可以计算出消毒水中H2O2物质的量浓度为868.15 mmol·L-1,而H2O2理论含量为869.56 mmol·L-1,检测误差为-0.16%.添加3种不同浓度的过氧化氢标准样得到的加标回收率在99.83%~110.1%,结果表明了制备的(ZrIP6/PB)5/PDDA/GCE电化学H2O2传感器可用于实际样品的测定.
3 結 论
利用磷酸基团与金属离子的强络合作用及相反电荷离子间的静电作用,通过层层自组装的方法制备了ZrIP6/PB复合膜修饰电极.电化学结果表明,植酸锆促进了PB化学反应过程中抗衡离子在复合膜间的渗透,增强了复合膜修饰电极的电化学性能.另外制备的ZrIP6/PB复合膜修饰电极性能良好,且对H2O2有很好的电催化还原作用,响应范围较宽,该传感器已经成功地应用于3 % H2O2医用消毒水中过氧化氢浓度的测定.
参考文献:
[1] PYRASCH M,TOUTIANOUSH A,JIN W Q,et al.Selfassembled films of Prussian blue and analogues:optical and electrochemical properties and application as ionsieving membranes [J].Chemistry of Materials,2003,15(1):245-254.
[2] ITAYA K,UCHIDA I,NEFF V D.Electrochemistry of polynuclear transition metal cyanides:Prussian blue and its analogues [J].Accounts of Chemical Research,1986,19(6):162-168.
[3] OHALLORAN M P,PRAVDA M,GUILBAULT G G.Prussian blue bulk modified screenprinted electrodes for H2O2 detection and for biosensors [J].Talanta,2001,55(3):605-611.
[4] DE MATTOS I L,GORTON L,RUZGAS T,et al.Sensor for hydrogen peroxide based on Prussian blue modified electrode:improvement of the operational stability [J].Analytical Sciences,2000,16(8):795-798.
[5] RICCI F,AMINE A,TUTA C S,et al.Prussian blue and enzyme bulkmodified screenprinted electrodes for hydrogen peroxide and glucose determination with improved storage and operational stability [J].Analytica Chimica Acta,2003,485(1):111-120.
[6] KARYAKIN A A,KARYAKINA E E.Electroanalytical applied cation of Prussian blue and its analogs [J].Russian Chemical Bulletin,2001,50(10):1811-1817.
[7] RAMSDEN J J,LVOV Y M,DECHER G.Determination of optical constants of molecular films assembled via alternate polyion adsorption [J].Thin Solid Films,1995,254 (1/2):246-251.
[8] PYRASCH M,TIEKE B.Electroand photoresponsive films of Prussian blue prepared upon multiple sequential adsorption [J].Langmuir,2001,17(24):7706-7709.
[9] MILLWARD R C,MADDEN C E,SUTHERLAND I,et al.Directed assembly of multilayersthe case of Prussian blue [J].Chemistry Communications,2001(19):1994-1995.
[10] WANG Q F,ZHONG L,SUN J Q,et al.A facile layerbylayer adsorption and reaction method to the preparation of titanium phosphate ultrathin films [J].Chemistry of Materials,2005,17(13):3563-3569.
[11] CLEARFIELD A.Role of ion exchange in solidstate chemistry [J].Chemical Reviews,1988,88(1):125-148.
[12] PESSOA C A,GUSHIKEM Y,KUBOTA L T,et al.Preliminary electrochemical study of phenothiazines and phenoxazines immobilized on zirconium phosphate [J].Journal of Electroanalytical Chemistry,1997,431:23-27.
[13] WANG Q F,YU H J,ZHONG L,et al.Incorporation of silver ions into ultrathin titanium phosphate films:in situ reduction to prepare silver nanoparticles and their antibacterial activity [J].Chemistry of Materials,2006,18(7):1988-1994.
[14] WANG Q F,ZHANG L,QIU L Y,et al.Fabrication and electrochemical investigation of layerbylayer deposited titanium phosphate/prussian blue composite films [J].Langmuir,2007,23(11):6084-6090.
[15] DONG J,WEN Y,MIAO Y,et al.A nanoporous zirconium phytate film for immobilization of redox protein and the direct electrochemical biosensor [J].Sensors and Actuators B:Chemical,2010,150(1):141-147.
[16] ZHAO B,LIU Z,LIU Z,et al.Silver microspheres for application as hydrogen peroxide sensor [J].Electrochemistry Communications,2009,11(8):1707-1710.
[17] LU W,LIAO F,LUO Y,et al.Hydrothermal synthesis of wellstable silver nanoparticles and their application for enzymeless hydrogen peroxide detection [J].Electrochimica Acta,2011,56(5):2295-2298.
[18] XU F,DENG M,LI G,et al.Electrochemical behavior of cuprous oxidereduced graphene oxide nanocomposites and their application in nonenzymatic hydrogen peroxide sensing [J].Electrochimica Acta,2013,88:59-65.
[19] LIU M,HE S,CHEN W.Co3O4 nanowires supported on 3D Ndoped carbon foam as an electrochemical sensing platform for efficient H2O2 detection [J].Nanoscale,2014,6(20):11769-11776.
[20] DONG S,XI J,WU Y,et al.High loading MnO2 nanowires on graphene paper:facile electrochemical synthesis and use as flexible electrode for tracking hydrogen peroxide secretion in live cells [J].Analytica Chimica Acta,2015,853:200-206.
[21] CHABRI S,DHARA A,SHOW B,et al.Mesoporous CuOZnO pn heterojunction based nanocomposites with high specific surface area forenhanced photocatalysis and electrochemical sensing [J].Catalysis Science & Technology,2016,6(9):3238-3252.
[22] ZHANG N,ZHENG J.Synthesis of AgFe2O3RGO nanocomposites for the electrocatalytic reduction of H2O2 [J].Journal of Materials Science:Materials in Electronics,2017,28(15):11209-11216.
[23] DAEMI S,GHASEMI S,AKBAR A A.Electrospun CuOZnO nanohybrid:tuning the nanostructure for improved amperometric detection of hydrogen peroxide as a nonenzymatic sensor [J].Journal of Colloid and Interface Science,2019,550:180-189.
(責任编辑:郁 慧)
