不同油相微乳液性质及其增溶菲的性能研究
2019-10-23张瀚元鹿豪杰任黎明杨朝格
张瀚元,鹿豪杰,任黎明,范 野,杨朝格,董 军*
不同油相微乳液性质及其增溶菲的性能研究
张瀚元1,2,鹿豪杰1,2,任黎明1,2,范 野1,2,杨朝格1,2,董 军1,2*
(1.吉林大学新能源与环境学院,吉林 长春 130021;2.吉林大学地下水资源与环境教育部重点实验室,吉林 长春 130021)
以Tween 80为表面活性剂,正戊醇为助表面活性剂,3种不同的植物油(大豆油、棕仁油、葵花油)作为油相构建微乳相图,探究不同油相对微乳液性质的影响.制备了不同油相与表面活性剂质量比(O/S)的3种植物油基系列微乳液,并对比了它们对菲的增溶效果.结果表明,不同油相对微乳液的成相能力及稀释特性影响较大,其中棕仁油>葵花油>大豆油.3种油相微乳液在不同含水量下具有相似的电导率变化趋势且均为牛顿型流体.制备的3种植物油基系列微乳液对菲的增溶能力均随体系中油含量的增加而提高,其中大豆油基微乳液对菲的增溶效果最差,而棕仁油微乳液在O/S值为0.1时对菲的增溶效果最好,可达2.18g/L.
微乳液;菲;增溶
多环芳烃(PAHs)是一类持久性疏水有机污染物,具有“三致”效应[1].其中,菲是具有三个苯环的PAHs类化合物,被美国环境保护署列入了16种有害的多环芳烃之中[2].由于其水溶性低,辛醇-水分配系数高且易被土壤有机质强烈吸附等特性,所以可以长期存在于土壤中[3],直接或间接地进入食物链,对人类及其他生物的生命健康构成威胁[4].因此,PAHs污染的土壤亟待修复.
在过去几十年中,针对土壤中菲的去除,人们尝试了各种修复技术,包括热处理[5]、生物处理[6]、高级氧化[7]、光催化降解[8]、植物修复[9]、电动修复[10]、土壤淋洗[11]等.其中土壤淋洗由于其修复周期短、处理效率高、成本低等优点,被认为是土壤有机污染治理的可靠技术[12].目前,用于土壤淋洗的一些常用增溶试剂主要有非离子表面活性剂[13]、阴离子表面活性剂[14]、生物表面活性剂[15]、腐殖酸[16]、环糊精[17]、植物油[18]等,它们均已被应用于土壤修复研究之中.但阴离子表面活性剂增溶能力有限;非离子表面活性剂易吸附于土壤,吸附损失量大;生物表面活性剂虽然生物降解性好、增溶能力强,但价格昂贵,大部分还未实现商品化;腐殖酸、环糊精等对难溶有机污染物的增溶能力较弱[19].因此,开发经济、高效的增溶试剂对菲污染土壤的修复具有重要意义.
微乳液是由水、油、表面活性剂、助表面活性剂等组分,在适当比例下,形成的透明或半透明、热力学稳定、光学各向同性的体系[20-21].它具有良好的润湿能力、适中的黏度、超低界面张力以及对疏水、亲水化合物高溶解度等优点,在食品[22]、药物[23]、驱油[24]、环境[25]等方面均具有广泛的应用.然而,微乳液的增溶能力取决于它们的成分、配比及类型.其中,油相的类型及含量会直接影响体系的成相能力、稳定性和增溶效果[26].研究表明,大分子油与小分子油会以不同方式掺入到微乳液中,且大分子油的掺入量要低于小分子油[27];中链油(辛酸/癸酸甘油三酯)和长链不饱和油(甘油三油酸酯)组合使用可以扩大体系的微乳区域,进而提高对目标药物的溶解能力[28];大豆油掺入精油微乳液体系之后,提高了其可稀释性[29].因此,确定不同油相及其含量对微乳液相行为的影响,选择并配制出合适的微乳体系对增强修复菲污染的土壤至关重要.
本文以菲为PAHs代表物,选择了食品级表面活性剂Tween 80、低碳链的戊醇以及对PAHs具有较高溶解度的3种植物油(大豆油、葵花油和棕仁油)构建绿色微乳液体系;探究了不同油相及其含量对微乳液性质的影响;此外,配制了不同O/S值的3种植物油基系列微乳液并对比了它们对菲的增溶效果.
1 材料与仪器
1.1 实验材料
Tween80(C24H44O6),化学纯,天津百伦斯生物技术有限公司;正戊醇,分析纯,国药集团化学试剂有限公司;葵花油,工业级,市售;大豆油,食品级,市售;棕仁油,工业级,市售;甲醇,分析纯,北京化工厂有限责任公司;菲(C14H10),上海麦克林试剂公司;
1.2 实验仪器
THZ-82型恒温振荡器(国华);3-15型离心机(SIGMA);IT-09C15型磁力搅拌器;Thermo Evolution 200紫外-可见光分光光度计(北京泰科施普技术有限公司);DDS-307A型电导率仪(上海仪电科学仪器股份有限公司);SX721型pH计(上海三信仪表厂);DV2TLVCJ0型锥板式黏度计(BROOKFIELD); ZS910型Zeta电位仪(马尔文).
2 实验方法
2.1 绘制拟三元相图
以葵花油、大豆油、棕仁油3种植物油作为油相,采用“水滴定法”绘制拟三元相图.将Tween80与正戊醇的质量比固定为3:1,按照Tween80与植物油的质量比为9:1至1:9依次配制不同比例下Tween80、正戊醇和植物油的混合体系.然后,在450r/min磁力搅拌下,逐滴滴加去离子水,当体系由澄清开始变得浑浊时记录此时所加入的去离子水质量,并计算混合体系中各组分的百分含量绘制拟三元相图.每组实验重复3次,取平均值.
2.2 不同含水量下微乳液的电导率
根据拟三元相图的结果选择微乳区域中的一个体系(O/S=0.08),在室温下测定3种植物油基微乳液在不同含水量时的电导率,以区分微乳液类型.重复测定2次,取平均值.
2.3 不同植物油对微乳液物理特性的影响
为了研究不同油相对微乳液物理特性的影响,分别探究了不同植物油基微乳液的成相能力、可稀释性和流体特性.其中成相能力可用拟三元相图中单相区域面积占总面积的百分比来表征.采用AutoCAD软件辅助计算拟三元相图中封闭单相区域面积占总面积的百分比,以此对比3种植物油基微乳液的成相能力.
利用微乳体系中所加入的极性相(H2O)含量(m,式1)来表征微乳液的可稀释性[30].
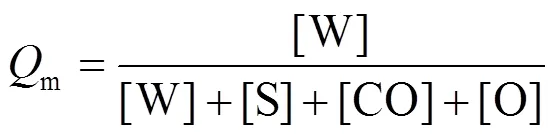
式中:[W]、[S]、[CO]和[O]分别是当微乳体系开始变浑浊时极性相、表面活性剂、助表面活性剂和油相的质量.m值较大表明混合物中含有较多的极性相,微乳液的可稀释性较好.把m=90%且仍能保持光学透明的微乳液认为是完全可稀释的微乳液[29].
利用DV2TLV锥板黏度计测定不同植物油基微乳液的剪切应力随剪切速率变化来表征微乳液的流体特性.
2.4 菲的增溶实验
为了探究油相与表面活性剂的质量比(O/S)及3种植物油微乳液对菲增溶效果的影响,设计并配制了几种不同的水包油型(O/W)微乳液.制备过程如下:按不同O/S比例,将油相缓慢加入Tween80和戊醇的混合物中,在450r/min的磁力搅拌作用下,加入相应体积的去离子水,使表面活性剂溶解,最后再利用0.1mol/L NaOH溶液调节体系的pH值至中性.相关配制参数如表1所示.
移取2mL所配制的微乳液于20mL棕色顶空瓶中,加入过量固体污染物菲,加盖密封后置于恒温振荡器中.保持振荡速度为150r/min,在(25±1)℃下恒温振荡72h.然后将悬浮液利用0.45μm的滤膜过滤以去除未溶解的固体菲.最终的样品用甲醇稀释,然后利用紫外-可见光分光光度计在波长为250nm处测定样品中菲的含量.每组实验重复3次,取平均值.
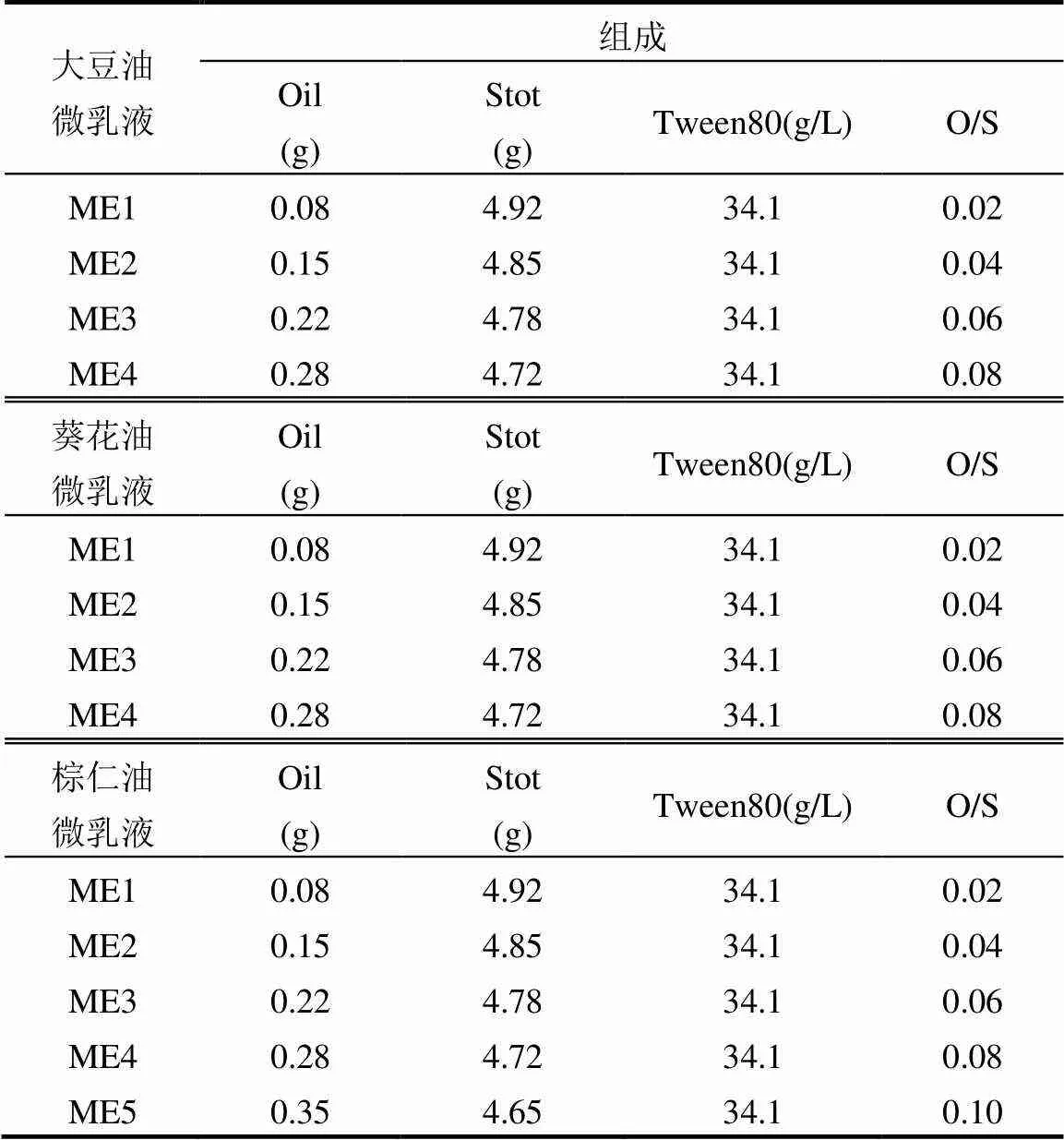
表1 大豆油,葵花油和棕仁油基微乳液的配制参数
注:Stot为Tween80和戊醇的总质量.ME为微乳液英文缩写.
3 结果与讨论
3.1 相图分析
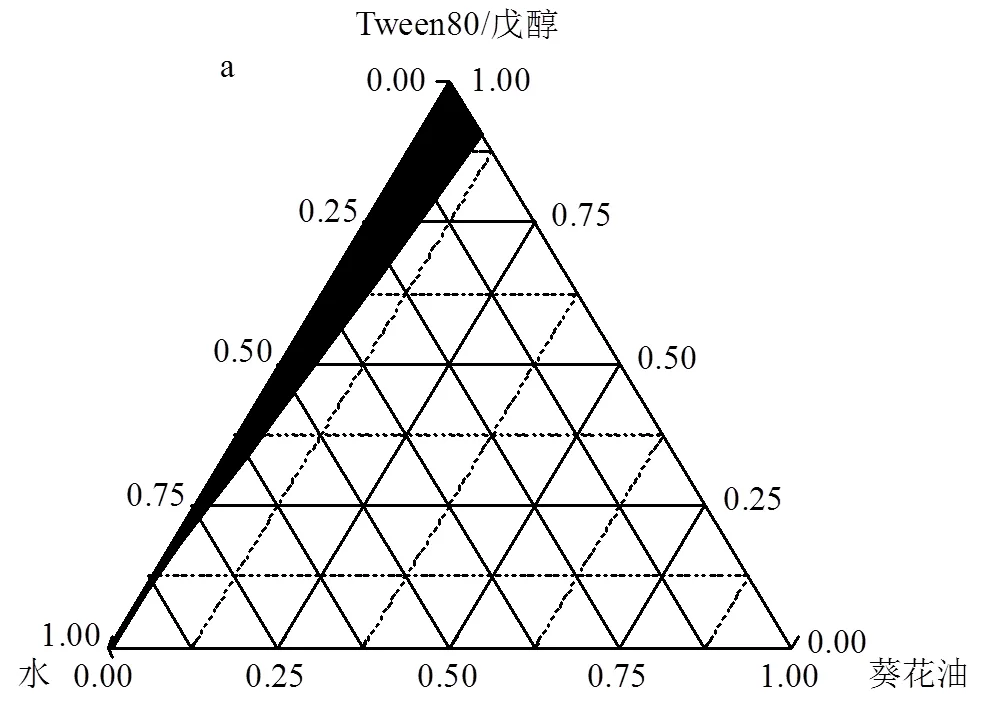
拟三元相图是研究微乳液体系相行为最方便、有效的手段.如图1所示为用葵花油、棕仁油、大豆油3种植物油构建微乳体系的拟三元相图.相图中,黑色区域为光学透明的单相微乳区域,Tween 80、正戊醇和植物油三者比例在黑色区域内即可形成微乳体系.从图中可以看出3种植物油参与构建微乳体系的拟三元相图中都出现了黑色区域,该结果表明3种植物油均可构建微乳液体系.
3.2 含水量对微乳液类型的影响
微乳液可分为油包水型(W/O)、水包油型(O/W)和双连续型(B),不同类型的微乳液体系的电导率不同.因此,可以通过测定微乳液电导率来判断其类型.
通常情况下,微乳液的类型与含水量有着重要的关系.从图2可以看出,3种植物油基微乳液的电导率都随着含水量增多呈先上升后下降趋势,并且都具有两个明显的导电区.以棕仁油基微乳液为例,在含水量很低时,由于植物油及非离子表面活性剂的低电导率,导致整个微乳液体系的电导率值较低,此时的微乳液体系属于W/O型微乳液;随着含水量增多,体系中溶胀的胶束开始相互作用,电导率值急剧增加,达到渗滤阈值[31];当含水量在60%~70%之间时,电导率随含水量的升高继续缓慢上升,此时的体系中油和水皆为连续相,属于B型微乳液;当含水量大于70%时,小油滴开始逐渐分散至水介质中,水的稀释作用导致体系电导率下降,此时的微乳液体系属于O/W型微乳液.
O/W型微乳液对疏水有机污染物具有极大的增溶能力,它可以提高疏水污染物在水中的溶解度,因此本文选择制备不同植物油基O/W型微乳液.由实验结果可知,制备O/W型微乳液体系的含水量需大于70%.
3.3 不同植物油相对微乳液物理特性的影响
3.3.1 成相能力 如图3所示为葵花油、棕仁油和大豆油所构建的微乳体系中单相区域面积占拟三元相图总面积的比例.可以看出3种天然植物油所构建的微乳体系中单相区域面积的大小顺序为:棕仁油>葵花油>大豆油.该结果表明棕仁油的成相能力最大,这是因为棕仁油中含有大量的中链甘油三酯,与大豆油和葵花油中的长链甘油三酯相比,中链甘油三酯具有更高的自乳化能力,从而使得微乳区域扩大[32].微乳区域越大表明在相同的表面活性剂用量下,水和油结合到微乳液中的量越多,为疏水性污染物分散到油相中提供的机会越大.
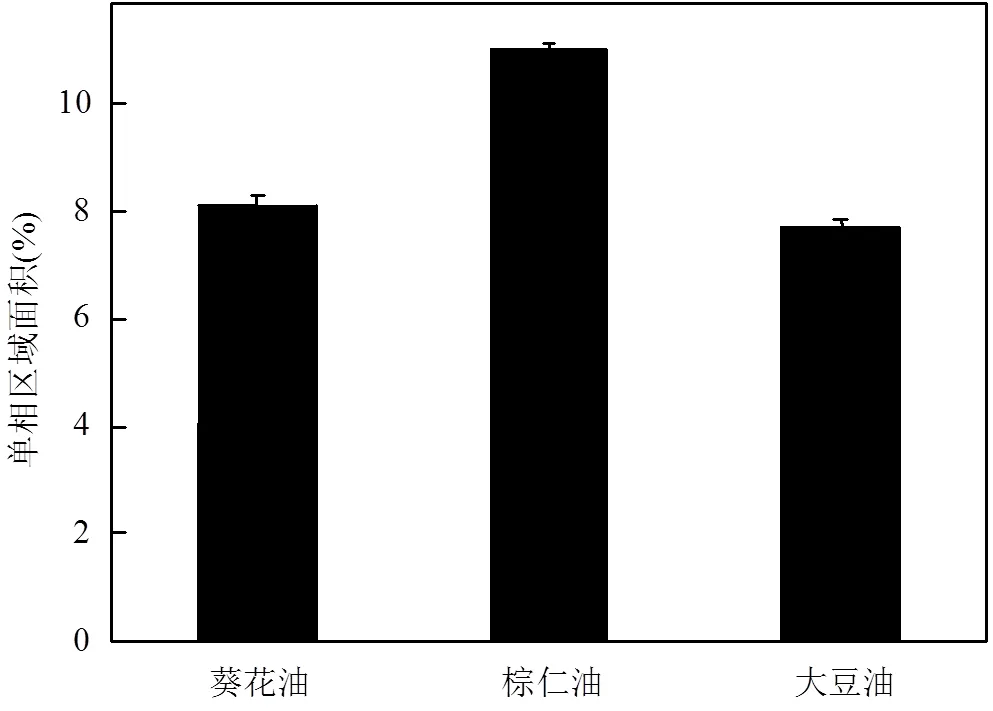
图3 植物油基微乳液体系的单相区域面积
3.3.2 可稀释性 如图4所示为在不同表面活性剂与油的质量比(S/O)下3种植物油基微乳液的m值.可以看出,当S/O值在10:1至7:1范围内时,3种植物油所构成的微乳液均具有可稀释性,且随S/O值的降低而降低,说明随油含量的增加,微乳液的可稀释能力有所下降.当S/O=6:1时,仅棕仁油构成的微乳液具有可稀释性,而大豆油和葵花油在此比例下不能形成微乳液.此外,在所研究的S/O值范围内,棕仁油构成微乳液的可稀释能力均高于大豆油和葵花油,且当S/O=10:1时,棕仁油微乳液的可稀释能力最大,为95.23%,属于完全可稀释微乳液.综上可知3种植物油中,棕仁油构成的微乳液可稀释性最强.
3.3.3 流体特性 如图5所示,3种植物油基微乳液的剪切应力与剪切速率都呈线性相关,表明在所研究的剪切范围内3种植物油基微乳液均为牛顿型流体.当含水量相同时,由于体系中含油量相对较少,3种植物油基微乳液的剪切应力随剪切速率的变化基本相同;而当含水量不同时,微乳液的剪切应力随剪切速率的变化明显不同.以棕仁油微乳液为例,当体系中含水量由60%升高至70%时,微乳液的剪切应力减小,这是由体系中含水量升高时微乳液黏度降低而导致的(表2).这表明微乳液在较高含水量下表现出较低的黏度,有利于微乳液在土壤淋洗中的应用.
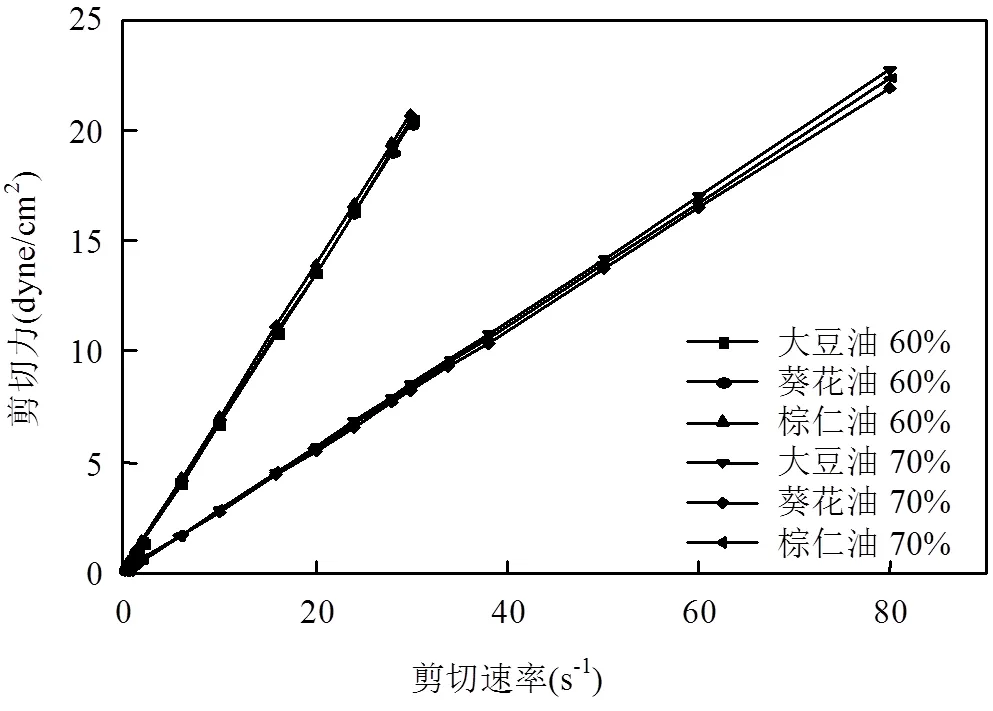
图5 三种植物油基微乳液在不同含水量时剪切力与剪切速率的关系
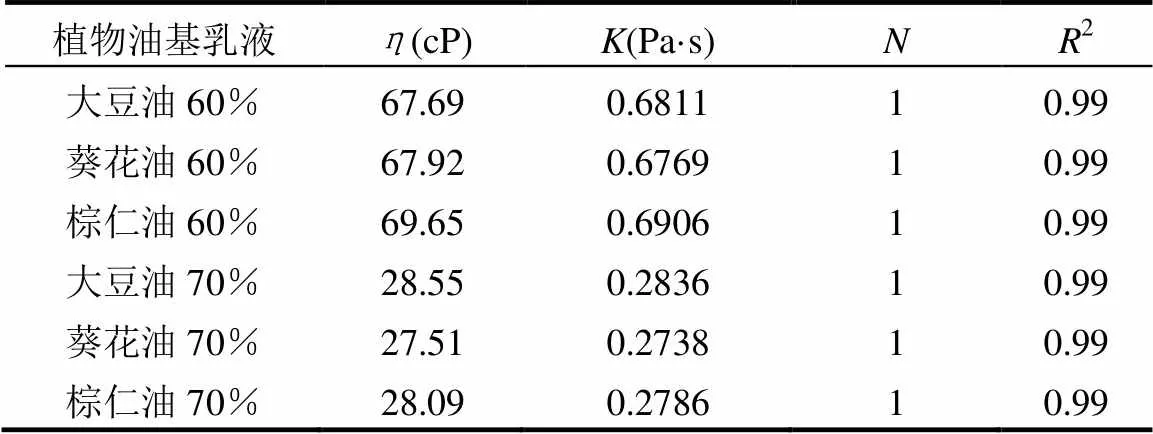
表2 三种植物油基微乳液在不同含水量时的流变性质
注:为黏度;为稠度系数;为流动指数.
3.4 菲的增溶性能
当疏水性物质溶解在微乳液中时,它可以存在于油相或界面层中[33],因此油相的类型及含量对于微乳液体系增溶疏水性有机污染物有重要的影响.为了明确油相对微乳液增溶效果的影响,在不同O/S值条件下配制了3种植物油基微乳液并以菲为目标污染物进行了增溶实验.对所配制的微乳液进行了表征,如图6所示,经5000r/min离心30min后,不同O/S值条件下所配制的3种植物油基微乳液都未发生沉淀、浑浊及相分离等现象,且仍具有丁达尔现象,说明它们具有较好的物理稳定性;由表3可知,当体系的pH在7左右时,所有微乳液的zeta电位均在-8.8~-15.9mV的范围内带负电荷.由于一般情况下土壤颗粒的表面电位为负,因此当其应用于土壤中难溶性有机污染物的增溶时,因土壤颗粒的静电排斥作用可有效降低其吸附损失.不同O/S值条件下所配制的3种植物油基微乳液的电导率均大于100μS/cm,表明这几种微乳液都属于O/W型微乳液.

图6 三种植物油基微乳液的离心稳定性,(a)葵花油(b)棕仁油(c)大豆油
由图7可以看出,所考察的3种植物油基微乳液体系中菲的溶解度均有所提高(菲在纯水中的溶解度为1mg/L),且随着O/S值的增加,体系中含油量越高,对菲的增溶能力越强.这是因为,由于油相的掺入,微乳液具有更强的疏水性以及更大的胶束空间,有利于疏水性污染物的进入,进而增大了溶解度[34].此外,通过对比3种植物油基微乳液对菲的增溶效果可知,在所有O/S值下大豆油微乳液对菲的增溶效果最差;当O/S值为0.02和0.04时棕仁油对菲的增溶效果最好,当O/S值为0.06和0.08时葵花油对菲的增溶效果最好,而当O/S值为0.1时,仅棕仁油可形成完全可稀释微乳液,且其对菲增溶效果最好,为2.18g/L.
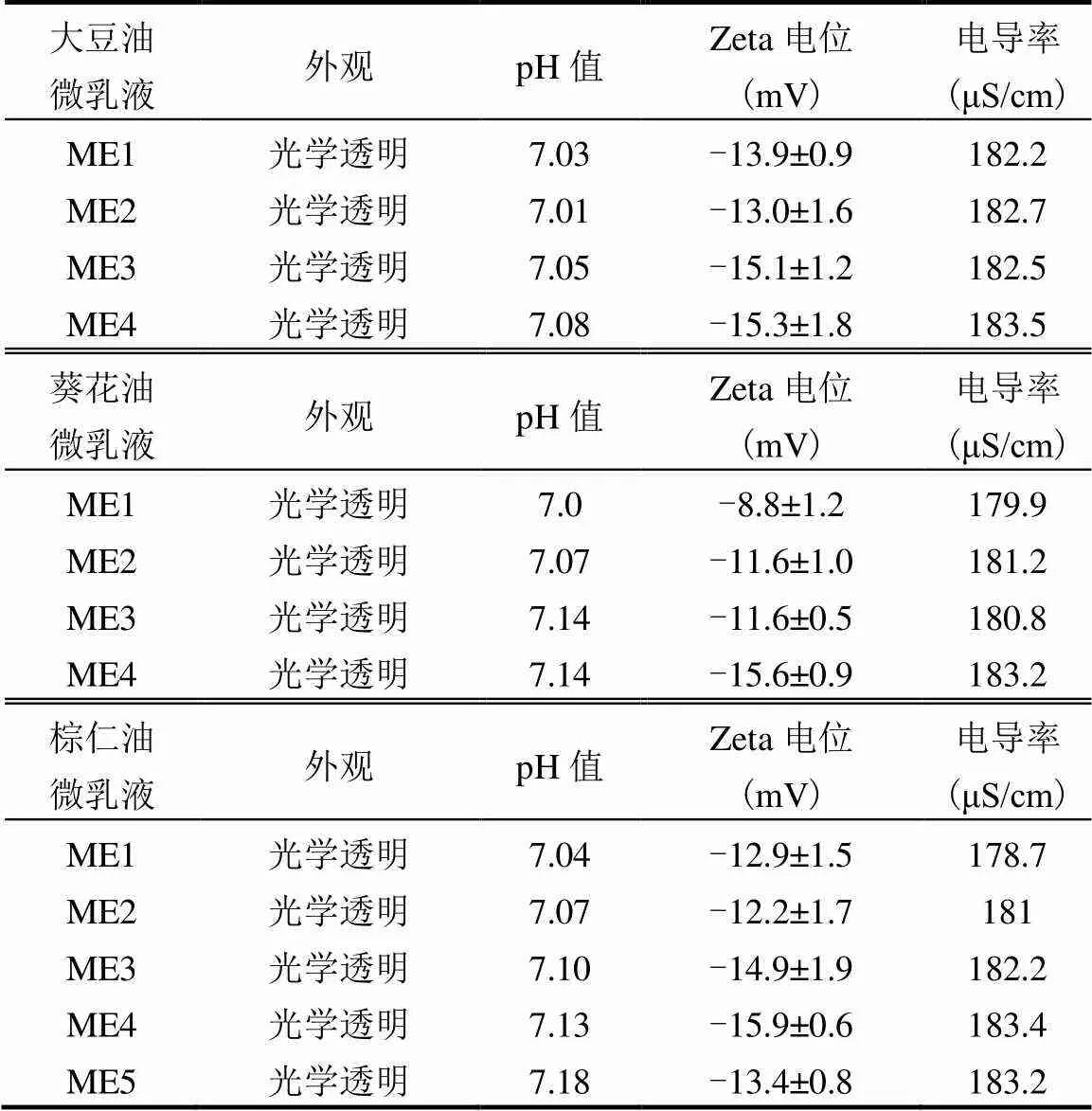
表3 大豆油、葵花油和棕仁油基微乳液的外观、pH值、zeta电位和电导率
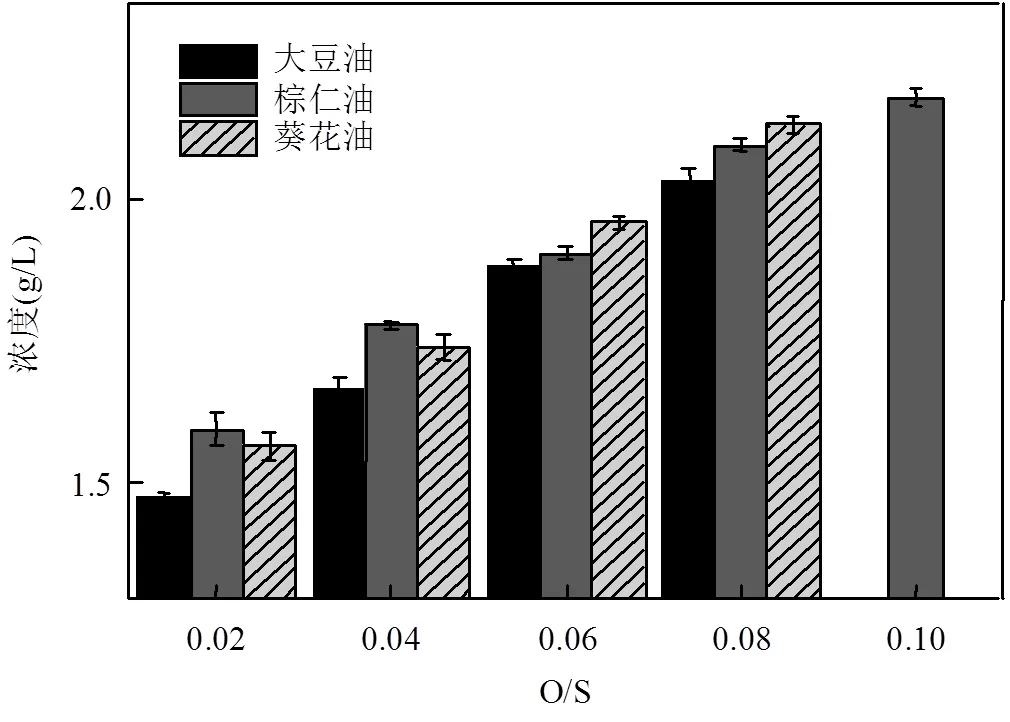
图7 三种植物油基微乳液在不同O/S值下对菲的增溶效果
4 结论
4.1 3种植物油作为油相均可成功参与构建微乳液.其中棕仁油构建的微乳液的成相能力最大.在所考察的S/O值范围内,棕仁油微乳液的可稀释能力均最大,最高可达95.23%.在不同含水量下3种植物油微乳液具有相似的电导率变化趋势且均显示出牛顿流体特性.
4.2 制备的3种植物油基系列微乳液稳定性高、黏度低、带负电,有利于在土壤淋洗中的应用.
4.3 3种植物油微乳液对菲的增溶能力均随体系中油含量(O/S)的增加而提高,说明体系中的含油量是影响增溶能力的一个重要因素.对比3种植物油微乳液在相同O/S值下对菲的增溶效果发现,大豆油微乳液增溶效果最差.在3种植物油中,当O/S值为0.1时,仅棕仁油可形成完全可稀释微乳液,此时它对菲的增溶效果最好,为2.18g/L.
[1] 李瑞娟,丁光辉,李雪瑶,等.酸化时间对磁性碳纳米管制备及吸附菲的影响[J]. 中国环境科学, 2019,39(4):1542-1550. Li R J, Ding G H, Li X Y, et al. Effect of acidification time on preparation of magnetic multi-walled carbon nanotubes and adsorption of phenanthrene in water [J]. China Environmental Science, 2019,39(4):1542-1550.
[2] 张 明,唐访良,吴志旭,等.千岛湖表层沉积物中多环芳烃污染特征及生态风险评价[J]. 中国环境科学, 2014,34(1):253-258. Zhang M, Tang F L, Wu Z X, et al. Pollution characteristics and ecological risk assessment of polycyclic aromatic hydrocarbons (PAHs) in surface sediments from Xin'anjiang Reservoir [J]. China Environmental Science, 2014,34(1):253-258.
[3] Wild S R, Obbard J P, Munn C I, et al. The long-term persistence of polynuclear aromatic hydrocarbons (PAHs) in an agricultural soil amended with metal- contaminated sewage sludges [J]. Science of the Total Environment, 1991,101(3):235-253.
[4] White P A, Claxton L D. Mutagens in contaminated soil: A review [J]. Mutation Research, 2004,567(2/3):227-345.
[5] Harmon T C, Burks G A, Aycaguer A C, et al. Thermally enhanced vapor extraction for removing PAHs from lampblack- contaminated soil [J]. Journal of Environmental Engineering, 2001,127(11):986- 993.
[6] Chang B V, Shiung L C, Yuan S Y. Anaerobic biodegradation of polycyclic aromatic hydrocarbon in soil [J]. Chemosphere, 2002, 48(7):717-724.
[7] Flotron V, Delteil C, Padellec Y, et al. Removal of sorbed polycyclic aromatic hydrocarbons from soil, sludge and sediment samples using the Fenton's reagent process [J]. Chemosphere, 2005,59(10):1427- 1437.
[8] Zhang L H, Li P J, Gong Z Q, et al. Photocatalytic degradation of polycyclic aromatic hydrocarbons on soil surfaces using TiO2under UV light [J]. Journal of Hazardous Materials, 2008,158(2/3):478-484.
[9] Lee S H, Lee W S, Lee C H, et al. Degradation of phenanthrene and pyrene in rhizosphere of grasses and legumes [J]. Journal of Hazardous Materials, 2008,153(1/2):892-898.
[10] 马建伟,王 慧,罗启仕.电动力学作用下土壤中菲的迁移特征及其机理[J]. 中国环境科学, 2007,27(2):241-245. Ma J W, W H, Luo Q S. Mobilization characteristic and its mechanism of phenanthrene in soils by electrokinetics [J]. China Environmental Science, 2007,(2):241-245.
[11] Kobayashi T, Kaminaga H, Navarro R R, et al. Application of aqueous saponin on the remediation of polycyclic aromatic hydrocarbons- contaminated soil [J]. Journal of Environmental Science and Health, 2012,47(8):1138-1140.
[12] West C C, Harwell J H. Surfactant and subsurface remediation [J]. Environmental Science & Technology, 1992,26(12):2324-2330.
[13] Takeuchi E, Matsuoka K, Ishii S, et al. Solubilization of polycyclic aromatic hydrocarbons in C16E7 nonionic solutions surfactant [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2014,441(20):133-139.
[14] Chun C L, Lee J J, Park J W. Solubilization of PAH mixtures by three different anionic surfactants [J]. Environmental Pollution, 2002,118(3): 307-313.
[15] Li S D, Pi Y R, Bao M T, et al. Effect of rhamnolipid biosurfactant on solubilization of polycyclic aromatic hydrocarbons [J]. Marine Pollution Bulletin, 2015,101(1):219-225.
[16] Sari G L, Trihadiningrum Y, Wulandari D A, et al.Compost humic acid-like isolates from composting process as bio-based surfactant: Properties and feasibility to solubilize hydrocarbon from crude oil contaminated soil [J]. Journal of Environmental Management, 2018, 225(1):356-363.
[17] Audrey P, Mokhtar D, Jacques P, et al. PAH contaminated soil remediation by reusing an aqueous solution of cyclodextrins [J]. Chemosphere, 2009,75(6):714-718.
[18] Gong Z Q, Alef K, Wilke B M, et al. Dissolution and removal of PAHs from a contaminated soil using sunflower oil [J]. Chemosphere, 2005, 58(3):291-298.
[19] 赵保卫.增效试剂对难降解有机物的增溶作用、机理及生物可利用性影[D]. 杭州:浙江大学, 2004. Zhao B W. Solubilization and bioavailability enhancements of hydrophobic organic compounds by surface active agents [D]. Hangzhou: Zhejiang Unversity, 2004.
[20] Hoar T P, Schulman J H. Transparent water-in-oil dispersions: the oleopathic hydro-micelle [J]. Nature, 1943,152(102/103):102-103.
[21] Schulman J H, Stoeckenius W, Prinec L. Mechanism of formation and structure of micro emulsions by electron microscopy [J]. The Journal of Physical Chemistry, 1959,63(10):1677-1680.
[22] Garti N, Clement V, Fanun M, et al. Some characteristics of sugar ester nonionic microemulsions in view of possible food applications [J]. Journal of Agricultural and Food Chemistry, 2000,48(9):3945-3956.
[23] Gupta S, Moulik S, Lala S, et al. Designing and testing of an effective Oil-in-Water microemulsion drug delivery system for in VIVO application [J]. Drug Delivery, 2005,12(5):267-273.
[24] Santanna V, Curbelo F, Dantas T C, et al. Microemulsion flooding for enhanced oil recovery [J]. Journal of Petroleum Science and Engineering, 2009,66(3/4):117-120.
[25] Zhao B W, Zhu L Z, Gao Y Z. A novel solubilization of phenanthrene using Winsor I microemulsion-based Sodium castor oil sulfate [J]. Journal of Hazardous Materials, 2005,119(1-3):205-211.
[26] Zheng G Y, Zhao Z Y, Jonanhan W W. Role of non-ionic surfactants and plant oils on the solubilization of organochlorine pesticides by oil-in-water microemulsions [J]. Environmental Technology, 2011, 32(3):269-279.
[27] Warisnoicharoen W, Lansley A B, Lawrence M L. Nonionic oil-in-water microemulsions: the effect of oil type on phase behaviour [J]. International Journal of Pharmaceutics, 2000,198(1):7-27.
[28] Chen Y Z, Tuo J, Huang H Z, et al. Optimized mixed oils remarkably reduce the amount of surfactants in microemulsions without affecting oral bioavailability of ibuprofen by simultaneously enlarging microemulsion areas and enhancing drug solubility [J]. International Journal of Pharmaceutics, 2015,487(1/2):17–24.
[29] Ma Q M, Zhong Q X.Incorporation of soybean oil improves the dilutability of essential oilmicroemulsions [J]. Food Research International, 2015,71(5):118-125.
[30] Mehta S K, Kaur G, Mutneja R, et al. Solubilization, microstructure, and thermodynamics of fully dilutable U-type Brij microemulsion [J]. Journal of Colloid and Interface Science, 2009,338(2):542-549.
[31] Eicke H F, Borkovec M, Das-Gupta B.Conductivity of water-in-oil microemulsions: A quantitative charge fluctuation model [J].Journal of Physical Chemistry, 1989,93(1):314-317.
[32] Shah N H, Carrvajal M T, Patel C I, et al. Self-emulsifying drug delivery systems (SEDDS) with polyglycolyzed glycerides for improving in vitro dissolution and oral absorption of lipophilic drugs [J]. Journal of Pharmaceutical Sciences, 1994,106(1):15-23.
[33] Testard F, Zemb T, Excess of solubilisation of lindane in nonionic surfactant micelles and microemulsions [J]. Langmuir, 1998,14(12): 3175–3181.
[34] 赵保卫,朱利中.微乳液对部分难溶芳烃的增溶作用及机理[J].自然科学进展, 2003,13(8):870-873.Zhao B W, Zhu L Z. Solubilization and mechanism of partially insoluble aromatic hydrocarbons by microemulsion [J]. Progress in Natural Science, 2003,13(8):870-873.
Properties of microemulsions with different oil phase and their solubilization capacities for phenanthrene.
ZHANG Han-yuan1,2, LU Hao-jie1,2, REN Li-ming1,2, FAN Ye1,2, YANG Chao-ge1,2, DONG Jun1,2*
(1.College of New Energy Resource and Environment, Jilin University, Changchun 130021, China;2.Key Laboratory of Groundwater Resources and Environment (Jilin University), Ministry of Education, Changchun 130021, China)., 2019,39(10):4296~4302
The phase diagrams of microemulsion systems comprised of Tween 80 as surfactant, pentanol as co-surfactant and three different vegetable oils (soybean oil, palm kernel oil, sunflower oil) as oil phase were constructed for studying the effect of different oils on the properties of microemulsions. Three different vegetable oil-based microemulsions were prepared with different mass ratios of oil/surfactant (O/S), and the solubilization of phenanthrene were compared. The results indicated that different oils had great influence on the phase forming ability and dilution characteristic. The phase forming and dilution abilities of three microemulsions were weakened in the order: palm kernel oil > sunflower oil > soybean oil. The three vegetable oil-based microemulsions with different water contents had similar conductivity trends and showed Newtonian behavior. The solubilization capacities of the prepared microemulsions for phenanthrene increased with the increase of oil content in the system. The soybean-based microemulsion had the lowest solubilization capacity for phenanthrene. The palm kernel oil-based microemulsion had the maximal solubilization capacity for phenanthrene at O/S=0.1, which can up to 2.18g/L.
microemulsion;phenanthrene;solubilization
X53
A
1000-6923(2019)10-4296-07
张瀚元(1995-),女,吉林省吉林市人,吉林大学硕士研究生,主要从事难溶污染物增溶方面研究.
2019-03-11基金项目:国家重点研发计划(2018YFC1802503);水体污染控制与治理科技重大专项(2018ZX07109-003)
* 责任作者, 教授, dongjun@jlu.edu.cn
