局部晚期非小细胞肺癌患者放化疗的预后相关因素分析
2019-10-15张惠姗王捷忠吴淑婷
张惠姗,王捷忠,张 伟,吴淑婷
目前肺癌的发生率仍不断上升,是全世界癌症的主要死亡原因[1],其中非小细胞肺癌(non-small cell lung cancer,NSCLC)的发生率最高,鳞癌和腺癌是最常见的病理类型,占肺癌总数的70%~80%,大多数肺癌患者确诊时已是局部晚期或Ⅳ期病变,失去了手术机会[2]。局部晚期非小细胞肺癌(locally advanced non-small cell lung cancer,LA-NSCLC)一般是指临床分期为ⅢA或ⅢB期的NSCLC患者。目前对于LA-NSCLC中鳞癌及无基因突变的腺癌,放化疗仍是其标准治疗方法[3]。由于患者个体之间存在异质性,根据个体化治疗原则,不同患者采用不同的治疗方案,预后也存在一定的差异。为探讨影响NSCLC的预后因素,现筛选并收集2012年1月1日-2016年6月30日初诊的LA-NSCLC患者177例,回顾分析患者的临床资料,探讨影响其不良预后的因素,进而优化临床诊疗方案,提高患者的生存率。
1 对象与方法
1.1对象 177例中,男性159例,女性18例,年龄(59.88±9.40)岁(37~83岁)。入选标准:(1)经病理组织学或细胞学、基因检测等证实的以鳞癌为主、上皮生长因子受体(epidermal growth factor receptor,EGFR)基因检测阴性的腺癌、腺鳞癌、大细胞癌等NSCLC患者;(2)根据2009年国际肺癌研究协会肺癌第七版TNM分期标准,确诊为Ⅲ期(ⅢA及ⅢB)的患者;(3)不合并第二原位癌;(4)未进行EGFR靶向治疗;(5)接受放化疗的综合治疗。排除标准:(1)存在放化疗禁忌者;(2)合并其他类型的恶性肿瘤;(3)病历资料临床数据缺失。患者的基本情况见表1。
1.2治疗方式
1.2.1放疗 调强放疗:采用高能直线加速器治疗,计划采用5~9个共面射野,根据影像资料(CT或PET-CT)勾画靶区后,由物理师完成适性调强放疗计划。根据CT或PET-CT上可见肺癌肿瘤原发灶及转移淋巴结为GTV-Tp及GTV-Np,95%等剂量线包绕PTV,计划6MV-X直线加速器照射,总DT6300cGy/30f(GTV-Tp及GTV-Np),每天1次,每周5次。其中有37例患者因无法继续耐受放疗或体质较差等原因未能完成放疗总生物效应剂量(biological effective dose,BED)70 Gy。BED被用于比较不同分次剂量治疗条件下某组织产生特定生物效应所需要的总剂量。
BED=n×d×(1+d/α/β)
其中n为分次数,d为分次剂量,n×d实际上是总剂量(D),不同组织的α/β值可查表获得。正常组织剂量脊髓Dmax≤45 Gy,双肺V20≤28%、V30≤20%;单侧肺V20≤45%;食管Dmax≤50 Gy,全食管受量≤30 Gy,心脏V40不超过40%。
1.2.2化疗 91例配合同步化疗,81例配合辅助化疗,5例未进行化疗;化疗方案主要以紫杉醇(135~175 mg/m2)+铂类及多西他赛(75 mg/m2)+铂类为主,其中采用顺铂(30 mg/m2,连续3 d)120例、卡铂45例、奈达铂(80~100 mg/m2)5例、奥沙利铂(130 mg/m2)3例。

表1 177例NSCLC患者的一般资料
COPD:慢性阻塞性肺疾病. 病理类型中其他包括大细胞癌及腺鳞癌等混合成分的癌.
卡铂剂量(mg)=AUC(5-7)(mg/mL/min)×[肌酐清除率(mL/min)+25]
男性肌酐清除率(mL/min)={[140-年龄(岁)]×体质量(kg)×1.23}÷血清肌酐(μmol/L)
女性肌酐清除率(mL/min)=男性肌酐清除率(mL/min)×0.85
1.2.3热疗 放化疗期间,78例同时配合BSD-2000射频热疗,第一周放疗开始,每周热疗两次,设置食管内测温点,温度达39~41 ℃,维持30 min以上。余99例未配合热疗治疗。
1.3调查方法 通过查阅局部晚期NSCLC患者病历资料、打电话、发信息、门诊随访等方式追踪随访,随访截止日期为2017年12月30日,回访总病例数共计177例。生存期是以患者确诊NSCLC之日算起至死亡或末次随访时间,生存时间以月计算。
1.4统计学处理 采用SPSS 21.0软件对随访病例建立数据库并进行研究。以患者的中位生存期及1,2,3年生存率为观察指标。采用Kaplan-Meier法进行生存率估计、Log-rank法进行两组生存率比较,并对NSCLC患者中N3组进行亚组单因素分析;对于单因素分析中P<0.1的因素采用Cox风险比例模型行多因素分析,显著性水准为α=0.05。P<0.05为差别具有统计学意义。
2 结 果
2.1生存情况及生存率 177例患者随访的中位生存时间为23月,1,2及3年的生存率分别为81.7%,47.6%及34.5%。
2.2影响患者预后的单因素分析 单因素分析显示,患者确诊后化疗周期数是否足够4周期、确诊时有无合并上腔静脉综合征、有无合并COPD是影响局部晚期NSCLC患者预后的因素(均为P<0.05,表2)。对N3患者具体淋巴结转移部位进行单因素亚组分析显示,N3患者中对侧纵隔淋巴结及单侧锁骨上淋巴结转移的患者,其生存率高于对侧肺门淋巴结及双侧锁骨上淋巴结转移的患者,差别具有统计学意义(P<0.05,表3,图1)。而患者的年龄、性别、病理类型、临床分期(2009年国际肺癌研究协会肺癌第七版TNM分期标准)、是否配合热疗、是否进行同步放化疗、放疗BED是否≥70 Gy、放疗总时间是否超过预期完成总时长1周、是否合并内科并发症、是否合并肺不张等对生存期无影响(P>0.05,表2)。
2.3影响患者预后的多因素分析 将单因素分析中P<0.1的因素引入Cox模型进行多因素分析,结果显示,化疗周期数是否足够4周期、放疗总时间是否超过预期完成总时长1周、有无合并COPD等是影响局部晚期NSCLC患者预后的独立因素(P<0.05,表4)。

表2 局部晚期NSCLC预后因素的单因素分析
COPD:慢性阻塞性肺疾病. 病理类型中其他包括大细胞癌及腺鳞癌等混合成分的癌.

表3 局部晚期NSCLC中N3患者具体淋巴结转移部位的单因素分析
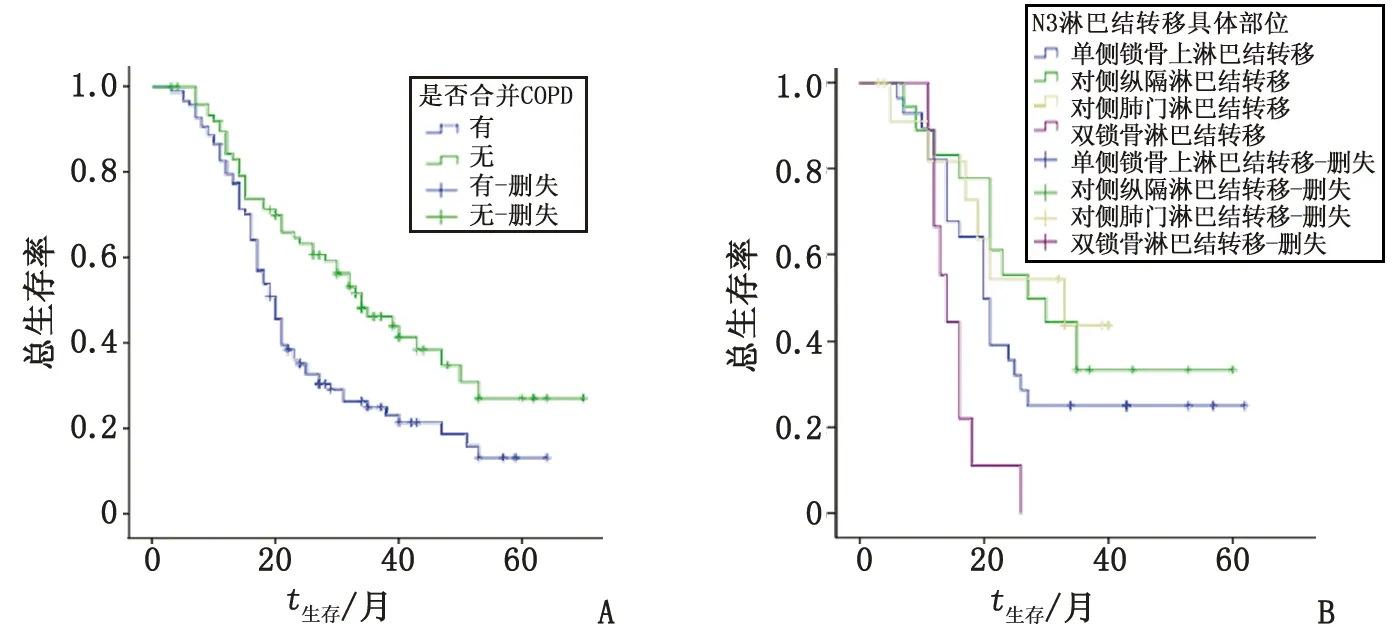
A:是否合并COPD Kaplan-Meier法生存曲线图;B:N3患者淋巴结位置Kaplan-Meier法生存曲线图.

方程中的变量系数标准误Waldχ2PExp(B)HR值(95%CI)放疗时间是否超过预期完成总时长1周0.630.2685.5230.0191.8781.878(1.110~3.176)化疗总周期数是否足够4周0.3770.1814.3530.0371.4581.458(1.023~2.078)是否合并COPD-0.5580.1978.0090.0050.5720.572(0.389~0.842)是否合并上腔静脉综合征-0.5950.3592.7450.0980.5510.551(0.273~1.115)
COPD:慢性阻塞性肺疾病.
3 讨 论
LA-NSCLC的治疗手段包括手术、化疗、放疗、免疫治疗、热疗等,目前综合治疗是标准治疗手段,针对LA-NSCLC的综合治疗已进行了多项临床研究[4-6]。本研究中177例LA-NSCLC患者的中位生存期为23月,与既往的报道类似[7]。
化放疗的综合治疗是几十年来逐渐形成的治疗模式,既往报道显示,同步放化疗是NSCLC的主要治疗手段之一[8]。刘晓梅等对84例Ⅲ期NSCLC患者的临床资料进行回顾性研究,发现同步放化疗的有效率高于序贯放化疗[9]。本研究单因素分析显示,是否同步化疗与LA-NSCLC患者的预后虽无明显相关性,但同步放化疗组的1,2,3年生存率均较辅助化疗组高,这可能与有效的化疗药物能够抑制放疗期间残留的肿瘤细胞加速再增殖有关[10]。积极的治疗是延长生存率的关键,本研究将LA-NSCLC患者化疗周期数是否达到4周期进行单因素及多因素分析,发现化疗周期数是否达到4周是LA-NSCLC预后因子的独立因素之一。
本研究从单因素分析显示,ⅢA期及ⅢB期患者与LA-NSCLC患者预后无明显相关,ⅢB期的LA-NSCLA患者的生存均值及中位生存率虽均较ⅢA期患者好,但在单因素分析中,总体上患者预后与分期未见明显相关性。这与既往的报道不一致[11],可能与本研究中ⅢA期患者较少,且个别ⅢA患者其他内科合并症相对较多、不能进行手术治疗、总体状态相对较差等情况有关。本研究对LA-NSCLC中N3患者淋巴结转移的具体部位进行单因素亚组分析,发现N3患者中对侧纵隔及单侧锁骨上淋巴结转移的患者的生存率高于对侧肺门及双侧锁骨上淋巴结转移的患者。这可能与放疗计划设计中因正常组织受量的限制导致颈部淋巴结肿瘤受量不能进一步提高有关。
此外,将合并COPD的患者进行单因素及多因素分析发现,合并COPD的LA-NSCLC患者生存率较低,是影响其预后的独立因素之一。有学者报道,合并COPD的患者比一般人群患肺癌的风险高1~10倍[12]。但对于COPD是否会影响肺癌预后的报道甚少。毛昌追对93例主要以Ⅲ期和Ⅳ期(83.3%)为主的患者进行预后分析,也发现合并COPD的NSCLC患者生存时间明显缩短,认为COPD患者会造成基质金属蛋白酶(guinea matrix metalloproteinase,MMP)/基质金属蛋白抑制酶(tissueinhibitor of metalloproteinase, TIMP)比值失衡,而MMP和TIMP在肺癌的侵袭与转移中起到重要作用,当合并COPD时,这一平衡被打破,增加了肺癌的侵袭与转移,从而使得肿瘤进展增快[12]。Gullòn等研究表明,合并COPD是NSCLC患者预后不良的因素[13]。本研究结果与之一致。一方面合并COPD的患者因肺功能较差,难以耐受放疗;另一方面,此类患者较其他人群更易发生肺部感染以及其他器官的器质性病变,病程反复且不可逆,使得机体处于一个免疫状态欠佳的状况,从而加速肿瘤的发生发展。
尽管单因素分析结果未体现出放疗总时间是否超过预期完成总时长1周会使LA-NSCLC患者生存率下降,但多因素分析显示,其是LA-NSCLC独立的预后影响因子之一,这可能与在一定的范围内随着时长的增加放疗的BED下降有关。本研究中,放疗的BED与预后未见明显相关性,可适当扩大研究中心、扩大样本量再行进一步研究。
热疗是近几年来逐渐发展起来的肿瘤综合治疗手段之一,是一种利用物理能量在组织中聚集产生的热能去提高肿瘤病灶的温度从而杀死肿瘤细胞的治疗方法[14]。热疗与放疗、化疗联合的综合治疗方案不仅可以有效杀伤肿瘤细胞,还可以提高肿瘤细胞对放化疗等的敏感性,同时可以增强患者机体的免疫力。本研究试图探索热疗是否能为LA-NSCLC带来生存获益,但单因素分析结果并未体现二者之间的生存率有明显差别。既往研究表明,应用热疗配合放化疗的综合治疗方案可以有效延长患者的生存期[15]。也有报道显示,热疗在食管癌及NSCLC的治疗上均体现出它的独特之处,Saeki等研究发现,放化疗联合热疗组的生存率高于放化疗组[16];也有研究表明,热疗联合放化疗组治疗期间白细胞减少、放射性肺炎、放射性食管炎等毒副反应均有所减轻[17]。
本研究通过回顾性研究的方法分析各种可能影响LA-NSCLA的预后因素,但由于随访时间较短,患者的病例数有限,患者局限于笔者所在医院,未能观察其他医疗机构的治疗病例,后续可行多中心研究扩大样本量继续探索,也可设置前瞻性实验,与本研究结果相论证,以获得更可靠的数据和资料来指导临床工作。
