浅谈运用“席明纳教学模式”在化学复习课中的应用
2019-09-10许华君
许华君
【摘要】:在化学学业水平考试复习中,引入“席明纳”教学模式,本文以“学考30题计算复习”为例,采用“直入主题——课堂展示——自由讨论——总结反思”的流程,展示学生的解题方法,学生积极参与,在合作中共享了学习方法,在辩论与比较中清晰了学习内容,极大地提高了学生的学习主动性和兴趣。
【关键词】:席明纳 化学复习课 学考30题计算 化学解题方法
引言
从近几年浙江的“三位一体”招生人数上来看,呈不断增大的趋势。而学生参加“三位一体”,就必须要学考成绩。所以学考对于学生来说很重要。两考同卷时,我们学校化学学考安排在高二上学期的11(10)月,现在学考和选考两卷分开,我们学校化学学考安排在高一下的6月。而新课在5月上旬结束,从时间角度来说,复习时间很短。所以一直在思考,如何在新课完成后,在所剩下短短的时间内,如何去提高复习课的效率。“席明纳教学模式”便走进了我的视野,下面,就以“学考30题计算复习”为例,谈谈自己在课堂中实施“席明纳教学模式”的过程。
一.席明纳模式
从具体内容上看,“席明纳”教学模式主要指的是学生在老师公布的课题中选择其一并写出专题研究报告,之后在老师主持下向全班陈述报告并与全班同学就该题内容进行讨论交流的教学组织形式。所以在探索“席明纳”教学模式时,在下一节上课之前,预先布置主题内容,学生课前准备,指派几个同学发言或讲解,最后师生一起总结。采用“直入主题——课堂展示——自由讨论——总结反思”的流程。
二.课堂流程设计
(一)课前布置主题,选好讲解代表
在下一节课要复习30题计算时,布置一个题目:
将2.80g含氧化镁的镁条完全溶于50.0mL硫酸溶液后,滴加2.00mol·L-1氢氧化钠溶液,恰好完全沉淀时用去200.0mL。将所得沉淀灼烧、冷却后称得固体质量为4.40g。请计算:
(1)上述硫酸的物质的量浓度c(H2SO4)=____________。
(2)镁条中氧化镁和镁的物质的量之比n(MgO):n(Mg)=__________。
要求学生详细地写出解题过程,然后通过学生交上来的作业批改,选定好哪几位同学上台讲解和板演。
(二)直入主题,学生代表课堂展示
就本节课而言,学生展示如下:
【学生展示1】根据化学方程式计算和解二元一次方程
设Mg的物质的量为xmol,MgO的物质的量为ymol。
n()=2.00mol·L-1×0.02000L=0.0400mol
Xmolxmolxmol
ymolymolymol
0.400-2(x+y)mol
(x+y)mol2(x+y)mol(x+y)mol
(x+y)mol(x+y)mol
列方程组:
24x+40y=2.80
40(x+y)=4.40
解得:x=0.1moly=0.01mol
则n(H2SO4)=xmol+ymol+=0.200mol
c(H2SO4)=0.200mol/0.0500L=4.00mol·L-1
n(MgO):n(Mg)=0.01mol:0.1mol=1:10
【学生展示2】解二元一次方程和守恒思想
设Mg的物质的量为xmol,MgO的物质的量为ymol。
n()=2.00mol·L-1×0.02000L=0.0400mol
Xmolxmolxmol
ymolymolymol
(x+y)mol(x+y)mol
(x+y)mol(x+y)mol
列方程组:
24x+40y=2.80
40(x+y)=4.40
解得:x=0.1moly=0.01mol
n(MgO):n(Mg)=0.01mol:0.1mol=1:10
当滴加氢氧化钠溶液,恰好完全沉淀时,此时溶液中的溶质只有,根据和守恒:2可推出,得:c(H2SO4)×50.0mL×2=2.00mol·L-1×200.0mL
c(H2SO4)==4.00mol·L-1
【学生展示3】抓住镁元素的始态与终态变化关系和图像+守恒思想
根据题意,本题发生了以下反应:
始态:Mg+MgO,终态:MgO
m(O)=m(MgO)終-m(Mg+MgO)始=4.40g-2.80g=1.60g
n(Mg)=n(O)==0.100mol
n(MgO)==0.0100mol
n(MgO):n(Mg)=0.01mol:0.1mol=1:10
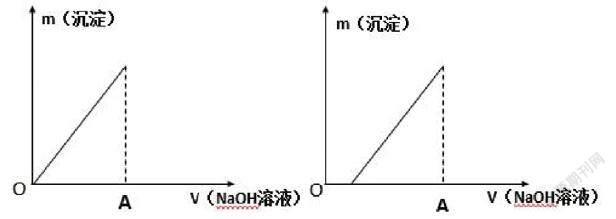
无论硫酸溶液与氧化镁的镁条反应是否过量,当加入氢氧化钠溶液好完全沉淀时,即为A点,此时溶液的溶质仅有,根据和守恒:2可推出,得:c(H2SO4)×50.0mL×2=2.00mol·L-1×200.0mL
c(H2SO4)==4.00mol·L-1
(三)学生自由讨论
三位学生对题目分别做了讲解后,让同学们对这三种解题方法的解题思维和优劣进行评价。有以下几种主要观点:
第1位同学是根据化学方程式进行计算,化学反应方程式很熟悉,不会写错。所以这个方法比较直接,也很容易想到。但是计算过程有点繁琐,很费时间。
第2位同学在计算硫酸浓度时采用了和守恒思想,找到了之间的关系,从而简化了计算过程。但是很难抓住题目的特点,能分析出终态的溶液中溶质只有。这一点很难想得到,但是对这个方法很感兴趣,希望老师给同学们多加训练。
第3位同学计算n(MgO):n(Mg)用了一个很巧妙的方法,抓住了MgO+Mg到MgO的过程中,增加的质量就是O元素的质量,可以看成Mg+O=MgO,从而很快地计算出了第(2)题。
第(1)题最终的思路和第2位同学一样,但是结合了图像,更加直观,理解起来容易些。图像在化学计算中的應用比较薄弱,希望老师多出些题目。
(四)总结与反思
这一阶段,主要是对节课的内容进行归纳总结,从方法上、思维上切合学生的认知水平,了解学生存在的问题所在,根据实际情况灵活运用。
例如本节课,可以适当拓展质量守性、电荷守恒、电子守恒的思想及相关课后练习,还可以关于简单计算的图像问题。
如:2017年4月浙江的29题:
分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份。
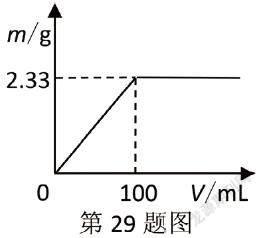
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]∶n(NH4Cl)为________。
(2)另一份固体混合物中NH与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl)=________(溶液体积变化忽略不计)。
三、关于实施“席明纳教式”教学的几点思考
1.前提条件是学生能自觉完课前布置的学案,会对布置内容积极思考。如果学生的学习主动性不高,那么整节课无法开展。学生有思考,才会形成在课堂上的积极参与讨论。
2.这种课堂形式充分体现了学生的学习主动性,他人会有更大的兴趣和热情,上课精神会更加的集中。在课堂上常常会有意想不到的思路,也常常会看到学生争论辩解的精彩和解决问题之后脸上露出成功的喜悦,极大地培养了学生的学习兴趣和学习积极性。
3.实施“席明纳教式”课堂教学,课堂上生成的太多,往往难以控制上课的时间,这就需要教师精心设计教学,紧紧抓住课堂主线,合理组织教学,这就对教师的备课提出了更高的要求。
【参考文献】:
【1】左菁.德国“席明纳”教学模式研究.教育教学论坛,2015年12月48期。
【2】杨静慧.“习明纳”教学模式:优势、功能及其实施原则.广州广播电视大学学报,2009(4)。
