不同剂量非布司他与别嘌醇治疗痛风有效性和安全性的系统评价与Meta分析
2019-09-10袁洪波张伶俐杨春松曾静
袁洪波 张伶俐 杨春松 曾静


中圖分类号 R983+.2 文献标志码 A 文章编号 1001-0408(2019)23-3281-07
DOI 10.6039/j.issn.1001-0408.2019.23.20
摘 要 目的:系统评价非布司他80、40 mg/d与别嘌醇300 mg/d相互对比治疗痛风的有效性和安全性,以为临床治疗提供循证参考。方法:计算机检索PubMed、Embase、Cochrane图书馆、中国期刊全文数据库、万方数据、中国生物医学文献数据库(CBM),检索时限为建库起至2019年3月,收集非布司他80 mg/d(试验组)、40 mg/d(观察组)与别嘌醇300 mg/d(对照组)治疗痛风的疗效和安全性的随机对照试验(RCT),对符合纳入标准的临床研究进行资料提取后,采用Cochrane系统评价员手册5.1.0进行质量评价,采用Rev Man 5.1、Stata 13.0软件对血尿酸降低水平、血尿酸浓度达标率、肝功能异常发生率、肾功能异常发生率、消化道反应发生率、急性痛风发作频率进行Meta分析。结果:共纳入17项RCT,合计1 816例患者。Meta分析结果显示,试验组患者血尿酸降低水平[MD=-70.17,95%CI(-97.41,-42.93),P<0.001]、血尿酸浓度达标率[RR=1.58,95%CI(1.20,2.08),P=0.001]显著高于观察组,血尿酸降低水平[MD=-34.68,95%(-61.35,-8.00),P=0.01]、血尿酸浓度达标率[RR=1.39,95%CI(1.04,1.85),P=0.03 ]显著高于对照组,急性痛风发作频率[RR=1.54(1.02,2.31),P=0.04]显著高于观察组;观察组患者肝功能异常发生率[RR=0.71,95%CI(0.52,0.99),P=0.04]显著低于对照组,以上差异均有统计学意义。其余各组指标比较,差异均无统计学意义(P>0.05)。结论:非布司他80 mg/d对比非布司他40 mg/d和别嘌醇300 mg/d治疗痛风在降低痛风患者血尿酸水平方面效果较好。
关键词 非布司他;别嘌醇;剂量;痛风;Meta分析
Systematic Evaluation and Meta-analysis of Efficacy and Safety of Different Doses of Febustrinol and Allopurinol in the Treatment of Gout
YUAN Hongbo1,2,3,ZHANG Lingli1,2,3,YANG Chunsong1,2,3,ZENG Jing1,2,3(1.Dept. of Pharmacy, West China Second University Hospital, Sichuan University, Chengdu 610041, China;2.Evidence-based Pharmacy Center, West China Second University Hospital, Sichuan University, Chengdu 610041, China;3.Key Lab of Birth Defects and Related Diseases of Women and Children, Ministry of Education, Chengdu 610041, China)
ABSTRACT OBJECTIVE: To systematically evaluate the efficacy and safety of febustrin (80 mg/d and 40 mg/d) and allopurinol (300 mg/d) in the treatment of gout, and to provide evidence-based reference for clinical treatment. METHODS: Retrieved from PubMed, Embase, Cochrane library, CJFD, Wanfang database and CBM during from database establishment to Mar. 2019, randomized controlled trial (RCT) about efficacy and safety of febustrin 80 mg/d (trial group), 40 mg/d (observation group) and allopurinol 300 mg/d (control group) in the treatment of gout were collected. After extracting data of clinical studies met inclusion criteria and quality evaluation with Cochrane system evaluator manual 5.1.0, Meta-analysis was conducted for blood uric acid decrease level, the compliance rate of serum uric acid concentration, incidence of liver dysfunction, incidence of renal dysfunction, incidence of digestive tract reaction and frequency of acute gout attack with Rev Man 5.1 software and Stata 13.0 software. RESULTS: A total of 17 RCTs were included, involving 1 816 patients. Meta-analysis results showed that, the serum uric acid decrease level of patients in trial group [MD=-70.17, 95%CI (-97.41, -42.93), P<0.001] and the compliance rate of serum uric acid concentration [RR=1.58, 95%CI (1.20, 2.08), P=0.001] were higher than observation group; the decrease of serum uric acid level [MD=-34.68,95%(-61.35, -8.00), P=0.01] and the compliance rate of serum uric acid concentration [RR=1.39,95%CI(1.04,1.85), P=0.03] in trial group were significantly higher than control group; the frequency of acute gout attack [RR=1.54(1.02,2.31), P=0.04] in trial group was significantly higher than observation group. The incidence of liver dysfunction in observation group [RR=0.71,95%CI(0.52,0.99),P=0.04] was significantly lower than control group, with statistical significance. There was no statistical significance in other indexes among other indexes (P>0.05). CONCLUSIONS: Compared with febulostat 40 mg/d and allopurinol 300 mg/d, the efficacy of febulostat 80 mg/d is superior in reducing uric acid levels of gout patients.
KEYWORDS Febuxostat; Allopurinol; Dose; Gout; Meta-analysis
痛风是一种由单钠尿酸盐沉积所致的晶体相关性关节病,与嘌呤代谢紊乱及/或尿酸排泄减少所致的高尿酸血症直接相关,属代谢性疾病范畴,高尿酸血症(Hyperuricemia,HUA)与痛风之间密不可分[1]。 随着生活水平的不断提高,HUA所致的痛风患病率呈逐年上升趋势,患病率男性高于女性[2]。特别是在我国经济发达的城市和沿海地区,HUA患病率达5%~23.5%,接近西方发达国家的水平[3]。HUA也是代谢性疾病(糖尿病、代谢综合征、高脂血症等)、 慢性肾病、心血管疾病、脑卒中的独立危险因素[4]。
目前认为发生HUA 80%的原因是体内嘌呤代谢异常和尿酸排泄减少所致[5]。血中尿酸水平主要受两个因素的影响,一是尿酸的生成,二是尿酸的排泄。目前临床常用的降尿酸药物包含增加尿酸排泄的药物和抑制尿酸合成的药物,前者以苯溴马隆和丙磺舒为代表,后者以别嘌醇和非布司他(Febuxostat,又译为非布索坦,商品名:Uloric)为代表。对HUA患者而言,抑制尿酸的合成是关键。别嘌醇及其代谢产物氧嘌呤醇通过抑制黄嘌呤氧化酶的活性(后者能使次黄嘌呤转变为黄嘌呤,再使黄嘌呤转变成尿酸),使尿酸生成减少。非布司他是一种较为新型的降尿酸剂,能够对黄嘌呤氧化酶进行有选择性的抑制,对嘌呤代谢起到较好的纠正作用,同时非布司他还能提高尿酸的排泄率,减少血清中的尿酸含量[6]。
目前关于别嘌醇和非布司他对痛风患者的有效性和安全性存在一定的分歧。吴敏等[7]在一项为期24周的研究结果中显示非布司他与别嘌醇对降低血尿酸浓度均有显著作用,但组间差异无统计学意义。而黎可京等[8]在一项为期20周的研究中显示非布司他与别嘌醇对降低血尿酸浓度组间差异有统计学意义。本研究系统评价临床常用剂量非布司他80 mg/d、非布司他40 mg/d和别嘌醇300 mg/d对痛风患者的有效性和安全性,为临床治疗提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 国内外公开发表的随机对照试验(RCT),无论是否采用盲法均纳入研究,语种限定为中文和英文。
1.1.2 研究對象 符合原发性痛风诊断标准[9];或血尿酸≥405 μmol/L(6.8 mg/dL),其中诊断标准依据2012美国风湿病学会(American College of Rheumatology,ACR) 制订的痛风指南[10];或根据临床确诊。性别、年龄不限。
1.1.3 干预措施 试验组患者采用非布司他80 mg/d;观察组患者采用非布司他40 mg/d;对照组患者采用别嘌醇300 mg/d。疗程不限。
1.1.4 结局指标 ①血尿酸降低水平;②血尿酸浓度达标率;③肝功能异常发生率;④肾功能异常发生率;⑤消化道反应发生率;⑥急性痛风发作频率。
1.1.5 排除标准 ①综述;②观察对象有其他并发症者;③相关数据资料不完整的研究文献;④动物实验;⑤重复文献等。
1.3 检索策略
计算机检索Cochrane图书馆、PubMed、Embase、中国期刊全文数据库(CJFD)、万方数据、中国生物医学文献数据库(CBM)等搜索引擎并纳入符合要求的文献,检索时限为建库至2019年3月。中文检索词包括:“非布司他”“非布索坦”“别嘌醇”或“别嘌呤醇”;英文数据库检索策略使用主题词加自由词检索,英文检索词包括:“Allopurinol”“Allopurin”“Febuxostat”“Uloric”等。
1.4 资料提取
根据所设定的纳入与排除标准,由两位评价员独立对检索得到的文献进行阅读,当意见不一致时由第三位评价员参与讨论并解决。资料提取内容包括:方法学质量、基本信息(题目、作者、发表时间等)、病例特征(各组 病例数、干预措施、疗程等)、结局指标等。
1.5 质量评价
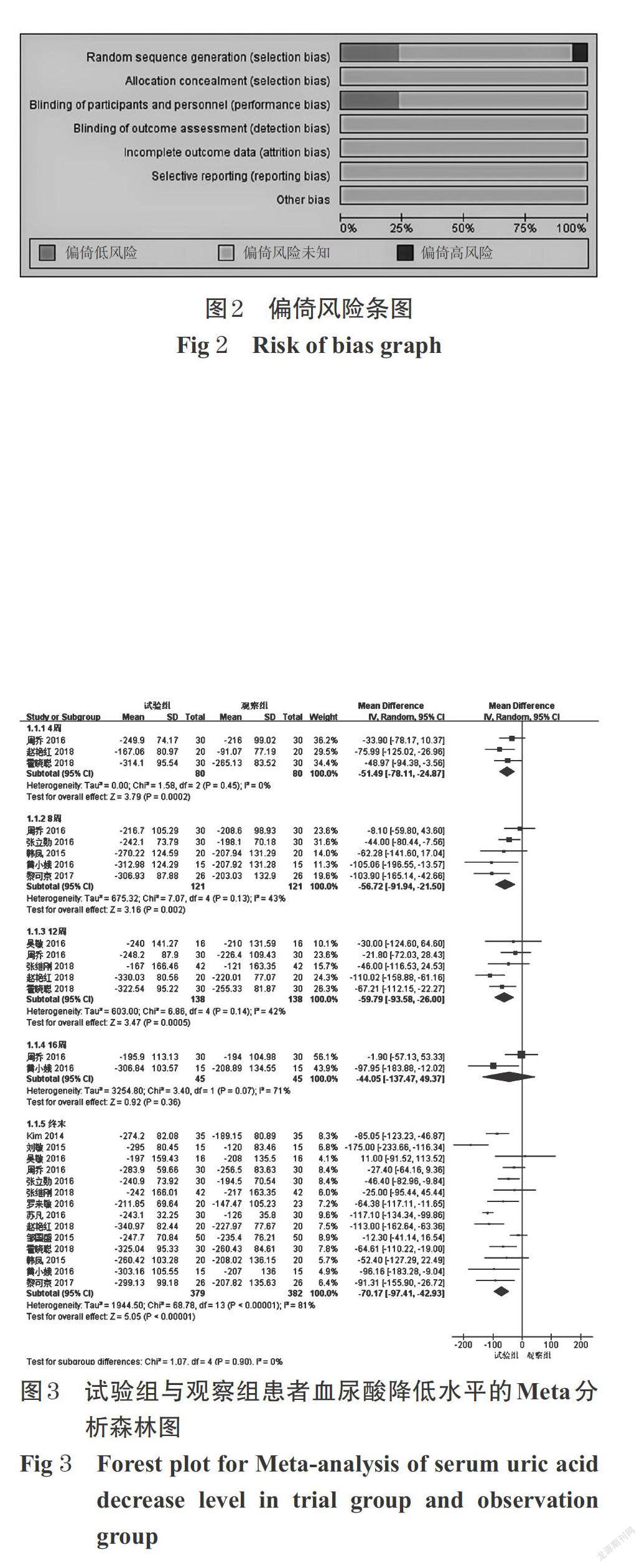
文献质量评价采用Cochrane系统评价员手册5.1.0所推荐的“偏倚风险评估”工具。评价内容包括:随机方法、分配方案隐藏、盲法、结果数据的完整性、选择性报告研究结果、其他偏倚的来源。所有评价条目依研究具体情况按“是”“否”及“不清楚”进行评价。
1.6 统计学方法
采用Cochrane协作网提供的Rev Man 5.1统计软件和Stata 13.0软件进行Meta分析。对纳入研究进行异质性检验,根据I 2及P来判断异质性大小。若各研究结果间无统计学异质性(P>0.10,I 2≤50%),采用固定效应模型进行 Meta分析;反之,则采用随机效应模型进行Meta分析。连续型变量使用标准差(Mean difference,MD)表示,二分类变量采用相对危险比(Risk ratio,RR)表示,区间估计采用 95%置信区间(CI)表示。P<0.05为差异有统计学意义。
2 结果
2.1 文献筛选及纳入研究基本信息
检索得2 516篇文献,阅读题目及摘要,初筛得35篇; 阅读全文后排除18篇,最终纳入研究17篇(项)研究[7-8,11-25],合计1 816例患者。文献筛选流程见图1。纳入研究基本信息见表1。
2.2 纳入研究质量评价结果
纳入的17篇[7-8,11-25]文献,其中16篇[7-8,10-23]文献为中文文献,为国内研究;有1篇[24]英文文献,为韩国学者所做的研究。17篇文献除1篇[17]未提及随机,其余16篇文献均提及使用随机方法分组。有4篇文献[7,10-11,13]提及随机方法,有4篇文献[14,19,23-24]提及使用盲法。偏倚风险图见图2。
2.3 Meta分析结果
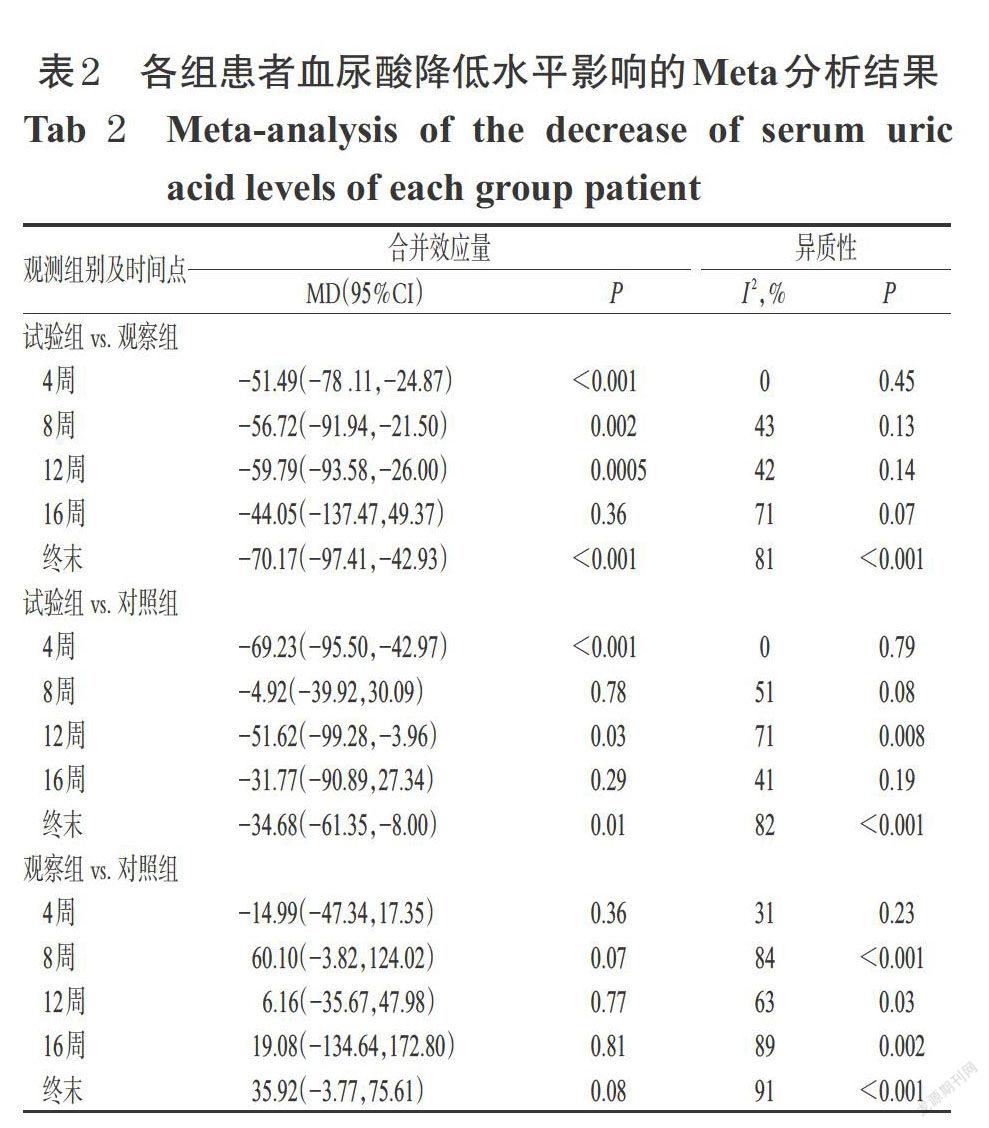
2.3.1 血尿酸降低水平 (1)非布司他80 mg/d vs. 非布司他40 mg/d。14项研究(761例患者,由于部分患者脱落或存在其他情况,故患者数据可能与表1中不完全一致,下同)报道了试验组对比观察组患者血尿酸降低水平[7-8,11-15,17-19,21-23,25]。各研究间有统计学异质性(I 2=81%,P<0.001),采用随机效应模型进行分析。结果显示,试验组患者血尿酸降低水平高于观察组,差异有统计学意义,[MD=-70.17,95%CI(-97.41,-42.93),P<0.001]。对不同观察时点进行比较,结果,4周[MD=-51.49,95%CI(-78.11,-24.87),P<0.001]、8周[MD=-56.72,95%CI(-91.94,-21.50),P=0.002]、12周[MD=-59.79,95%CI(-93.58,-26.00),P<0.001]时,试验组患者血尿酸降低水平高于观察组,差异均有统计学意义。16周[MD=-44.05,95%CI(-137.47,49.37),P=0.36]时,两组血尿酸降低水平相当,差异无统计学意义,详见图3及表2。
(2)非布司他80 mg/d vs. 别嘌醇300 mg/d。14项研究(760例患者)报道了试验组对比对照组患者血尿酸降低水平[7-8,11-15,17-19,21-23,25]。各研究间有统计学异质性(I 2=82%,P<0.001),采用随机效应模型进行分析。结果显示,试验组患者血尿酸降低水平高于对照组,差异有统计学意义[MD=-34.68,95%CI(-61.35,-8.00),P=0.01]。对不同观察时点的比较,4周[MD=-69.23,95%CI(-95.50,-42.97),P<0.000]、12周[MD= -51.62,95%CI(-99.28,-3.96),P=0.03]时,试验组患者血尿酸降低水平高于对照组,差异均有统计学意义。8周[MD=-4.92,95%CI(-39.92,30.09),P=0.78]、16周[MD=-31.77,95%CI(-90.89,27.34),P=0.29]时,两组患者血尿酸降低水平相当,差异无统计学意义,详见表2。
(3)非布司他40 mg/d vs. 別嘌醇300 mg/d。14项研究(760例患者)报道了观察组对比对照组患者血尿酸降低水平[7-8,11-15,17-19,21-23,25]。各研究间有统计学异质性(I 2=82%,P<0.001),采用随机效应模型进行分析。结果显示,观察组患者血尿酸降低水平与对照组比较差异无统计学意义[MD=35.92,95%CI(-3.77,75.61),P=0.08]。对不同观察时点的比较,4周[MD=-14.99,95%CI(-47.34,17.35),P=0.36]、8周[MD=60.10,95%CI(-3.82,124.02),P=0.07]、12周[MD=-6.16,95%CI(-35.67,47.98),P=0.77]、16周[MD=19.08,95%CI(-134.64,172.80),P=0.81]时,两组患者血尿酸降低水平相当,差异均无统计学意义,详见表2。
2.3.2 血尿酸浓度达标率 (1)非布司他80 mg/d vs. 非布司他40 mg/d。4项研究(495例患者)报道了试验组对比观察组患者血尿酸浓度的达标率[12,16,20,24]。各研究间无统计学异质性(I 2=44%,P=0.15),采用固定效应模型进行分析。结果显示,试验组患者血尿酸水平达标率高于观察组,差异有统计学意义[RR=1.58,95%CI(1.20,2.08),P=0.001],详见图4。
(2)非布司他80 mg/d vs. 别嘌醇300 mg/d。4项研究(276例患者)报道了试验组对比对照组患者血尿酸浓度的达标率[12,16,20,24]。各研究间有统计学异质性(I 2=65%,P=0.04),采用随机效应模型进行分析。结果显示,试验组患者血尿酸水平达标率高于对照组,差异有统计学意义[RR=1.39,95%CI(1.04,1.85),P=0.03],详见图4。
(3)非布司他40 mg/d vs. 别嘌醇300 mg/d。4项研究(223例患者)报道了观察组对比对照组患者血尿酸浓度的达标率[12,16,20,24]。各研究间无统计学异质性(I 2=48%,P=0.13),采用固定效应模型进行分析。结果显示,观察组患者血尿酸水平达标率与对照组相当,差异无统计学意义[RR=0.88,95%CI(0.64,1.21),P=0.41],详见图4。
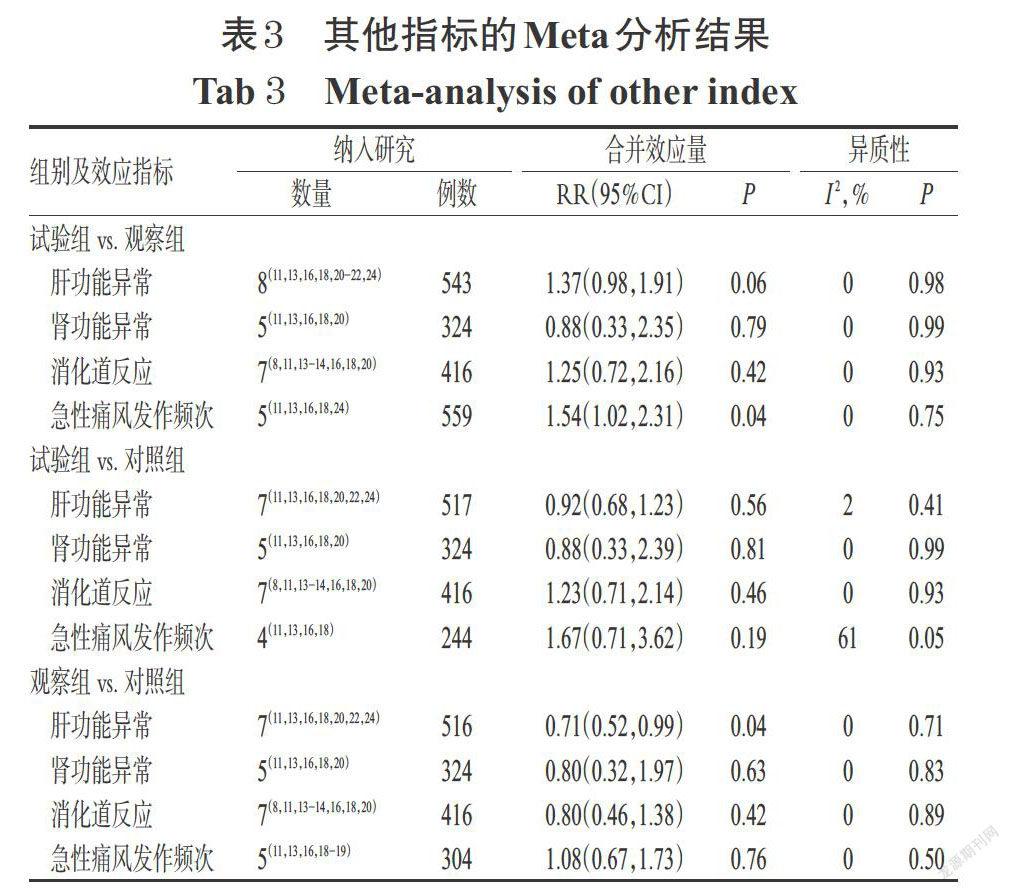
2.3.3 其他指标 其他指标的Meta分析结果见表3。
(1)非布司他80 mg/d vs. 非布司他40 mg/d。Meta分析结果显示,两组患者肝功能异常发生率[RR=1.37,95%CI(0.98,1.91),P=0.06]、肾功能异常发生率[RR=0.88,95%CI(0.33,2.35),P=0.79]、消化道反应发生率[RR=1.25,95%CI(0.72,2.16),P=0.42]比较,差异均无统计学意义。试验组患者急性痛风发作的频率[RR=1.54,95%CI(1.02,2.31),P=0.04]显著高于观察组,差异有统计学意义。
(2)非布司他80 mg/d vs. 别嘌醇300 mg/d。Meta分析结果显示,两组患者肝功能异常发生率[RR=0.92,95%CI(0.68,1.23),P=0.56]、肾功能异常发生率 [RR=0.88,95%CI(0.33,2.39),P=0.81]、消化道反应发生率[RR=1.23,95%CI(0.71,2.14),P=0.46]、急性痛风发作频率[RR=1.67,95%CI(0.77,3.62),P=0.19]比较,差异均无统计学意义。
(3)非布司他40 mg/d vs. 别嘌醇300 mg/d。Meta分析结果显示,观察组患者肝功能异常发生率[RR=0.71,95%CI(0.52,0.99),P=0.04 ]显著低于对照组,差异有统计学意义。两组患者肾功能异常发生率 [RR=0.80,95%CI(0.32,1.97),P=0.63]、消化道反应发生率[RR=0.80,95%CI(0.46,1.38),P=0.42]、急性痛风发作的频次 [RR=1.08,95%CI(0.67,1.73),P=0.76]比较,差异均无统计学意义。
2.4 异质性检验
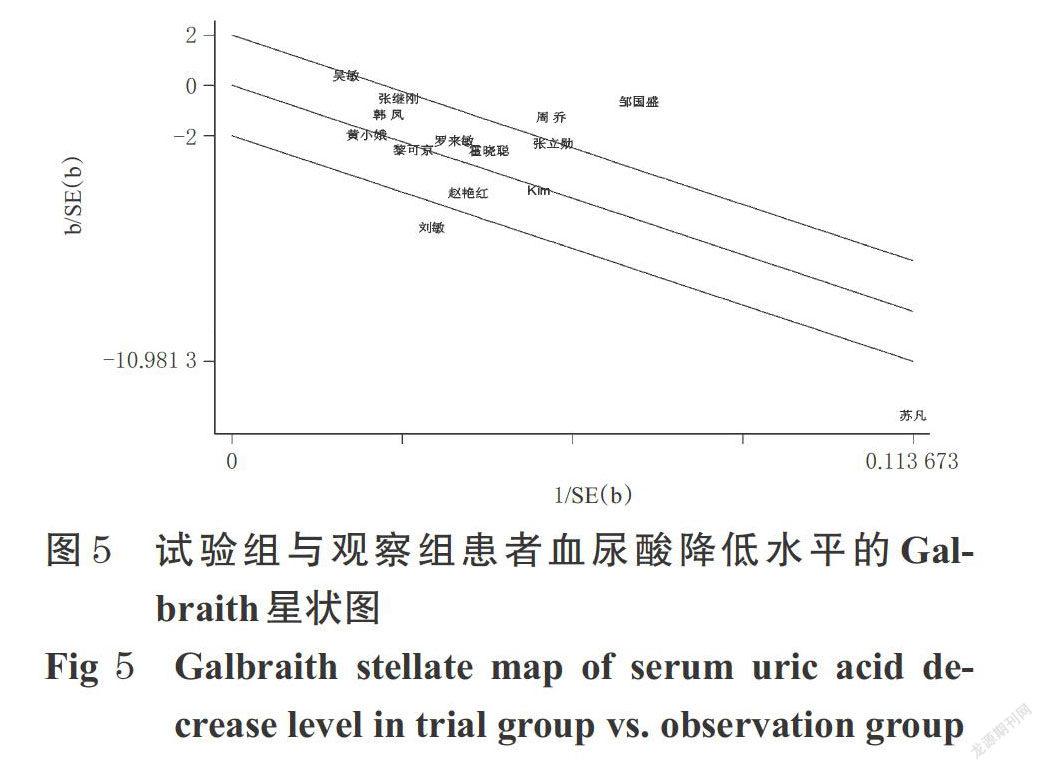
在非布司他对血尿酸水平影响的研究中,Meta分析显示各研究存在较明显的异质性,本研究采用Galbraith星状图来检验存在异质性的文献[26]。在试验组对比观察组治疗痛风的研究中,通过Galbraith星状图发现本项研究异质性主要来自于4项研究[18-19,21-22],剔除后异质性显著降低(由81.1%降至10.7%),效应指标未发生反转。在观察组对比对照组治疗痛风的研究中,通过Galbraith星状图发现本项研究异质性主要来自于6项研究[7,14-15,18-19,21],剔除后异质性显著降低(由81.6%降至16.3%),效应指标亦未发生反转。在试验组对比对照组治疗痛风的研究中,通过Galbraith星状图发现本项研究异质性主要来自于5项研究[8,15,18-19,22],剔除后异质性显著降低(由92.2%降至0),效应指标发生反转(由差异无统计学意义变为差异有统计学意义)。试验组与观察组患者血尿酸水平的Galbraith星状图见图5。
2.5 发表偏倚检验
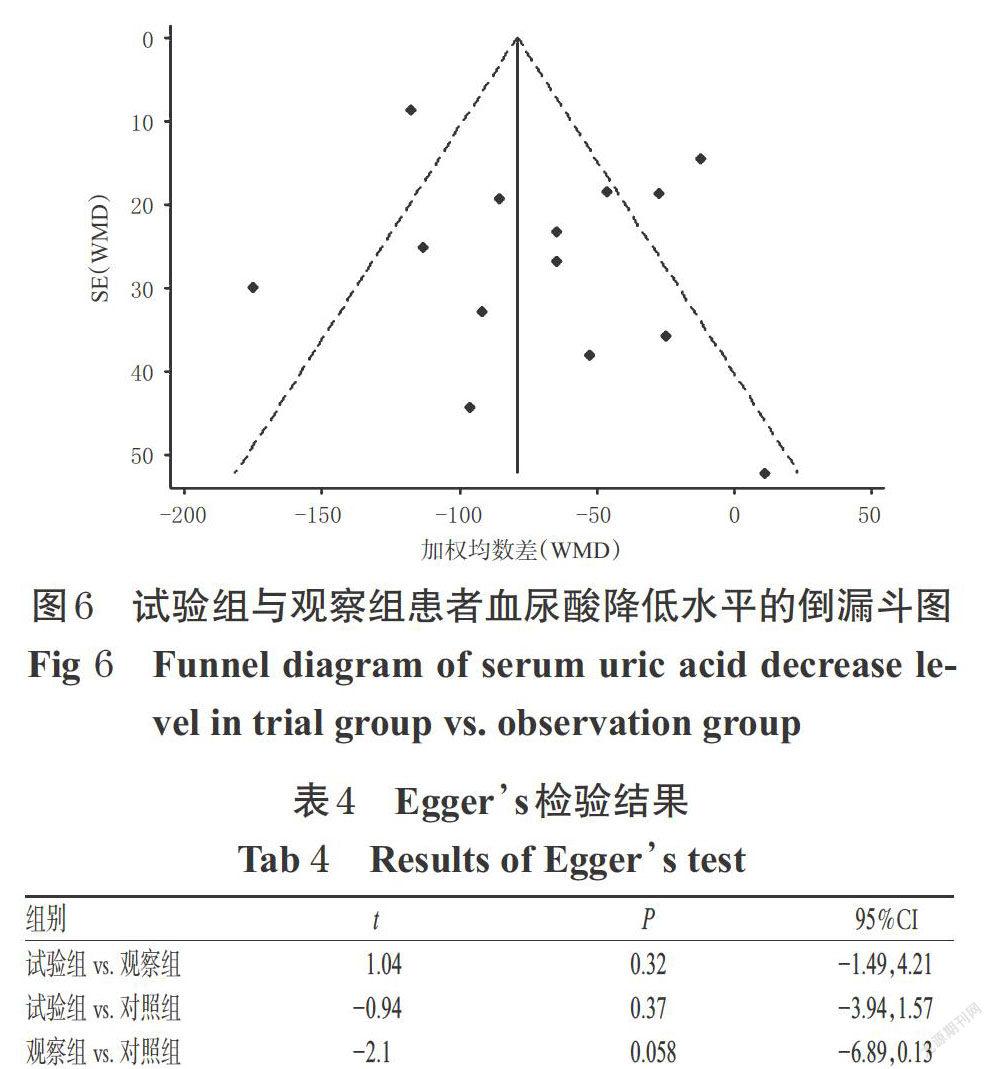
从试验组对比观察组治疗痛风的比较研究的漏斗图观察,该组纳入文献无明显发表偏倚。本研究采用Stata软件中Egger’s检验对主要结局指标的纳入文献的发表偏倚进行定量检验[27]。对血尿酸水平影响的指标Meta分析的Egger’s检验P均>0.05,均未见明显的发表偏倚。试验组与观察组患者血尿酸降低水平的倒漏斗图见图6,Egger’s检验结果见表4。
3 讨论
痛风是由HUA引起的,血清尿酸浓度超过溶解度(6.8 mg/dL)的上限,痛风治疗的主要目标是长期将尿酸降低到饱和水平(<6 mg/dL)下。目前有两类药物可用于此目的:增加尿酸肾排泄的尿酸类药物和减少尿酸合成的黄嘌呤氧化酶抑制剂,其中减少尿酸合成最为关键。
临床常用抑制尿酸合成的药物以别嘌醇和非布司他为代表,两药各有特点。本研究系统性评价了非布司他80、40 mg/d和别嘌醇300 mg/d的各治疗方案对痛风患者血尿酸水平的影响,Meta分析结果显示试验组对血尿酸降低水平或血尿酸浓度达标率均高于观察组和对照组。观察组和对照组在这两方面效果相似,这与Becker MA等[28]的研究结论一致。在数据合并过程中,发现各研究间异质性较大,这可能与各研究观察时间、采样时间、检测方法不同等有关。剔除引起较大异质性的文献后重新合并,试验组对比观察组、试验组对比对照组结果没有发生反转,说明结果较稳定。剔除观察组对比对照组引起较大异质性的文献,重新合并,结果发生反转(从差异无统计学意义变为差异有统计学意义),说明该组结果不太稳定。
虽然非布司他总体效果高于別嘌醇,但是其不良反应也应考虑。本研究显示试验组发生风险是观察组的1.54倍[RR=1.54,95%CI(1.02,2.31),P=0.04],这可能与血尿酸的迅速降低导致单钠尿酸盐晶体从身体尿酸池中移动,从而引发炎症反应[29]有关。虽本研究纳入所有文献并无心血管不良事件的报道,但美国FDA近年来发布非布司他心血管不良事件警示也应重视[30]。在本研究中,无论是在不同剂量的非布司他之间比较,还是不同剂量非布司他与别嘌醇比较,非布司他都表现出对肾功能影响较小的作用,这可能与非布司他主要在肝中代谢[31],且对肾具有一定的保护作用[32]有关。这也间接地解释了中度/重度肾病的存在[33]。
本研究有一定的局限性:纳入文献几乎为中文文献,文献质量有限;大部分研究未报告分配隐藏方法,可能存在选择偏倚。纳入文献样本量较小;观察时间普遍较短;文献检索存在漏检的可能;由于纳入研究对象为单纯性高血尿酸的痛风患者,本研究的结果外推有一定的局限性。
综上所述,非布司他对血尿酸水平的影响总体高于别嘌醇,在较低剂量时,其效果与别嘌醇相似。非布司他不良反应发生率随剂量增加有增加趋势。但上述结论尚需高质量的研究予以证实。
参考文献
[ 1 ] RAGAB G,ELSHAHALY M,BARDIN T. Gout:an old disease in new perspective:a review[J]. J Adv Res,2017,8(5):495-511.
[ 2 ] 李阅东,姚成娥,沈如杰,等.选择性黄嘌呤氧化酶抑制剂非布司他的临床研究进展[J].中国药房,2013,24(26):2472-2475.
[ 3 ] 高尿酸血症和痛风治疗的中国专家共识[J].中华内分泌代谢杂志,2013,29(11):913-920.
[ 4 ] ZHU Y,PANDYA BJ,CHOI HK. Comorbidities of gout and hyperuricemia in the US general population:NHAN- ES 2007-2008[J]. Am J Med,2012,125(7):679-687.
[ 5 ] 杨雪,薛愉,邹和建.非布司他临床应用及不良反应[J].药物不良反应杂志,2014,16(3):168-170.
[ 6 ] 陶小军,金星,陶沙,等.不同剂量非布司他对痛风伴高尿酸血症的效果及对内皮素-1水平的影响[J].中国全科医学,2014,17(2):170-172.
[ 7 ] 吴敏,黄淑玉,晏益民,等.不同剂量非布司他对高尿酸血症伴痛风患者内皮素-1水平的影响[J].国际医药卫生导报,2016,22(3):370-372.
[ 8 ] 黎可京,邱小蕾.非布司他治疗痛风伴高尿酸血症的临床疗效[J].临床合理用药杂志,2017,10(30):86-87.
[ 9 ] 中华医学会风湿病学分会. 2016中国痛风诊疗指南[J].中华内科杂志,2016,55(11):892-899.
[10] KHANNA D,FITZGERALD JD,KHANNA PP,et al. 2012 American college of rheumatology guidelines for management of gout part Ⅰ:systematic non-pharmacologic and pharmacologic therapeutic approaches to hyperuricemia[J]. Arthritis Care Res,2012,64(10):1431-1446.
[11] 张立勋. 90例痛风合并高尿酸血症患者应用非布司他的临床疗效及安全性分析[J].医药前沿,2016,6(24):62- 63.
[12] 霍晓聪,黄新翔,王曼,等.不同剂量非布司他与别嘌呤醇对痛风患者尿酸、NACHT-LRR-PYD结构域蛋白3及白细胞介素-1β水平影响的对比研究[J].广西医学,2018,40(4):378-381.
[13] 张继刚,臧义献.不同剂量非布司他治疗痛风伴高血尿酸症126例临床分析[J].北方药学,2018,15(8):66-67.
[14] 赵艳红.非布司他和别嘌呤醇治疗原发性痛风疗效和安全性的比较[J].浙江医学,2018,40(10):1088-1090.
[15] 韩凤.非布司他治疗痛风伴高尿酸血症的临床效果[J]. 中国当代医药,2015,22(33):81-82,85.
[16] 贾彬.非布司他治疗痛风伴高尿酸血症的有效性及安全性分析[J].中国现代药物应用,2016,10(16):136-137.
[17] 黄小娥,何成松.非布司他治疗痛风伴高尿酸血症患者的有效性及安全性[J].大家健康(学术版),2016,10(4):147.
[18] 周乔,苏江,吴晓丹,等.非布司他与别嘌醇在降尿酸治疗中的有效性和安全性对比研究[J].实用医院临床杂志,2016,13(6):68-70.
[19] 苏凡,林静霞,蔡冬梅.非布司他治疗痛风伴高尿酸血症疗效观察[J].齐齐哈尔医学院学报,2016,37(19):2422- 2423.
[20] 赵瑛,刘小庆,苏阳,等.非布司他治疗痛风及其肝肾毒性的相关研究[J].中国地方病防治杂志,2018,33(3):324-326.
[21] 刘敏,项新,冯振伟.非布索坦和别嘌呤醇对痛风患者血清肌酐影响的对比研究[J].内科,2015,10(4):471-473.
[22] 邹国盛,黄志祥.非布索坦治疗痛风合并高尿酸血症50例[J].中国药业,2015,24(17):111-112.
[23] 罗来敏,陈钦开,杨小娟.降尿酸治疗对痛风高尿酸血症患者IL-1β和 NALP3水平的影响[J].南昌大学学报(医学版),2016,56(1):63-66.
[24] 王丽英,赵燕,郑毅,等.随机双盲三模拟对照多中心临床研究非布索坦降低痛风患者高尿酸水平的疗效和安全性[J].中华临床医师杂志(电子版),2013,7(7):2798- 2803.
[25] KIM HA,SEO YI,SONG YW. Four-week effects of allopurinol and febuxostat treatments on blood pressure and serum creatinine level in gouty men[J]. J Korean Med Sci,2014,29(8):1077-1081.
[26] 王丹,翟俊霞,牟振云,等. Meta分析中的异质性及其处理方法[J].中国循证医学杂志,2009,9(10):1115-1118.
[27] 張天嵩,钟文昭,徐同成.漏斗图的绘制与不对称检验在Stata中的实现[J].循证医学,2009,9(2):110-114.
[28] BECKER MA,SCHUMACHER HR,ESPINOZA LR, et al. The urate-lowering efficacy and safety of febuxostat in the treatment of the hyperuricemia of gout:the CONFIRMS trial[J]. Arthritis Res Ther,2010,12(2):R63.
[29] MARTINON F. Mechanisms of uric acid crystal-mediated autoinflammation[J]. Immunol Rev,2010,233(1):218- 232.
[30] CHOI H,NEOGI T,STAMP L,et al. New perspectives in rheumatology:implications of the cardiovascular safety of febuxostat and allopurinol in patients with gout and cardiovascular morbidities trial and the associated food and drug administration public safety alert[J]. Arthritis Rheumatol (Hoboken,NJ),2018,70(11):1702-1709.
[31] BECKER MA,KISICKI J,KHOSRAVAN R,et al. Febuxostat (TMX-67),a novel,non-purine,selective inhibitor of xanthine oxidase,is safe and decreases serum urate in healthy volunteers[J]. Nucleosides Nucleotides Nucleic Acids,2004,23(8/9):1111-1116.
[32] CHINCHILLA SP,URIONAGUENA I,PEREZ-RUIZ F. Febuxostat for the chronic management of hyperuricemia in patients with gout[J]. Expert Rev Clin Pharmacol,2016,9(5):665-673.
[33] MARCONI E,BETTIOL A,LOMBARDI N,et al. Prescribing patterns of allopurinol and febuxostat according to directives on the reimbursement criteria and clinical guidelines:analysis of a primary care database[J]. Curr Med Res Opin,2019,35(4):683-688.
(收稿日期:2019-06-28 修回日期:2019-08-09)
(编辑:刘明伟)
