应用心脏超声组织多普勒技术评估2型糖尿病合并非酒精性脂肪肝患者的心功能改变特点
2019-08-30杨晓燕罗安果高雪花
杨晓燕,罗安果,高雪花
(1.成都市第七人民医院特检科,四川 成都 610041;2.四川省医学科学院·四川省人民医院心脏超声及心功能科,四川 成都 610072)
在2型糖尿病患者中,非酒精性脂肪肝(Non-alcoholic fatty liver disease,NAFLD)的发生率高达70%~75%[1]。2型糖尿病患者更容易发展成为严重类型的NAFLD,如NAFLD以及严重的肝硬化[1]。世界范围内的流行病学调查亦显示,2型糖尿病患者发生肝硬化、肝衰竭甚至肝癌的风险可增加2到4倍[2]。心血管疾病是2型糖尿病患者最常见的致死原因。当2型糖尿病患者并发NAFLD时,不仅患者发生肝脏相关的致死性疾病的风险增加,其发生心血管相关疾病的风险亦增加[3]。新近研究发现,在非糖尿病人群中,NAFLD的发生与左心室舒张功能不良相关,同时也增加患者发生心房颤动等心律失常的风险[4]。不合并高血压及缺血性心肌病的2型糖尿病患者亦多出现心脏结构及功能异常,而2型糖尿病患者中NAFLD的发病率极高,且NAFLD的发生可能与心脏功能的改变相关[5]。NAFLD是否会影响2型糖尿病患者的心脏功能以及如何影响,尚不明确。本研究拟通过研究2型糖尿病合并NAFLD患者的心功能改变特点以回答上述。
1 资料与方法
1.1 一般资料2017年1月至2018年3月收治于成都市第七人民医院及四川省人民医院的2型糖尿病患者253例,纳入标准:年龄≥18岁,临床诊断2型糖尿病患者。诊断标准:2型糖尿病诊断标准为:空腹血糖≥7.0 mmol/L 或餐后2小时血糖≥11.1 mmol/L或糖化血红蛋白≥6.5%。排除合并缺血性心肌病、慢性心力衰竭、瓣膜性心脏疾病、心房颤动、终末期肾脏疾病、排除病毒性肝脏疾病、排除过量饮酒者。根据肝脏B超检查是否合并NAFLD分为研究组178例,对照组75例。研究分别经成都市第七人民医院及四川省人民医院伦理委员会分别讨论通过,所有纳入本研究的患者均签署知情同意书
1.2 方法
1.2.1基础资料及血清学检查 采集所有最终纳入研究者的基础资料,包括性别、年龄、身高、体重、既往史、饮酒史、吸烟史、家族史,患者至少安静休息5分钟后,由有经验的内科护士用自动血压计测量血压。采集所有最终纳入研究者的清晨空腹外周静脉血,以己糖激酶法检测血糖、以比色法测定糖化血红蛋白、血脂(总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、甘油三酯)以及反应肝功能的各项血液指标(包括谷丙转氨酶、谷草转氨酶、谷氨酰转肽酶)。
1.2.2心脏超声组织多普勒检查 分别由两名有经验的心脏超声专科医生在不了解患者基础信息及肝脏超声检测结果的情况下,应用心脏超声及组织多普勒检测仪器(vivid7,GE)对所有纳入研究者进行心脏超声组织多普勒检查,每项检测指标分别测量三次取均值。通过采集心尖四腔心及二腔心切面测量并计算左心室直径、左心室室壁厚度及重量、左室舒张晚期容积(EDV)及收缩晚期容积(ESV)、左室射血分数(EF值)以及左房容积指数;应用组织多普勒技术测量舒张早期最大峰速(E′)、收缩晚期最大峰速(A′)、E峰减速时间(Dte)及左室等容舒张期时间(IVRT)。通过室间隔及二尖瓣环侧壁的彩色多普勒超声测量舒张早期组织血流速度(e′)、舒张晚期组织血流速度(a′)及收缩晚期组织血流速度(s′)。等容舒张时间常数(tau)根据公式tau=(14.7-100×e′)/0.15计算。舒张末期收缩压(EDP)根据公式EDP= 11.96+0.596×(E/e′的比值)计算。所有超声心动图检测结果均根据美国心脏超声协会(ASE)制定的标准将其舒张功能不全的程度进行分级[6]。
1.3 统计学方法采用SPSS 17.0软件系统。分类变量采用率或百分数表示,两组或三组分类变量比较选用卡方检验,连续性变量采用均数±标准差表示,两组比较采用t检验。趋势检验选用线性趋势检验,即Mantel-Haenszel卡方检验。P<0.05为差异有统计学意义。
2 结果
2.1 所有入组患者中左室舒张功能发生情况所有纳入研究者中,根据ASE所制定的标准,发生轻度舒张功能不良者66例(26.1%),发生中度左室舒张功能不良者87例(30.1%),无左室舒张功能不良者100例(30.5%),未检出重度左室舒张功能不良者,未检出门静脉高压及肝硬化者。
2.2 两组资料及血液指标比较研究组中女性比例更高,体重指数相对更高,确诊2型糖尿病的年限更长,糖化血红蛋白值及谷氨酰转肽酶更高,并发慢性肾脏疾病的风险更大[eGFR<60 ml(min·1.73 m2)],差异有统计学意义(P<0.05),余指标组间差异无统计学意义。见表1。
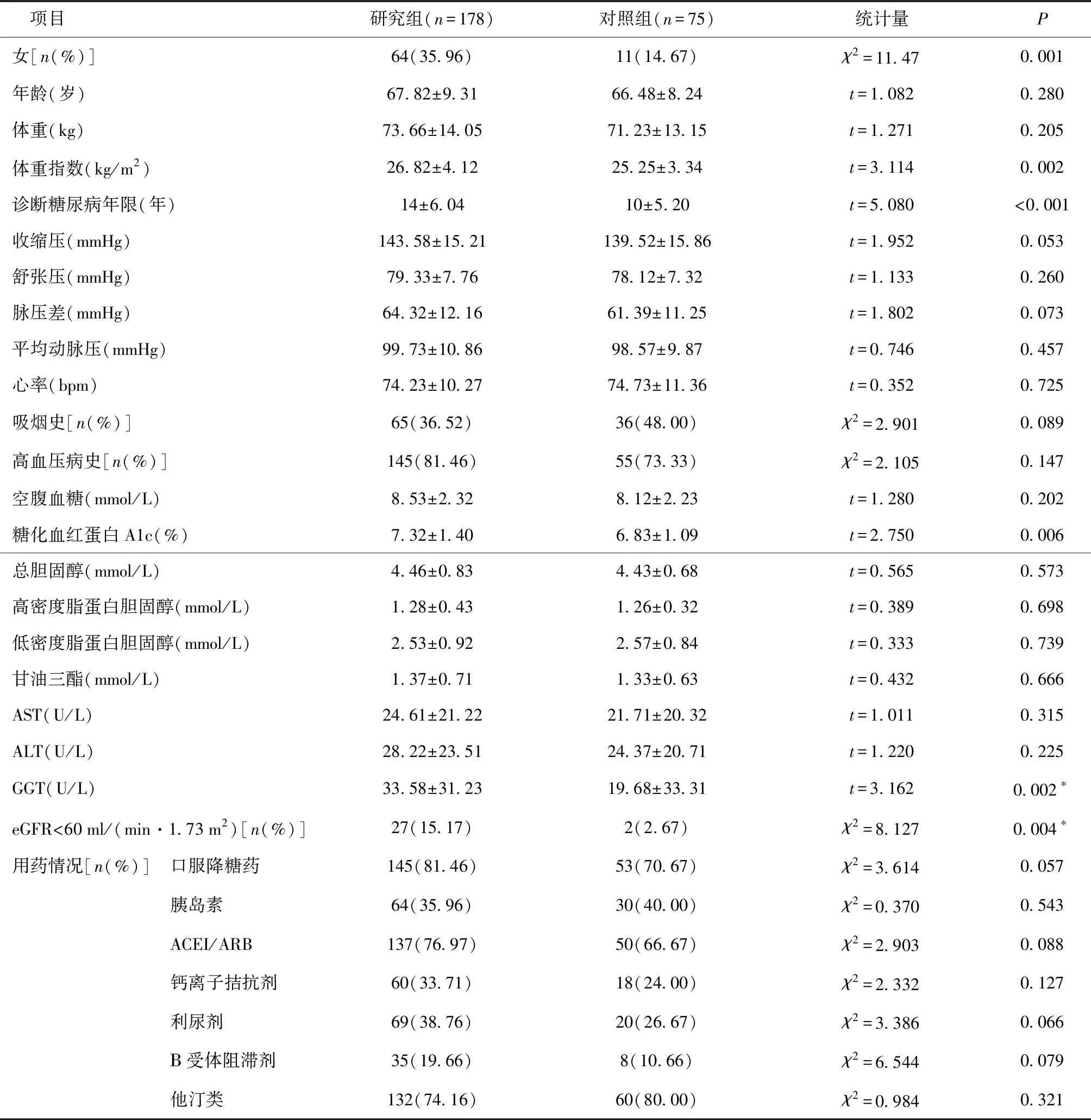
表1 两组一般资料及血液指标比较
2.3 两组心脏超声组织多普勒检查指标对比与对照组比较,试验组具有较低的e’峰速以及左室射血分数;而左房容积指数、E/e’比值、等容舒张常数(Tau值)、左室舒张末期收缩压(LV-EDP值)及左室舒张末期压力容积比(EDP/EDV比值)均更高,差异有统计学意义(P<0.05),见表2。
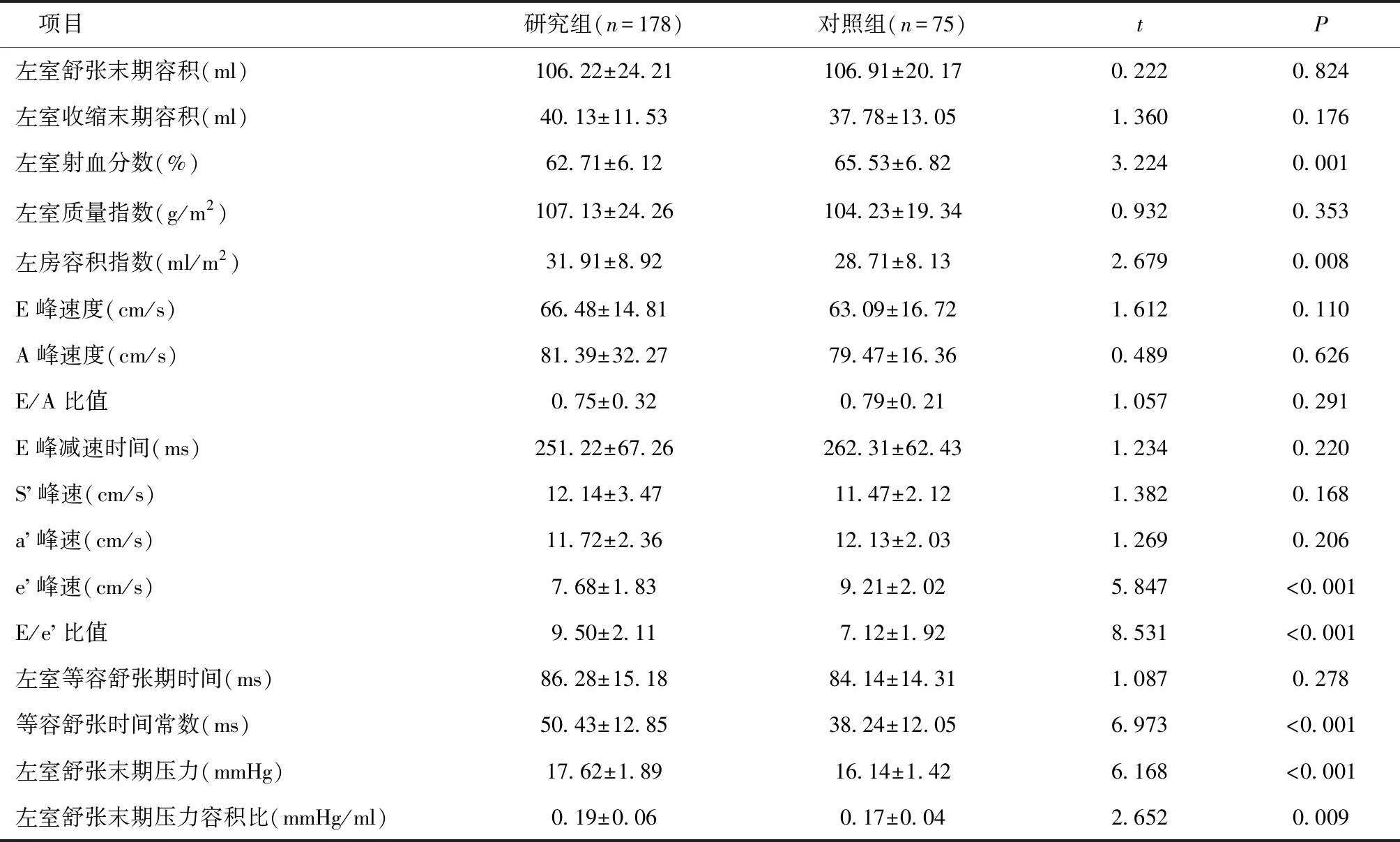
表2 两组间心脏超声组织多普勒检查指标比较
2.4 不同分级的左室舒张功能不良患者中NAFLD的检出率比较无左室舒张功能不良患者中检出NAFLD患者47例(47%);轻度左室舒张功能不良患者中检出NAFLD患者55例(80.9%);中度左室舒张功能不良患者中检出NAFLD患者72例(84.7%)。三组患者中NAFLD检出率随舒张功能不良的分级程度增加而升高,差异有统计学意义(χ2=36.77,P<0.01)。
3 讨论
在既往大量的对照研究中,超声心动图检查均提示不合并2型糖尿病的NAFLD患者(包括成年人和儿童)较无NAFLD的对照组都表现出比较明显的早期左室舒张功能不全的特征[7]。Pacifico等[8]针对108名超重及肥胖儿童的研究指出,NAFLD的组织学病变程度与早期的左室舒张功能不全的部分指标呈正相关,同时通过多元回归分析证明了NAFLD是与E/e’比值的增加密切相关的唯一变量,且具有统计学意义。我们在2型糖尿病患者这样一个特定的人群中进行了NAFLD组及非NAFLD组的对照研究,亦发现合并NAFLD的研究组出现了反应左室舒张功能不全的特征性改变,同时发现NAFLD在发生左室舒张功能不全程度更重的人群中检出率更高,亦提示NAFLD可能还影响左室舒张功能不全的程度。
那么NAFLD究竟是作为一种可能引起异常的脂肪沉积的因素与其它心脏代谢性疾病的危险因素并存于机体,增加其罹患心血管疾病的风险[9];还是作为一种影响心脏结构及功能变化的独立危险因素存在,目前的研究更倾向于后者。
越来越多的证据显示,NAFLD可能是导致心脏结构及功能异常的发病机理之一,而不单是这种心脏病理改变的简单伴随症状[10]。NAFLD引起心脏功能异常的根本机制可能源于NAFLD所致的内脏脂肪细胞的大量增殖及炎症变化,即所谓的脂中毒学说。诸如脂肪因子、游离脂肪酸、激素等因子大量释放时,可引起胰岛素抵抗,最终导致心脏结构及功能的异常[11]。在这个复杂的过程中,肝脏不仅是多器官功能异常所影响到的靶器官之一,还能作为疾病发展的病理调节机制加重心脏及血管的损伤[12]。事实上,NAFLD诱发的胰岛素抵抗及细胞因子释放在左室舒张功能不全及其它结构性心脏疾病的发展进程中扮演了十分重要的角色。另一些研究发现,NAFLD可能通过引起患者心脏基质代谢异常,最终导致心脏结构及功能的异常[13]。亦有证据表明,肥胖相关的心肌以及心外膜脂肪堆积可能引起心脏局部病变,最终亦可引起导致心脏结构及功能的变化[14]。心肌细胞学的研究发现,心脏收缩功能正常的男性2型糖尿病患者心肌脂肪变性发生率更高,而心肌细胞内甘油三酯的含量与左室舒张功能不全的发生密切相关[6]。然而,Graner等在新近的研究中指出,仅肝内的甘油三酯含量及内脏脂肪组织可作为左室舒张功能不全的独立预测因素,而心脏脂肪含量、心外膜及心内膜脂肪与左室舒张功能不全的发生并无关系[15]。该研究进一步佐证了前文所述的脂中毒学说。
本研究虽初步发现了在2型糖尿病这样一个特定的人群中,NAFLD可能与左室舒张功能不全的发生密切相关,为此类病人的远期综合防治提供了新思路。然而NAFLD引起心脏结构及功能改变的具体机制尚且存争议,需要临床与基础相结合的研究进一步证实。
2型糖尿病合并NAFLD患者存在心脏舒张功能降低,且在2型糖尿病患者中,随着左室舒张功能的降低,合并NAFLD的发生概率亦增加。对2型糖尿病合并NAFLD患者的远期综合防治需兼顾对其心功能的保护及改善。
