腐植酸钠中钠含量的电位法测定研究
2019-08-29张彩凤
田 芳 张彩凤 ,2
1 太原师范学院化学系 晋中 030619
2 山西省腐植酸工程技术研究中心 晋中 030619
腐植酸钠是腐植酸的钠盐,可广泛应用于医药、兽药、饲料添加剂、水处理剂等方面[1~5]。物质中钠含量的测定方法有:Na+选择性电极和复合电极测定法[6,7]、原子吸收光谱法[8,9]、离子色谱法[10]、高效液相色谱法[11]、HPCE高效毛细管电泳法[12]和酶法[13]。相对于其他分析方法[14,15],选择性电极电位法测量Na+含量更简便、更具有实际应用价值。
1 实验过程
1.1 试剂与仪器
二次去离子水、氯化钠(优级纯,天津光复),其他相关试剂都为分析纯。样品:山西省腐植酸工程技术研究中心腐植酸钠1,腐植酸钠2。仪器主要采用6801-1型Na+选择电极,Ag/AgCl电极(内参比液为饱和氯化钾),北京哈纳pH 211c型高精度实验室酸度计。
1.2 研究方法及原理
采用电位分析法测定腐植酸钠中Na+含量。具体方法是:用Na+选择电极为工作电极,Ag/AgCl电极为参比电极,待测液为电解液,构成原电池,通过电位计测得电池电动势,测量腐植酸钠中的钠含量。电位响应与待测液浓度对数值关系接近理想的能斯特方程:E=a+klgc,其中E为电池电动势,c为Na+的浓度,a为截距,k为响应斜率。
1.3 研究内容
探究Na+测量最佳pH值范围、Na+测量线性范围和标准线性方程、电位法测量的重现性,研究干扰元素、回收率等。
2 结果与讨论
2.1 溶液最佳pH值范围
溶液的pH对Na+测定有很大影响。分别用pH为6~10的0.06 mol/L盐酸三乙醇胺缓冲溶液为底液配制0.06 mol/L的Na+标准溶液,分别测量其电动势值。测量结果见图1。由图可知,缓冲底液pH<8时,酸度大,对测定有较大影响。当缓冲底液pH≥8时,弱碱性缓冲底液条件下,Na+测量的电动势稳定,灵敏度也高,选择pH为8~10为最佳pH值范围。下面的研究均采用pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液为底液。

图1 pH对电动势的影响Fig.1 Influence of pH on electrode performance
2.2 Na+选择电极的线性范围
采用优级纯NaCl为溶质,120 ℃下烘2 h至恒重。pH为9的0.06 mol/L盐酸三乙醇胺为底液,采用逐级稀释法配制浓度分别为60、50、40、34.5、23、6.9、4.485、3.795、3.45、1.725、1.38、0.69、0.621、0.552、0.483、0.414、0.345、0.276、0.138、0.069、0.0552、0.0483、0.0414、0.02208、0.01932、0.0138、0.0069、0.00276、0.001242、0.001104、0.000966、0.000828 mg/mL的Na+标准溶液,进行测量。其中,二次去离子水的空白电动势值为-121.1 mV。用Na+选择电极作工作电极,Ag/AgCl电极作参比电极测量各标准溶液对应电池电动势,以lgc为横坐标,以电动势E为纵坐标,Origin软件绘图(图2),研究得出Na+选择电极测量Na+的线性范围为1.0×10-3~23 mg/mL,线性回归方程为E=53.1780lgc+83.8768,线性回归相关系数R为0.9997。
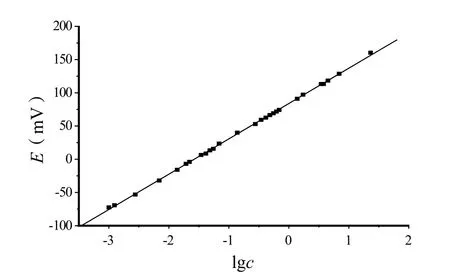
图2 Na+线性回归图Fig.2 Na+ linear regression graph
2.3 重现性
选取样品腐植酸钠1,将其配成10 mg/mL的溶液,平行测定10次,Na+含量为0.69 mg/mL 。所测定的数据见表1。结果显示,样品测量的相对标准偏差(RSD)为0.077%,表明电极测量的重现性好。
2.4 干扰测定
作者研究得出:H+对Na+选择电极干扰是主要干扰。通过加入pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液,控制溶液pH为8~10范围内时,测量电动势稳定,可排除H+的干扰。华秀等[16]研究得出:K+浓度超过Na+浓度的10倍,NH4+浓度超过Na+浓度的70倍时对测定有影响。Li等[17]研究得出:Ca2+、Al3+、Fe3+浓度超过Na+浓度的20倍时对测定有影响,Mg2+浓度超过Na+浓度的40倍时对测定有影响。
2.5 回收率的测定
采用标准加入法来测定回收率。配制10 mg/mL的腐植酸钠样品浓度(用pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液定容),各取50 mL于4个100 mL的容量瓶中。称取12.7106 g NaCl,用二次去离子水定容至100 mL,配成49.97 mg/mL的Na+标准溶液。向上面4个装有等量腐植酸钠样品的容量瓶中分别加入4、6、10、25 mL的Na+标准溶液(Na+的总量要控制在线性范围内),最后用pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液定容,测量电池电动势。再由线性回归方程计算出Na+的总含量。另单独取10 mg/mL的腐植酸钠样品50 mL,直接用pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液定容至100 mL,测定其响应的电池电动势,同理根据线性回归方程得出样品Na+浓度值。Na+的总浓度减去样品Na+浓度所得值为加入标样的浓度实测值,加入标样的浓度实测值与已知加入标样的浓度真实值相比为加标回收率,结果见表2。可以看出,加标回收率在99.99%~100.02%,回收率很好,说明该测定方法准确可靠。
2.6 样品的测量
选取2个腐植酸钠样品各1份。各精确称取1.0000 g,分别用pH为9的0.06 mol/L盐酸三乙醇胺缓冲溶液定容到100 mL。平行3次测量电池电动势,测量电动势在线性范围内,利用标准线性方程和样品称量质量,求得样品的体积含量和质量含量(表3)。

表1 Na+电极响应电位的重现性Tab.1 The reproducibility of Na+ electrode response potential

表2 回收率的测定Tab.2 Determination of recovery rate
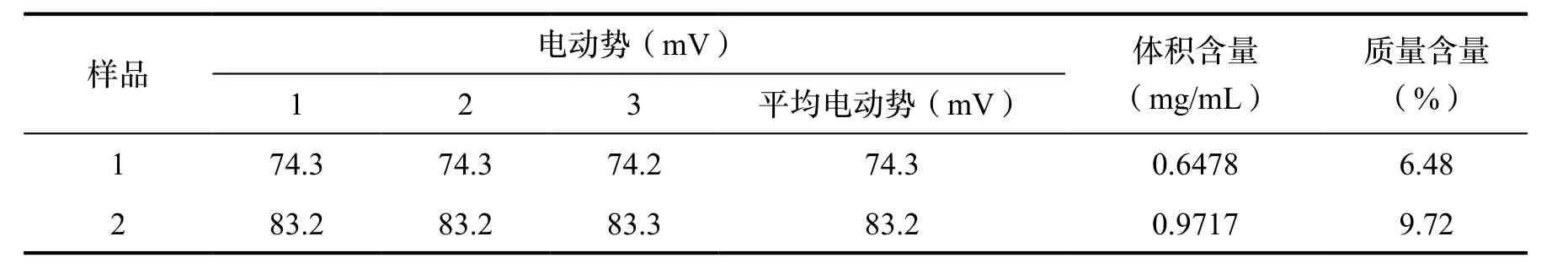
表3 样品的测定Tab.3 Determination of samples
3 结论
研究结果表明:采用Na+选择电极为工作电极,以pH为9的0.06 mol/L的盐酸三乙醇胺缓冲溶液为底液测量腐植酸钠中钠含量,Na+浓度测量的线性范围为1.0×10-3~23 mg/mL,线性回归方程为E=53.1780lgc+83.8768,平均加标回收率为100.00%,相对标准偏差为0.077%。该测定方法线性范围宽,重现性好,准确度高。因此,利用该方法测量腐植酸钠原料及产品中Na+含量更简便、更具有实际应用价值。
