裂殖壶菌高产油突变体的高通量筛选
2019-08-22段光前李硕硕李鑫黄开耀
段光前,李硕硕,李鑫,黄开耀
裂殖壶菌高产油突变体的高通量筛选
段光前1,2,李硕硕3,李鑫3,黄开耀1
1 中国科学院水生生物研究所 中国科学院藻类生物学重点实验室,湖北 武汉 430072 2 中国科学院大学,北京 100049 3 武汉轻工大学 生物与制药工程学院,湖北 武汉 430023
二十二碳六烯酸 (DHA) 具有促进婴幼儿大脑和视网膜发育等多种生理功能,被广泛应用于食品、医药和养殖等行业。为了获得适合于工业化生产的高产油、高产DHA的裂殖壶菌工程株,文中建立了一套操作简单、快速准确的基于尼罗红染色的高通量筛选方案。首先利用紫外线 (UVC) 诱变的方式快速构建裂殖壶菌的随机突变体库。然后采用优化后的筛选条件如裂殖壶菌的最佳尼罗红染色条件 (二甲基亚砜浓度为20%,尼罗红终浓度为2.0 μg/mL,孵育时间为10 min,孵育温度为40 ℃) 和更合理的筛选依据 (多功能酶标仪实现高通量测量的单位细胞密度油脂量) 等,对3 648株突变体进行筛选,得到了3株高产油突变体 (D03432、D05106和D01521)。摇瓶发酵实验表明,这3株突变体在生物量、油脂含量和DHA产量上均高于野生型菌株,其中突变体D03432和D05106的油脂量分别达到了干重的64.74%和63.13%,远高于野生型菌株的43.19%。而且这两株突变体的DHA产量分别是野生型菌株的2.26倍和2.37倍。最后,对突变体D03432和D05106进行了5 L发酵罐发酵培养,相较于野生型菌株,这两株突变体不仅生物量和油脂含量有所增加,而且DHA产量更是分别增加了45.51%和66.46%,展现出较好的工业应用潜力。此外,本筛选方案对其他产油微生物高产油突变体的高通量筛选具有借鉴作用。
油滴,高通量选育,二十二碳六烯酸 (DHA),尼罗红染色
二十二碳六烯酸 (All-cis-4,7,10,13,16,19- docosahexaenoic acid, DHA) 属于ω-3多不饱和脂肪酸,作为一种重要的营养成分,因具有多种生理功能如维持婴幼儿视觉和神经系统的正常发育[1]、预防多种心血管疾病的发生[2]等而备受关注。随着人们健康意识的日益增强,富含DHA的高质量油脂的需求和市场与日俱增[3]。传统DHA来源是深海鱼油,但其可利用性、安全性和可持续性越来越受到诸多因素的挑战,如鱼类资源过度捕捞、海洋环境污染严重和高昂的纯化成本等[4-5]。为了克服这些限制,人们早在1990年就开始尝试利用一些海洋真核微生物如破囊壶菌sp.和裂殖壶菌sp.等,并借助生物技术实现了富含DHA油脂的工业化生产[6-7]。
为了进一步提高裂殖壶菌的DHA产量和降低富含DHA油脂的生产成本,科研工作者们做了多方面的研究,主要集中在以下方面:1) 优化发酵培养基,如采用混合型碳源 (葡萄糖和甘油)[8]、不同种类氮源的添加与限量[9-10]、添加DHA合成的前体物质和加强能量供应 (苹果酸和乙醇[11],丙基没食子酸和丁基苯甲醇[12]的添加) 以及利用不同工业生产中的廉价副产物或废料 (粗甘油[13],废番茄汁和废糖水[14]以及烧酒蒸馏废水[15]) 作为发酵培养基等方法;2) 调控发酵过程参数,如利用在线监测的溶氧数据并结合发酵动力学理论,总结氧传质系数变化的规律,进而制定不同的氧供应策略,从而实现DHA的增产[16-17];3) 改进发酵方式,早期主要是采用分批发酵或补料分批发酵的发酵方式[18-20]生产富含DHA油脂,虽然这种发酵方式具有操作简单、污染率低和体系成熟的优势,但是也存在明显劣势如发酵批次差异性大、单位体积产率低和产品质量不稳定[21]。后来发展的连续发酵虽能有效提高容积产率、设备利用率以及产品质量的稳定性,但常以牺牲产品的浓度或转化产率为代价[22],Guo等研究提出的多阶段连续发酵策略有望避免这些缺陷[21]。然而,在裂殖壶菌遗传改造和优良菌株的选育方面鲜有报道。由于基因组信息的匮乏,以及DHA合成机制的不完善,外加没有成熟的转化系统,对裂殖壶菌遗传改造也只是停留在含有单个内源或外源基因的表达载体转化上[23-24],而且存在转化系统不稳定的问题,关键是转化子的DHA产量并无明显提升。另外,在优良菌株选育上,利用持续的环境压力如高氧[4]、高盐[25]对菌株进行驯化,虽然能部分增加DHA产量,但是驯化周期过长,不适合作为大规模选育策略。因此,低成本、高通量的高产油 (富含DHA) 突变体的筛选方案,对实现优良菌株大规模选育是迫切需要的。
尼罗红 (Nile red, NR) 是一种脂溶性的荧光染料,能与细胞内中性油脂结合并发出荧光,而且荧光的强度与中性油脂量存在线性相关,故可用于中性油脂含量的检测[26]。NR染色法检测中性油脂相较于传统油脂检测方法更为简单、省时,结合荧光检测仪器如酶标仪[27]、流式细胞仪[28]的使用,可显著提高检测效率,已被应用于多种细胞的中性油脂检测,如哺乳动物细胞[29]、细菌[30]、酵母[31]和微藻[32]等。因此,可以选用NR染色法并结合多功能酶标仪来高通量检测裂殖壶菌染色荧光,从而判断裂殖壶菌细胞内中性油脂含量高低。
鉴于此,本着低成本、高通量和操作简单的原则,设计出此套筛选方案:1) 以裂殖壶菌SR21 (曾被命名为SR21[33]) 作为出发菌株,并利用紫外线 (UVC) 诱变的方式来快速构建随机突变体库;2) 突变体培养于96孔板一段时间后,利用多功能酶标仪检测突变体细胞密度 (595) 和NR染色荧光强度 (Fluorescence intensity, FI),从而筛选出高产油、高产DHA突变体;3) 对筛选出来的突变体进行表型验证。最后,对表现较好的两株高产油突变体进行了5 L发酵罐发酵培养,相较于野生型菌株,不仅生物量与油脂量增加显著,而且DHA产量也分别超过45.51%和66.46%,初步展示出其工业应用潜力。
1 材料与方法
1.1 菌种与培养
菌株裂殖壶菌SR21 (ATCC- MYA-1381) 购自美国模式培养物保藏所 (The Type Culture Collection, ATCC),保存在固体种子培养基上,并留种保藏于−80 ℃冰箱的甘油管中。
种子培养基 (g/L):葡萄糖5;酵母提取物1;蛋白胨1;海水晶30;琼脂15。
筛选培养基修改于种子培养基,将海水晶浓度增至40 g/L。
初始摇瓶培养基 (g/L):葡萄糖30;酵母提取物10;NaCl 0.3;Na2SO415;谷氨酸钠15;K2SO41;MgSO4∙7H2O 4;KH2PO40.1;CaCl20.05;vitamin B10.008;vitamin B60.002;vitamin B120.008。
初始发酵罐培养基 (g/L):葡萄糖50;酵母提取物10;NaCl 0.3;谷氨酸钠15;K2SO41;MgSO4∙7H2O 4;KH2PO40.1;CaCl20.05;vitamin B10.008;vitamin B60.002;vitamin B120.008。
摇瓶发酵培养[8]:将培养至对数期的种子培养液,以4% (/) 的接种量接种于装有100 mL摇瓶发酵培养基的锥形瓶 (500 mL) 中,于28 ℃、200 r/min的恒温摇床上培养。在培养第3天加入40 g/L的葡萄糖和10 g/L甘油,第4天加入20 g/L的甘油。每12 h收集1 mL培养液,测量595值,发酵结束后,收获培养液用于细胞干重 (Dry cell weight, DCW)、油脂含量和DHA含量测定。每个菌株设置3个生物学重复。
5 L发酵罐补料发酵:发酵策略修改于文献[8]中单碳源 (仅葡萄糖) 补料策略,氮源的补料时间为24 h和36 h。发酵时的工作液为2 L,用16 mmol/L HNO3调节pH值使保持在6.5–8.0 之间,培养温度为28 ℃。通气策略:保持转速为300 r/min,空气流速为90 L/h。每12 h取发酵液80 mL用于DCW、总油脂量和脂肪酸组成的测定。
1.2 紫外线 (UVC) 诱变构建裂殖壶菌突变体库
以裂殖壶菌作为出发菌株,接种于种子培养基培养至对数生长期,取培养液10 mL稀释到一定细胞密度 (约105个/mL) 分装于培养皿中,在2支15 W紫外灯 (辐照度约为0.5 mW/cm2) 下分别照射不同时间,照射结束后,放置黑暗条件12 h 左右,取出培养皿,将培养液均匀涂布于平板上培养2 d后,分别计数菌落数,计算致死率。
致死率=(1–不同处理菌落数/未处理菌落数) ×100%。
通过致死率曲线,得出紫外线最佳诱变时间。以最佳诱变时间进行多次紫外诱变,基本步骤同上,最后将单克隆挑取、转接于新平板并编号、弱光保存,以此构建裂殖壶菌突变体库。
1.3 裂殖壶菌的NR染色条件优化与突变体筛选
取裂殖壶菌培养至对数期的培养液适量, 3 000×离心15 min,弃上清,细胞沉淀用新鲜的种子培养基重悬,使细胞密度约为107个/mL,分别取1 mL重悬液于棕色离心管中,分别加入250 μL的一定体积分数的DMSO溶液,振荡混匀,再加入适量的0.1 mg/mL NR染液,再次振荡混匀,于恒温水浴锅中孵育一段时间后,取96孔黑色酶标板,每孔加入200 μL NR菌细胞染液,使用多功能酶标仪 (Filter Max F5, Molecular Devices, USA) 检测激发光波长为 (485±20) nm、发射光波长为 (595±10) nm的荧光强度,并扣除未染色菌液的荧光强度,即为所测得的荧光强度。
裂殖壶菌的NR染色条件优化:初始NR染色条件,溶剂载体DMSO溶液浓度为25%;NR染液的用量为15 μL;孵育的时间为15 min;孵育的温度为50 ℃。然后对这4个条件逐一进行优化。所有染色组和未染色组均设置3个生物学平行。
裂殖壶菌突变体的筛选:分别挑取裂殖壶菌突变体接种于装有200 μL筛选培养基的96孔透明板,培养一段时间,先利用多功能酶标仪测量595值,然后用排枪将各孔培养液转于96孔黑色酶标板中,进入优化的NR染色步骤,利用多功能酶标仪进行NR荧光测量。筛选出每板FI/595值前五的突变体,进行重复筛选,并转板保存。
1.4 裂殖壶菌油滴形态的荧光显微镜观察
取适量裂殖壶菌培养液,3 000×离心5 min,加一定新鲜培养基重悬,加入适量DMSO,用NR染液染色一段时间后,吸取10 μL菌细胞染液制片,并加入2 μL荧光抗淬灭剂 (P0126, Beyotime, China),置于激光扫描共聚焦显微镜 (Leica TCS SP8, USA) 下进行观察。使用488 nm的氩激光器激发,在560–600 nm过滤通道检测标记油滴形态的NR荧光[28],荧光图片由Leica自带软件 (LAS AF Lite) 处理。
1.5 细胞干重、总油脂量和脂肪酸组成的测量
细胞干重的测量:收集发酵液适量,3 000×离心15 min,用磷酸盐缓冲液洗涤,再次离心去上清,置于−80 ℃冰箱冷冻后,用真空冷冻干燥机 (FreeZone 6 Plus, Labconco, USA) 进行干燥后称重,测得DCW。
总油脂提取与测量 (采用Blight-Dyer法[34],略有修改):称取少量菌体干粉,加入1.5 mL氯仿/甲醇 (1∶2,/) 涡旋1 min,离心 (2 057×, 15 min) 后收集上清液于15 mL离心管中,下层残留液继续用1 mL氯仿/甲醇 (1∶2,/) 萃取3次后,合并所有有机相于预先称重的玻璃管中,置于氮吹仪下吹干,再称重,获得总油脂量。
脂肪酸甲酯化 (参考文献[35]中方法,略有优化):向提取的油脂中加入0.5 mol/L NaOH-甲醇溶液1 mL,60 ℃水浴加热至油脂完全溶解,再加入1 mL的14% BF3-甲醇溶液,60 ℃水浴酯化20 min,流水冷却至室温后,多次加入2 mL色谱级正己烷 (Sigma公司,美国) 萃取至有机相为无色透明,加入0.5 g 无水Na2SO4吸收残余水,离心后,用注射器吸取,经0.45 μm有机滤膜过滤后注入棕色瓶,用于气相色谱质谱联用 (Gas chromatograph- mass spectroscopy, GC-MS) 分析。
GC-MS分析:采用Agilent HP 7890A (Avondale, PA, USA) 气相色谱与MSD-5957C质谱检测联用装置进行检测分析,使用Agilent HP-88 (60 m× 0.25 mm×0.25 μm) 色谱柱,喷射器温度保持250 ℃,分流比1∶20,氦气流速为1.0 mL/min,柱温165 ℃维持10 min,5 ℃/min速率升至210 ℃并保持5 min,进样口接口温度250 ℃,探测器电压1.50 kV,采用自动进样装置 (GC Sampler 80, Agilent Technologies) 进样,进样量为1.0 μL。采用全扫描模式 (/, 20–500),使用外标法进行定量分析。
2 结果与分析
2.1 紫外线 (UVC) 诱变构建裂殖壶菌突变体库
为了安全、快速构建裂殖壶菌突变体库,本研究选用UVC (253 nm) 作为裂殖壶菌随机突变的诱变剂。如图1所示,在UVC的辐照度约为0.5 mW/cm2下,随着UVC照射时间增加 (0–20 s),细胞的致死率急剧上升,直到照射时间为40 s时,致死率达到92.40%,随后 (40–80 s) 呈缓慢上升趋势,在照射时间为100 s时,只有少数几个克隆存活,致死率几乎达到100%。根据育种工作者长期的研究和实践经验,一般认为致死率以90%–99%效果较好,且较低的致死率有利于正突变的产生[36],故选择UVC照射40 s作为诱变剂量。确定好诱变剂 (UVC) 和诱变剂量 (照射40 s)后,对出发菌株进行诱变处理,构建了一个约含3 600个克隆的随机突变体库。
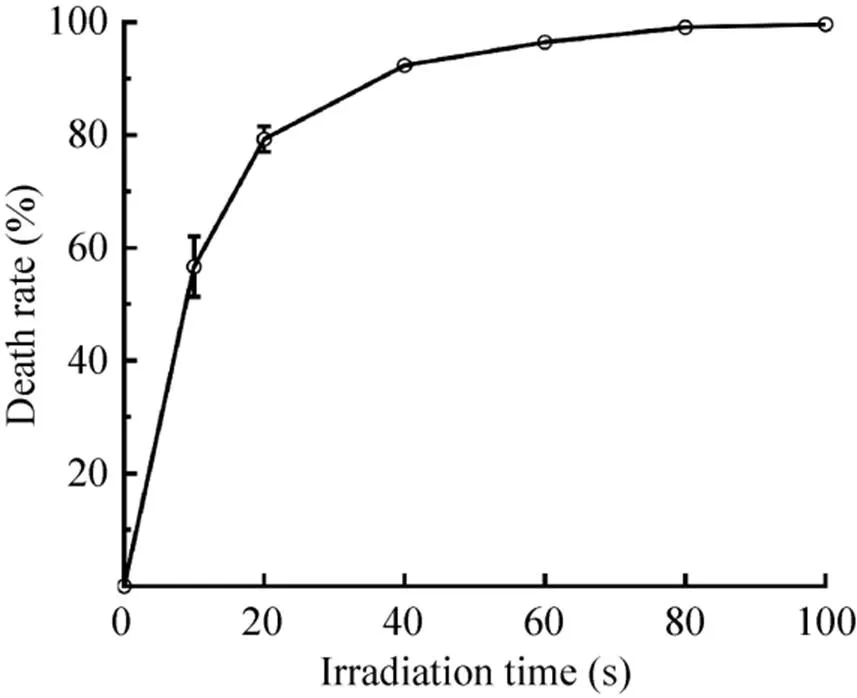
图1 紫外线(UVC)照射时间对裂殖壶菌的致死效应
2.2 裂殖壶菌NR染色条件的优化
为了更准确地通过NR染色荧光强度表征裂殖壶菌的中性油脂含量,则需要优化裂殖壶菌 NR染色的如下条件:1) 溶剂载体二甲基亚砜 (DMSO) 浓度;2) NR的终浓度;3) 孵育时间;4) 孵育温度。
2.2.1 溶剂载体DMSO浓度的优化
由于细胞壁的存在以及NR是脂溶性的染料,这会很大程度影响NR扩散进入细胞,进而影响NR染色效果,最终使得中性油脂含量的测量结果缺乏准确性[37]。NR染色时,加入适量的NR溶剂载体如DMSO[32],能有效增加细胞壁的渗透性和NR的扩散能力,增强NR染色荧光强度。本研究选用DMSO作为NR染色的溶剂载体,并摸索适用于裂殖壶菌的最佳DMSO溶液浓度。如图2A,在DMSO溶液浓度 (/) 为0–20%时,NR染色的荧光强度逐渐增加;直到DMSO溶液浓度为20%时,NR染色的荧光强度达到最大值;在DMSO溶液浓度为20%–50%时,NR染色的荧光强度反而逐渐降低。因此,随后的其他NR染色条件优化实验,均以DMSO溶液浓度为20%来进行。

2.2.2 NR终浓度的优化
在一定的细胞密度情况下,过低的NR终浓度会使荧光强度偏低,无法切实反映出细胞中性油脂高低。而过高的NR终浓度也会使荧光强度偏低,是因为过多的NR分子会发生堆积现象,从而使与中性油脂结合的NR分子更多地暴露在样品中的亲水性淬灭剂中,所测的荧光强度就自然偏低[38]。如图2B所示,当NR终浓度为2.0 μg/mL时,染色荧光强度最大,而过低 (<1.0 μg/mL) 或过高 (>3.0 μg/mL) 的NR浓度都会出现荧光强度明显下降的现象。所以选择2.0 μg/mL作为最佳的NR终浓度。
2.2.3 孵育时间的优化
NR分子需要一定时间的扩散才能透过细胞壁、细胞膜,与胞内中性油脂充分接触产生荧光,但过长的孵育时间,会导致NR分子的堆积而使其溶解度降低,加之待测样中水溶性淬灭剂的存在,最终会加快荧光的淬灭[38-39],因此适当的孵育时间对中性油脂的准确测量很是重要。如图2C所示,分析了不同NR孵育时间对荧光强度的影响,随着NR孵育时间增加,NR染色荧光强度也逐渐增加,直到孵育时间为10 min时达到最大值,随后NR染色荧光强度逐渐下降。由此,选择10 min 作为最佳孵育时间。
2.2.4 孵育温度的优化
较高的NR孵育温度会加快NR分子扩散进入细胞,增强NR染色荧光,但过高的孵育温度会加速NR染色荧光的淬灭,所以寻求合适的孵育温度很有必要。如图2D所示,发现当NR孵育温度为10–40 ℃时,NR染色荧光逐渐增强,并在40 ℃达到最大值;而当NR孵育温度从40 ℃到70 ℃时,荧光逐渐减弱。类似的结论,也出现在Chen等[32]优化小球藻NR孵育温度的研究中。因此,得到最佳NR孵育温度为40 ℃。
2.3 选用荧光强度 (Fluorescence intensity, FI) 与OD595的比值 (FI/OD595) 作为筛选高产油突变体的依据
在实际筛选裂殖壶菌高产油突变体过程中,由于各个突变体的接种量和培养过程中的生长状态均存在差异,使得NR染色时各突变体的细胞密度不一,会直接影响到油脂量高低的判断。因此需要测量细胞密度,得到单位细胞密度的荧光强度,以解决由细胞密度不同带来的影响。为了快速、高通量地获得细胞密度,本研究巧妙地采用了多功能酶标仪测光密度 (Optical density,) 的方法。
理论上,在某一时刻、某一培养条件下,裂殖壶菌的单位细胞密度油脂量应该是一个常数,即FI/595是一个常数。如图3所示,对同一培养条件下的裂殖壶菌细胞的不同595值与其对应的荧光强度进行相关性分析 (取截距为0),发现两者存在极显著的相关性 (相关系数为0.999 7),荧光强度 () 与595值 () 的比值是一个常数 (26.423×107)。因此,可以用荧光强度与595的比值 (FI/595) 来表示裂殖壶菌单位细胞密度中性油脂量,并作为高产油突变体的筛选依据。
2.4 裂殖壶菌NR染色时间点的选择
在实际筛选过程中,为了在保证能最大程度地区分高产油突变体的前提下进一步缩短筛选时间,则需要缩短裂殖壶菌发酵过程的3个时期[7],即细胞快速生长期、油脂大量积累期和稳定期。为此,选用了能维持裂殖壶菌经历发酵过程3个时期的筛选培养基[8]。如图4所示,采用筛选培养基培养裂殖壶菌,经过较短 (0–18 h) 的细胞快速生长期直接进入了稳定期,其中,在0–6 h时,细胞密度 (595) 快速上升,虽细胞油脂 (FI) 有少量积累,但单位细胞密度油脂量 (FI/595) 反而下降;随后的6–18 h过程中,细胞密度快速上升的同时细胞油脂积累也是急剧增加。进入18–30 h的稳定期,细胞密度几乎保持平稳,细胞油脂 (FI) 积累稍微增加,单位细胞密度油脂量在30 h时达到最大值。最后,进入衰弱期 (发酵时一般在此时期前就停止发酵,因此发酵时无此时期),细胞死亡量增加、细胞破碎以及自身油脂反耗,细胞密度和细胞油脂积累均下降。为了尽可能地提高筛选的准确性,则需要突变体的单位细胞密度油脂量大于WT的最大单位细胞密度油脂量。综上所述,选择培养30 h时作为NR染色的时间点。

图3 OD595值与荧光强度的相关性

图4 裂殖壶菌在筛选培养基培养下的细胞生长与油脂积累的时间过程
2.5 裂殖壶菌随机突变体库的筛选结果
利用多功能酶标仪以及摸索好的筛选条件,对裂殖壶菌随机突变体库进行了高通量的筛选。为了更进一步提高筛选的准确性,初筛出每两个96孔板FI/595值前5的突变体,然后重复第一轮筛选流程进行复筛。如图5所示,展现的是复筛的结果,以野生型 (Wild type, WT) 裂殖壶菌的FI/595值作为分界线,将复筛的突变体分为两组:一组是FI/595值高于WT的油脂量上升组 (Up group),包含55个突变体;另一组是FI/595值低于WT的油脂量下降组 (Down group),包含40个突变体。在油脂量上升组中,突变体的FI/595值超出WT在0–50%之间的有74.55% (41/55),超出WT 50%以上的有25.45% (14/55),其中FI/595值前3的突变体 (★表示),更是分别超出了85.37%、93.28%和116.33%。在油脂量下降组中,多数突变体的FI/595值集中在低于WT的30%以内,最低FI/595值的突变体仅为WT的40.42%。

图5 裂殖壶菌随机突变体库的复筛结果
2.6 高产油突变体的表型验证
为了证实所筛选出的突变体为高产油的突变体以及筛选方案的准确性,选取FI/595值前3位的突变体 (D03432、D05106和D01521) 作进一步的表型鉴定。首先,对这3株突变体进行摇瓶发酵培养,从生长状态 (生物量)、油脂积累 (油滴) 以及DHA含量等表型来进行鉴定分析。如图6所示,记录的是3株突变体与WT摇瓶培养的发酵过程,观察到3株突变体均要比WT生长得快,其中D03432和D05106的细胞生长速率较WT有显著的提高 (<0.01,检验)。发酵至稳定期132 h时,这两株突变体的595值分别比WT高31.85%和27.45%。另外,突变体D01521也比WT高16.46%。
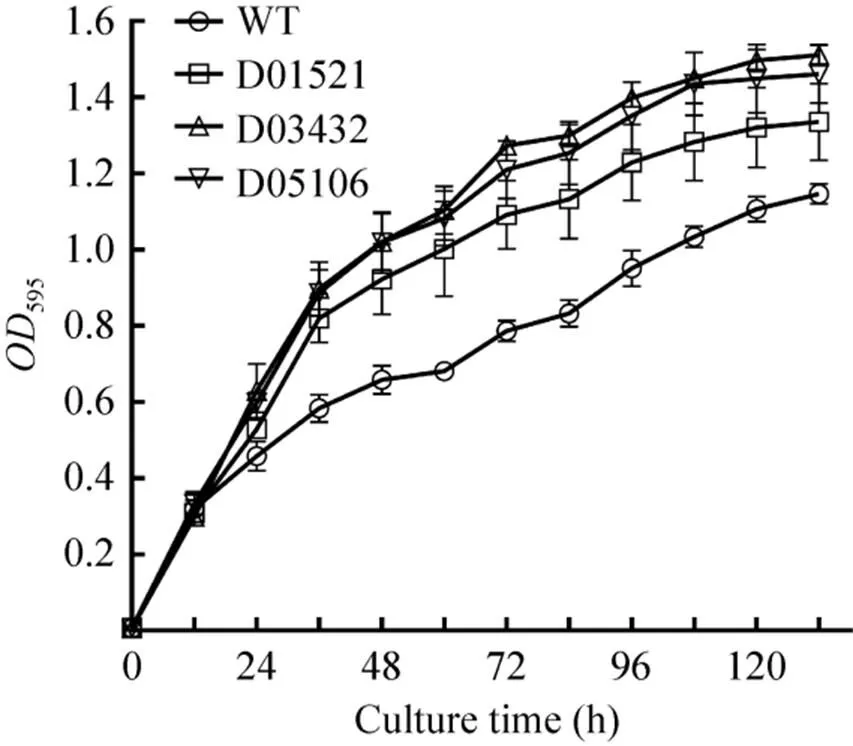
图6 裂殖壶菌野生型与候选的高产油突变体在摇瓶发酵下的生长曲线
裂殖壶菌细胞内的油脂积累变化规律是前期缓慢上升,对数期时快速上升,到稳定期时经缓慢上升后达到最高峰[7],而合成的油脂则主要储存于油滴 (Lipid droplets or oil bodies) 这一细胞器中[40-41],因而为了更明显区分突变体与WT油脂积累的差异,选择在细胞积累油脂最快的时期 (36 h) 进行油滴观察。如图7所示,NR染色后,采用激光扫描共聚焦显微镜对细胞进行观察,发现这3株的突变体细胞内油滴直径均要大于WT,而且突变体的细胞内油滴数目较WT更多。

图7 裂殖壶菌野生型与候选的高产油突变体在发酵36 h时的油滴形成情况
发酵结束后,测得突变体D01521、D03432 和D05106的干重依次为 (23.35±0.55) g/L、(30.10±0.35) g/L和 (28.49±1.35) g/L,均高于WT的干重 (20.22±1.18) g/L,其中突变体D03432更是比WT高出了有48.88%。同时,这3株突变体的油脂含量均显著高于WT的43.19% (<0.05,检验),突变体D03432和D05106的油脂量更是分别达到了干重的64.74%和63.13% (图8A)。由此,证实这3株突变体均为高产油突变体,进一步确认了筛选方案的可行性和准确性。除此之外,对这3株高产油突变体中DHA含量作了进一步的分析,如图8B所示,发现这3株突变体DHA含量 (占干重) 也明显高于WT,WT的DHA含量 (占干重) 仅20.11%,而突变体D03432和突变体D05106的DHA含量 (占干重) 分别达到了32.00%和32.11%。然而,除了突变体D01521的DHA占总油脂的含量与WT有差异外,突变体D03432与D05106的DHA占总油脂的含量与WT并没有显著的差异 (>0.05,检验),这说明筛选得到的高产油突变体积累的油脂仍保持着高品质。由于筛选出来的高产油突变体的生物量明显高于WT,在DHA最终产量上,3株高产油突变体都明显高于WT (<0.05,检验),突变体D05106达到了WT的2.26倍,而突变体D03432更是达到了WT的2.37倍。这说明筛选的这3株突变体不仅油脂含量高于WT,DHA产量也远远高于WT。
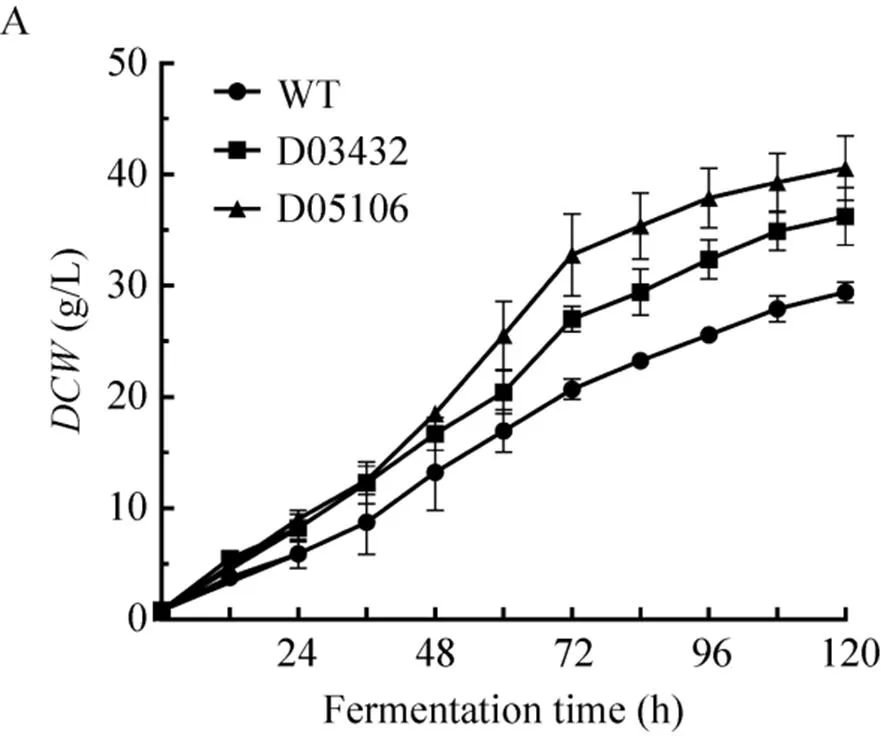
最后,选取油脂量、DHA产量增加比较明显的突变体D03432与D05106进行5 L发酵验证,如图9所示,这两株突变体的最终干重分别达到了(36.25±2.58) g/L和(40.59±2.91) g/L,分别比WT的 (29.43±0.91) g/L提高23.17%和37.92%;在油脂含量方面,均达到干重的65%多,且均高于WT的52.44%;在最终DHA的产量上,突变体D03432达到 (11.54±0.47) g/L,是WT (7.88±0.84) g/L的1.47倍,D05106更是WT的1.66倍。根据油脂代谢途径的理论计算得出DHA的理论得率为33.15%,而这两个突变体的DHA实际得率分别为(8.31±0.41)%和 (7.72±0.24)%,比WT的 (5.27±0.47)%分别提高了57.69%和46.49%。综上可知,筛选得到的突变体不仅在生物量和油脂含量均高于WT,而且DHA的产量和得率也都增加了50%左右,这将在工业应用上凸显出优势,同时再一次证明了本筛选方案的可靠性。

3 讨论
如何提高裂殖壶菌的油脂量、DHA产量,一直是利用裂殖壶菌这类微生物生产富含DHA油脂的重要研究内容。本研究从获取高产油、高产DHA裂殖壶菌突变体为目的出发,设计出一套易操作的基于尼罗红染色的高通量筛选方案。此方案大大缩短了高产油菌株育种时间,从突变体建库到高产油菌株的获得与验证,仅仅只需要3周。利用本筛选方案,成功地筛选出3株高产DHA油脂的突变体,并对其中两株表现较好的突变体 (D03432和D05106) 进行扩大培养至5 L发酵,发现这两株突变体在生物量、油脂含量和DHA产量上均优于野生型,可能具有更好的工业应用潜力。与此同时,本方案不仅能高通量筛选出高产油突变体,也能筛选出低产油突变体,而这些低产油突变体恰好是研究裂殖壶菌油脂代谢通路的重要资源,这有助于我们对脂肪酸的合成机制有更深入的了解,从而更好地开展相关研究工作。
本研究中筛选得到的这3株突变体已证实油脂量均有所增加,但进一步分析发现,相较于WT,它们在摇瓶发酵时的各脂肪酸组成的变化趋势并不一致 (表1)。这说明这3株突变体可能突变的基因或通路存在差异。目前发现,裂殖壶菌可能同时存在两种脂肪酸合成通路:负责肉豆蔻酸 (C14:0)、软脂酸 (C16:0) 和硬脂酸 (C18:0) 等饱和脂肪酸合成的Ⅰ型脂肪酸合酶通路 (Type Ⅰ fatty acid synthase pathway, FAS) 和负责如EPA (C20:5)、DPA (C22:5) 和DHA (C22:6) 等多不饱和脂肪酸合成的多聚酮合酶通路 (Polyketide synthase pathway, PKS),并且这两条通路都是由乙酰辅酶A (Acetyl-CoA) 作为前体物质和由NADPH提供还原力的[42-46]。突变体D01521的脂肪酸组成结果显示,饱和脂肪酸如C14:0、C16:0和C18:0均不同程度上升,其中C16:0占油脂含量 (34.24%) 较WT (25.51%) 上升明显,而不饱和脂肪酸DPA和DHA含量则相对下降了。那么在突变体D01521中,突变的基因可能发生在FAS通路后端,导致C16:0等饱和脂肪酸合成增加,而PKS通路中基因并未发生突变,从而使得DPA与DHA占总油脂的含量相对下降。而突变体D03432和D05106的脂肪酸组成结果显示,相较于WT,C16:0等饱和脂肪酸含量均有所增加,但DHA等不饱和脂肪酸含量并未出现明显差异。这说明D03432和D05106中突变的基因可能发生在乙酰辅酶A的合成通路前端或者乙酰辅酶A其他消耗通路中,导致乙酰辅酶A更多地流入脂肪酸合成通路中,从而使得各脂肪酸的含量都相对增加了。裂殖壶菌脂肪酸合成通路的具体机制并没有完全解析清楚,因此这3株高产油突变体的具体突变基因或通路还有待进一步验证。
值得一提的是,本筛选方案中如尼罗红染色条件、筛选指标选择以及尼罗红染色时间点的选择等步骤可以针对不同产油微生物进行个性化的优化,从而大大扩宽本筛选方案的适用范围与参考价值。另外,试验还发现,将紫外诱变的单克隆从恢复平板上挑取后,无需进行中间的突变体建库,直接接种96孔板培养后进入尼罗红染色筛选流程 (经过尼罗红染色后,突变体仍能存活),然后仅将高或低FI/595值的突变体进行保存,这样可以省去中间建库步骤,进一步节省时间成本,提高筛选效率。
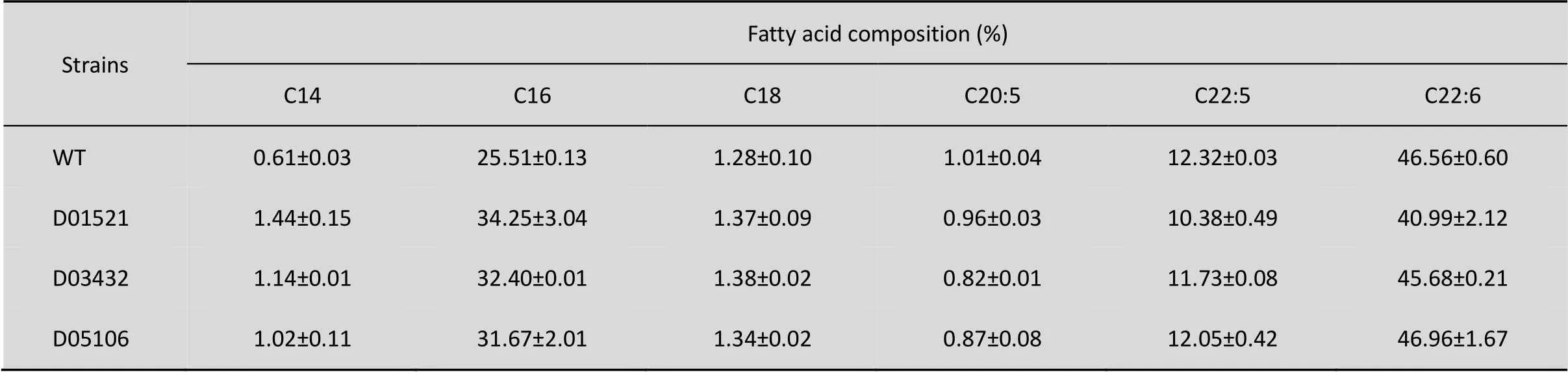
表1 高产油突变体在摇瓶发酵时的脂肪酸组成
[1] Mulder KA, Elango R, Innis SM. Fetal DHA inadequacy and the impact on child neurodevelopment: a follow-up of a randomised trial of maternal DHA supplementation in pregnancy. Br J Nutr, 2018, 119(3): 271–279.
[2] Guo DS, Ji XJ, Ren LJ, et al. Improving docosahexaenoic acid production bysp. using a newly designed high-oxygen-supply bioreactor. AIChE J, 2017, 63(10): 4278–4286.
[3] Aasen IM, Ertesvåg H, Heggeset TMB, et al. Thraustochytrids as production organisms for docosahexaenoic acid (DHA), squalene, and carotenoids. Appl Microbiol Biotechnol, 2016, 100(10): 4309–4321.
[4] Sun XM, Ren LJ, Ji XJ, et al. Adaptive evolution ofsp. by continuous high oxygen stimulations to enhance docosahexaenoic acid synthesis. Bioresour Technol, 2016, 211: 374–381.
[5] Guo DS, Ji XJ, Ren LJ, et al. Development of a real-time bioprocess monitoring method for docosahexaenoic acid production bysp. Bioresour Technol, 2016, 216: 422–427.
[6] Sijtsma L, de Swaaf ME. Biotechnological production and applications of the ω-3 polyunsaturated fatty acid docosahexaenoic acid. Appl Microbiol Biotechnol, 2004, 64(2): 146–153.
[7] Ren LJ, Ji XJ, Huang H, et al. Development of a stepwise aeration control strategy for efficient docosahexaenoic acid production bysp. Appl Microbiol Biotechnol, 2010, 87(5): 1649–1656.
[8] Li J, Liu RJ, Chang GF, et al. A strategy for the highly efficient production of docosahexaenoic acid bySR21 using glucose and glycerol as the mixed carbon sources. Bioresour Technol, 2015, 177: 51–57.
[9] Sun LN, Ren LJ, Zhuang XY, et al. Differential effects of nutrient limitations on biochemical constituents and docosahexaenoic acid production ofsp. Bioresour Technol, 2014, 159: 199–206.
[10] Ren LJ, Sun LN, Zhuang XY, et al. Regulation of docosahexaenoic acid production bysp.: effect of nitrogen addition. Bioprocess Biosyst Eng, 2014, 37(5): 865–872.
[11] Ren LJ, Huang H, Xiao AH, et al. Enhanced docosahexaenoic acid production by reinforcing acetyl-CoA and NADPH supply insp. HX-308. Bioprocess Biosyst Eng, 2009, 32(6): 837–843.
[12] Singh D, Mathur AS, Tuli DK, et al. Propyl gallate and butylated hydroxytoluene influence the accumulation of saturated fatty acids, omega-3 fatty acid and carotenoids in thraustochytrids. J Funct Foods, 2015, 15: 186–192.
[13] Lung YT, Tan CH, Show PL, et al. Docosahexaenoic acid production from crude glycerol bySR21. Clean Technol Environ Policy, 2016, 18(7): 2209–2216.
[14] Patil KP, Gogate PR. Improved synthesis of docosahexaenoic acid (DHA) usingSR21 and sustainable media. Chem Eng J, 2015, 268: 187–196.
[15] Yamasaki T, Aki T, Shinozaki M, et al. Utilization ofdistillery wastewater for production of polyunsaturated fatty acids and xanthophylls using thraustochytrid. J Biosci Bioeng, 2006, 102(4): 323–327.
[16] Qu L, Ren LJ, Huang H. Scale-up of docosahexaenoic acid production in fed-batch fermentation bysp. based on volumetric oxygen-transfer coefficient. Biochem Eng J, 2013, 77: 82–87.
[17] Chang GF, Gao NS, Tian GW, et al. Improvement of docosahexaenoic acid production on glycerol bysp. S31 with constantly high oxygen transfer coefficient. Bioresour Technol, 2013, 142: 400–406.
[18] Song XJ, Zhang XC, Kuang CH, et al. Batch kinetics and modeling of DHA production by.OUC88. Food Bioprod Process, 2010, 88(1): 26–30.
[19] Rosa SM, Soria MA, Vélez CG, et al. Improvement of a two-stage fermentation process for docosahexaenoic acid production bySR21 applying statistical experimental designs and data analysis. Bioresour Technol, 2010, 101(7): 2367–2374.
[20] Kim K, Jung Kim E, Ryu BG, et al. A novel fed-batch process based on the biology ofsp. KRS101 for the production of biodiesel and docosahexaenoic acid. Bioresour Technol, 2013, 135: 269–274.
[21] Guo DS, Ji XJ, Ren LJ, et al. Development of a multi-stage continuous fermentation strategy for docosahexaenoic acid production bysp.. Bioresour Technol, 2018, 269: 32–39.
[22] Xie DM, Miller E, Sharpe P, et al. Omega-3 production by fermentation of: from fed-batch to continuous. Biotechnol Bioeng, 2017, 114(4): 798–812.
[23] Cui GZ, Ma ZX, Liu YJ, et al. Overexpression of glucose-6-phosphate dehydrogenase enhanced the polyunsaturated fatty acid composition ofsp. SD116. Algal Res, 2016, 19: 138–145.
[24] Geng LJ, Chen SL, Sun XM, et al. Fermentation performance and metabolomic analysis of an engineered high-yield PUFA-producing strain ofsp. Bioprocess Biosyst Eng, 2019, 42(1): 71–81.
[25] Sun XM, Ren LJ, Bi ZQ, et al. Adaptive evolution of microalgaesp. under high salinity stress to alleviate oxidative damage and improve lipid biosynthesis. Bioresour Technol, 2018, 267: 438–444.
[26] Alemán-Nava GS, Cuellar-Bermudez SP, Cuaresma M, et al. How to use Nile Red, a selective fluorescent stain for microalgal neutral lipids. J Microbiol Methods, 2016, 128: 74–79.
[27] Yan CS, Fan JL, Xu CC. Analysis of oil droplets in microalgae. Methods Cell Biol, 2013, 116: 71–82.
[28] Terashima M, Freeman ES, Jinkerson RE, et al. A fluorescence-activated cell sorting-based strategy for rapid isolation of high-lipidmutants. Plant J, 2015, 81(1): 147–159.
[29] Genicot G, Leroy JLMR, Van Soom A, et al. The use of a fluorescent dye, Nile red, to evaluate the lipid content of single mammalian oocytes. Theriogenology, 2005, 63(4): 1181–1194.
[30] Izard J, Limberger RJ. Rapid screening method for quantitation of bacterial cell lipids from whole cells. J Microbiol Methods, 2003, 55(2): 411–418.
[31] Sitepu IR, Ignatia L, Franz AK, et al. An improved high-throughput Nile red fluorescence assay for estimating intracellular lipids in a variety of yeast species. J Microbiol Methods, 2012, 91(2): 321–328.
[32] Chen W, Zhang CW, Song LR, et al. A high throughput Nile red method for quantitative measurement of neutral lipids in microalgae. J Microbiol Methods, 2009, 77(1): 41–47.
[33] Yokoyama R, Honda D. Taxonomic rearrangement of the genussensu lato based on morphology, chemotaxonomic characteristics, and 18S rRNA gene phylogeny (Thraustochytriaceae, Labyrinthulomycetes): emendation forand erection ofandgen. nov. Mycoscience, 2007, 48(4): 199–211.
[34] Blight EG, Dyer WJ. A rapid method of total lipid extraction and purification. Can J Biochem Physiol, 1959, 37(8): 911–917.
[35] Huang TY, Lu WC, Chu IM. A fermentation strategy for producing docosahexaenoic acid inSR21 and increasing C22:6 proportions in total fatty acid. Bioresour Technol, 2012, 123: 8–14.
[36] Shi QQ, Wu SG. Industrial Microbial Breeding Science. 3rd ed. Beijing: Science Press, 2009: 73–74 (in Chinese). 施巧琴, 吴松刚. 工业微生物育种学. 3版. 北京: 科学出版社, 2009: 73–74.
[37] Huang GH, Chen G, Chen F. Rapid screening method for lipid production in alga based on Nile red fluorescence. Biomass Bioenerg, 2009, 33(10): 1386–1392.
[38] Pick U, Rachutin-Zalogin T. Kinetic anomalies in the interactions of Nile red with microalgae. J Microbiol Methods, 2012, 88(2): 189–196.
[39] Balduyck L, Veryser C, Goiris K, et al. Optimization of a Nile red method for rapid lipid determination in autotrophic, marine microalgae is species dependent. J Microbiol Methods, 2015, 118: 152–158.
[40] Morita E, Kumon Y, Nakahara T, et al. Docosahexaenoic acid production and lipid-body formation inSR21. Mar Biotechnol, 2006, 8(3): 319–327.
[41] Ashford A, Barclay WR, Weaver CA, et al. Electron microscopy may reveal structure of docosahexaenoic acid-rich oil withinsp.. Lipids, 2000, 35(12): 1377–1387.
[42] Metz JG, Roessler P, Facciotti D. Production of polyunsaturated fatty acids by polyketide synthases in both prokaryotes and eukaryotes. Science, 2001, 293(5528): 290–293.
[43] Uttaro AD. Biosynthesis of polyunsaturated fatty acids in lower eukaryotes. IUBMB Life, 2006, 58(10): 563–571.
[44] Hauvermale A, Kuner J, Rosenzweig B, et al. Fatty acid production insp.: involvement of a polyunsaturated fatty acid synthase and a type I fatty acid synthase. Lipids, 2006, 41(8): 739–747.
[45] Lippmeier JC, Crawford KS, Owen CB, et al. Characterization of both polyunsaturated fatty acid biosynthetic pathways insp. Lipids, 2009, 44(7): 621–630.
[46] Nagano N, Sakaguchi K, Taoka Y, et al. Detection of genes involved in fatty acid elongation and desaturation in thraustochytrid marine eukaryotes. J Oleo Sci, 2011, 60(9): 475–481.
Screening for hyper-accumulating lipid mutants inAurantiochytrium limacinum using high-throughput fluorescence-based method
Guangqian Duan1,2, Shuoshuo Li3, Xin Li3, and Kaiyao Huang1
1 Key Laboratory of Algal Biology, Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, Hubei, China 2 University of Chinese Academy of Sciences, Beijing 100049, China 3 School of Biology and Pharmaceutical Engineering, Wuhan Polytechnic University, Wuhan 430023, Hubei, China
Docosahexaenoic acid (DHA) has many unique physiological functions such as promoting the development of brain and retina in infants. Therefore, it is widely applied to food, pharmacy, breeding and other industries. To obtain engineered strainsofSR21 suitable for industrial application with increased lipid and DHA production, we designed a simple, fast, accurate and high-throughput screening method based on Nile red staining of oil droplets. First, ultraviolet C (UVC) mutagenesis was used to generate a random mutant library of. Second, screening conditions were optimized including staining conditions of Nile red and the sorting criterion. Thereby, three putative high-lipid mutants (D03432, D05106 and D01521) were selected from the mutant library containing 3 648 mutated clones. The three mutants grew faster and produced higher amounts of lipids and DHA compared to wild type (WT). In 100 mL cultures, the lipid content of D03432 and D05106 mutants reached 64.74% and 63.13% of dry cell weight respectively, whereas the wild strain exhibited only 43.19%. DHA yield in these two mutants were even 2.26-fold and 2.37-fold higher than that of the wild strain. Experiment with 5 L fermentor further confirmed that D03432 and D05106 mutants had better performance than the wild strain on DHA yield (45.51% and 66.46% more than that of the wild strain, respectively), and demonstrated their high potential for industrial application. This work not only generated several high-DHA content mutants with high potential for industrial use, but also provided vital guidance for high-throughput screening of lipid hyper-accumulating mutants in other oil-producing microorganisms.
oil droplets, high-throughput screening, docosahexaenoic acid (DHA), Nile red staining
March 4, 2019;
May 8, 2019
Key Project of Technological Innovation in Hubei Province (No. 2016ABA120).
Kaiyao Huang. Tel: +86-27-68780901; E-mail: huangky@ihb.ac.cn
湖北省技术创新专项 (重大项目) (No. 2016ABA120) 资助。
段光前, 李硕硕, 李鑫, 等. 裂殖壶菌高产油突变体的高通量筛选. 生物工程学报, 2019, 35(7): 1335–1347.
Duan GQ, Li SS, Li X, et al. Screening for hyper-accumulating lipid mutants inusing high-throughput fluorescence-based method. Chin J Biotech, 2019, 35(7): 1335–1347.
(本文责编 郝丽芳)
