鲫鱼中硝基呋喃代谢物测定及呋喃唑酮代谢规律研究
2019-08-21任召珍陈志兵刘志敏
任召珍 陈志兵 刘志敏


摘要:建立鲫鱼中硝基呋喃代谢物残留量测定的液相色谱-串联质谱分析方法,并分析AOZ在鲫鱼中残留消除规律。样品采用盐酸、2-硝基苯甲醛衍生提取,乙酸乙酯萃取后,进行液相色谱-串联质谱测定,同位素内标定量。结果显示,该方法在0~20.0 μg/L范圍内线性关系良好,4种硝基呋喃类代谢物回收率在91.7%~98.5%之间,相对标准偏差为1.87%~6.93%,方法检出限为SEM 0.40,AOZ 0.25,AMOZ 0.20,AHD 0.45。鲫鱼内AOZ残留消除试验发现,AOZ停药后最高蓄积残留量为218.25 μg/kg。鲫鱼肉内AOZ代谢消除缓慢,120 d后代谢残留物低于0.5 μg/kg。
关键词:液相色谱-串联质谱;硝基呋喃代谢物;鲫鱼;代谢规律
中图分类号:TS207 文献标志码: A 文章编号:1002-1302(2019)12-0238-04
硝基呋喃类药物是一种抗生素,其代谢物主要有5-甲基吗啉-3-氨基-2-唑烷基酮(AMOZ)、氨基脲(SEM)、1-氨基-2-内酰脲(AHD)、3-氨基-2-唑烷基酮(AOZ)4种,对大多数革兰氏阳性菌、革兰氏阴性菌、真菌和原虫等病原体均有杀灭作用,主要用于防治敏感菌所致的细菌性痢疾、肠炎、霍乱。由于其广谱的杀菌能力曾被广泛应用于养殖业,但研究发现该类药物具有相当大的毒性,可致胎儿畸形、诱发癌症等[1-2]。欧盟关于修订有关指定用于确定最大残留限量的共同体程序的第2377/90/EEC(1995)号指令中把硝基呋喃列入A类禁用药[3],并于2003年规定最低残留限量(MRL)为1 μg/kg[4]。我国动物性食品中兽药最高残留限量——农业部235公告也明确规定,此类药物不得在动物性食品中检出[5]。即便如此,硝基呋喃类代谢物在动物源食品中仍时有检出。据山东省食品药品监督管理局发布的食品安全通报发现,黄花鱼、松花鱼、鸡肉等多起动物源食品中呋喃唑酮代谢物超标[6]。目前,硝基呋喃代谢物的分析方法有酶联免疫法[7]、高效液相色谱法[8-9]和高效液相色谱-串联质谱法[10-13]。其中,液相色谱-串联质谱法因其灵敏度高、准确性和重复性好等特点得到广泛应用。本试验在此基础上以鲫鱼为研究对象,采用更为便捷的检测方法对鲫鱼中硝基呋喃类代谢物进行测定,并对呋喃唑酮的代谢规律进行研究。
1 材料与方法
1.1 材料与试剂
1.1.1 甲醇、乙酸乙酯、正己烷、甲酸、2-硝基苯甲醛、醋酸铵皆为色谱纯;盐酸、氢氧化钠、磷酸氢二钾皆为分析纯;标准品购自德国Dr. Ehrenstorfer标准品公司,纯度≥99.0%;水为超纯水。
1.1.2 硝基呋喃代谢物标准储备溶液 采用甲醇溶液分别将AOZ、AMOZ、AHD、SEM溶解配制成100 mg/L的标准溶液,置于-18 ℃冰箱避光保存。
1.1.3 混合标准中间溶液 分别准确吸取适量标准储备溶液,将以上4种硝基呋喃代谢物配制成浓度为10 mg/L的混合标准中间溶液,置于-18 ℃冰箱避光保存。
1.2 仪器和设备
高效液相色谱串联质谱仪(LC-MS/MS):Thermo TSQ Quantum Access Max,电子天平[奥豪斯仪器(上海)有限公司];旋转蒸发器(东京理化器械株式会社);离心机(株式会社日立制作所);均质器(IKAT18);旋涡混合器(德国IKA公司);pH计(梅特勒—托利多集团);恒温水浴振动器(常州国华电器有限公司,SHA-B);氮吹仪(郑州安晟科学仪器有限公司)。
1.3 水解和衍生
准确称取制备均匀的鲫鱼样品2.00 g(精确至0.01 g)于 50 mL 离心管中,加入10 mL 0.2 mol/L盐酸溶液,加入适量内标标准溶液(100 μL 100 mmol/L 2-硝基苯甲醛溶液),旋涡均匀,放入37 ℃水浴避光振荡16 h。
1.4 提取净化
将水解衍生完成的样品取置室温,于离心管中加入 1.5 mL 1 mol/L磷酸氢二钾溶液,并用3 mol/L氢氧化钠溶液调节pH值至7.0~7.5间。10 000 r/min离心5 min,上清溶液转移至另一离心管中并加入10 mL乙酸乙酯,高速涡旋振荡 1 min,再次10 000 r/min离心5 min,取乙酸乙酯层于 15 mL 离心管中,40 ℃氮气吹干。准确加入1.0 mL甲醇-水溶液(体积比为8 ∶ 2),2 mL正己烷,涡旋振荡30 s,取下层溶液于 1.5 mL EP管中,15 000 r/min离心10 min,定容液经 0.22 μm 微孔滤膜过滤,于进样瓶中待测。
标准品采用与样品相同方法处理后待测。
1.5 色谱-质谱条件
1.5.1 液相条件 色谱柱:C18,10 cm×5 μm×0.21 mm(Thermo);柱温:30 ℃;流速:250 μL/min;进样量:10 μL;流动相:甲醇/5 mmol/L乙酸铵溶液(0.1%甲酸)。
1.5.2 质谱条件 离子源温度(配备ESI源):350 ℃;喷雾电压:4 500 V;鞘气:40arb;辅助气:10arb;硝基呋喃代谢物的离子参数见表1。
1.6 AOZ在鲫鱼中的代谢试验
配制含AOZ 2 mg/kg浓度饲料,鲫鱼苗体长约4 cm,养殖水温为(20±2) ℃,养殖密度为30尾/m3,投喂量为3%,每天投喂2次(上午、下午各1次),投喂时间为5 d。养殖密9度和饲料粒径随鲫鱼增长进行调整。投喂结束后2、4、6、12 h,1、2、4、8、16、20、30、40、60、90、120 d取样测定鲫鱼肉中AOZ残留量。
2 结果与分析
2.1 质谱条件优化
取2.0 mg/L标准品,由蠕动泵进入质谱,离子源切换到正离子模式,调试离子源的喷雾电压,观察硝基呋喃化合物Full Scan模式下母离子的响应情况,确定喷雾电压、鞘气和辅助气流量;在MRM模式下自动扫描,确定响应最高、最稳定的碰撞能量,由此确定该方法的质谱条件,参数见表1。2 μg/L 浓度混合标准品参考图谱(图1)。在优化的质谱条件下,4种硝基呋喃代谢物8 μg/L浓度混合标准品分离度合理,峰形对称且峰形良好,并且在仪器上表现出良好的响应,灵敏度高,在此条件下可以进行4种硝基呋喃代谢物的分离测定。
2.2 液相条件的优化
根据硝基呋喃类药物性质及质谱条件,采用乙腈或甲醇作为有机相,0.1%甲酸和5 mmoL/L乙酸铵溶液(含0.1%甲酸)作为水相。根据调试,甲醇可更好地提高检测灵敏度和分离效果,水相中加入乙酸铵可提高离子化效率,以获得理想色谱峰,因此确定使用甲醇-5 mmoL/L乙酸铵溶液(含 0.1% 甲酸)做流动相,具体的流动相比例详见表2。
2.3 线性方程和检出限
配制浓度为0、0.5、1.0、2.0、5.0、10.0、20.0 μg/L的混合标准曲线,以内标法定量绘制标准曲线,硝基呋喃化合物在0~20.0 μg/L浓度范围内响应呈线性关系(r2>0.99),以信噪比(S/N)=3及标准品浓度计算硝基呋喃类代谢物检出限,详见表3。
2.4 衍生条件的优化
2.4.1 2-硝基苯甲醛溶剂的选择 由于硝基呋喃类代谢物分子量小,HPLC-MS/MS直接测定响应不好,灵敏度低,因此一般对其衍生化后再进行测定,常用衍生化试剂是2-硝基苯甲醛[14]。2-硝基苯甲醛常用二甲亚砜[10-11]和甲醇[12]溶解。试验过程中衍生浓度2 μg/L混合标准品,分别使用甲醇和二甲亚砜溶解,2-硝基苯甲醛作为衍生化试剂,详见表4。由结果可知,甲醇和二甲亚砜溶解的衍生化试剂对结果并无太大影响,考虑二甲亚砜易渗入皮肤,低温易凝固的特点,本试验采用甲醇溶解2-硝基苯甲醛。
2.4.2 衍生方式的选择 根据目前硝基呋喃代谢物检测标准,衍生方式有避光衍生[10-11]和直接衍生[12],本试验对 2 μg/L 标准品分别进行避光衍生和直接衍生,结果见表5。由于硝基呋喃类药物代谢快速且对光敏感[15],所以进行避光衍生。
2.5 提取条件的优化
2.5.1 离心速率影响 通常硝基呋喃类药物在提取时采用4 000 r/min离心[10-11],但对于蛋白和脂肪含量高的样品,在此速率下即使离心10 min,离心管上层仍漂浮有杂质,另外用乙酸乙酯提取时,也易出现乳化现象,若分离不完全,对于检测结果会造成一定影响。提高离心速率对这类现象有明显改善,离心速率越高效果越好,因此本试验在分离和提取过程中皆采用10 000 r/min离心分离。氮吹后,采用正己烷除脂后易出现定容液与正己烷乳化现象,在15 000 r/min下离心 10 min,可使正己烷漂浮于上层,可彻底除去提取的脂肪,降低样品基质干扰。
2.5.2 乙酸乙酯提取次数的影响 农业部781号公告-4-2006[10]和GB/T 21311—2007《动物源性食品中硝基呋喃类代谢残留量监测方法》[12]标准方法中乙酸乙酯皆提取2次。因硝基呋喃类药物采用内标法进行定量,通过质控样品分析发现,乙酸乙酯提取1次,硝基呋喃类药物的回收率和相对标准偏差均在范围内,详见表6。因此采用1次提取法,不仅可简化提取步骤,还可减少试剂使用。
2.6 回收率试验
取阴性鲫鱼肉样,分别加入硝基呋喃类标准品,使添加浓度分别为0.5、1.0、5.0 μg/L,每个浓度6个平行样品,测其回收率及相对标准偏差。由表6可知,本方法4种硝基呋喃类代谢物的回收率均为91.7%~98.5%,相对标准偏差(RSD)为1.87%~6.93%,回收率和相对标准偏差均符合标准要求。
2.7 AOZ在鯽鱼内的代谢规律
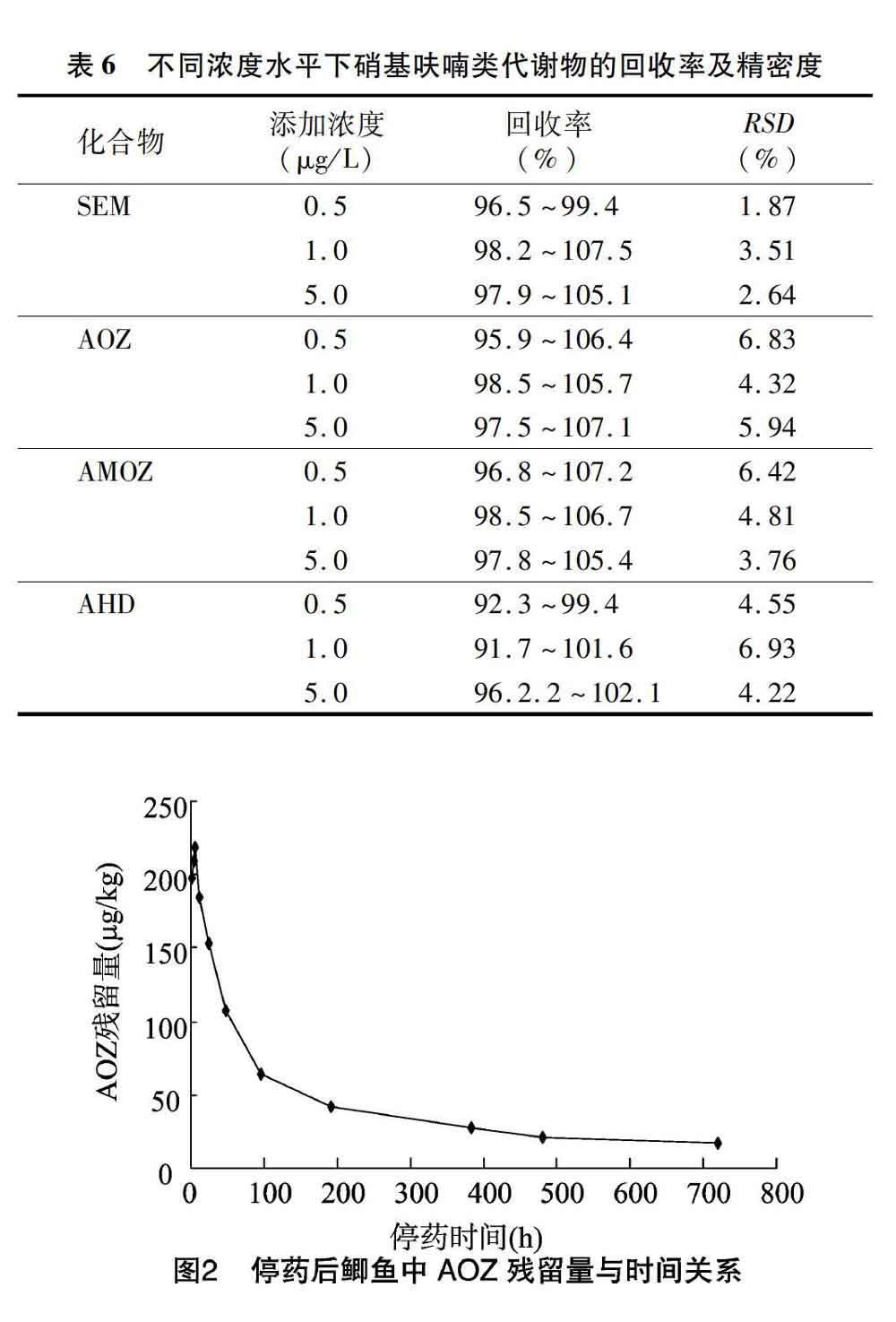
由图2可知,AOZ在鲫鱼中投喂结束后0~6 h,AOZ含量呈上升趋势,在 6 h时测得最高含量为218.25 μg/kg,在 6~96 h 间AOZ残留量下降趋势明显,之后呈缓慢下降趋势,直至120 d后在鲫鱼中无AOZ检出。这与谭志军等研究呋喃唑酮对大菱鲆内的代谢规律[16]和刘书贵等研究呋喃唑酮在杂交鳢(斑鳢♀×乌鳢♂)体内残留消除规律[17]有相似之处。据食品药品监督管理局的食品安全抽查结果显示,当前水产品中呋喃唑酮仍时有检出,说明仍存在违禁使用现象。本试验结果显示,AOZ在鲫鱼体内代谢消除仍然非常缓慢,如果违禁使用还是存在很大风险。
3 结论
本研究建立了以盐酸溶液衍生提取,乙酸乙酯萃取,经液相色谱-串联质谱测定,并以对应同位素内标定量的硝基呋喃类代谢物残留测定方法。方法准确度高、精密度好、符合残留检测要求。通过对饲喂鲫鱼中AOZ残留消除规律的研究发现,AOZ在本试验条件下,120 d后鲫鱼中AOZ残留完全消除。如果试剂使用剂量大或时间长,消除时间还可能更长,因此违禁使用AOZ存在很大风险,这为硝基呋喃类药物的监管提供了一定试验依据。
参考文献:
[1]Bartel L C. Montalto de M M,Castro J A.Nitroreductive metabolic activation of some carcinogenic nitro heterocyclic food contaminants in rat mammary tissue cellular fractions[J]. Food and Chemical Toxicology,2008,47(1):140-144.
[2]Vass M,Hruska K,Franek M. Nitrofuran antibiotics:a review on the application,prohibition and residual analysis[J]. Veterinarni Medicina,2008,53(9):469-500.
[3](EEC)No 2377/90. Laying down a community procedure for the establishment of maximum residue limits of veterinary medicinal products in foodstuffs of animal origin[S]. 1990.
[4](EC) No 181/2003.Amending decision 2002/657/EC as regards the setting of minimum required performance limits (MRRLs) for certain residues in food of animal origin[S]. 2003.
[5]中华人民共和国农业部公告第235号[Z].北京:中华人民共和国农业部,2002.
[6]SFDA:山東省食品安全监督抽检信息通告018年第5期(总第134期),2017年第26期(总第105期),2007年第19期(总第98期)[Z].
[7]国家质量监督检验检疫总局. 出口动物源食品中硝基呋喃代谢物残留量的测定 酶联免疫吸附法:SN/T 3380—2012[S]. 北京:国家质量监督检验检疫总局,2013.
[8]农业部. 水产品中硝基呋喃类代谢物残留量的测定 高效液相色谱法:农业部1077号公告-2—2008[S]. 北京:农业部,2008.
[9]王 媛,蔡友琼,贾东芬,等. 高效液相色谱法检测水产品中硝基呋喃类代谢物残留量[J]. 分析试验室,2009,28(12):86-90.
[10]农业部. 动物源食品中硝基呋喃类代谢物残留量的测定 高效液相色谱-串联质谱法:农业部781号公告-4—2006[S]. 北京:农业部, 2006.
[11]国家质量监督检验检疫总局,国家标准化管理委员会. 猪肉、牛肉、鸡肉、猪肝和水产品中硝基呋喃类代谢物残留量的测定 液相色谱-串联质谱法:GB/T 20752—2006[S]. 北京:国家质量监督检验检疫总局,国家标准化管理委员会, 2006.
[12]国家质量监督检验检疫总局,国家标准化管理委员会. 动物源性食品中硝基呋喃类药物代谢物残留量检测方法 高效液相色谱/串联质谱法:GB/T 21311—2007[S]. 国家质量监督检验检疫总局,国家标准化管理委员会, 2007.
[13]王 狄,张嘉楠. 超高效液相色谱串联质谱法对水产品中硝基呋喃代谢物的测定[J]. 河北渔业,2016(7):47-51.
[14]Pereira A S,Pampana L C,Donato J L,et al. Analysis of nitrofuran metabolic residues in tissues by liquid chromatography-tandem mass spectrometry[J]. Analytica Chimica Acta,2004,514(1):9-13.
[15]司红彬,梁 军. 硝基呋喃类药物的残留检测(上)[J]. 兽医导刊,2007(9):48-49.
[16]谭志军,翟毓秀,冷凯良,等. 呋喃西林和呋喃唑酮代谢物在大菱鲆组织中的消除规律[J]. 中山大学学报(自然科学版),2008,47(增刊1):63-69.
[17]刘书贵,郑光明,王 群,等. 呋喃唑酮代谢物在杂交鳢(斑鳢♀×乌鳢♂)体内的残留消除规律[J]. 中国渔业质量与标准,2013,3(3):248-253.
