扶正培本方联合替莫唑胺对高级别胶质瘤患者外周血miRNA的影响
2019-08-15陈祖鹏李徐张昕黄李法杨超
陈祖鹏,李徐,张昕,黄李法,杨超
浙江中医药大学附属第一医院神经外科,浙江 杭州 310006
胶质瘤是颅内主要的原发恶性肿瘤,其中高级别胶质瘤(WHO分类Ⅲ、Ⅳ级)的中位生存期仅有15个月左右,呈现出高发病率、术后高复发性、高病死率及治愈率低等特点[1-3]。miRNA是一类长约18~25个核苷酸的内源性单链非编码小分子RNA,通过对靶mRNA进行降解或抑制翻译来调节靶基因的表达,参与细胞增殖、迁移、分化和凋亡等过程[4,5]。miR-1193在胶质瘤的发病机制中起重要作用,本课题组前期研究表明,胶质瘤细胞中,miR-1193通过胰岛素样生长因子2结合蛋白2(IGF2BP2)的表达抑制胶质细胞的增殖活化,其作用与ERK-JNK通路密切相关[6]。中医药治疗胶质瘤有其独特的优势,扶正培本方是中医临床治疗胶质瘤的代表方剂[7],本研究通过观察扶正培本方联合替莫唑胺对高级别胶质瘤术后病人miR-1193的影响来进一步阐明其作用机制。
1 资料与方法
1.1 一般资料
选取2014年1月-2017年6月在我院神经外科就诊的胶质瘤患者80例为研究对象,中医辨证主要证型为正气亏虚、脾肾不足。采用区组随机化分组分为两组,对照组42例,其中男性患者27例、女性患者15例,平均年龄(50.33±11.47)岁;治疗组38例,其中男性患者25例,女性患者13例,平均年龄(54.25±12.16)岁;两组患者年龄、性别、肿瘤级别及KPS评分等指标比较差异无统计学意义。
1.2 诊断标准
依据外科学(五年制第八版,人民卫生出版社,陈孝平主编),结合王忠诚神经外科学(第二版,湖北科学技术出版社)中胶质瘤的诊断,胶质瘤的恶性程度分为WHOⅠ-Ⅳ级。入组患者均经手术或活检证实为胶质瘤,并确认分级为Ⅲ、Ⅳ级。外院手术患者需经本院病理科行病理切片会诊再次确认胶质瘤分级。病例纳入标准:(1)符合上述诊断标准;(2)Karnofsky评分≥50分、预计生存时间≥3个月;(3)年龄≥18周岁;(4)近3月内无系统使用中药史;无急诊手术指征;既往无其他中枢神经系统疾病及手术史。本研究经过医院医学伦理委员会审核及批准,并签署知情同意书。
1.3 排除标准
(1)病情迅速进展的;(2)经知情告知后不同意,或是无法长期随访的患者;(3)入选前3个月内接受其他中药治疗的;(4)血常规:绝对中性粒细胞计数<1.5×109/L,血小板计数<100×109/L;存在化疗禁忌证以及严重心、肝、肾功能异常者;(5)孕妇及哺乳期妇女。
1.4 中医辨证分型
采用证候规律研究病理报告表,中医辨证为:脾肾不足、风痰凝结、瘀毒内阻。主症:(1)头痛目涩;(2)眩晕;(3)肢体活动不利;(4)面色晦暗;(5)舌质暗红或瘀斑,苔薄白或微黄、脉弦细。次症:(1)欠寐、纳差;(2)头晕、胸闷;(3)自汗/盗汗;(4)腰膝酸软;(5)口干、口苦、多尿。辨证:(1)具有所有主症者,即为本证;(2)具有主症1项和次症3项者即为本证;(3)具备次症4项者即为本证。
1.5 治疗方法
对照组及治疗组均使用替莫唑胺(默沙东制药),口服本品,每日剂量为75 mg/m2,共42天,同时接受放疗(60 Gy分30次);随后接受6个周期的150 mg/m2辅助治疗,每日1次,共5天,然后停药23天,28天为1个周期。治疗组加扶正培本方,予以扶正培本方水煎剂口服,每天1剂,水煎至240 ml,每天分2次服用,每次120 ml,14天为一疗程;每一疗程结束2周后开始下一疗程,一共7个疗程,共随访2年。扶正培本方以四君子汤和六味地黄丸相合而成组成为:人参、白术、茯苓、丹皮、泽泻各9 g,甘草6 g,熟地15 g,山茱萸肉12 g,山药12 g。根据辨证论治加减。煎煮方法:先用凉水浸泡1小时,大火煮沸后,小火煎煮20分钟,倒出药汁,再加热水大火煮沸后,小火煎煮20分钟再将药汁倒出。两次倒出药汁相合,分早晚两次服用。对照组加用中药模拟剂(以焦糖为主要成分,含10%四君子汤剂及少量淀粉的配置液,色泽及口味与治疗组相似,本院中药房制剂中心提供)每天1剂,水煎取汁240 mL,分早晚口服,疗程同治疗组。
1.6 研究的终点
本研究的终点设置为肿瘤术后进展,定义为病人出现肿瘤进展或病人死亡的时间。符合以下条件之一的即到达本研究设定的终点:(1)病理证实肿瘤复发的病例;(2)根据Macdonald标准判断肿瘤进展:MRI增强像上肿瘤强化影的两最大垂直径乘积较之前增大超过25%;或者出现新的肿瘤病灶,判断肿瘤为进展;(3)临床随访GCS评分下降大于等于3分或KPS评分下降大于等于20分;(4)随访期间任何原因引起的死亡。按照上述分类标准判定有疑议的,由本研究两位神经外科医师共同判定,最终达成一致。随访时间为入组后2年,此时设为尚未发生病情进展病人的终点。
1.7 中止的条件及执行、不良反应控制和记录
治疗过程中出现依从性差,出现血液及肝肾功能损害等难以完整的完成随访的,应中止试验,予以相应对症治疗并详细记录。
1.8 随访方法
入组患者治疗期间可门诊或者住院进行,治疗期间接受电话及门诊随诊。随访时间为入组后2年。
1.9 实验室检查
入组患者当日完成血液标本的保存,治疗结束和研究终点时需再次留取。抽取外周血后收集于NaF/KOx管中,于4℃、3 000 g离心15 min,提取上层血清置于-80℃冰箱备用。为保证样本的质量,选择血清中较为常见的miRNA即hsa-miR-16作为参照,通过实时定量PCR法检测RNA含量,确定样本是否可进入下一步实验。hsa-miR-16在血清中的Ct值范围分别为16~22。按照试剂盒说明书对血样中总RNA进行提取,试剂盒为Arraystar(美国)公司血浆/血清RNA小量纯化试剂盒。提取的总RNA测量浓度后进行反转录合成cDNA作为实时荧光定量模板。最后进行免疫荧光定量PCR,结果采用2-△△CT表示。miRcute、miRNAs提取分离试剂盒、miR-1193(3’-GGGAUGGUAGA CCGGUGACGUGC-5’)的上游引物和内参引物由北京天根生化提供,下游引物为试剂盒通用引物。
1.10 统计学方法
利用SPSS17.0统计软件进行分析,计量资料以均数±标准差(±s)表示,采用t检验;计数资料采用χ2检验或秩和检验;以P<0.05表示差异具有统计学意义。
2 结果
2.1 治疗组2例入组后3个月内病情即显著进展,未完成治疗计划;对照组1例失访,其他病人均完成治疗。
2.2 两组患者治疗前后在不同的时间点miR-1193水平比较(表1)。入组前两组患者miR-1193在各时间点差异均无统计学意义。入组后7个月即治疗刚结束时,治疗组miR-1193水平低于对照组,差异有统计学意义。完成治疗、随访期间肿瘤进展的患者,两组患者治疗前及进展后的miR-1193水平相比无显著差异。2年内均无进展的患者,随访结束时两组患者miR-1193水平均显著低于治疗前,并且治疗组治疗后要显著低于对照组治疗后(P<0.05)。疾病进展时,对照组及治疗组miR-1193相比未进展患者都低,差异有统计学意义。
2.3 到达研究终点时,治疗组因疾病进展比例为45.0%(18/40),对照组为 70.27%(26/37),P<0.05,两组比较差异有统计学意义。治疗组无进展生存时间(Progress Free Survival,PFS)为 21.3个月,对照组17.2个月,P>0.05,统计学上差异无意义。
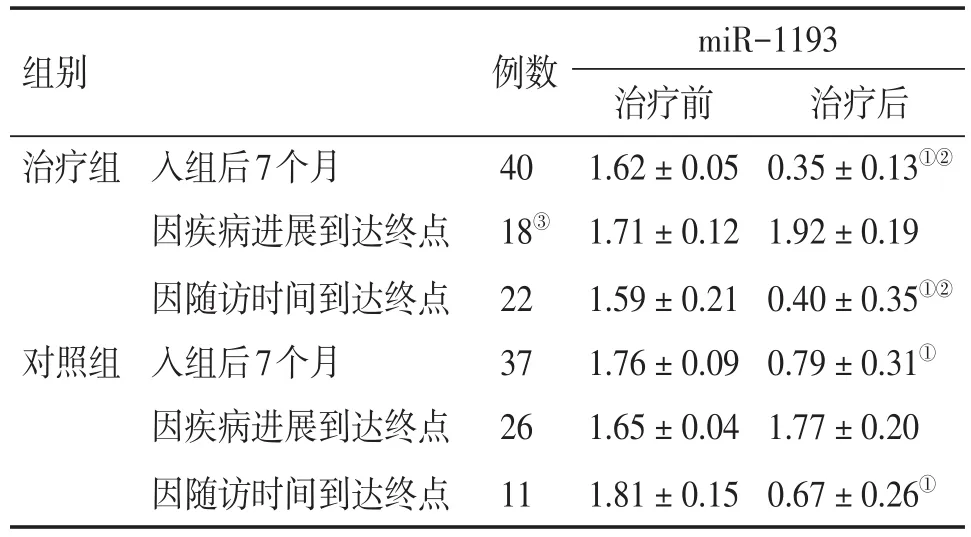
表1 两组患者治疗前后在不同的时间点血清miR-1193水平比较
2.4 两组不良反应发生率比较。治疗组胃部不适2例,白细胞下降4例;对照组皮疹2例,白细胞下降3例,呕吐3例,经对症处理后均可耐受,两组相比差异无统计学意义。
3 讨论
胶质瘤术后病情再次复发进展是影响患者生存的主要因素。积极采用放疗,辅助化疗以及一些创新治疗技术如免疫治疗、分子靶向治疗和基因治疗等,可以延长患者的无进展生存期。替莫唑胺作为一种新型的口服烷化剂,是目前高级别胶质瘤特别是O6-氧甲基鸟嘌呤-DNA甲基转移酶(O6-methylguanine-DNA methyltansferase,MGMT)阳性患者术后常规化疗方案,对各个时期的肿瘤细胞均有抑制效果,且对不同病理分型的胶质瘤均可发挥其细胞毒作用。但复发胶质瘤患者的中位总生存期仍维持在9.6个月和35.9个月之间,治疗效果并不乐观[8]。
1993年,Ambross和Collagues发现了miRNA,报告miRNA在功能上与癌症有关。后续研究表明,miRNAs与胶质瘤的发生密切相关[9,10]。Weeraratne等人研究显示miR-183~96~182与胶质瘤细胞的增殖和迁移相关[11]。Li等报道的miR-613通过靶向CDK14等抑制胶质瘤细胞的增殖和侵袭,miR-613的表达水平与胶质瘤干细胞分化呈正相关,与胶质瘤细胞迁移、运动、侵袭和集落形成能力呈负相关[12]。Chen等研究显示,miR-1193的过表达抑制了胶质瘤细胞的增殖,IGF2BP2是miR-1193的靶点[6]。本研究显示,miR-1193的水平与胶质瘤细胞的复发密切相关,肿瘤进展时miR-1193水平降低明显。同时,在疾病进展比例上,治疗组应用扶正培本方后,进展比例要显著小于对照组,可见扶正培本方可能具有控制脑胶质瘤进展的作用,此作用与miR-1193呈正相关。虽然治疗组与对照组肿瘤无进展生存期无显著差异,但治疗组PFS要多于对照组4个月,考虑目前随访时间仍短,延长随访时间差异可能进一步增加。
我国传统的中医药治疗是肿瘤治疗重要的手段之一。结合中医药辨证论治、整体观念的优势,不仅可以辅助手术、放化疗提高治疗效果,而且可以明显降低各种药物的毒性作用,提高肿瘤患者的生活质量[13]。本研究采用扶正培本中药方剂辅助替莫唑胺对神经胶质瘤患者进行术后治疗,结果显示,该方法的临床疗效显著高于对照组,并不增加化疗药物的毒副作用,中药在神经胶质瘤患者进行术后化疗的辅助治疗方面具有很好的实用价值。结合血清miR-1193,可以更有效的判断胶质瘤复发及进展,更好地监控疾病的发展。
