依鲁替尼及其磷脂复合物在比格犬体内的药动学比较研究Δ
2019-08-13林琳鲁梅邓意辉沈阳药科大学药学院沈阳110016
林琳,鲁梅,邓意辉(沈阳药科大学药学院,沈阳110016)
依鲁替尼是一种新型的Bruton酪氨酸激酶(BTK)抑制剂,能够通过与BTK酶激活区域内的Cys481位点结合进而发挥抑制该酶活性、阻止肿瘤细胞转移的作用[1-2]。目前,依鲁替尼主要用于治疗包括慢性淋巴细胞白血病、套细胞淋巴瘤和Waldenstrom巨球蛋白血症在内的多种淋巴瘤[3]。但依鲁替尼的水溶性极差,口服制剂的生物利用度极低,导致临床用药剂量偏大,患者在治疗过程中易出现出血、高血压等毒副反应,导致该药的临床应用受到了极大限制[4]。磷脂复合物给药系统能极大地提高难溶性药物的水溶性,增加其血药浓度并延长药物在体内的滞留时间,并显著改善其生物利用度[5-7]。故本课题组前期制备了依鲁替尼磷脂复合物。本研究在此基础上,建立了测定比格犬血浆中依鲁替尼浓度的高效液相色谱法(HPLC);并以依鲁替尼原料药为对照,比较了两者在比格犬体内的药动学差异,以期为其新剂型的研发提供实验基础。
1 材料
1.1 仪器
P230型高压恒流泵、UV200Ⅱ型紫外可变波长检测器、HW-2000色谱数据处理工作站(大连依利特分析仪器有限公司);AT-130型柱温箱(天津市金洲科学仪器有限公司);S3100型自动进样器、SVC-Ⅱ型高精度全自动交流稳压器(中川电气科技有限公司);XS105型电子分析天平(瑞士Mettler-Toledo公司);DF-101S型磁力搅拌器(巩义市英峪予华仪器有限责任公司);Anke TDL80-2B型离心机(上海安亭科学仪器厂);XH-D型涡旋仪(上海启前电子科技有限公司)。
1.2 药品与试剂
依鲁替尼原料药(南京熙泽生物科技有限公司,批号:20161213,纯度:≥99%);甲苯磺丁脲对照品(内标,大连美仑生物技术有限公司,批号:J1010AS,纯度:≥99%);蛋黄磷脂酰甘油(上海艾韦特医药科技有限公司,批号:B40643,纯度:≥97%);乙腈、冰醋酸均为色谱纯,乙醇、三乙胺等试剂均为分析纯,水为超纯水。
1.3 动物
清洁级健康比格犬6只,雄性,8月龄,体质量10~15 kg,由沈阳药科大学实验动物中心提供,动物使用许可证号:SYXK(辽)2014-0004。
2 方法与结果
2.1 依鲁替尼磷脂复合物的制备
参照本课题组前期研究方法制备依鲁替尼磷脂复合物:称取依鲁替尼原料药10.0 mg和蛋黄磷脂酰甘油18.0 mg,以乙醇为反应溶剂,于40℃反应0.5 h后,减压蒸发除去乙醇,加入适量二氯甲烷洗涤以除去游离药物,抽滤,收集沉淀,常温减压干燥24 h,即得依鲁替尼磷脂复合物(每克磷脂复合物约含依鲁替尼0.35 g)。
2.2 溶液的制备
2.2.1 依鲁替尼系列标准溶液 精密称取依鲁替尼原料药5.00 mg,用甲醇稀释,制得质量浓度为10 μg/mL的贮备液。精密量取上述贮备液适量,用甲醇稀释至相应质量浓度,制得依鲁替尼系列标准溶液,密封,于4℃保存,备用。
2.2.2 内标溶液 精密称取内标对照品10.00 mg,用甲醇稀释,制得质量浓度为1.0 mg/mL的内标贮备液。精密量取上述内标贮备液适量,用甲醇稀释,制得质量浓度为50 ng/mL的内标溶液,密封,于4℃保存,备用。
2.2.3 依鲁替尼混悬液 精密称取依鲁替尼原料药适量,用0.5%交联羧甲基纤维素钠溶液稀释,充分搅拌,制得质量浓度为5 mg/mL的依鲁替尼混悬液,备用。
2.2.4 依鲁替尼磷脂复合物混悬液 精密称取“2.1”项下依鲁替尼磷脂复合物适量,加入预热至40℃的水中,充分搅拌,制得质量浓度为5 mg/mL的依鲁替尼磷脂复合物混悬液,备用。
2.3 分组与给药
将比格犬随机分为两组,即依鲁替尼混悬液组和依鲁替尼磷脂复合物组,每组3只。所有比格犬均禁食、不禁水12 h后,分别单次灌胃“2.2.3”“2.2.4”项下相应药物混悬液,给药剂量均为15 mg/kg(根据临床使用剂量按等效剂量系数折算法[8]换算而得)。
2.4 血浆样品处理
精密量取血浆样品300µL,置于1.5 mL离心管中,加入50 ng/mL内标溶液100µL,加入甲醇600µL,涡旋混匀10 min,10 000 r/min离心10 min,取上清液于室温下以氮气流挥干,残渣用流动相100µL复溶,涡旋混匀5 min,10 000 r/min离心10 min,取上清液适量,进样分析。
2.5 色谱条件
色谱柱:Betasil C18(200 mm×4.6 mm,5µm);流动相:乙腈-水(含0.5%三乙胺,用冰醋酸调节pH至3.2)(45∶55,V/V);流速:1.0 mL/min;检测波长:256 nm;柱温:25℃;进样量:20µL。
2.6 方法学考察
2.6.1 专属性 分别取空白血浆、空白血浆+依鲁替尼(250 ng/mL)、依鲁替尼磷脂复合物组比格犬给药后12 h时的血浆样品各适量,按“2.4”项下方法处理后(空白血浆不加内标),再按“2.5”项下色谱条件进样分析,记录色谱图,结果见图1。由图1可见,内标和依鲁替尼的保留时间分别为7.37、11.66 min,且血浆中的内源性物质对待测物的定量分析无明显干扰,表明本法的专属性良好。
2.6.2 标准曲线的绘制与定量下限、最低检测限的考察 精密量取空白血浆270 μL,置于1.5 mL离心管中,分别加入“2.2.1”项下不同质量浓度的依鲁替尼系列标准溶液各30 µL,制得质量浓度分别为5、10、50、100、500、1 000、5 000 ng/mL的系列含药血浆样品,按“2.4”项下方法处理后,再按“2.5”项下色谱条件进样分析,记录峰面积。以待测物质量浓度(x,ng/mL)为横坐标、待测物与内标的峰面积比值(y)为纵坐标进行线性回归,得回归方程为y=0.007 86x-0.003 91(r=0.999 8)。结果,依鲁替尼检测血药浓度的线性范围为5~5 000 ng/mL,定量下限为5 ng/mL(信噪比为10);以信噪比为3测得最低检测限为1.3 ng/mL。
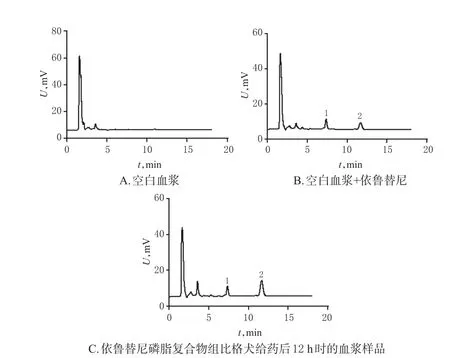
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.6.3 精密度与准确度试验 按“2.6.2”项下方法配制同一分析批的依鲁替尼定量下限以及低、中、高质量浓度(10、100、4 000 ng/mL,下同)血浆样品各5份,按“2.4”项下方法处理后,进样分析,考察批内精密度和准确度;同法配制3个分析批的定量下限以及低、中、高质量浓度血浆样品,连续测定3 d,每质量浓度平行测定5次,考察批间精密度和准确度。结果,批内、批间RSD均小于10%,准确度(检测值,下同)为98.81%~106.20%,详见表1。

表1 精密度与准确度试验结果Tab 1 Results of precision and accuracy tests
2.6.4 提取回收率试验 按“2.6.2”项下方法配制依鲁替尼低、中、高质量浓度血浆样品,按“2.4”项下方法处理后,再按“2.5”项下色谱条件进样分析,得依鲁替尼峰面积(A提取);另取空白血浆适量,按“2.4”项下方法处理至“挥干”,残渣加入相应质量浓度的依鲁替尼标准溶液,混匀,使最终质量浓度与前者对应,再按“2.5”项下色谱条件进样分析,得依鲁替尼峰面积(A未提取),提取回收率=(A提取/A未提取)×100%。每质量浓度平行5样本分析。结果,低、中、高质量浓度血浆样品的提取回收率分别为(84.36±2.43)%、(79.17±2.39)%、(87.50±2.33)%,RSD分别为2.89%、3.02%、2.67%(n=5);内标的提取回收率为(86.17±1.36)%,RSD为1.82%(n=5)。
2.6.5 稳定性试验 按“2.6.2”项下方法配制依鲁替尼低、中、高质量浓度血浆样品,考察室温放置3 h、反复冻融(-20℃至室温)3次、-20℃冷冻放置3周后再处理以及处理后室温放置24 h的稳定性。每质量浓度平行3样本分析。结果,在上述条件下,各样品实测血药浓度的RSD均小于10%(n=3),表明其稳定性良好,详见表2。
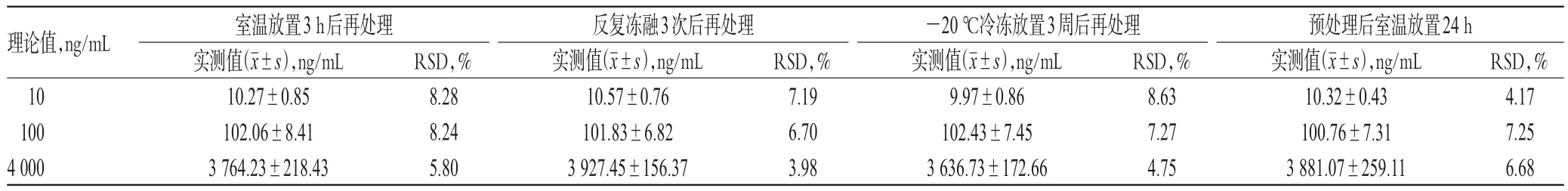
表2 稳定性试验结果(n=3)Tab 2 Results of stability tests(n=3)
2.7 药动学研究
6只比格犬按“2.3”项下方法分组并给药,分别于给药前及给药后0.017、0.083、0.25、0.5、1、2、4、8、12 h于左前肢静脉取血2 mL,置于肝素化管中,4 500 r/min离心10 min,分离血浆,并置于-20 ℃保存,待检。取上述血浆样品适量,按“2.4”项下方法处理后,再按“2.5”项下色谱条件进样分析,代入随行标准曲线计算依鲁替尼的血药浓度,并使用DAS 2.1.1软件绘制平均药-时曲线,结果见图2。
采用DAS 2.1.1软件处理上述平均药-时曲线数据,计算主要药动学参数和相对生物利用度{F,F=[(AUC0-12h)依鲁替尼磷脂复合物组/(AUC0-12h)依鲁替尼混悬液组]×100%},结果见表3。采用SPSS 20.0软件对两组比格犬的药动学参数进行统计分析。数据均以±s表示,组间比较采用t检验。P<0.05为差异有统计学意义。
由图2可见,比格犬灌胃依鲁替尼磷脂复合物混悬液后,药物在体内吸收迅速,给药后约0.25 h即可达最高血药浓度,且1 h内均维持在较高水平;而灌胃依鲁替尼混悬液后,药物在体内吸收较缓慢,给药后约2 h才达到峰值。由表3可见,依鲁替尼磷脂复合物组比格犬的cmax、AUC0-12h、AUC0-∞分别为依鲁替尼混悬液组的 3.78、2.08、1.74倍,其F为207.99%。与依鲁替尼混悬液组比较,依鲁替尼磷脂复合物组比格犬体内药物的cmax、AUC0-12h、AUC0-∞均显著增加,tmax显著缩短,差异均有统计学意义(P<0.05)。
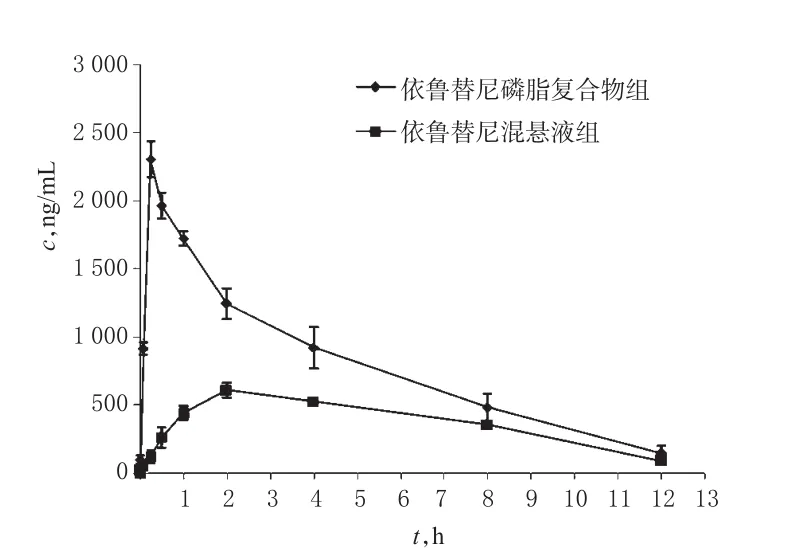
图2 比格犬单次灌胃依鲁替尼混悬液和依鲁替尼磷脂复合物混悬液的平均药-时曲线(n=3)Fig 2 Mean plasma concentration-time curves of ibrutinib in Beagle dogs after single intragastric administration of Ibrutinib suspension and Ibrutinib phospholipid complex(n=3)
表3 比格犬单次灌胃依鲁替尼混悬液和依鲁替尼磷脂复合物混悬液的主要药动学参数(±s,n=3)Tab 3 Main pharmacokinetic parameters of ibrutinib in Beagle dogs after single intragastric administration of Ibrutinib suspension and Ibrutinib phospholipid complex(±s,n=3)

表3 比格犬单次灌胃依鲁替尼混悬液和依鲁替尼磷脂复合物混悬液的主要药动学参数(±s,n=3)Tab 3 Main pharmacokinetic parameters of ibrutinib in Beagle dogs after single intragastric administration of Ibrutinib suspension and Ibrutinib phospholipid complex(±s,n=3)
注:与依鲁替尼混悬液组比较,*P<0.05Note;vs.Ibrutinib suspension group,*P<0.05
组别依鲁替尼混悬液组依鲁替尼磷脂复合物组AUC0-∞,ng·h/mL 6 174.32±525.27 10 717.33±897.62*tmax,h 2.00±0.09 0.25±0.03*cmax,ng/mL 610.67±21.36 2 308.72±100.41*AUC0-12 h,ng·h/mL 4 516.67±383.43 9 394.16±874.21*
3 讨论
笔者查阅相关文献后发现,测定依鲁替尼在大鼠血浆中浓度的方法已有相关报道[9-10],但尚未见其在比格犬体内药动学研究的相关文献。本研究参考上述报道,对血浆处理方法进行了改进,最终选择了操作简便、重复性较好的直接蛋白沉淀法。在沉淀试剂的筛选过程中,笔者发现甲醇的提取回收率最为稳定,且处理后内源性杂质的干扰较小,故最终选择甲醇作为蛋白沉淀试剂。同时,本研究采用乙腈-水(含0.5%三乙胺,用冰醋酸调节pH至3.2)作为流动相,并通过预试验将其等度洗脱的比例确定为45∶55(V/V)。方法学考察结果显示,依鲁替尼和内标可基线分离,且两者色谱峰的峰形均较好;依鲁替尼检测血药浓度的线性范围为5~5 000 ng/mL,批间、批内RSD均小于10%,稳定性良好,其提取回收率稳定(RSD<5%),表明本研究建立的HPLC法可用于比格犬体内依鲁替尼血药浓度的测定。
磷脂复合物是指在合适溶剂中将药物和磷脂按一定化学计量比混合而成的复合物,可显著提高药物的水溶性,并改善其稳定性和透膜性,从而提高药物的生物利用度[11]。依鲁替尼在pH 4.5~8.0的水中几乎不溶(溶解度仅为3 μg/mL),严重影响其在胃肠道中的吸收,故在临床治疗中必须使用大剂量才能保证药效的充分发挥[12]。但大剂量的使用可能会增加患者发生出血、高血压等多种毒副反应的风险[4]。将依鲁替尼制成磷脂复合物后,由于磷脂与生物膜的亲和性更高,可“带领”药物顺利穿过胃肠道而被吸收入血,因此显著增加了依鲁替尼的口服吸收程度[13]。药动学研究结果显示,在分别灌胃依鲁替尼混悬液和依鲁替尼磷脂复合物后,药物在比格犬体内的药动学行为发生了明显变化。其中,依鲁替尼磷脂复合物的吸收速度更快,体内血药浓度在给药后约0.25 h即达到了峰值,且其cmax、AUC0-12h、AUC0-∞均显著高于依鲁替尼混悬液组,tmax显著短于依鲁替尼混悬液组,F为207.99%。这提示将依鲁替尼制备成磷脂复合物可加快药物在体内的吸收,并提高其生物利用度。但本研究仅选用了6只比格犬,样本量偏小,且药动学指标有限,后续研究将进一步扩大样本量以减小个体差异,并深入研究依鲁替尼磷脂复合物在比格犬体内的代谢过程。
综上所述,本研究建立的HPLC法操作简便、专属性强、灵敏度高,可用于比格犬血浆中依鲁替尼质量浓度的测定和药动学的研究。将依鲁替尼制成磷脂复合物后,其药动学参数变化明显,药物吸收明显加快,生物利用度明显提高。
