沥青质分子聚集体中π-π相互作用的研究
2019-07-31代振宇
任 强,龙 军,代振宇,周 涵
(中国石化 石油化工科学研究院,北京 100083)
在石油的生产、储运和加工过程中,沥青质所引起的问题越来越受到人们的重视,目前已成为石油工业中需重点研究和解决的技术问题之一。沥青质的缔合、聚集、沉积、生焦等问题的最终结果导致了生产成本的大幅度增加。这一切的根源均与沥青质分子形成的超分子结构的聚集体有关。因此,进一步认识沥青质分子聚集体的结构,研究形成沥青质超分子结构的作用力,破坏沥青质的超分子结构,使沥青质以单分子形式参与反应,对于重油加工具有重要的意义。
由于胶质、沥青质中存在较大的芳香环系和较多的杂原子,可通过芳香环系的π-π堆积以及与杂原子形成的氢键进行自组装,形成超分子聚集体[1-2]。但是,导致沥青质缔合的主要作用力长期以来却颇有争议[3-4],对于沥青质分子形成这种超分子结构的分子间作用力至今没有清晰的一致认识。许多学者认为氢键是沥青质缔合的主要作用力[5-6],但也有人认为沥青质胶粒之间的缔合主要是由分子片层之间的π-π相互作用[7]、极性诱导作用、静电引力作用等引起的[8-9]。
笔者拟采用分子模拟方法,通过模拟计算沥青质分子聚集体的π-π相互作用力,找到形成沥青质超分子结构的分子间π-π相互作用力大小及影响因素,确定沥青质分子聚集的主要推动力,为沥青质分子聚集体的解聚提供思路,为沥青质的加工提供一定的帮助。
1 分子模拟工具和模拟方法
1.1 分子模拟工具和方法
进行相关分子模拟计算采用的计算机硬件为IBM Flex System集群服务器,软件为Materials Studio 8.0,ADF 2014.10。
分子尺度的模拟方法主要有量子力学(Quantum mechanics,QM)[10]、分子动力学(Molecular dynamics,MD)[11]、分子力学(Molecular mechanics,MM)[12]和蒙特卡洛(Monte Carlo,MC)[13]等方法。
受体系规模和计算机硬件的制约,目前学者针对重油中体系的模拟主要采用分子动力学方法,而针对化学反应过程则采用精度更高的量子力学方法。本研究采用分子动力学和量子力学相结合的方法,对于π-π作用力的计算,采用分子动力学方法确定沥青质分子的聚集位置,采用量子力学方法对沥青质分子间的π-π作用力的大小进行计算。
1.2 模型化合物的确定
在分析沥青质分子的元素组成和相对分子质量的基础上,通过核磁共振法、傅里叶变换红外光谱仪和X射线光电子能谱分别获得碳氢结构信息和杂原子官能团信息,可确定模型沥青质分子中芳碳、环烷碳和链烷碳的相对比例以及芳氢和脂肪氢的相对比例,进而确定模型沥青质分子中大致的芳环、环烷环及支链的个数。沥青质中的硫主要以噻吩环形式存在;氮主要以吡咯环形式存在;而氧的形态主要有羟基氧和羰基氧。根据实验分析数据,利用分子模拟确定本研究的沥青质分子的模型化合物如图1所示。其中图1(a)为带有短侧链的沥青质分子;图1(b)为带有长侧链的沥青质分子;图1(c)为无侧链的沥青质分子。
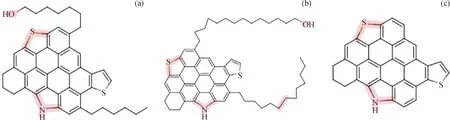
图1 沥青质分子模型化合物结构图Fig.1 Model structures of asphaltene molecules(a)Asphaltene molecule with short side chains;(b)Asphaltene molecule with long side chains;(c)Asphaltene molecule without side chains
1.3 模拟参数的设置
用Materials Studio软件对模型分子进行分子动力学结构优化时,采用NVE系综,Andersen方法,温度控制在600 K,Compass力场,时间步长为1 fs,总模拟时间为500 ps,结果记录文件为每计算500步输出一个结构,截取半径为1.35 nm。
在ADF(Amsterdam density functional)进行模拟中,分子轨道使用Slater基组TZ2P展开(不含任何Gaussian函数)。对于C、N、O、S原子,冻结了1s轨道[14]。在自洽场(SCF)计算过程中,计算库仑、交换相关势时,软件自动采用一套包含s、p、d、f、g的Slater函数来拟合分子的电子密度[15]。泛函采用的是BLYP-D3(BJ),BLYP为GGA泛函的一种,-D3(BJ)是一种对泛函的长程行为进行“经验参数式”修正的所谓“色散修正”方法[16]。色散修正主要用于弱相互作用体系,例如氢键、超分子。需要进行色散修正的原因主要是一般的密度泛函势函数随着离原子核距离增大衰减过快,因此对距离较远的原子的相互作用描述得不好,-D3(BJ)修正之后,原子间长程相互作用势的衰减形式为C6/(R6+c)[17]。其中c、C6为拟合得到的常数,R为离原子核的距离。简单地说就是呈6次方衰减。结构优化使用的是软件默认的解析梯度方法。
2 结果与讨论
π-π相互作用是指存在于有共轭结构的一些化合物分子内或分子间的一种弱相互作用。由于π-π相互作用在芳环体系中最为常见,故又被称为芳环作用(Aromatic interactions)。由于沥青质分子由多个芳环构成,故沥青质分子间的π-π相互作用是研究人员长期关注的问题。
2.1 稠合芳环个数对π-π相互作用的影响
π-π相互作用能是分子非键相互作用能的一种,沥青质分子含有多个稠合芳环,为了研究芳环数量对分子间π-π相互作用的影响,分别对图2中具有不同芳环数的分子二聚体间的π-π相互作用进行量化计算,结果如表1所示。
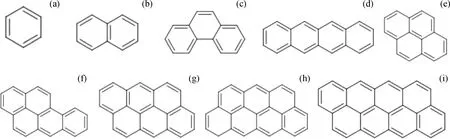
图2 不同稠合芳环数的模型化合物分子Fig.2 Model compound molecules with different aromatic ring numbers(a)Monocyclic aromatic hydrocarbon;(b)Bicyclic aromatic hydrocarbon;(c)Tricyclic aromatics hydrocarbon;(d)Tetracyclic aromatic hydrocarbon (Cata condensed);(e)Tetracyclic aromatic hydrocarbon (Peri condensed);(f)Pentacyclic aromatic hydrocarbons;(g)Hexacyclic aromatics hydrocarbons;(h)Seven-ring aromatics hydrocarbons;(i)Eight-ring aromatics hydrocarbons
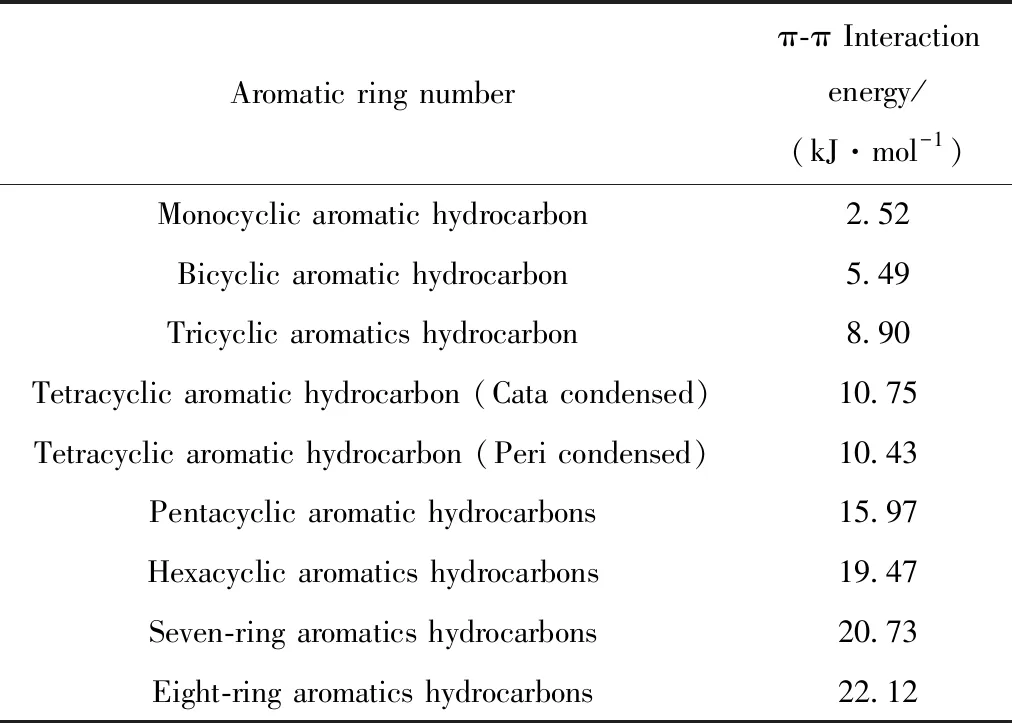
表1 不同稠合芳环数间的π-π相互作用Table 1 π-π Interactions between different numbers of aromatic hydrocarbons
从表1可以看出,随着芳环数的增加,2个分子间的π-π相互作用能增加,说明芳环数越多的分子其分子间的π-π相互作用能越强。沥青质分子的稠合芳环数大多在7~8环,因此其分子间存在着π-π相互作用。但从数值来看,2个具有8个芳环的分子间的作用能也只有22 kJ/mol,与氢键的大小差不多,说明2个具有稠合芳环的分子间的π-π作用力也是弱相互作用。
由于沥青质分子多以3~4个分子缔合在一起,为了考察多个稠环芳烃分子缔合时的π-π作用力,分别计算了3个图2(g)所示和4个图2(i)所示稠环芳烃分子间的π-π作用能,同时分别计算了图1(a)所示2个、3个、4个沥青质分子间的π-π作用能,结果如表2所示。

表2 不同分子个数间的π-π相互作用能Table 2 π-π Interaction energies between different number of molecules
由表2可以看出,3个稠环芳烃分子形成的聚集体中,分子间π-π相互作用能比2个稠环芳烃分子聚集体的π-π相互作用能大。3个六环芳烃分子的π-π相互作用能可以达到31.09 kJ/mol;3个八环芳烃分子可以达到47.67 kJ/mol;4个八环芳烃分子则可达到55.54 kJ/mol。由此可见,随着聚集体中稠环芳烃分子个数的增加,其π-π相互作用能逐渐提高。由于分子间的π-π相互作用使聚集体的总能量降低,体系更稳定,因此具有稠环芳烃结构的分子容易形成多分子聚集体。从表2还可以看出,随着形成聚集体时沥青质分子(含有杂原子)数量的增多,其分子间的π-π相互作用能增大。
另外,2个八环芳烃分子的π-π相互作用能仅为22.12 kJ/mol,比2个沥青质分子的 π-π 相互作用能小得多,说明沥青质分子中的S、N、O杂原子对沥青质分子间的π-π相互作用能影响很大。
2.2 分子间排列方式对π-π相互作用的影响
具有稠环芳烃结构的沥青质分子的空间构象一般类似圆盘状结构,因此,沥青质分子间的排列存在多种形式,有平行排列结构,也有垂直排列结构,还有介于两者之间的倾斜排列结构。为了考察不同排列方式对沥青质分子间π-π相互作用的影响,对图1(a)所示的2个沥青质分子在不同的排列方式下π-π相互作用能进行了研究,结果见表3。

表3 图1(a)中2个沥青质分子间不同排列角度时的π-π相互作用能Table 3 π-π Interaction energies for different arrangement angles of two asphaltene molecules in Fig.1(a)
由表3可以看出:当2个分子平行排列即分子间的夹角为0°时,分子间的π-π相互作用能最大;而2个分子相互垂直,即分子间的夹角为90°时,分子间的π-π相互作用能最小;当2个分子间排列存在一定的夹角时,分子间的π-π相互作用能均小于分子完全平行时的π-π相互作用能。这说明沥青质分子间的π-π相互作用能只有在2个分子互相平行时才能达到最大,此时形成的聚集体降低的能量最多,体系也最稳定,沥青质分子更趋向于平行排列方式。因此,要想减少沥青质分子间的π-π相互作用能,就要破坏沥青质分子间平行结构,使其变为垂直结构或者加大分子间距离。
2.3 烷基侧链对π-π相互作用的影响
沥青质分子除具有稠环芳核外,在稠环芳核的外围还连接一定数量的烷基侧链,且烷基侧链的长短也会有所不同。由于烷基侧链的存在,有可能影响沥青质分子的空间构象,从而对π-π相互作用产生一定影响。为了考察这一影响,分别选取了如图1(a)所示的带2个短侧链的沥青质分子、图1(b)所示的带2个长侧链的沥青质分子及图1(c)所示的无侧链的沥青质分子为模型化合物,分别计算其 π-π 相互作用能,考察侧链对π-π相互作用能的影响。
通过计算得知:2个带2个长侧链的沥青质分子的π-π相互作用能为42.35 kJ/mol;2个带2个短侧链的沥青质分子的π-π相互作用能为53.53 kJ/mol;而2个无侧链的沥青质分子的π-π相互作用能为61.28 kJ/mol。由此可以看出,稠环芳烃连接烷基侧链将使其π-π相互作用能下降,且随着烷基侧链长度的增加,π-π相互作用能也随之降低。这是由于烷基侧链间的排斥作用改变了沥青质分子的空间构象,使2个平行的沥青质分子间距变大,分子间电子云的作用减小,从而导致沥青质分子间的π-π相互作用能降低。烷基侧链越长,侧链间的排斥作用越大,从而对沥青质分子间π-π相互作用的影响越显著。因此,烷基侧链的存在能够减小沥青质分子间的π-π相互作用。
除烷基侧链的长短影响分子间π-π相互作用外,侧链类型也会对沥青质分子间π-π相互作用产生影响。笔者分别计算了图3所示的4种类型模型化合物分子间的π-π相互作用能。为了便于比较并简化计算,图3中模型化合物中的稠环芳烃部分完全相同,均选用五环的稠环芳烃为母体,侧链则选用了不同的类型。其中,图3(a)和图3(b)中的侧链带有吸电子基团;图3(c)和图3(d)中的侧链带有供电子基团。图3中灰色的球为C原子,白色的小球为H原子,红色的球为O原子,蓝色的球为N原子。通过对带不同类型侧链的2个沥青质分子间的π-π相互作用能计算得知:2个侧链含COOH(中吸电子基团)的沥青质分子的π-π相互作用能为38.05 kJ/mol;2个侧链含NO2(强吸电子基团)的沥青质分子的 π-π 相互作用能为34.74 kJ/mol;2个侧链含NH2(强给电子基团)的沥青质分子的π-π相互作用能为24.35 kJ/mol;2个芳烃直连NH2(强给电子基团)的沥青质分子的π-π相互作用能为28.36 kJ/mol。
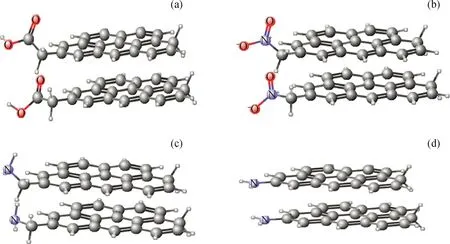
图3 不同类型侧链的沥青质模型化合物Fig.3 Asphaltene model compounds containing different kinds of side chains(a)Side chains with electron-withdrawing groups;(b)Side chains with electron-withdrawing groups;(c)Side chains with electron donating groups;(d)Aromatic hydrocarbons directly linked to electron-donating groups
由此可以看出,当侧链为吸电子基团(—COOH或—NO2)时,分子间π-π相互作用能大于侧链为供电子基团(—NH2)的。这是由于—COOH或—NO2基团中都含有双键,双键之间也形成共轭作用,导致分子间π-π相互作用能变大。另外,图3(d)所示的强供电子基团—NH2与芳环直接相连时,分子间π-π相互作用能为28.36 kJ/mol;而图3(c)所示 —NH2基团在侧链上时,分子间π-π相互作用能为24.35 kJ/mol。两者相差不大,故杂原子基团在侧链上的位置对分子间π-π相互作用能影响不大。因此,侧链类型对沥青质分子间的π-π相互作用起到一定的影响作用,具有吸电子基团的侧链能够增强分子间的π-π相互作用。
2.4 氢键作用与π-π相互作用共同的影响
由于沥青质分子中会同时含有S、N、O等杂原子,因此,2个沥青质分子间有可能同时形成2个甚至多个氢键。同时,沥青质分子聚集体中会有多个沥青质分子通过π-π相互作用聚集在一起。定义2个沥青质分子间的π-π相互作用方式为“π-π”,3个沥青质分子间的π-π相互作用为“2π-π”,4个沥青质分子间的π-π相互作用为“3π-π”。同时,定义2个沥青质分子间形成的1个 S…H—O氢键为“SO氢键”,2个沥青质分子间形成的2个S…H—O氢键为“2SO氢键”,2个沥青质分子间形成的3个 S…H—O 氢键为“3SO氢键”。
对图1(a)所示的沥青质分子的聚集体中形成的多氢键和多π-π相互作用进行计算,结果如表4所示。由表4可以看出:在相同的π-π相互作用能下,随着沥青质聚集体中氢键数量的增加,其分子间的相互作用能增加;在相同的氢键数量下,分子间的π-π相互作用的数量越多,相互作用能越大。因此,沥青质分子中虽然单个氢键能或者π-π相互作用能较小,但形成的聚集体含有多个氢键和多个π-π相互作用时,其分子间作用力会大大增加,故沥青质分子聚集体在多种作用力的共同作用下,分子间作用力较强,要削弱这种作用力,使沥青质分子以单分子形式存在,需要的能量也较大。因此,要使沥青质分子聚集体解聚就要分别消除其各种类型的作用力。

表4 沥青质分子聚集体中多氢键和多π-π相互作用Table 4 Interactions between multiple hydrogen bonds and multiple π-π in asphaltic aggregates
2.5 沥青质分子中π-π相互作用的本质
为研究沥青质分子聚集体中分子间π-π相互作用的本质,用ADF软件对图1 (a)所示的沥青质分子形成的聚集体的轨道及其能量进行分析。图4是具有π-π相互作用的沥青质分子二聚体与沥青质分子单体之间的部分轨道关系图。中间为二聚体轨道,两边分别为2个相同单体的沥青质分子1和沥青质分子2的轨道。该图并未显示完整的单体与二聚体的轨道关系,只展示了HOMO、HOMO-1、LUMO、LUMO+1等几个关键轨道的关系。
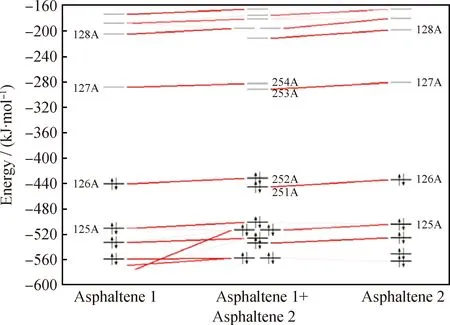
图4 沥青质分子二聚体的π-π相互作用部分轨道关系Fig.4 Partial orbital relationship of π-π interactions in asphaltene molecular dimers
图4中左边Asphaltene 1上方的127A是Asphaltene 1的LUMO,126A即Asphaltene 1的HOMO;右边Asphaltene 2的前线轨道与Asphaltene 1的类似。Asphaltene 1+ Asphaltene 2上方的251A和252A 是具有π-π相互作用的沥青质分子二聚体的 HOMO-1 和HOMO,更上方的253A和254A对应沥青质分子二聚体的2个空轨道LUMO和LUMO+1。
用ADF软件对不同的轨道进行分析,可以得到如图5所示的该二聚体轨道的组分主要来源。图5 中最高占有轨道252A的组分来源于Asphaltene 1的126A和Asphaltene 2的126A,Asphaltene 1的126A占有绝大多数,Asphaltene 2的126A则占有很小的比例,说明这个二聚体的最高占有轨道主要是由Asphaltene 1的电子组成,Asphaltene 2则贡献了少量的电子。同样,作为HOMO-1的251A的组分来源则与HOMO相反,Asphaltene 2贡献了较多的电子,而Asphaltene 1则贡献了较少的电子。另外,对沥青质分子二聚体的LUMO、LUMO+1轨道253A和254A进行分析,发现LUMO主要由Asphaltene 2和Asphaltene 1共同组成,但Asphaltene 2占据了主要部分,Asphaltene 1只占据了很少一部分,而LUMO+1与LUMO正好相反,Asphaltene 1占据了主要部分,Asphaltene 2只占据很少一部分,所不同的是该轨道由Asphaltene 1的127A轨道和Asphaltene 2的127A、128A轨道共同组成,即该轨道是由沥青质分子的3个轨道组成,而且距离前线轨道越远的轨道组成越复杂,如二聚体的249A轨道,由5个不同的分子轨道组成。因此,沥青质分子通过π-π相互作用形成二聚体后,其轨道变得愈加复杂,不同单体间的多条轨道共同作用形成二聚体。由此可见,形成二聚体时2个单体都对二聚体的轨道产生了一定的影响,只是在不同的轨道,一个单体占据主要组分,另一个单体只占有一小部分(大约占5%左右,但相比于氢键的占比0.75%,π-π相互作用形成的二聚体的轨道组成相对更均匀一些)。由此也说明,在形成π-π相互作用的过程中,单体间有少量的电子转移,导致形成弱的次级键。

图5 形成二聚体轨道的组分主要来源Fig.5 Main sources of orbital components for dimers
2.6 沥青质分子中π-π相互作用能的组成
对形成π-π相互作用的沥青质分子二聚体的π-π相互作用能ΔE定义如下:
ΔE=Edimer-Emonomer1-Emonomer2
(1)
其中,Edimer表示优化得到的沥青质分子二聚体的能量;Emonomer1和Emonomer2分别表示沥青质分子1和沥青质分子2优化得到的能量。总的π-π相互作用能ΔE在物理含义上包含两部分:
ΔE=ΔEprep+ΔEint
(2)
式中,ΔEprep是从单分子自由状态发生构象变化,变为二聚体中的构象所需要消耗的能量[18](这个能量显然一般情况下为正值,因为自由状态的结构能量肯定是局域最小的);ΔEint是2个构象已经“准备好”的单分子,保持构象不变,形成二聚体时释放的能量(这个能量一般情况下为负值,否则二聚体能量高于单体能量之和,则无法形成二聚体)。
该体系的相互作用能ΔEint在Kohn-Sham分子轨道框架下进行定量的能量分解(Energy decomposition analysis,EDA),分解成静电相互作用能、Pauli排斥轨道相互作用能、“吸引”轨道相互作用能以及色散相互作用能[19]:
ΔEint=ΔEelstat+ΔEPauli+ΔEoi+ΔEdisp
(3)
ΔEelstat表示经典概念下,单分子构象已经完成“形变准备”(即单分子已经从自由状态的构象调整为二聚体中的构象),2个单分子之间的电子密度还互不影响时,2个沥青质分子之间的静电相互作用。电子密度空间分布为2个孤立单分子的电子密度直接叠加。通常,这是吸引作用(否则无法形成二聚体)。
Pauli排斥轨道相互作用ΔEPauli包括占据轨道之间的倾向于破坏稳定的相互作用,即产生了占据轨道之间的在空间上互相排斥的效果。
轨道相互作用ΔEoi在任何分子轨道理论模型中,当然也包括密度泛函Kohn-Sham理论,都是产生电荷转移的原因所在(也就是施主、受主,一者的占据轨道和另一者的空轨道之间的相互作用,即互相混合所造成。HOMO-LUMO之间的相互作用,或者说互相混合也包括在其中。这部分轨道的相互作用,或者说这部分轨道的混合,导致了单体之间出现电荷转移)。另外,ΔEoi也导致极化(由于另一个单分子的存在,导致此单分子自身的空、占轨道之间也在一定程度上互相混合。这部分轨道的相互作用,或者说这部分轨道的混合,导致了单分子的极化)。
ΔEdisp代表色散修正能量。
表5列出了1个只形成π-π相互作用的沥青质分子二聚体的π-π相互作用能ΔE的分解值。
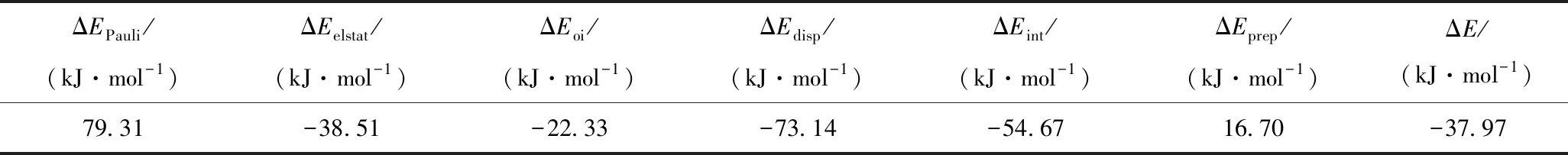
表5 沥青质分子二聚体π-π相互作用能的分解Table 5 The decomposition of the π-π interaction energies in the asphaltene molecule dimer
表5中,π-π相互作用能首先分解为单分子的“形变准备”能ΔEprep以及单分子之间的相互作用能ΔEint。前者非常小,是由于π-π相互作用导致的构象变化很小所致;而ΔEint则相对较大。进一步分解ΔEint发现,静电作用ΔEelstat不提供净的键能,只能部分补偿Pauli排斥轨道相互作用ΔEPauli,因此,如果没有轨道之间的相互作用能ΔEoi,单分子之间将会互相排斥,因此这两种作用能是相伴而生的。ΔEPauli和ΔEelstat总和的大小反映了分子间的空间相互作用的位置,即位阻效应,因为ΔEelstat是分子间的吸引力,而在吸引到一定的距离,由于分子中原子间的电子云的排斥作用,使2个分子在一定的空间位置附近保持平衡振荡,因此反映出了分子在空间上的排布特征,故这两个能量的总和可以看作一个相互作用能即空间相互作用能ΔEsteric,又称空间位阻能,反映的是相邻分子间的空间位阻效应。
从表5还可以看出,在沥青质分子二聚体形成的 π-π 相互作用中,空间相互作用能ΔEsteric为40.8 kJ/mol,大于ΔEoi但小于ΔEdisp。因此,在π-π相互作用中,起主要作用的是空间相互作用能和色散作用能,空间相互作用能为正值,表现出斥力,使两分子尽可能地远离;而色散作用能使两分子之间相互吸引;两者共同作用,使沥青质分子聚集在一起。由此可见:沥青质分子的空间构象对聚集体有重要的影响;色散作用力是π-π相互作用力中的主要因素。而色散作用是范德华力的主要组成部分,由于范德华力具有加和性,因此分子越大,范德华力也越大,分子间的π-π相互作用能也越大。
3 结 论
(1)沥青质分子间的π-π相互作用能随着分子中芳香环数的增加而增大;随着聚集体中稠环芳烃分子个数的增加,其π-π相互作用能逐渐增大;沥青质分子中的S、N、O杂原子对沥青质分子间的π-π相互作用能影响很大;色散作用是π-π相互作用中的主要因素。
(2)沥青质分子间的π-π相互作用能只有在两个分子互相平行时才能达到最大;稠环芳烃中的烷基侧链可使π-π相互作用能下降,且随着烷基侧链长度的增加,π-π相互作用能也随之降低。
(3)沥青质分子聚集体含有多个氢键相互作用和多个π-π相互作用时,其分子间的作用力会大大增加。
(4)沥青质分子间形成π-π相互作用的过程中,分子间有少量的电子转移,色散作用力是π-π相互作用力中的主要因素。
