艾滋病相关的机会性感染性疾病的临床病理特征
2019-07-17肖冠英肖艳华陈谐捷李宝金粟海霞
肖冠英,肖艳华,陈谐捷,李宝金,粟海霞
(1.广州市第八人民医院病理科,广东 广州 510060; 2.广州市第八人民医院感染科,广东 广州 510060; 3.广州市第八人民医院外科,广东 广州 510060)
机会性感染(opportunistic infections,OI)是指条件性病原体在人体免疫功能损伤、防御功能降低情况下所发生的炎症性疾病。条件性病原体包括许多细菌、真菌、病毒及原虫等,在健康人体中不致病,在5种危险人群(恶性肿瘤患者、器官移植受者、严重创伤与感染者、胶原性疾病患者、艾滋病毒(HIV)感染和AIDS患者)中由于人体免疫防御功能降低,可引起比较严重的甚至播散性OI[1]。HIV所致的免疫功能损伤呈进行性加重,以致免疫功能丧失殆尽,不可恢复,使所患机会性感染更加严重或更加复杂,几乎80%患者由于免疫功能缺陷而继发机会性感染并导致死亡[2,3]。近年来,我国HIV感染率及AIDS发病率呈逐年上升趋势,为提高对艾滋病相关的机会性感染的诊疗水平,本研究回顾分析我院AIDS患者的病理活检组织标本3258例,探讨艾滋病相关的机会性感染性疾病中的特异性病原体种类、感染部位及感染的临床病理特征。
1 材料与方法
1.1 研究对象
回顾分析我院2013-2017年临床确诊为艾滋病患者不同部位的病理活检标本3 258例,其中查出特异性病原体感染1294例。
1.2 试剂
六胺银(GMS)、PAS、抗酸及Warthin-Starry银染染色试剂盒购自珠海贝索生物技术有限公司,真菌及抗酸荧光染色试剂盒购自江苏供赢联生物科技有限公司,鼠抗人肺孢子菌(pneumocystisjiroveri,Pj) 及鼠抗人巨细胞病毒(cytomegalovirus,CMV) 单克隆抗体购自北京中衫金桥公司,免疫组化Envision两步法检测试剂盒和DAB显色试剂盒购自DAKO公司。
1.3 方法
1.3.1组织活检 由临床医生进行相应的检查,对病变部位取活检。
1.3.2病理学检查 取病理活检组织,常规固定、包埋、切片、HE染色。由两位高年资病理医师阅片,采用特殊染色、荧光染色及免疫组化染色进行病理学检查。
1.3.3特殊及荧光染色 切片脱蜡至水,按试剂盒说明书中的技术操作规范进行六胺银、PAS、抗酸、Warthin-Starry银染色及真菌、抗酸荧光检测。
1.3.4免疫组化 切片脱蜡至水,置于DAKO抗原修复液中修复20 min,采用DAKO全自动免疫组化仪AutostainerLink 48进行免疫组化操作,苏木素复染。操作步骤按DAKO公司免疫组化Envision两步法试剂盒说明书进行。
2 结 果
2.1 检出特异性感染的病原谱及感染部位
2.1.13 258例艾滋病活检标本中查出特异性病原体感染1 294例,检出率39.7%。
1 294例次(含单独感染1 179例及混合感染115例)艾滋病患者感染的病原谱包括:分支杆菌感染406例(50%),Pj感染308例(23.8%),CMV感染278例(21.5%),马尔尼菲蓝状菌感染173例(13.7%),隐球菌感染103例(8.0%),白色假丝酵母菌、曲霉菌、毛霉菌及组织胞浆菌感染共20例,弓形虫及梅毒螺旋体感染6例,见表1。
115例混合感染包括:肺孢子菌合并CMV, 肺孢子菌合并真菌,肺孢子菌合并结核,CMV合并真菌,CMV合并结核,结核合并真菌,混合真菌,肺孢子菌合并CMV及真菌,结核合并CMV及隐球菌,其中以肺孢子菌合并CMV为最多见,见表2。
2.1.21 294例艾滋病患者感染病原谱的感染部位包括了呼吸系统、消化系统、淋巴结、皮肤组织、脑组织、骨与软组织等各系统各器官,最常见的部位是肺、肠及淋巴结组织,见表3。
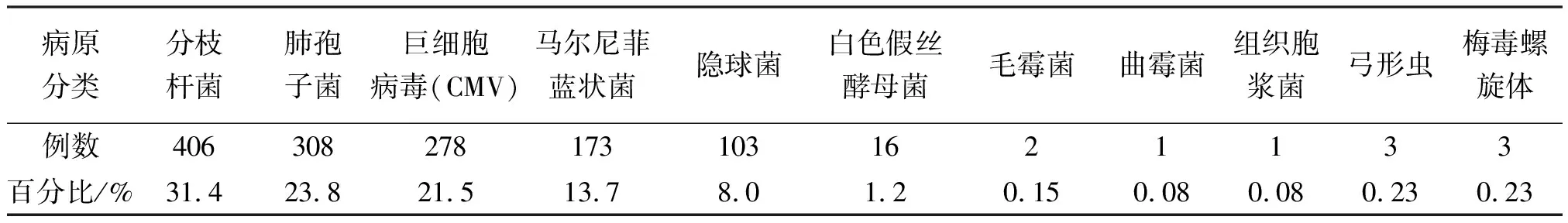
表1 1 294例特异性感染的病原谱
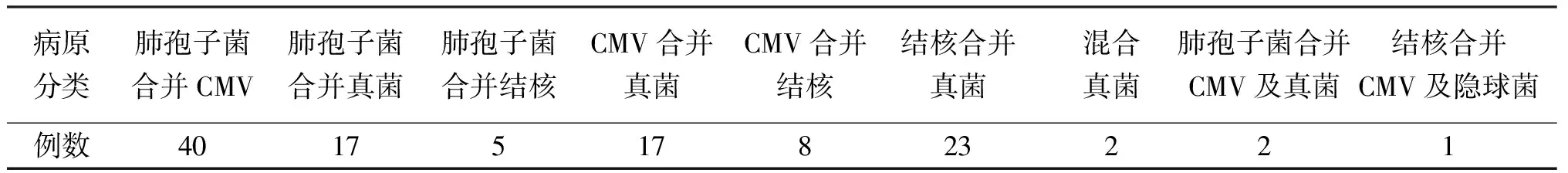
表2 115例混合感染的病原谱
2.2 各种病原体感染的组织病理学特征
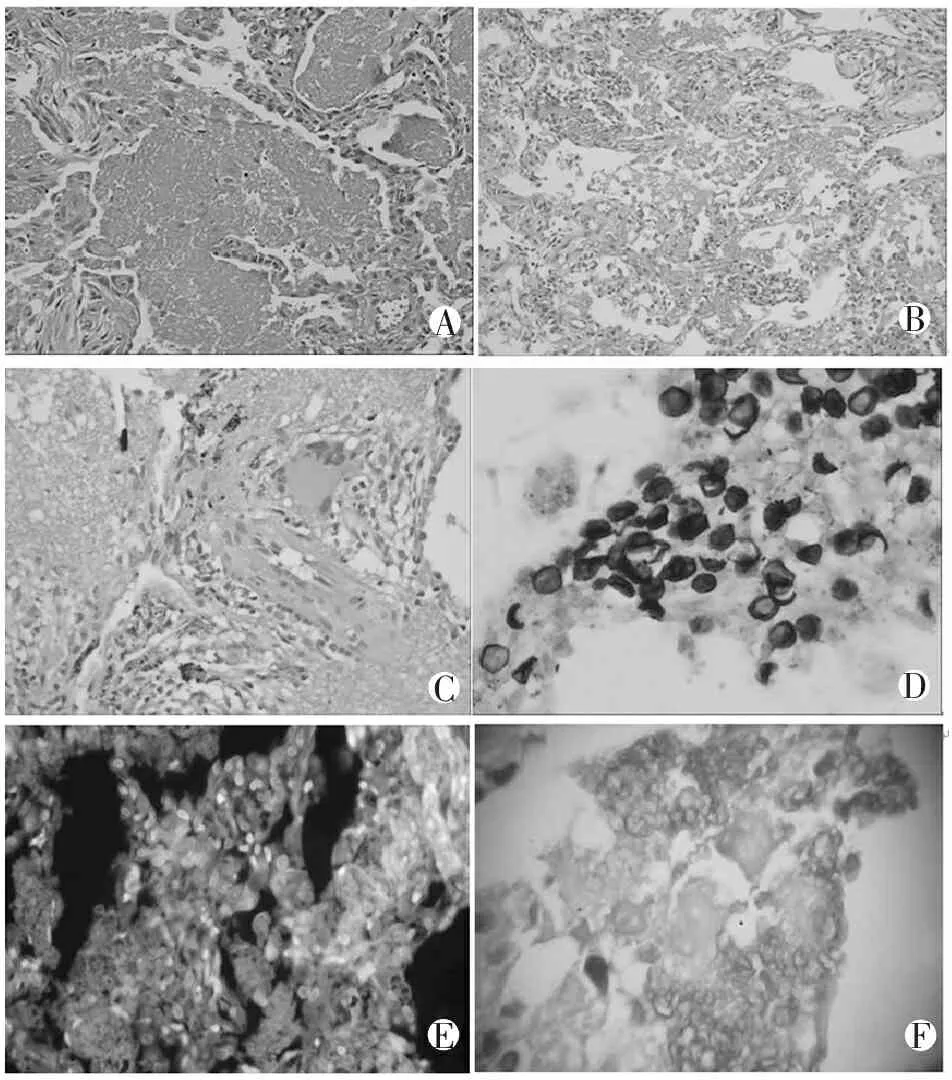
2.2.1耶氏肺孢子菌肺炎 PCP镜下主要表现为肺组织间质性炎和肺泡性肺炎。在扩张的细支气管末端及肺泡腔内粉红色泡沫状或蜂窝状渗出物,肺间质充血增厚伴巨噬细胞、淋巴细胞、浆细胞浸润,有时这种表现不明显,代之以上皮样肉芽肿、间质纤维化等,肺泡腔内也可能缺乏典型的泡沫样渗出物,此时应排除结核,GMS染色可确诊。GMS染色示肺孢子菌为类圆形囊状菌体、某些囊破裂或萎陷而呈新月形或括号形,真菌荧光染色则更为清楚地显示了单个或成对的囊内小体。免疫组化标记显示肺泡腔内肺孢子菌菌体(图1)。
2.2.2结核杆菌 感染早期,患者免疫功能较好,体内可产生典型的肉芽肿反应,病灶内结核杆菌(MTB)数量较少。感染中期,患者CD4+T细胞减少,病灶中肉芽肿反应不明显,干酪样坏死区扩大,MTB增殖,数量增多;感染晚期,患者细胞免疫功能严重受损,发生粟粒性播散性反应性结核,少见典型肉芽肿形成,代之以化脓性及凝固性坏死,MTB大量增殖。抗酸染色见红色的短杆状分枝杆菌,抗酸荧光染色可见黄绿色或红色荧光的短杆状分枝杆菌(图2)。
2.2.3非结核分枝杆菌(NTM) 在406例分枝杆菌中仅1例为非结核分枝杆菌(NTM)鸟-胞内复合型分枝杆菌(MAC)。典型病理变化表现为局灶性组织细胞增生,其胞质丰富呈泡沫样或空泡状,抗酸染色见胞质内含大量红色的短小杆状分枝杆菌(图3)。
2.2.4巨细胞病毒感染 在慢性炎症背景下,发现巨噬细胞、上皮细胞或血管内皮细胞体积增大,即形成巨细胞,其内可见核内包涵体。经典的核内包涵体见于细胞核内,呈紫蓝或紫红色,圆形或卵圆形,周围有空晕,呈所谓“鹰眼”样表现。有时,细胞质内亦可见包涵体,但不清晰。光镜下寻找典型包涵体费时费力,特别是出现不典型包涵体时,可借助免疫组化技术显示CMV抗体分布(图4)。
ABCDFE
A、B. HE染色示PCP组织学形态:肺泡间隔增宽,间质纤维化,肺泡腔内见多少不一的泡沫状或蜂窝状粉红染渗出物(×200);C.HE染色示肺泡腔内见泡沫状或蜂窝状粉红染渗出物,并见多核巨细胞,肉芽肿形成(×200);D. GMS染色示肺泡腔泡沫样渗出物中见较多圆形、卵圆形或新月形、括号形肺孢子菌(×400);E.真菌免疫荧光染色见泡沫样渗出物中见较多圆形、卵圆形肺孢子菌包囊,有些可见囊内小体(×400);F. 免疫组织化学染色显示阳性表达的肺孢子菌抗原,SP法(×400)
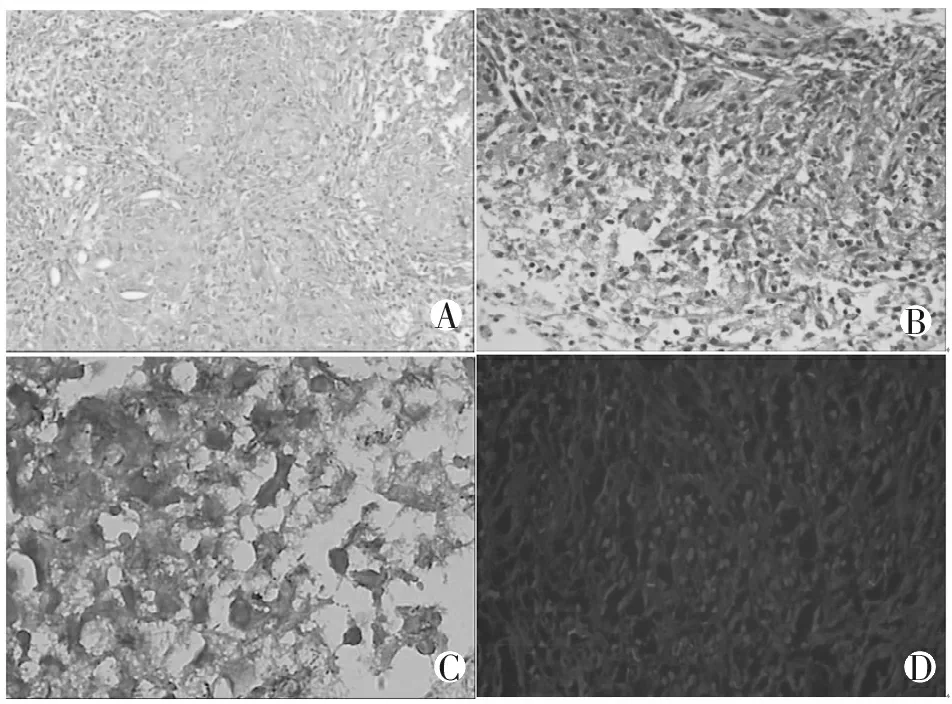
图1 病理学检查示肺孢子菌
A.HE染色示上皮样肉芽肿性结核结节(×100);B.HE染色示大量凝固性坏死(×200);C.抗酸染色见大量红染的短杆状分枝杆菌(×400);D抗酸荧光染色显示大量黄绿色或红色荧光的短杆状分枝杆菌(×400)。
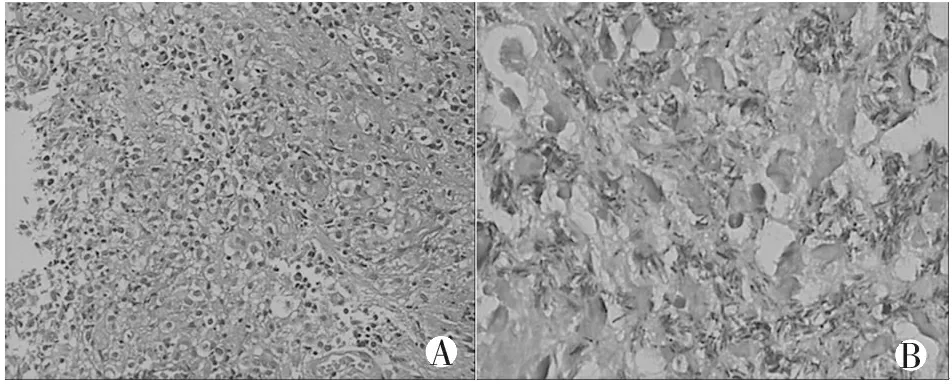
图2 病理学检查示结核
A. HE染色示局灶性组织细胞增生,其胞质丰富呈泡沫样或空泡状(×40,×200);C.抗酸染色见大量红染的短小杆状分枝杆菌(×400)。
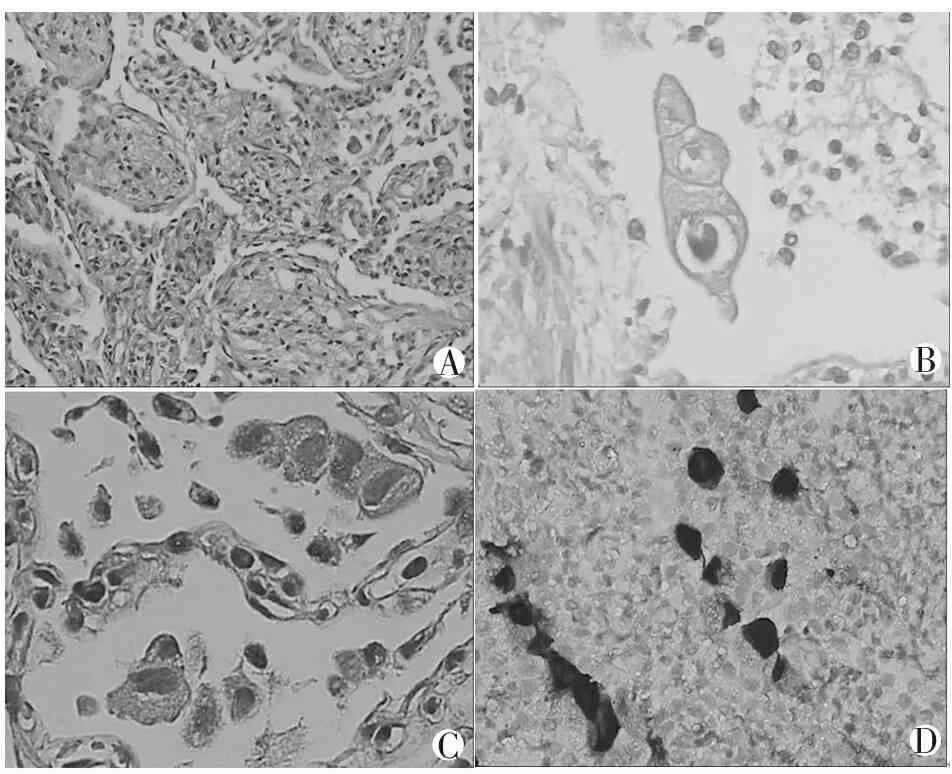
图3 病理学检查示非结核分枝杆菌
A. HE染色示巨噬细胞、上皮细胞或血管内皮细胞体积增大,形成巨细胞,(×100);B.C.经典的核内包涵体见于细胞核内,呈紫蓝或紫红色,圆形或卵圆形,周围有空晕,呈所谓“鹰眼”样表现(×400);D.免疫组化技术显示CMV抗体分布。
图4 病理学检查示CMV
2.2.5真菌感染 艾滋病患者常见真菌感染:马尔尼菲蓝状菌、隐球菌、念珠菌、曲霉菌。真菌病的病理表现:渗出性、坏死性或肉芽肿性病变或有空洞形成。病变常呈小灶状散在分布,亦可融合成大片,有时渗出性或肉芽肿病变可阻塞细支气管形成特征性的真菌球,或继发细菌等感染。不同真菌所致病变不同,诊断真菌感染的关键在于识别各种菌丝及孢子。
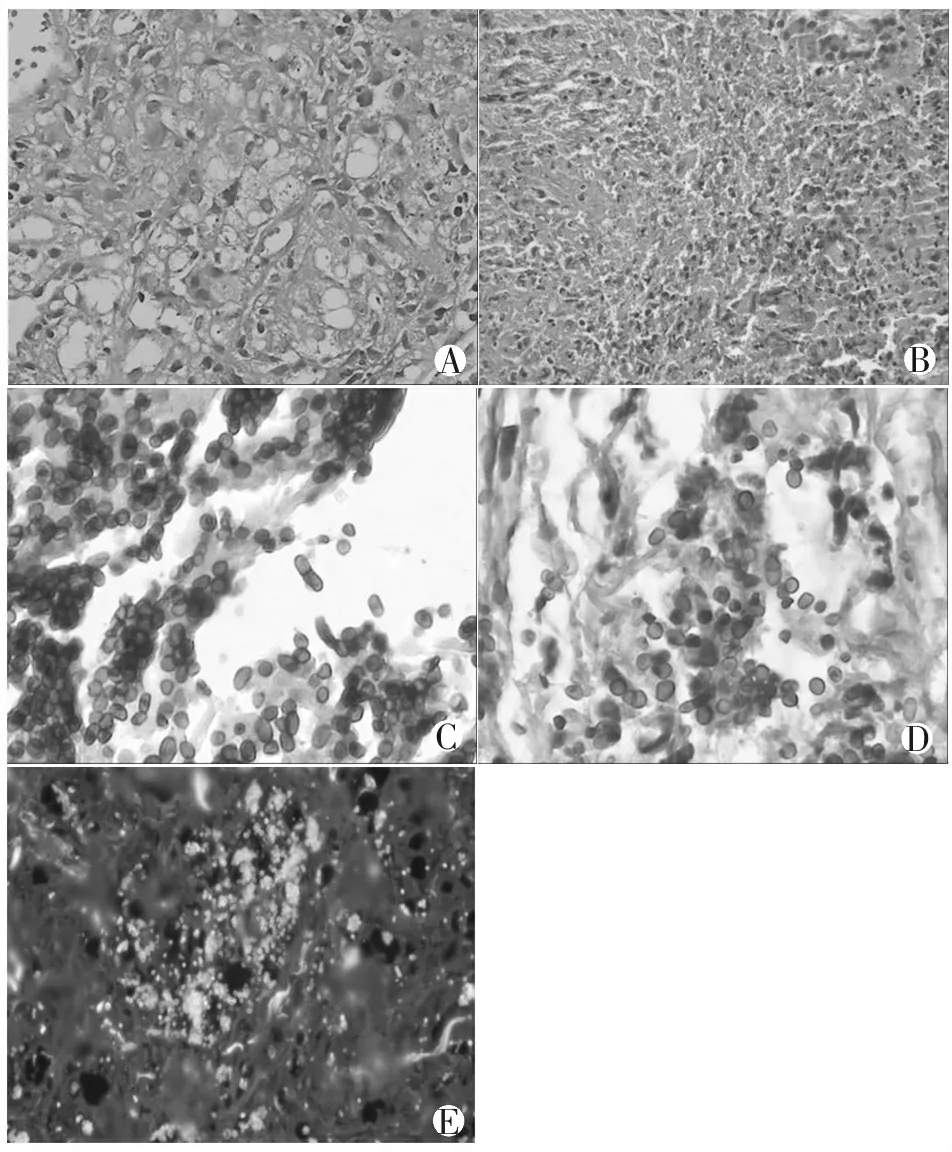
2.2.5.1 马尔尼菲蓝状菌病理改变 马尔尼菲蓝状菌侵入人体后先在巨噬细胞内增殖形成肉芽肿,抵抗力较低时多表现为坏死或无反应。由于艾滋病患者免疫力较低,大部分并未形成肉芽肿,而表现为坏死及弥漫增生的组织细胞及巨噬细胞。胞质内外或坏死灶内充满大量酵母状真菌,菌体多呈小圆形或卵圆形,HE染色菌体壁着色不良。六胺银和PAS染色可较清晰显示,菌体多呈小圆形或卵圆形,部分呈两端钝圆粗细均匀的腊肠状,有时可见横隔(图5)。
ABCDE
A、B. HE染色示马尔尼菲蓝状菌侵入巨噬细胞内形成肉芽肿,或表现为坏死及弥漫增生的组织细胞及巨噬细胞(×400);C、D、E. 六胺银、PAS染色及真菌荧光染色显示马尔尼菲蓝状菌菌体多呈小圆形或卵圆形,部分呈两端钝圆粗细均匀的腊肠状,有时可见横隔(×400)。
图5 病理学检查示马尔尼菲蓝状菌
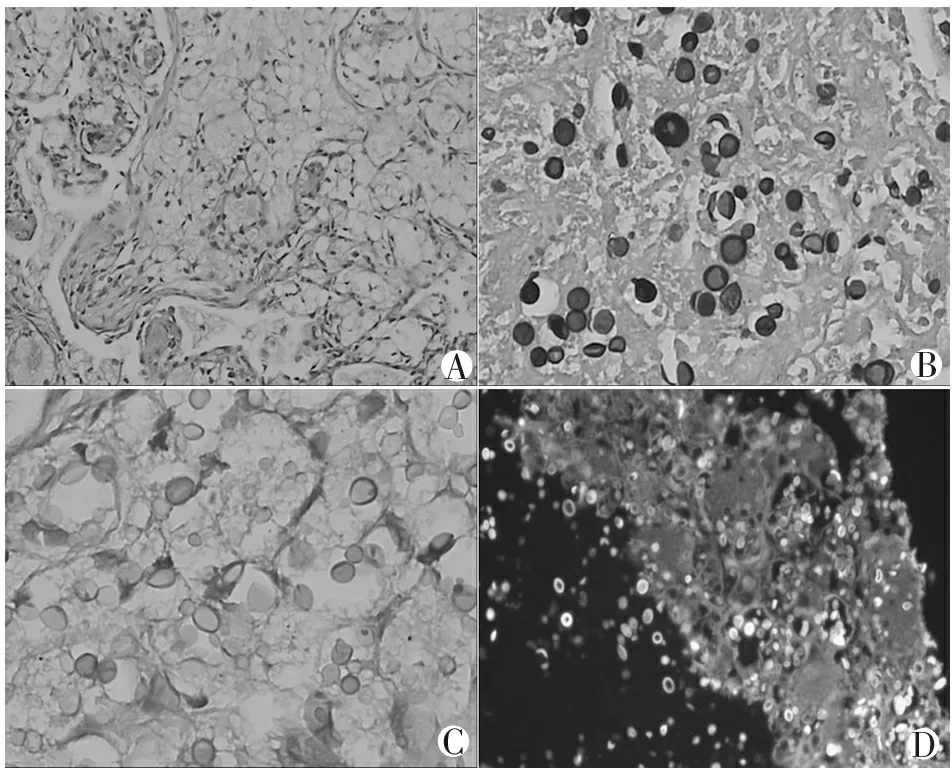
2.2.5.2 隐球菌感染病理表现为渗出性、坏死性或肉芽肿性病变,病灶内有淋巴、单核细胞浸润,组织细胞、巨噬细胞增生形成的肉芽肿,可伴纤维化,少数有空洞形成。诊断关键在于识别隐球菌厚壁荚膜孢子,六胺银染色为黑色类圆形菌体,偶呈煤球样或新月形,见厚壁荚膜;PAS 染色为紫红色,双折光,类圆形菌体,见厚壁荚膜(图6)。
2.2.5.3 组织胞浆菌病理特点 巨噬细胞增生及吞噬反应,肉芽肿形成;晚期病灶可发生纤维化和钙化。炎症灶中可见酵母样组织胞浆菌:位于巨噬细胞中的圆形或椭圆形,并见窄颈单芽孢的菌体(图7)。
2.2.5.4 白色假丝酵母菌病理特点:局部慢性炎症改变伴有白色假丝酵母菌的假菌丝和芽生孢子可确定诊断(图7)。
2.2.5.5 曲霉菌病理特点 主要引起急性化脓性和坏死性炎症,常累及肺部。曲霉菌常形成大小不等的菌丝群,菌丝呈杆状,常向同一方向分支生长,呈放射状或珊瑚状向周围扩展。菌丝较细,粗细较一致,并有锐角分支,高倍镜下有时可见菌丝内有横的分隔,菌丝周围有中性粒细胞浸润(图7)。
ABCD
A. HE染色示隐球菌感染病灶内组织细胞、巨噬细胞增生形成的肉芽肿,组织细胞内见半透明类圆形隐球菌孢子,染色浅淡,不易辨别(×400);、B. 六胺银染色为黑色类圆形菌体,偶呈煤球样或新月形,见厚壁荚膜(×400);C. PAS染色为紫红色,双折光,类圆形菌体,见厚壁荚膜(×400);D. 真菌荧光染色见发蓝绿色荧光的具有厚壁荚膜的类圆形菌体(×400)。
图6 病理学检查示隐球菌
2.2.5.6 毛霉菌病理特点 急性化脓性炎或慢性肉芽肿性炎。毛霉菌菌丝较粗,粗细不均匀,壁较厚,直径10-20 um,分支少,常呈钝角或直角,无分隔(图7)。
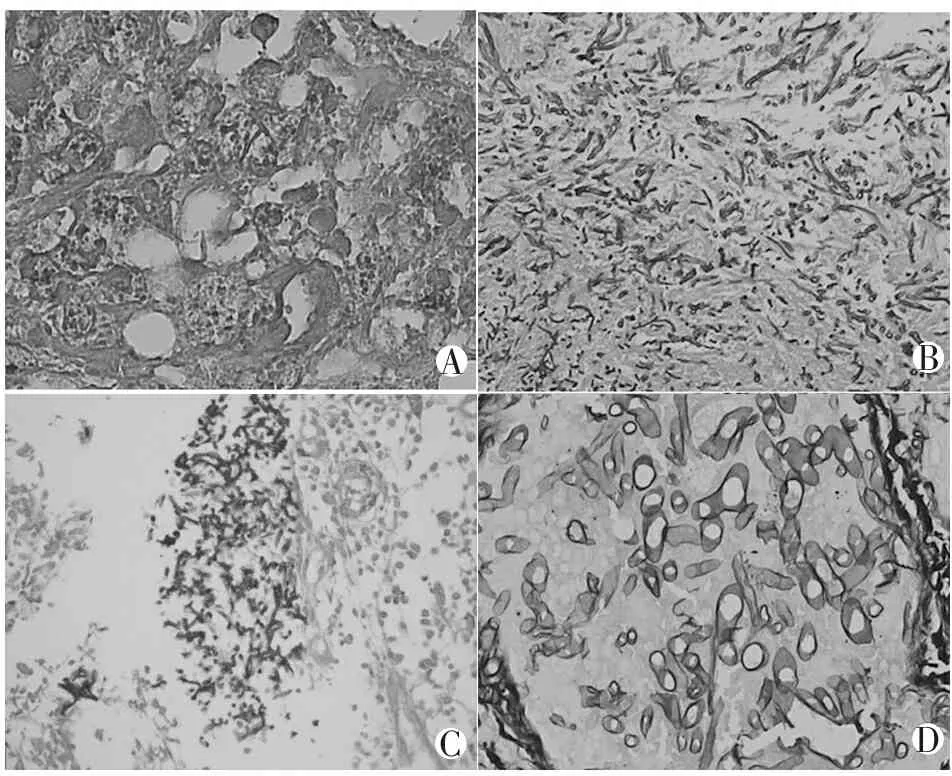
ABCD
A. HE染色示位于巨噬细胞中的圆形或椭圆形组织胞浆菌(×400);B. 六胺银染色示染成黑色的白色假丝酵母菌;C. 六胺银染色示染成黑色的曲霉菌(×400);D 六胺银染色示染成黑色的毛霉菌(×400)。
图7 病理学检查示各类真菌
2.2.5.7 弓形虫感染病理特点 弓形虫最常侵犯中枢神经系统引起弓形虫性脑炎,其病理特征为形成多发性“脓肿”样病灶;镜下表现主要为多灶性液化性坏死,病灶中心神经细胞变性坏死消失,周围血管充血,伴淋巴细胞、巨噬细胞浸润和小胶质细胞增生,边缘区较易查见弓形虫假囊和游离的速殖子(滋养体)(图8)。
2.2.5.8 梅毒螺旋体感染病理 主要累及淋巴结和皮肤,可见明显的血管炎和大量的浆细胞浸润,部分区域可见片状坏死。Warthin-Starry银染色可见螺旋状黑色螺旋体(图8)。
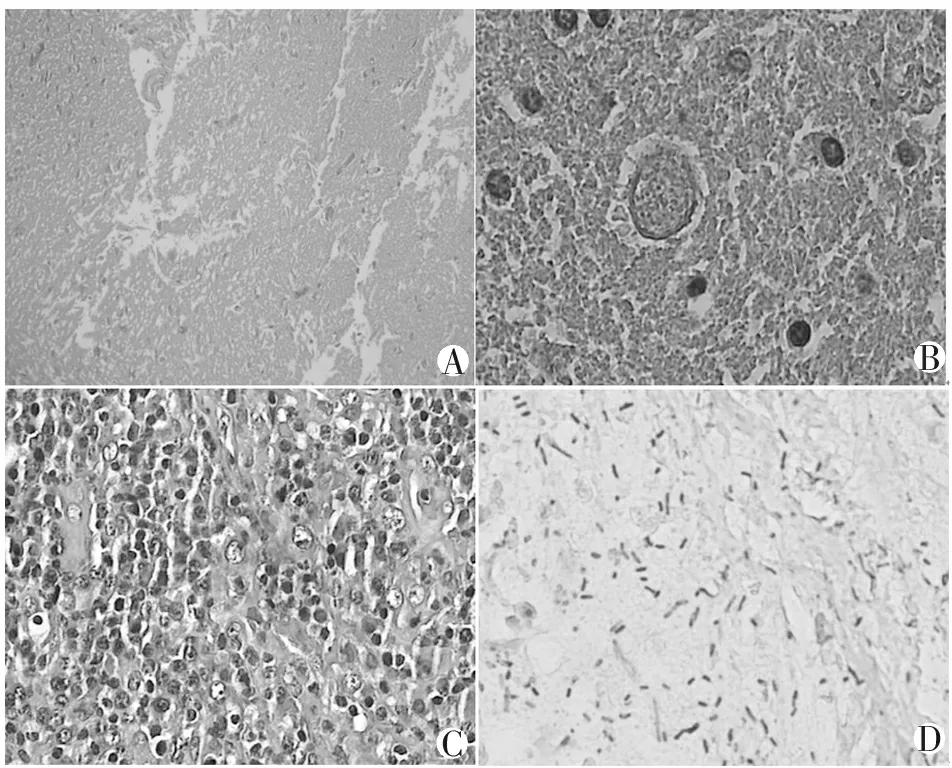
ABCD
A、B. HE染色示弓形虫感染病理特点:A示液化性坏死(×100),B示弓形虫假囊和速殖子(×400);C、D. 示梅毒螺旋体感染病理特点:C示可见明显的血管炎和大量的浆细胞浸润(×400);D示Warthin-Starry银染色见螺旋状黑色螺旋体(×400)。
图8 病理学检查示弓形虫及梅毒螺旋体
3 讨 论
机会性感染是艾滋病患者重要的并发症和致死原因,也常常是首发症状;其发生与体内CD4+T淋巴细胞计数密切相关,当CD4+T细胞计数减少至0.2×109/L(200/mm3)以下时几乎100%均发生机会性感染[4]。
研究结果表明,AIDS患者机会性感染病原体种类繁多,据统计,与AIDS相关的机会性感染已有30多种,包括细菌、真菌、病毒、寄生虫等;我科目前检出的特异性病原体有11种,最常见的为结核杆菌、肺孢子菌、马尔尼菲蓝状菌、巨细胞病毒(CMV)、隐球菌等。在AIDS患者,常常发生混合性感染,同一器官中常有多种病原体混合感染,最常见于肺部;可见2-3种病原体混合感染:如肺孢子菌合并结核、真菌、CMV等,结核合并真菌、CMV,或CMV合并真菌……等。常发生播散性感染: 一种病原体可同时累及多个器官,形成播散性或全身性疾病;在艾滋患者机会性感染可累及全身几乎所有脏器,我科检出的感染脏器有11个,其中以肺、肠及淋巴结中机会性感染最常见。
AIDS的感染性病变复杂:相同病因可呈现不同病变(渗出性、坏死性及肉芽肿性),相同病变可由不同病因(细菌、真菌、病毒、寄生虫)引起,识别病原体是关键,所以在病理诊断中寻找特异性病原体是关键。根据镜下特异性病原体引起的特异性组织学改变作为诊断线索,如肺孢子菌的肺泡腔内嗜酸性泡沫状渗出物、结核的干酪样坏死和结核结节、巨细胞病毒感染的“鹰眼”样核内病毒包涵体、特异的真菌菌丝及孢子等[5];采用多种检测技术明确病因;从而结合HE染色提供的线索,利用特殊染色(六胺银、PAS、抗酸染色等)、荧光染色(真菌和抗酸菌的荧光染色)、免疫组化等寻找病原体确定病因;必要时辅以电镜、PCR、原位杂交等技术寻找病原体。同时,一定要注意密切联系临床(尤其实验室检查)对病理确诊至关重要。
耶氏肺孢子菌(Pj)引起的肺炎(PJP,乳名“PCP”),是艾滋病患者最常见的机会性感染和最主要的致死原因之一[6]。由于尚无Pj 的体外培养技术,目前主要通过组织活检染色(六胺银染色)镜检来确诊,同时真菌荧光染色也能较好地显示。AIDS患者结核病发病率明显高于普通人,结核病已被认为是发展中国家HIV感染者中最常见的机会性感染,且常为免疫缺陷的第一个临床症状[7]。结核病主要发生在肺部,肺外结核主要发生在淋巴结及肠道。在HIV感染不同阶段,结核病的表现亦有所不同。可产生典型的肉芽肿反应或仅见化脓性及凝固性坏死,故无结核结节者也不能排除结核病。在AIDS患者中也常发生病毒感染,以巨细胞病毒(CMV)感染最多见[8,9]。在AIDS病人中CMV常呈活动性感染,90%以上病人血清CMV抗体阳性,50%以上有病毒血症[10]。CMV感染最常累及肺及消化道(主要是肠道)。其组织学形态中查找核内见包涵体与巨细胞形成有诊断价值。典型核内包涵体见于细胞核内,呈紫蓝或紫红色,圆形或卵圆形,周围有空晕,呈 “鹰眼”样表现。有时,细胞质内亦可见包涵体,但不清晰。光镜下寻找典型包涵体费时费力,特别是出现不典型包涵体时,可借助免疫组化技术显示CMV抗体分布。
艾滋病患者常见真菌感染:马尔尼菲蓝状菌、隐球菌、念珠菌、曲霉菌。真菌病的病理表现:渗出性、坏死性或肉芽肿性病变。不同真菌所致病变不同,诊断真菌感染的关键在于识别各种菌丝及孢子[11,12]。马尔尼菲蓝状菌可形成肉芽肿,由于艾滋病患者免疫力较低,大部分并未形成肉芽肿,而表现为坏死及弥漫增生的组织细胞及巨噬细胞。胞质内外或坏死灶内充满大量酵母状真菌,菌体多呈小圆形或卵圆形,HE染色菌体壁着色不良。六胺银、PAS染色及真菌荧光染色可较清晰显示,菌体多呈小圆形或卵圆形,部分呈两端钝圆粗细均匀的腊肠状,有时可见横隔。隐球菌表现为渗出性、坏死性或肉芽肿性病变,病灶内有淋巴、单核细胞浸润,组织细胞、巨噬细胞增生形成的肉芽肿,可伴纤维化。HE染色见半透明类圆形隐球菌孢子,染色浅淡,不易辨别。诊断关键在于识别隐球菌厚壁荚膜孢子,六胺银染色为黑色类圆形菌体,偶呈煤球样或新月形,见厚壁荚膜。PAS 染色为紫红色,双折光,类圆形菌体,见厚壁荚膜。另外白色假丝酵母菌、毛霉菌、曲霉菌及组织胞浆菌的识别也在于其各自的不同的菌丝及孢子特点。
在AIDS病人,弓形虫病,尤其是弓形虫性脑炎比较常见,且是AIDS的主要死因之一[13]。具有组织坏死和炎性渗出等活动性病变者,常称为弓形虫性炎症。可以查见弓形虫包囊、假囊及速殖子。自AIDS流行以来,HIV合并梅毒者屡有报道[14],梅毒组织学形态表现为小动脉周围炎(围管性单核细胞、淋巴细胞和浆细胞浸润),浆细胞恒定出现是本病的病变特点之一,还可形成梅毒树胶肿。可采用银染(Warthin-Starry法)显示梅毒螺旋体,显示为螺旋状黑色螺旋体。
本文结果显示,AIDS患者机会性感染病原体种类繁多,且常常发生混合性感染。AIDS的感染性病变复杂:相同病因可呈现不同病变,相同病变可由不同病因引起,所以在病理诊断中寻找特异性病原体是关键。采用多种检测技术,结合HE染色提供的线索,利用特殊染色(六胺银、PAS、抗酸染色等)、荧光染色、免疫组化等寻找病原体确定病因;必要时辅以电镜、PCR、原位杂交等技术寻找病原体。同时,一定要注意密切联系临床(尤其实验室检查)对病理确诊至关重要。
