新型FTS联合营养风险筛查在胃肠肿瘤治疗中的作用
2019-06-30黄金梅刘兴玲李美连
黄金梅 刘兴玲 李美连


[摘要]目的研究分析新型FTS(快速康复外科治疗)联合营养风险筛查在胃肠肿瘤治疗中的作用。方法选取2015年8月- 2018年8月在我院普通外科接受诊治的160例胃肠肿瘤患者作为研究对象,根据筛查结果将160例患者分为营养正常组和营养异常组,采用随机分配法将两组患者分为两组,营养正常组再分为常规1组和新FTS1组,营养异常组再分为常规2组和新型FTS2组,两组常规组患者给予常规护理干预,新FTS1组给予新型FTS进行干预,新FTS2给予新型FTS联合营养干预进行干预,对四组患者的干预效果进行探究。结果观察四组患者的并发症情况发现,两组常规组的并发症总发生率均分别高于对应的两组新型FTS组,差异有统计学意义(P<0.05)。观察四组患者的临床指标发现,两组常规组的指标均分别差于于对应的两组新型FTS组,差异有统计学意义(P<0.05)。观察四组患者的满意度发现,两组常规组的满意度均分别低于对应的两组新型FTS组,差异有统计学意义(P<0.05)。结论新型FTS联合营养风险筛查在胃肠肿瘤治疗中具有减少并发症情况,改善住院时间等临床指标和患者满意度的作用,值得在临床上推广应用。
[关键词]新型FTS;营养风险筛查;胃肠肿瘤;联合干预
[中图分类号] R735
[文献标识码]A
[文章编号]2095-0616( 2019) 01-30-04
胃腸肿瘤主要通过手术进行治疗,但由于患者术后会出现营养不良情况,导致其机体免疫力低下,从而使得其并发症增多等问题出现,对其的术后康复进程和预后效果造成严重的影响[1-7]。本研究通过将新型FTS联合营养风险筛查应用与胃肠肿瘤患者治疗中发现临床效果良好,可有效的对患者并发症发生率进行控制,使得患者的首次排气、排便及下床活动和住院天数和费用等临床指标显著改善,使得患者满意度得到提升,降低其经济负担,具有促进其围手术期康复进程作用。现报道如下。
1 资料与方法
1.1 一般资料
本研究选取2015年8月- 2018年8月我院普通外科接受诊治的160例胃肠肿瘤患者作为研究对象,根据筛查结果将160例患者分为营养正常组和营养异常组,每组80例,然后采用随机分配法将两组患者分别分为两组,营养正常组分为常规1组和新FTSI组,营养异常组分为常规2组和新型FTS2组,每组40例。常规1组中男23例,女17例;年龄38 - 81岁,平均(64.6±5.3)岁。新FTSI组中男21例,女19例;年龄37 - 80岁,平均(64.6±5.3)岁;常规2组中男22例,女18例;年龄38 - 82岁,平均(64.6±5.3)岁;新FTS1组中男20例,女20例;年龄37 - 81岁,平均(64.6±5.3)岁。四组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
常规1组和常规2组均给予常规护理进行干预,给予其术前健康教育、禁水禁食、药物护理及鼻胃管置入和护理,术中配合,术后镇痛护理、早期活动指导、引流管护理及饮食护理等。
新FTS1组应用新型FTS进行干预,具体干预方法:(1)强化术前健康教育和指导:术前2天与患者及其家属进行面对面健康教育,根据制定《快速康复外科护理手册》对患者及其家属进行康复知识教育。(2)术前准备:术前6小时开始禁食,术前2 - 4h开始禁水,手术前的晚上10点~凌晨0点给予患者lOOOmL浓度为10%的葡萄糖口服液进行饮用,术前2 - 4h给予患者200mL浓度为10%的葡萄糖口服液进行饮用,若患者为糖尿病患者将葡萄糖溶液改为矿泉水或者脉动等电解质饮料。(3)对患者术中、术后留置管道进行护理,尿管在患者术后12 - 24h内进行拔除,胃管根据患者情况肿瘤术后拔除胃管时间为术后2 - 3d,肠肿瘤术后拔除胃管时间术后12h内,甚至术后评估患者无恶心呕吐时即拔除。若患者留置腹部引流管,需对其引流液出入量、性质及颜色进行观察,待其病情允许后进行拔除,尽可能在早期进行拔除。(4)围术期疼痛管理和术中补液保温措施,手术麻醉根据患者需求和情况选取联合全麻或硬膜外麻醉,术后进行48h的静脉镇痛或硬膜外镇痛;术中采用加温至37℃补液及腹腔冲洗液,控制补液。(5)优化术后康复护理:①术后待其麻醉清醒后将其体位调整至半卧位,术后清醒后指导使用呼吸训练器进行肺功能康复,一天5次,每次20 - 30min。同时双下肢予压力泵进行压力治疗,一天两次,每次30min;使用康复脚踏车进行运动疗法,一天两次,每次45min;指导患者床上防DVT四步康复操,一天5次,每次20min。②术后第一天管床护士协助患者离床坐,进行生活护理:刷牙、擦浴更衣、温水足疗等,安排一天两次进行离床活动,借助助行器床边向室外过渡行走,每次行走时间在1 - 2h,一天2-3次,根据其耐受度逐渐增加次数和延长活动时间;③术后6h开始指导咀嚼口香糖,一天3-4次,每次30min。护士听诊肠鸣音恢复正常,评估患者吞咽功能,与管床医师沟通后,指导进食少许清流质,进食后无不适转由流质向半流质、正常食物逐渐过渡,建议为少量多餐。(6)患者出院后对其进行为期1周的随访,对其临床指标及体征指标进行询问记录。
新FTS2给予新型FTS联合营养干预进行干预,新型FTS干预措施与新FTS1组一样,营养干预措施如下阐述:由营养科对患者进行会诊后,根据对患者的热量进行估算后对其的能量供给水平进行确认,即30 - 35kcal/(kg·d),蛋白质摄人目标:1.5 - 2.Og/( kg·d),若患者经口摄入不足则给予其短肽型营养制剂口服,并将《等份食物交换表》和《消化道围术期患者饮食指导手册》发放给患者,对其进行相关营养干预知识的健康教育,根据患者术后不同阶段给予相应的饮食指导,告知其如何选择食物的类别,并根据饮食特点举例说明食谱。除外责任护士每日对患者的膳食情况和营养支持进行记录,对其摄入能量进行计算,及时对其饮食结构进行调整。
1.3 观察指标
观察四组患者的并发症、临床指标及满意度等情况。统计四组患者并发症发生例数,计算总发生率;临床指标主要观察患者的首次排氣时间、首次排便时间、首次下床活动时间、住院时间及住院费用;满意度应用我院自制的满意度调查问卷进行评价,问卷总分100分,主要对患者的基础护理、专科护理、个性化护理及服务态度这4方面进行调查,100分为非常满意,86 - 99分为基本满意,60 - 85分为一般,60分以下为不满意,满意度=(非常满意+基本满意)/总例数×100%;该问卷具有良好的信效度,Cronbach's α=0.86。
1.4 统计学处理
采用SPSS20.0统计学软件对数据进行处理,计量资料用(x±s)表示,采用t检验;计数资料用(%)表示,采用X2检验。P<0.05为差异有统计学意义。
2 结果
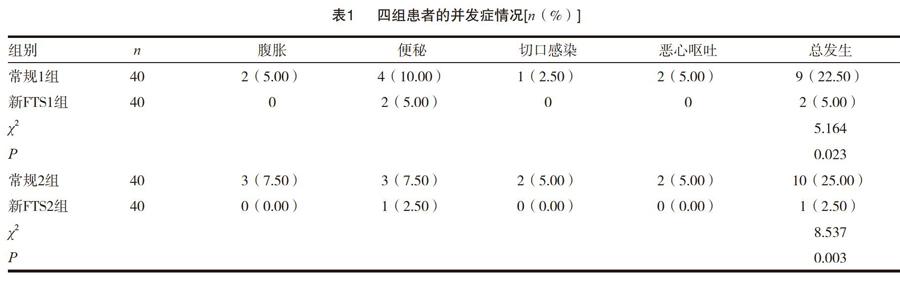
2.1 四组患者的并发症情况
观察四组患者的并发症情况发现,新FTS1组总发生率较低,与常规1组比较,差异有统计学意义(P<0.05);新FTS2组总发生率较低,与常规2组比较,差异有统计学意义(P<0.05)。见表l。
2.2 四组患者临床指标比较
观察四组患者的临床指标发现,新FTSI组指标较优,与常规l组相比,差异有统计学意义(P<0.05);新FTS2组指标较优,与常规2组比较,差异有统计学意义(P<0.05)。见表2。
2.3 四组患者满意度情况比较
观察四组患者的满意度发现,新FTS1组满意度较高,与常规1组比较,差异有统计学意义(P<0.05);新FTS2组满意度较高,与常规2组比较,差异有统计学意义(P<0.05)。见表3。
3 讨论
营养风险筛查是判断患者是否需要制定营养干预方案的常用方式,同时还可对患者是否制定肠内或肠外营养支持计划进行筛查[8]。在本次研究中,通过应用这一措施将160例患者分为营养正常组和营养异常组两大组,然后在分别分为两小组,对于营养正常组的新FTS1组不给予营养干预进行干预,而营养异常的新FTS2组则给予了营养干预进行干预,可见采取这一措施可针对性的对需要进行营养干预的患者进行干预。在本次研究中新FTSI组和新FTS2组均给予了新型FTS进行干预,对比两组患者分别与常规1组和常规2组的干预结果发现,与常规l组相比,新FTSI组的并发症总发生率、首次排气时间、首次排便时间、首次下床活动时间、住院时间及住院费用等临床指标和满意度均较优,差异有统计学意义(P<0.05);与常规2组比较,新FTS2组的并发症总发生率、首次排气时间、首次排便时间、首次下床活动时间、住院时间及住院费用等临床指标和满意度均较优,差异有统计学意义(P <0.05)。从这一研究结果可看出新FTSI组和新FTS2组在控制并发症发生率、改善临床指标和提升患者满意度方面更占优势。新型FTS干预模式是在FTS基础上添加普通外科元素进行组合改良的新型干预模式[9-11]。快速康复外科主要是指通过对循证医学能根据的围手术期多学科基础与处理措施进行优化的干预模式,旨在对患者的治疗过程中的生理上和心理上的创伤进行改善,并对其治疗应激反应及并发症情况进行控制,使得患者临床诊治的安全性和有效性得到提高[12-17]。
综上所述,新型FTS联合营养风险筛查在胃肠肿瘤治疗中的作用显著,有效的降低患者并发症发生率,缩短首次排气、排便和下床活动时间,同时缩短了住院时间,使得其住院费用降低,经济压力得到缓解,从而使得患者的满意度得到提升,具有较高的临床应用价值。
[参考文献]
[1]李会影,杨丽萍,安晓汾,等.营养风险筛查联合肠内营养支持在卵巢癌化疗患者中临床应用价值研究[J].中国妇幼保健,2016,31( 8): 1594-1596.
[2]冯少兰,刘冬梅,钟美华.胃肠道肿瘤患者术后责任制护理中营养风险筛查的应用效果分析[J].中国医药科学,2016,6(22):112-114.
[3]汤婷,吴艳,张丽,等.围术期肠内营养支持联合应用生长抑素对胃癌根治术患者的治疗作用研究叨.中国医学前沿杂志(电子版),2017,9 (3): 97-101.
[4]毛俊峰,陈橼,王小林,等.营养风险筛查在胃肠肿瘤患者术中的应用效果研究[J]_交通医学,2016,30(4):353-354.
[5]贾秀眉,徐芳,丁芳,等.在营养风险筛查中应用责任护理对胃肠肿瘤患者的影响[J].中华全科医学,2016,14( 3): 487-490.
[6]刘妮,方玉,李子禹,等.营养风险筛查和主观整体评估在胃肠肿瘤病人围手术期中的应用及临床意义[J].肠外与肠内营养,2016,23(6):346-350.
[7]宋玲.在营养风险筛查中应用责任护理对胃肠肿瘤患者的影响[J].实用临床护理学电子杂志,2017,2(36):133-135.
[8]刘纯,杨晓晨,陈伯文,等.重症脑卒中患者营养风险筛查与营养支持现状调查[J].药学实践杂志,2016,34(5):408-411.
[9]赵中海,朱立东,杨景国,等.术前强化口服辅助营养在老年胃肠道肿瘤外科中的应用研究[J].中国医刊,2016,51(8):40-43.
[10]尚闯,高阳,罗淼.胃肠肿瘤手术切口感染的预防研究[J].现代诊断与治疗,2017,28( 24):4627-4629.
[11]薛卫杰.腹腔镜手术治疗胃肠肿瘤疗效观察[J].现代诊断与治疗,2017,28( 22):4225-4227.
[12]常颖,张晴,范锐心,等.恶性肿瘤住院病人营养风险和营养支持与临床转归的研究[J].肠外与肠内营养,2016,23( 2): 71-73.
[13]刘飞,吴铎.术前营养风险筛查在胃癌患者术中的作用及对术后并发症发生率的影响[J].广西医科大学学报,2017, 34(11):1594-1597.
[14]朱亚琴,徐丽,陈晓玲,等.营养风险筛查在消化道癌症患者手术后并发症预测方面的功能[J].山西医药杂志,2017 ,46( 22):2720-2722.
[15]李艳,刘元元,冯莉霞.NRS 2002在结直肠癌患者化疗期间营养风险筛查中的应用效果观察[J].护士进修杂志,2016, 31(16):1488-1490.
[16]林丽,张吉才,谢飞,等.患者全面主观营养评定和营养风险筛查2002在消化系统肿瘤患者营养评估中的应用比较[J].中国食物与营养,2018,24(3): 78-81.
[17]陈博,徐阿曼,胡孔旺,等.营养支持干预对有营养风险胃肠恶性肿瘤病人临床结局和成本一效果比的影响[J].肠外与肠内营养,2016,23( 2): 78-81.
